La enfermedad de Alzheimer (EA) es una compleja condición neurodegenerativa caracterizada por una serie de cambios patológicos en el cerebro. Durante mucho tiempo, los estudios postmortem han sido fundamentales para identificar los sellos distintivos de esta enfermedad, revelando un panorama de lesiones que, en conjunto, explican el progresivo deterioro cognitivo que experimentan los pacientes. Estos hallazgos han sido cruciales no solo para el desarrollo de criterios diagnósticos reconocidos a nivel mundial, sino también para generar hipótesis sobre la fisiopatología subyacente de la enfermedad. A pesar de su naturaleza inherente de corte transversal, estos estudios han permitido establecer una cronología de la progresión de las patologías clave.
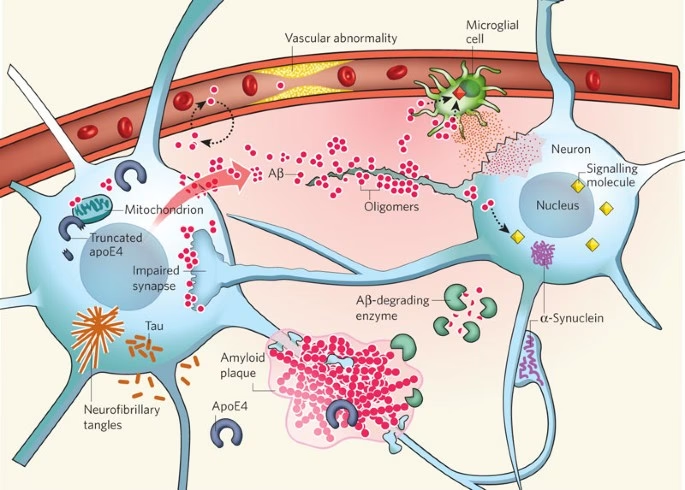
Las características neuropatológicas de la enfermedad de Alzheimer se dividen en lesiones 'positivas' y 'negativas'. Las lesiones positivas clásicas incluyen la acumulación de placas amiloides y ovillos neurofibrilares. Estas se acompañan de respuestas gliales, como la astrogliosis (proliferación de astrocitos) y la activación de células microgliales. Por otro lado, las lesiones negativas se refieren principalmente a la pérdida de neuronas y sinapsis.
- Los Sellos Distintivos Patológicos
- La Pérdida Sináptica y Neuronal
- La Progresión de la Enfermedad
- El Papel de los Oligómeros Solubles
- Cambios Macroscópicos en el Cerebro
- Criterios Diagnósticos Patológicos
- Comparativa de los Sellos Patológicos Principales
- Preguntas Frecuentes sobre los Sellos del Alzheimer
- ¿Cuáles son los principales sellos neurológicos de la enfermedad de Alzheimer?
- ¿Cuándo aparecen estas lesiones en el cerebro?
- ¿Cuál de estas lesiones se correlaciona mejor con la gravedad de los síntomas cognitivos?
- ¿Qué es la proteína tau y por qué es importante en el Alzheimer?
- ¿Qué son los oligómeros Aβ y cuál es su papel?
- ¿El diagnóstico de Alzheimer se basa solo en estos hallazgos patológicos?
- Conclusiones sobre la Neurodegeneración
Los Sellos Distintivos Patológicos
Los hallazgos patológicos más prominentes y definitorios de la enfermedad de Alzheimer son las placas amiloides y los ovillos neurofibrilares. Sin embargo, la comprensión de la enfermedad ha evolucionado para incluir otras alteraciones importantes.
Placas Amiloides
Las placas amiloides son depósitos extracelulares compuestos principalmente por el péptido beta-amiloide (Aβ). Este péptido se deriva de la proteína precursora amiloide (APP) mediante una secuencia de cortes enzimáticos. Las placas amiloides se encuentran abundantemente en la corteza cerebral de los pacientes con EA. Se clasifican comúnmente en dos tipos:
- Placas difusas: Depósitos amorfos con contornos poco definidos. Generalmente no se asocian con neuritas distróficas, respuestas gliales o pérdida sináptica. Son un hallazgo relativamente común en cerebros de personas mayores cognitivamente intactas y no se consideran para el diagnóstico patológico de EA.
- Placas de núcleo denso: Depósitos amiloides fibrilares con un núcleo compacto. Suelen estar rodeadas por neuritas distróficas (placas neuríticas), astrocitos reactivos y microglía activada, y se asocian con la pérdida sináptica. La presencia de placas neuríticas se utiliza para el diagnóstico patológico de EA, ya que su presencia generalmente se asocia con deterioro cognitivo.
Además de las placas en el tejido cerebral, el péptido beta-amiloide también puede depositarse en las paredes de los vasos sanguíneos del cerebro, una condición conocida como angiopatía amiloide cerebral (AAC). Aunque algún grado de AAC es común en la EA, si es severa, puede debilitar los vasos y causar hemorragias.
Ovillos Neurofibrilares
Los ovillos neurofibrilares (NFTs) son agregados intraneuronales de la proteína tau hiperfosforilada y mal plegada. Tau es normalmente una proteína asociada a los microtúbulos, crucial para el transporte axonal. En la EA, tau se acumula en el soma y las dendritas de las neuronas, formando estos ovillos. Cuando la neurona muere, los ovillos pueden persistir en el espacio extraneuronal como ovillos 'fantasma'.
A diferencia de las placas amiloides, que se distribuyen ampliamente en la corteza, los ovillos neurofibrilares tienen una progresión espacio-temporal estereotipada que se correlaciona estrechamente con la gravedad del declive cognitivo. Comienzan en regiones límbicas como la corteza entorrinal y perirrinal, luego se extienden a los subcampos de Ammon del hipocampo, después a la corteza de asociación y, finalmente, a la neocorteza primaria. Este patrón jerárquico es tan consistente que se utiliza un esquema de clasificación (estadios de Braak y Braak) para el diagnóstico patológico.
Otros Hallazgos Positivos
Además de las placas y los ovillos, se observan otras lesiones positivas como hilos de neurópilo (segmentos axonales y dendríticos que contienen tau agregada) y neuritas distróficas. En la formación del hipocampo, pueden encontrarse cuerpos de Hirano y degeneración granulovacuolar.
Respuestas Gliales
Las respuestas de las células gliales, incluyendo la astrogliosis (activación y proliferación de astrocitos) y la activación de la microglía (células inmunes residentes del cerebro), son características acompañantes de la patología de Alzheimer. Estas células responden a la acumulación de placas y ovillos, aunque su papel exacto (protector o perjudicial) en la progresión de la enfermedad es complejo y aún objeto de investigación.
La Pérdida Sináptica y Neuronal
Las lesiones 'negativas', es decir, la pérdida sináptica y la pérdida neuronal, son características centrales de la EA y se consideran los correlatos más importantes del deterioro cognitivo. La pérdida de sinapsis, en particular, parece ocurrir tempranamente en el proceso neurodegenerativo y se correlaciona mejor con la gravedad de los síntomas cognitivos que la carga total de placas o ovillos.
El proceso neurodegenerativo comienza con daño a las sinapsis, seguido de degeneración retrógrada de los axones, atrofia del árbol dendrítico y, finalmente, pérdida del cuerpo celular neuronal (pericarion). Aunque la pérdida neuronal y sináptica en gran medida sigue el patrón de distribución de los ovillos neurofibrilares, la relación causal exacta entre los ovillos y la muerte neuronal/sináptica sigue siendo un área de investigación activa.
La Progresión de la Enfermedad
Los estudios clinicopatológicos han establecido que existe un continuo entre el envejecimiento 'normal' y la demencia por EA. El acúmulo de placas amiloides parece ocurrir principalmente antes del inicio de los déficits cognitivos significativos. Por otro lado, los ovillos neurofibrilares, la pérdida neuronal y, sobre todo, la pérdida sináptica, parecen progresar paralelamente al empeoramiento del declive cognitivo.
Esta distinción temporal es crucial. La patología amiloide puede acumularse silenciosamente durante años, incluso décadas, antes de que aparezcan los síntomas clínicos. La patología tau (ovillos) y la neurodegeneración (pérdida de sinapsis y neuronas) se asocian más estrechamente con la manifestación clínica de la demencia.
El Papel de los Oligómeros Solubles
Investigaciones más recientes sugieren que no solo las formas agregadas e insolubles de Aβ y tau contribuyen a la patología, sino también las formas solubles y oligoméricas. Se cree que los oligómeros Aβ solubles, compuestos por 2 a 12 subunidades, son particularmente neurotóxicos y podrían ser responsables del daño sináptico temprano y los déficits de memoria. Estos oligómeros pueden alterar la función sináptica, dañar las espinas dendríticas e interferir con la plasticidad sináptica.
Se ha demostrado en modelos experimentales que la transmisión de Aβ a través de las sinapsis puede promover la neurodegeneración. Estos oligómeros tóxicos, identificados inicialmente in vitro y en modelos transgénicos, también se han encontrado en el líquido cefalorraquídeo y en el cerebro de pacientes con EA, acumulándose progresivamente.
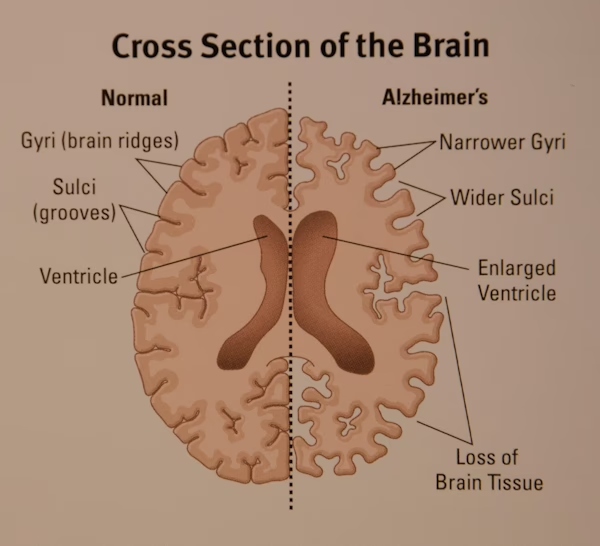
Cambios Macroscópicos en el Cerebro
Aunque el examen visual macroscópico del cerebro no es suficiente para diagnosticar la EA, un patrón típico de atrofia cortical simétrica, que afecta predominantemente los lóbulos temporales mediales y relativamente respeta las cortezas motoras, sensoriales y visuales primarias, es fuertemente sugestivo. Esta atrofia conduce a una dilatación prominente de los ventrículos laterales (hidrocefalia ex vacuo).
Otros hallazgos macroscópicos comunes en cerebros de ancianos, que a menudo coexisten con la EA, incluyen signos de enfermedad cerebrovascular, como microinfartos, infartos lacunares y desmielinización de la sustancia blanca periventricular. La presencia de microhemorragias o hemorragias lobares puede indicar una angiopatía amiloide cerebral severa concurrente.
Criterios Diagnósticos Patológicos
Históricamente, los criterios para el diagnóstico patológico de la EA se han basado en la evaluación cuantitativa y/o distribucional de las placas amiloides y los ovillos neurofibrilares.
Los primeros criterios (Khachaturian, 1985) se basaban en la densidad total de placas amiloides, ajustada por edad, pero tenían baja especificidad al no considerar los ovillos ni distinguir entre tipos de placas.
El Consorcio para Establecer un Registro para la Enfermedad de Alzheimer (CERAD, 1991) mejoró la especificidad al enfatizar la importancia de las placas neuríticas sobre las difusas. Utilizaban una puntuación semicuantitativa de la densidad de placas neuríticas en la región cortical más afectada y la edad del paciente. Sin embargo, aún carecían de suficiente especificidad al no incluir los ovillos.
Por otro lado, la clasificación basada únicamente en los estadios de Braak y Braak para los ovillos neurofibrilares mostraba alta especificidad pero baja sensibilidad.
Los criterios patológicos actuales, definidos en 1997 por un taller del Instituto Nacional del Envejecimiento y el Instituto Reagan (NIA-RI), combinan la puntuación semicuantitativa de placas neuríticas de CERAD con la clasificación de estadios de ovillos de Braak y Braak. Esto permite establecer categorías de probabilidad diagnóstica (alta, intermedia, baja) basándose en la carga y distribución de ambas patologías. Un diagnóstico de EA se realiza si se cumplen los criterios de probabilidad intermedia o alta y el paciente tenía un historial clínico de demencia.
Es importante notar que estos criterios están en revisión, ya que la experiencia ha mostrado casos con alta carga patológica pero pocos síntomas cognitivos, y viceversa. Además, los criterios actuales ya reconocen la alta prevalencia de patologías mixtas (como enfermedad vascular o cuerpos de Lewy) que contribuyen a la demencia en personas mayores.
Comparativa de los Sellos Patológicos Principales
| Característica | Placas Amiloides | Ovillos Neurofibrilares | Pérdida Sináptica/Neuronal |
|---|---|---|---|
| Composición Principal | Péptido Beta-Amiloide (Aβ) | Proteína Tau hiperfosforilada | Degeneración de neuronas y sinapsis |
| Localización Primaria | Extracelular (parénquima, vasos) | Intraneuronal (luego extraneuronal) | Tejido cerebral (corteza, sistema límbico) |
| Tipos/Formas | Difusas, Núcleo denso (neuríticas); Angiopatía | NFTs, Hilos de neurópilo | Daño dendrítico, axonal, muerte neuronal |
| Distribución Típica | Amplia en corteza, luego subcortical | Patrón jerárquico (Braak): Límbico → Cortical | Sigue en gran medida distribución de ovillos |
| Correlación con Síntomas | Aparecen antes, menos correlación directa con gravedad | Se correlacionan mejor con gravedad del declive | La mejor correlación con la gravedad del declive cognitivo |
| Considerado en Diagnóstico Patológico | Sí (placas neuríticas) | Sí (estadio de Braak) | Evaluado, pero menos central en criterios clásicos |
Preguntas Frecuentes sobre los Sellos del Alzheimer
¿Cuáles son los principales sellos neurológicos de la enfermedad de Alzheimer?
Los sellos principales son las placas amiloides (depósitos extracelulares de péptido Aβ) y los ovillos neurofibrilares (agregados intraneuronales de proteína tau hiperfosforilada). También son cruciales la pérdida de sinapsis y la pérdida de neuronas.
¿Cuándo aparecen estas lesiones en el cerebro?
Las placas amiloides tienden a acumularse en el cerebro muchos años, incluso una década o más, antes de que aparezcan los síntomas clínicos de demencia. Los ovillos neurofibrilares, la pérdida sináptica y la pérdida neuronal progresan más en paralelo con el declive cognitivo.
¿Cuál de estas lesiones se correlaciona mejor con la gravedad de los síntomas cognitivos?
La pérdida de sinapsis en la neocorteza y el sistema límbico es el factor que mejor se correlaciona con la gravedad del deterioro cognitivo en los pacientes con Alzheimer.
¿Qué es la proteína tau y por qué es importante en el Alzheimer?
La proteína tau es normalmente una proteína asociada a los microtúbulos, importante para el transporte dentro de las neuronas. En el Alzheimer, tau se vuelve hiperfosforilada y se agrega, formando los ovillos neurofibrilares dentro de las neuronas, lo que interrumpe la función neuronal y contribuye a la neurodegeneración.
¿Qué son los oligómeros Aβ y cuál es su papel?
Los oligómeros Aβ son formas solubles y pequeñas (compuestas por pocas unidades) del péptido beta-amiloide. Se considera que estas formas son particularmente tóxicas para las sinapsis y podrían ser responsables del daño sináptico temprano y los problemas de memoria, incluso antes de la formación de grandes placas.
¿El diagnóstico de Alzheimer se basa solo en estos hallazgos patológicos?
Tradicionalmente, el diagnóstico definitivo postmortem sí se basa en la cantidad y distribución de placas neuríticas y ovillos neurofibrilares. Sin embargo, en la práctica clínica, el diagnóstico se basa en criterios clínicos y se apoya en biomarcadores (en líquido cefalorraquídeo o mediante neuroimagen PET y resonancia magnética) que detectan estas patologías o sus consecuencias (atrofia cerebral). Los criterios patológicos también consideran la posible coexistencia de otras patologías.
Conclusiones sobre la Neurodegeneración
En resumen, si bien las placas seniles y los ovillos neurofibrilares son los sellos patológicos definitorios de la EA, es probable que representen solo una parte de las alteraciones que causan el declive cognitivo. La comprensión actual de la neurodegeneración en el Alzheimer se ha expandido para incluir alteraciones más tempranas, como el daño sináptico y dendrítico, las perturbaciones en la neurogénesis adulta, la disfunción de circuitos neuronales y la inervación aberrante.
La acumulación de estas lesiones patológicas comienza mucho antes del diagnóstico clínico de demencia. La pérdida sináptica, los cambios en la plasticidad, la pérdida neuronal y la presencia de formas oligoméricas solubles de Aβ y tau contribuyen progresivamente al fallo del sistema neural a lo largo de décadas.
Comprender esta historia natural de la enfermedad es fundamental. El desarrollo de nuevos biomarcadores y herramientas de imagen ha permitido detectar estas patologías en etapas muy tempranas. Esto es crucial para diseñar estrategias de prevención primaria o secundaria con el objetivo de detener la progresión de la enfermedad antes de que el daño al sistema neural se vuelva irreversible. Los hallazgos patológicos, validados por estudios longitudinales in vivo con biomarcadores modernos como la PET de amiloide y la resonancia magnética volumétrica, continúan guiando la investigación y el desarrollo de tratamientos neuroprotectores.
Si quieres conocer otros artículos parecidos a Sellos Neurologicos del Alzheimer puedes visitar la categoría Neurociencia.