La neurociencia es un campo vasto y en constante evolución que busca comprender el funcionamiento del órgano más complejo conocido: el cerebro. Durante mucho tiempo, la atención se centró en la secuencia de ADN como el determinante principal de nuestra identidad biológica y susceptibilidad a enfermedades. Sin embargo, una disciplina emergente conocida como epigenética ha revolucionado esta perspectiva, demostrando que la forma en que nuestros genes se expresan, sin alterar la secuencia de ADN subyacente, es igualmente crucial, especialmente en el contexto cerebral.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
Estos cambios epigenéticos, que literalmente significan 'por encima' o 'además' de la genética, actúan como un sistema de control que decide qué genes se activan o desactivan, cuándo y dónde. En el cerebro, esta regulación dinámica es fundamental para procesos tan diversos como el desarrollo neuronal, el aprendizaje, la memoria y nuestra respuesta al entorno. Comprender la epigenética en la neurociencia no solo nos ayuda a desentrañar los misterios de la función cerebral normal, sino que también ofrece nuevas y esperanzadoras vías para entender y tratar una amplia gama de trastornos neurológicos y psiquiátricos.

- ¿Qué es Exactamente la Epigenética?
- Los Principales Mecanismos Epigenéticos
- Epigenética en el Neurodesarrollo
- Epigenética y Trastornos Neuropsiquiátricos
- La Influencia del Ambiente: Epigenética y Plasticidad Fenotípica
- Epigenética como Biomarcador y Objetivo Terapéutico
- Preguntas Frecuentes sobre Epigenética y Neurociencia
- Conclusiones
¿Qué es Exactamente la Epigenética?
El término epigenética, aunque utilizado desde mediados del siglo XX para describir la interacción entre genes y ambiente en el desarrollo, ha cobrado una nueva relevancia con el descubrimiento de sus bases moleculares. En esencia, la epigenética se refiere a cambios en la función de los genes que pueden ser heredables (mitótica o meióticamente) y que no implican una modificación en la secuencia de nucleótidos del ADN. Es como si el ADN fuera el texto de un libro y las marcas epigenéticas fueran los acentos, subrayados o anotaciones que cambian la forma en que se lee o interpreta ese texto.
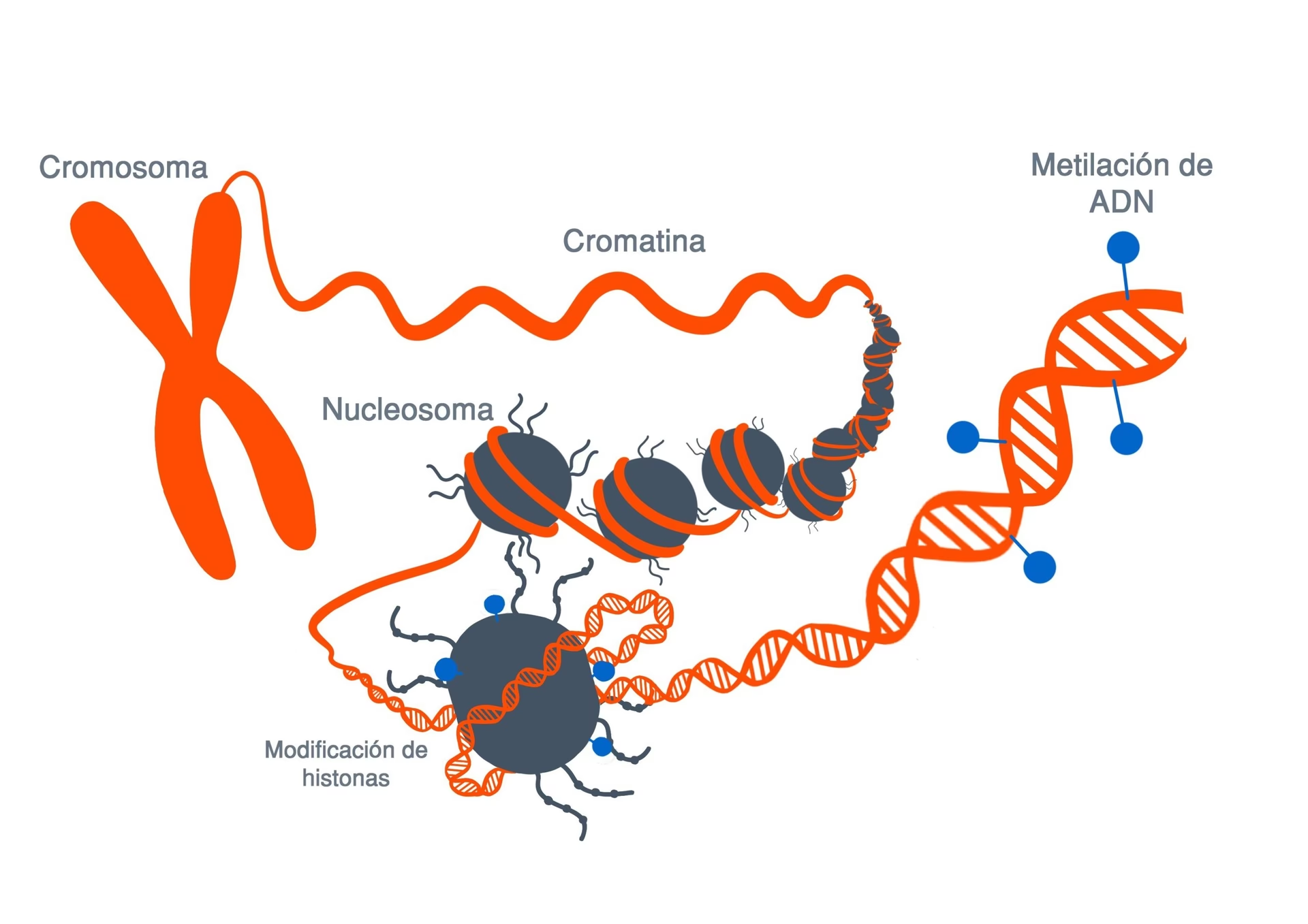
A diferencia de las mutaciones genéticas que alteran la secuencia del ADN, las modificaciones epigenéticas son adiciones químicas al ADN o a las proteínas que lo empaquetan (histonas), o bien la acción de moléculas de ARN no codificante. Estas modificaciones influyen en la estructura tridimensional de la cromatina (el complejo de ADN y proteínas) y determinan si un gen es accesible para la maquinaria de transcripción (activo) o si está empaquetado y silenciado (inactivo). Esta regulación dinámica es esencial para la diferenciación celular, permitiendo que todas las células de un organismo, a pesar de tener el mismo ADN, desempeñen funciones especializadas.
Los Principales Mecanismos Epigenéticos
La maquinaria epigenética es compleja e interactiva, involucrando varios mecanismos clave que trabajan en conjunto para regular la expresión génica. Los más estudiados y relevantes en neurociencia incluyen:
Metilación del ADN
La metilación del ADN es una de las marcas epigenéticas más estables y mejor caracterizadas. Consiste en la adición de un grupo metilo a una base de citosina, generalmente cuando va seguida de una guanina (sitios CpG). Las regiones del genoma ricas en sitios CpG, llamadas islas CpG, se encuentran a menudo en los promotores de los genes (regiones que controlan su inicio de transcripción). La metilación de estas islas CpG en los promotores suele estar asociada con la represión de la expresión génica, es decir, el silenciamiento del gen.
En el cerebro, la metilación del ADN tiene particularidades. Presenta una mayor abundancia de 5-hidroximetilcitosina (hmC) y metilación en sitios no-CpG (mCH) en comparación con otros órganos. Estas marcas tienen un papel importante en el desarrollo, el aprendizaje y la memoria. Enzimas como las ADN metiltransferasas (DNMTs) son responsables de establecer y mantener estos patrones de metilación. La metilación es crucial para procesos como la impronta genómica, donde solo se expresa el alelo heredado de uno de los padres, y su alteración puede causar trastornos del neurodesarrollo como los síndromes de Angelman y Prader-Willi. Proteínas como MeCP2 se unen al ADN metilado y regulan la expresión génica neuronal; mutaciones en MeCP2 causan el síndrome de Rett.
Modificación de Histonas
El ADN no flota libremente en el núcleo; se empaqueta alrededor de proteínas llamadas histonas para formar la cromatina. Las histonas pueden sufrir una amplia variedad de modificaciones químicas en sus colas terminales, incluyendo acetilación, metilación, fosforilación, ubiquitinación, entre otras. Estas modificaciones actúan como 'etiquetas' que pueden reclutar otras proteínas y alterar la estructura de la cromatina, haciéndola más abierta (eucromatina, generalmente activa) o más compacta (heterocromatina, generalmente silente).
La acetilación de histonas, catalizada por histona acetiltransferasas (HATs), generalmente relaja la cromatina y promueve la expresión génica. La desacetilación, mediada por histona deacetilasas (HDACs), tiende a compactar la cromatina y reprimir la expresión. La metilación de histonas es más compleja; su efecto (activador o represor) depende de la histona específica y la posición modificada. Por ejemplo, la metilación en ciertas lisinas de la histona H3 (como H3K9me3 o H3K27me3) se asocia típicamente con represión, mientras que la metilación en otras posiciones (como H3K4me3) se asocia con activación. Las enzimas que catalizan estas modificaciones (HMTs y HDMs) son actores clave en la regulación epigenética cerebral.
Remodelación de la Cromatina y RNAs No Codificantes
Además de las modificaciones químicas del ADN y las histonas, la estructura tridimensional de la cromatina puede ser activamente modificada por complejos proteicos remodeladores dependientes de ATP. Estos complejos pueden deslizar, desalojar o reestructurar los nucleosomas, alterando la accesibilidad del ADN para la maquinaria transcripcional. La alteración de estos complejos, como los del grupo BAF o NuRD, se ha asociado con trastornos del neurodesarrollo como los síndromes de Coffin-Siris o Sifrim-Hitz-Weiss.
Finalmente, diversas clases de ARN no codificantes (ncRNAs), que no se traducen en proteínas, también desempeñan roles epigenéticos importantes. Los microRNAs (miRNAs), por ejemplo, pueden regular la expresión génica post-transcripcionalmente, y algunos interactúan directamente con la maquinaria epigenética (epi-microRNAs). Otros ncRNAs, como los piRNAs o ciertos RNAs nucleares, pueden influir en la organización de la cromatina y el silenciamiento génico. Su desregulación se ha implicado en trastornos como el autismo.

Epigenética en el Neurodesarrollo
El desarrollo cerebral es un proceso extraordinariamente complejo y dinámico que abarca desde la formación del tubo neural en el embrión hasta la maduración postnatal y la plasticidad a lo largo de la vida. La epigenética juega un papel central en cada etapa de este proceso, asegurando que los genes correctos se activen en el momento y lugar adecuados para la diferenciación y función celular.
Durante la neurogénesis (formación de nuevas neuronas) y la migración neuronal, los mecanismos epigenéticos, incluyendo la remodelación de la cromatina por complejos como BAF y NuRD, son cruciales para controlar la proliferación y el movimiento de las células progenitoras neurales. La diferenciación neuronal, donde las células progenitoras se convierten en tipos neuronales o gliales específicos, está finamente regulada por patrones de metilación del ADN (por ejemplo, mediada por DNMT3A) y modificaciones de histonas.
La sinaptogénesis (formación de conexiones neuronales) y la apoptosis (muerte celular programada necesaria para refinar los circuitos) también están bajo control epigenético. Por ejemplo, la disfunción de la helicasa CHD8 se asocia con alteraciones en la sinaptogénesis y está implicada en el autismo. La estabilización y plasticidad sináptica, la base del aprendizaje y la memoria, dependen en gran medida de la desacetilación de histonas mediada por HDACs como HDAC4. La pérdida de la función de HDAC4 puede causar discapacidad intelectual.
Incluso procesos posteriores como la mielinización, la formación de la vaina aislante alrededor de los axones por oligodendrocitos, requiere la correcta función de las histona deacetilasas.
La siguiente tabla resume los principales mecanismos epigenéticos y su función general:
| Mecanismo Epigenético | Qué Modifica | Efecto General en Expresión Génica | Relevancia en Neurociencia |
|---|---|---|---|
| Metilación del ADN | Citosinas (principalmente en CpG) | Represión (si está en promotor) | Impronta genómica, desarrollo, memoria, enfermedades (Angelman, Prader-Willi, Rett, Autismo) |
| Modificación de Histonas | Colas de histonas (acetilación, metilación, fosforilación, etc.) | Depende de la modificación y posición (activación o represión) | Regulación transcripcional, plasticidad sináptica, memoria, enfermedades (esquizofrenia, autismo) |
| Remodelación de Cromatina | Estructura 3D de cromatina | Altera accesibilidad del ADN (activación o represión) | Neurogénesis, migración, diferenciación, sinaptogénesis, enfermedades (Coffin-Siris, Sifrim-Hitz-Weiss, Autismo) |
| RNAs No Codificantes | ARN (ej. miRNAs) | Regulación post-transcripcional o interacción con maquinaria epigenética | Regulación fina de expresión génica, plasticidad, enfermedades (Autismo) |
Epigenética y Trastornos Neuropsiquiátricos
La disfunción de los mecanismos epigenéticos no solo afecta el desarrollo cerebral normal, sino que también está fuertemente implicada en la etiología de una amplia gama de trastornos neurológicos y psiquiátricos. Las alteraciones pueden ser causadas por mutaciones en genes que codifican reguladores epigenéticos o por cambios aberrantes en las marcas epigenéticas inducidas por factores ambientales.
En trastornos como el autismo y la esquizofrenia, se han identificado mutaciones en genes que codifican proteínas implicadas en la metilación de histonas (ej. KMT2A, KMT2C, EHMT1, EZH2) o en la remodelación de la cromatina (ej. CHD8, ARID1B). El síndrome X frágil, una causa común de discapacidad intelectual hereditaria, se debe al silenciamiento epigenético (metilación) del gen FMR1.
La adicción es otro campo donde la epigenética ha revelado nuevos mecanismos. El consumo de drogas como la cocaína induce cambios duraderos en la expresión génica en regiones cerebrales clave del circuito de recompensa, mediados por modificaciones de histonas (acetilación) y metilación del ADN. Estos cambios epigenéticos contribuyen a la persistencia de la adicción al alterar la plasticidad sináptica y la respuesta a la droga.
Trastornos relacionados con el estrés, como el Trastorno de Estrés Postraumático (TEPT) y la depresión mayor, también muestran correlaciones epigenéticas. Se han encontrado patrones específicos de metilación del ADN en la sangre de pacientes con TEPT, especialmente en aquellos con antecedentes de abuso infantil. En gemelos monocigóticos discordantes para depresión, se han identificado regiones diferencialmente metiladas en el ADN. Esto sugiere que las experiencias de vida pueden dejar marcas epigenéticas que aumentan la vulnerabilidad a estos trastornos.
En enfermedades neurodegenerativas como el Alzheimer, la disfunción epigenética, particularmente alteraciones en la acetilación de histonas mediada por HDACs, parece contribuir a la pérdida de memoria y la neurotoxicidad. La restauración de la acetilación de histonas mediante inhibidores de HDAC ha mostrado resultados prometedores en modelos animales para mejorar la función cognitiva.

La Influencia del Ambiente: Epigenética y Plasticidad Fenotípica
Uno de los aspectos más fascinantes de la epigenética es cómo actúa como interfaz entre el genoma y el ambiente. Las experiencias de vida, especialmente durante períodos críticos del desarrollo cerebral, pueden inducir cambios epigenéticos duraderos que influyen en el fenotipo y la salud a largo plazo. Este concepto es fundamental para la plasticidad fenotípica, la capacidad de un organismo de generar diferentes fenotipos a partir de un mismo genotipo en respuesta a variaciones ambientales.
Factores ambientales como la nutrición materna durante el embarazo, el nivel de estrés prenatal o postnatal temprano, la exposición a toxinas ambientales (metales pesados, pesticidas), e incluso el tipo de cuidado parental recibido en la infancia, pueden dejar 'marcas' epigenéticas en el cerebro en desarrollo. Un estudio clásico en ratones demostró que el nivel de cuidado materno (lamer y acicalar) en las crías alteraba la metilación del ADN en el gen del receptor de glucocorticoides en el hipocampo, influyendo en la respuesta al estrés en la vida adulta. Estos cambios podían ser revertidos farmacológicamente.
Las exposiciones ambientales adversas durante períodos vulnerables pueden programar el cerebro para una mayor susceptibilidad a trastornos neuropsiquiátricos en la vida adulta. Esto se conoce como los 'orígenes tempranos de la salud y la enfermedad' (DOHaD). Sin embargo, no todos los cambios inducidos por el ambiente son necesariamente perjudiciales; algunos pueden ser adaptativos en el contexto original, aunque desadaptativos si el ambiente cambia posteriormente.
Un concepto aún más sorprendente es la herencia epigenética transgeneracional, donde las marcas epigenéticas inducidas por el ambiente en un individuo pueden transmitirse a las generaciones futuras a través de las células germinales (óvulos o espermatozoides), incluso si esas generaciones no están directamente expuestas al estímulo original. Aunque más estudiado en modelos animales, hay evidencia creciente que sugiere que esto también puede ocurrir en humanos, con implicaciones profundas para la salud pública y la comprensión de la evolución.
Epigenética como Biomarcador y Objetivo Terapéutico
El estudio de la epigenética en neurociencia no es solo una herramienta para entender los mecanismos de la enfermedad; también abre nuevas posibilidades para el diagnóstico y el tratamiento.
Las marcas epigenéticas, como los patrones de metilación del ADN, pueden servir como biomarcadores para identificar individuos en riesgo o para diagnosticar trastornos. La posibilidad de detectar estas marcas en tejidos accesibles como la sangre periférica o la saliva es particularmente prometedora, ya que podría permitir diagnósticos menos invasivos y un monitoreo más preciso de la progresión de la enfermedad o la respuesta al tratamiento. Por ejemplo, se están explorando patrones de metilación específicos en sangre como posibles indicadores de TEPT o depresión.
Además, dado que los cambios epigenéticos son potencialmente reversibles, las enzimas que catalizan estas modificaciones (DNMTs, HATs, HDACs, HMTs, HDMs, etc.) se convierten en objetivos terapéuticos atractivos. En oncología, ya hay inhibidores de HDAC aprobados para su uso clínico. Aunque el desarrollo de fármacos epigenéticos específicos para el cerebro ha sido más lento debido a la barrera hematoencefálica y la necesidad de una alta especificidad tisular y temporal, hay avances significativos.
Inhibidores de HDAC, como el ácido valproico, ya se utilizan para tratar la epilepsia y el trastorno bipolar, aunque tienen múltiples objetivos y efectos secundarios. La investigación más reciente se centra en inhibidores más selectivos. Por ejemplo, se ha demostrado que la inhibición selectiva de HDAC2 o HDAC3 mejora la memoria a largo plazo en modelos animales, lo que sugiere su potencial para tratar déficits cognitivos en enfermedades como el Alzheimer.
La promesa de las terapias epigenéticas en neurociencia radica en la posibilidad de 'reprogramar' la expresión génica aberrante que subyace a muchos trastornos, ofreciendo un enfoque complementario o alternativo a las terapias existentes que a menudo se centran en la función de proteínas individuales o neurotransmisores.
Preguntas Frecuentes sobre Epigenética y Neurociencia
Aquí respondemos algunas preguntas comunes sobre este fascinante campo:
¿La epigenética cambia mi ADN?
No, la epigenética no altera la secuencia de nucleótidos (A, T, C, G) de tu ADN. Lo que cambia es cómo se 'lee' o interpreta esa secuencia, es decir, qué genes se activan o desactivan.
¿Son heredables los cambios epigenéticos?
Algunos cambios epigenéticos pueden ser heredados de una célula a sus células hijas durante la división (herencia mitótica), lo cual es crucial para mantener la identidad celular. Un subconjunto de estos cambios puede ser heredado de padres a hijos a través de las células germinales (herencia meiótica o transgeneracional), aunque este fenómeno es más complejo y su extensión en humanos aún se investiga activamente.
¿Cómo influye el ambiente en la epigenética cerebral?
Factores ambientales como la dieta, el estrés, las toxinas, la exposición a drogas o las interacciones sociales pueden desencadenar cascadas de señalización dentro de las células cerebrales que, en última instancia, reclutan enzimas y complejos que modifican las marcas epigenéticas en genes específicos. Esto altera la expresión de esos genes y, por ende, la función neuronal.
¿Se pueden revertir los cambios epigenéticos?
Sí, a diferencia de las mutaciones genéticas, las marcas epigenéticas son dinámicas y pueden ser añadidas o eliminadas. Esto es la base de la esperanza para las terapias epigenéticas, que buscan corregir patrones de expresión génica aberrantes.
¿La epigenética explica por qué los gemelos idénticos pueden tener diferencias?
Exactamente. Los gemelos monocigóticos comparten la misma secuencia de ADN, pero a medida que crecen y se exponen a diferentes ambientes y experiencias, acumulan diferencias en sus patrones epigenéticos. Estas diferencias pueden contribuir a las variaciones en sus rasgos, su susceptibilidad a enfermedades e incluso sus patrones de comportamiento.
¿Puede la dieta afectar la epigenética de mi cerebro?
Sí. La dieta puede proporcionar o carecer de nutrientes esenciales (como donadores de grupos metilo como el folato) que son necesarios para las enzimas que establecen las marcas epigenéticas (como la metilación del ADN). La nutrición, especialmente en etapas tempranas de la vida, puede tener un impacto profundo y duradero en el epigenoma cerebral y la función cognitiva.
Conclusiones
La epigenética ha emergido como un pilar fundamental en la neurociencia moderna, revelando la intrincada danza entre nuestros genes y el entorno en la determinación de la salud y la enfermedad cerebral. Lejos de ser meros espectadores de un destino genético preescrito, nuestros cerebros son órganos dinámicos cuya función y estructura son moldeadas continuamente por las experiencias de vida a través de mecanismos epigenéticos. Comprender estos mecanismos no solo profundiza nuestra apreciación de la complejidad cerebral, sino que también abre nuevas y emocionantes avenidas para el desarrollo de biomarcadores diagnósticos y terapias innovadoras dirigidas a restablecer el equilibrio epigenético en trastornos tan devastadores como la adicción, la depresión, el TEPT, el autismo y las enfermedades neurodegenerativas. A medida que la investigación avanza, el campo de la epigenética en neurociencia promete seguir siendo una fuente de descubrimientos transformadores.
Si quieres conocer otros artículos parecidos a Epigenética y el Cerebro: Más Allá del ADN puedes visitar la categoría Neurociencia.