Comprender las funciones de genes específicos en órganos complejos como el cerebro, compuesto por innumerables tipos celulares y circuitos intrincados, presenta un desafío formidable para la investigación biomédica. La inactivación total de un gen (conocida como knockout total) a menudo resulta en letalidad embrionaria, impidiendo el estudio de su papel en etapas posteriores del desarrollo o en el organismo adulto. Aquí es donde las herramientas genéticas de precisión se vuelven indispensables, y el sistema Cre-LoxP ha revolucionado nuestra capacidad para manipular el genoma de manera controlada, particularmente en modelos animales como el ratón.
- ¿Qué es el Sistema Cre-LoxP?
- El Mecanismo de Acción de Cre
- Aplicaciones en la Investigación en Neurociencia
- Desafíos y Consideraciones
- El Impacto en la Neurociencia
- Preguntas Frecuentes sobre Cre-LoxP en Neurociencia
- ¿Qué significa que un gen esté "floxed"?
- ¿Por qué usar un knockout condicional en lugar de un knockout total?
- ¿La Cre recombinasa solo actúa en los sitios loxP que yo introduzco?
- ¿Cómo puedo controlar cuándo se activa la Cre recombinasa?
- ¿El marcaje de linaje con Cre-LoxP es permanente?
- ¿Se puede usar Cre-LoxP para activar la expresión de un gen en lugar de inactivarla?
¿Qué es el Sistema Cre-LoxP?
El sistema Cre-LoxP es una tecnología de recombinación sitio-específica que permite a los investigadores modificar el ADN en ubicaciones genómicas predefinidas. En esencia, consta de dos componentes clave: la enzima Cre recombinasa y las secuencias de ADN específicas llamadas sitios loxP.
La Cre recombinasa es una enzima (una proteína) derivada del bacteriófago P1. Su función principal es catalizar la recombinación del ADN entre dos secuencias loxP. Es una recombinasa sitio-específica, lo que significa que no actúa aleatoriamente en el genoma, sino que busca y se une a estas secuencias loxP específicas.
Los sitios loxP (locus of X-over P1) son secuencias de ADN cortas, de 34 pares de bases de longitud. Cada sitio loxP consiste en una secuencia central asimétrica de 8 pares de bases flanqueada por dos secuencias simétricas (palindrómicas) de 13 pares de bases. Esta estructura confiere direccionalidad al sitio loxP.
El nombre del gen que codifica la enzima Cre proviene originalmente de "Causes recombination" (Causa recombinación), aunque a veces se menciona "Cyclization recombinase". La proteína Cre tiene 343 aminoácidos y consta de dos dominios: un dominio carboxilo (C-terminal) más grande y un dominio amino (N-terminal) más pequeño. El dominio C-terminal es similar en estructura al dominio de las enzimas de la familia Integrasa y contiene el sitio catalítico de la enzima.
El Mecanismo de Acción de Cre
El funcionamiento del sistema Cre-LoxP es notablemente eficiente y preciso. Cuando la Cre recombinasa encuentra dos sitios loxP en una molécula de ADN, se une a ellos. Las proteínas Cre se unen a las regiones flanqueantes de 13 pares de bases de cada sitio loxP, formando dímeros. Luego, estos dímeros se unen para formar un tetrámero que mantiene los dos sitios loxP en estrecha proximidad y con una orientación paralela.
Una vez unida, la Cre recombinasa cataliza un evento de recombinación. Esto implica cortar ambas hebras de ADN en ambos sitios loxP y luego volver a unir las hebras de manera cruzada. Este proceso se realiza mediante un mecanismo de transesterificación directa, donde el grupo hidroxilo de un residuo de tirosina en la enzima ataca un grupo fosfato en la cadena principal del ADN, formando un enlace fosfo-tirosina. Esto conserva la energía del enlace fosfodiéster, permitiendo que la reacción sea reversible y no requiera cofactores de alta energía. Después del corte, las hebras se ligan con la ayuda de ligasas de ADN.
El resultado de la recombinación mediada por Cre depende crucialmente de la orientación relativa de los dos sitios loxP:
| Orientación de los Sitios loxP | Resultado de la Recombinación | Descripción |
|---|---|---|
| Misma Orientación (Repetición Directa) | Deleción | La secuencia de ADN flanqueada por los dos sitios loxP se elimina (excisión), dejando un único sitio loxP residual. Este es el uso más común para inactivar genes. |
| Orientación Opuesta (Invertida) | Inversión | La secuencia de ADN flanqueada por los dos sitios loxP se invierte dentro de la molécula de ADN. |
| En Cromosomas Diferentes | Translocación | Si los sitios loxP están en cromosomas diferentes, puede ocurrir un intercambio de segmentos entre ellos. |
La capacidad de eliminar o invertir secuencias de ADN de manera controlada es lo que hace que este sistema sea tan valioso para la ingeniería genética.
Aplicaciones en la Investigación en Neurociencia
La principal fortaleza del sistema Cre-LoxP en neurociencia reside en su capacidad para realizar manipulaciones genéticas de manera específica en tipos celulares particulares dentro del sistema nervioso y, a menudo, en momentos específicos del desarrollo o en el cerebro adulto. Esto supera las limitaciones de los knockouts totales, permitiendo a los investigadores estudiar la función de un gen en las células donde es relevante sin afectar otras células o causar problemas letales durante el desarrollo.
Las aplicaciones más comunes incluyen:
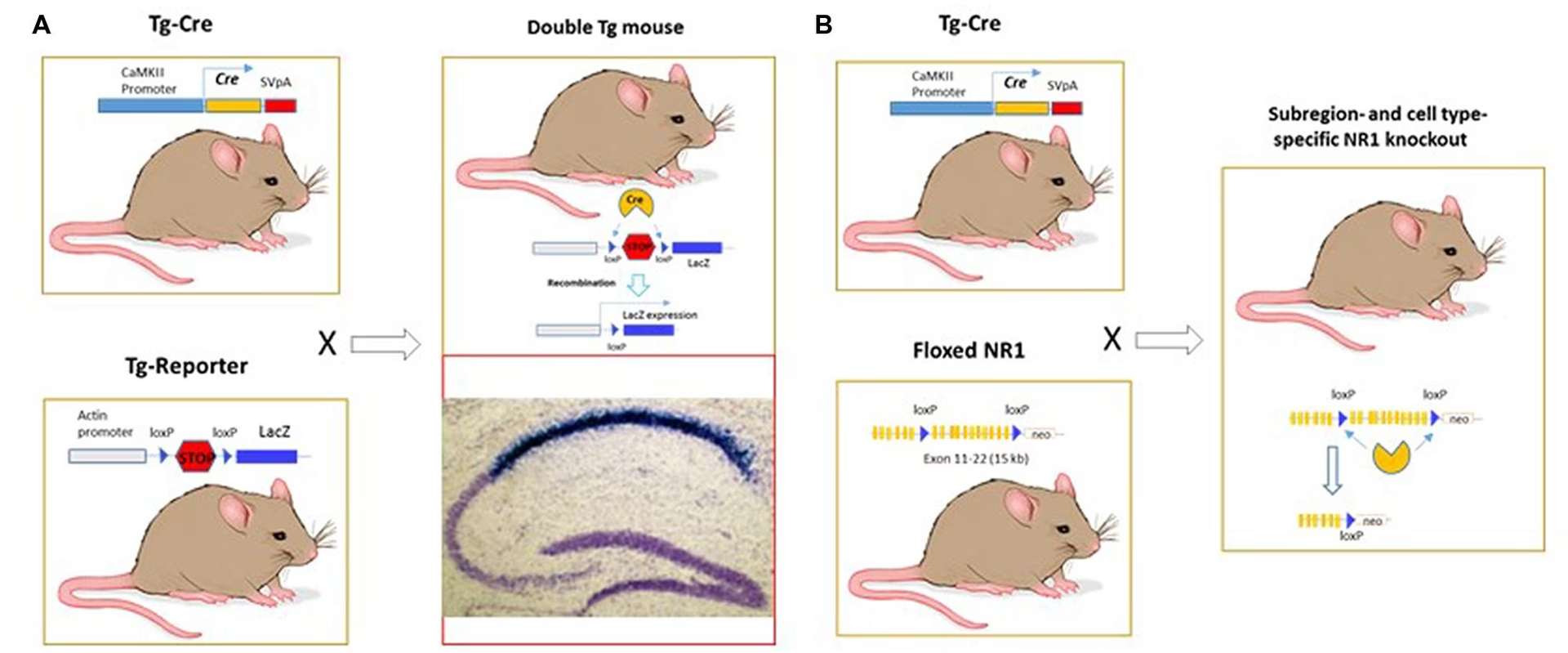
1. Knockout Condicional (Inactivación de Genes Específicos): Esta es quizás la aplicación más extendida. Se crea un ratón en el que el gen de interés está "flanqueado" por sitios loxP (un gen "floxed"). Este ratón se cruza con otro ratón que expresa la Cre recombinasa bajo el control de un promotor que solo está activo en un tipo celular específico (por ejemplo, un tipo particular de neurona) o en una región específica del cerebro. En las células donde la Cre recombinasa está presente, el gen flanqueado por loxP será eliminado, inactivando su función solo en esas células. Esto permite determinar el papel de ese gen en el funcionamiento de ese tipo celular específico o circuito neuronal.
Por ejemplo, si un gen es esencial para el desarrollo temprano del cerebro y su eliminación total causa la muerte del embrión, un knockout condicional puede permitir que el ratón se desarrolle normalmente, pero luego el gen puede ser inactivado específicamente en neuronas de la corteza cerebral adulta para estudiar su papel en el aprendizaje o la memoria.
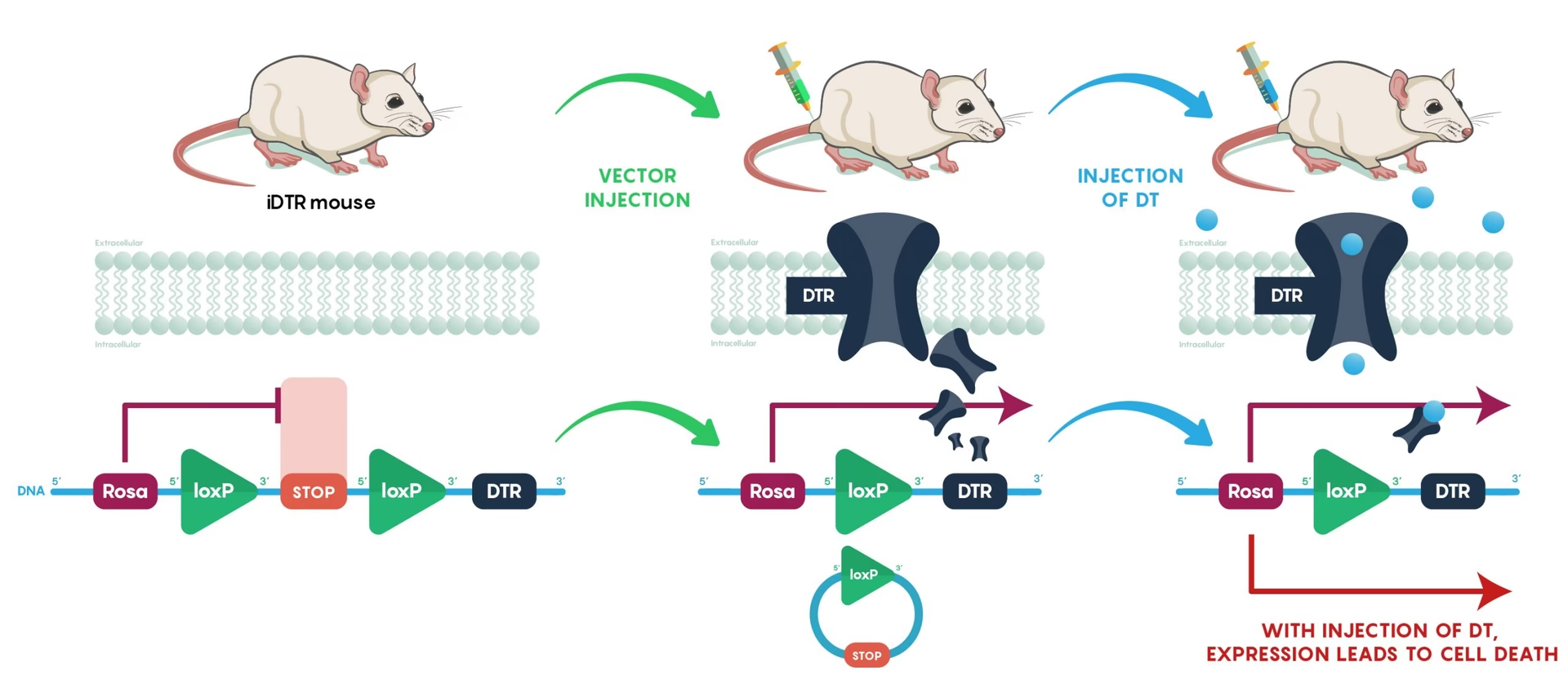
2. Marcaje de Linaje Celular (Cell Lineage Tracing): El sistema Cre-LoxP también se utiliza para marcar de forma permanente células específicas y seguir su destino (qué tipos celulares dan lugar o a dónde migran). Esto se logra utilizando un ratón que porta una secuencia de ADN que codifica una proteína reportera (como una proteína fluorescente como EGFP o mCherry), pero cuya expresión está bloqueada por un "casete de parada" flanqueado por sitios loxP. Este ratón se cruza con un ratón que expresa Cre en un tipo celular de interés en una etapa particular del desarrollo.
En las células donde Cre se expresa, el casete de parada se elimina, permitiendo la expresión de la proteína reportera. Dado que esta modificación genética es permanente, todas las células descendientes de las células marcadas inicialmente también expresarán la proteína reportera. Esto permite a los investigadores visualizar y rastrear el linaje de células específicas a lo largo del desarrollo y la vida del animal. Técnicas avanzadas como "Brainbow" utilizan múltiples variantes de sitios loxP y proteínas fluorescentes para marcar neuronas individuales con diferentes colores, permitiendo el estudio detallado de la arquitectura y conectividad neuronal.
3. Control Temporal de la Manipulación Genética: A menudo, es crucial controlar no solo *dónde* ocurre una manipulación genética, sino también *cuándo*. Para lograr esto, se han desarrollado versiones inducibles de la Cre recombinasa, como la CreER (Cre recombinasa fusionada a un dominio mutado del receptor de estrógeno). La CreER reside en el citoplasma y no puede entrar en el núcleo (donde está el ADN) a menos que se una a un ligando específico, como el tamoxifeno (un análogo del estrógeno).
Al administrar tamoxifeno al ratón, este se metaboliza a 4-hidroxitamoxifeno, que se une a la CreER, causando su translocación al núcleo. Una vez en el núcleo, la CreER activada puede catalizar la recombinación en los sitios loxP. Esto permite a los investigadores inducir la deleción de un gen o el marcaje de linaje en un momento preciso elegido por ellos, por ejemplo, en el cerebro adulto después de que el desarrollo ha concluido. La variante CreER(T2) ha sido optimizada para minimizar la actividad de Cre en ausencia de tamoxifeno (fuga) y maximizar la sensibilidad a la inducción.
Desafíos y Consideraciones
Aunque el sistema Cre-LoxP es increíblemente potente, no está exento de desafíos. Uno de los principales inconvenientes es la posibilidad de expresión de la Cre recombinasa en tejidos o tipos celulares no deseados, lo que puede llevar a fenotipos inesperados o confusos. Encontrar un promotor que sea estrictamente específico para el tipo celular de interés puede ser difícil. Además, la eficiencia de la recombinación mediada por Cre puede variar dependiendo de la ubicación genómica de los sitios loxP y del nivel de expresión de la propia Cre.
La recombinación incompleta, donde no todos los alelos flanqueados por loxP son eliminados en todas las células objetivo, también puede complicar la interpretación de los resultados. En aplicaciones de marcaje de linaje, la "fuga" de Cre (actividad de CreER sin tamoxifeno) puede resultar en un marcaje no deseado de células.
A pesar de estas limitaciones, los modelos de ratón que expresan Cre recombinasa bajo promotores específicos y los ratones que portan genes "floxed" o casetes reporteros han sido herramientas invaluables.
El Impacto en la Neurociencia
El advenimiento del sistema Cre-LoxP ha transformado la neurociencia moderna. Ha permitido a los investigadores ir más allá del estudio de genes individuales y comenzar a desentrañar cómo funcionan los circuitos neuronales y cómo contribuyen a funciones complejas como el comportamiento, el aprendizaje, la memoria y la respuesta a estímulos. Al inactivar genes o marcar células en poblaciones neuronales específicas, los científicos pueden identificar el papel de esas células o genes en enfermedades neurológicas como el Alzheimer, el Parkinson, la epilepsia o los trastornos del desarrollo.
La iniciativa NIH Blueprint for Neuroscience Research Cre-driver mouse projects es un testimonio de la importancia de esta tecnología, habiendo generado cientos de líneas de ratones Cre-driver que están disponibles para la comunidad científica mundial, facilitando el estudio de la función génica en diversos tipos de células neuronales.
En resumen, el sistema Cre-LoxP, con su capacidad para manipular el ADN de manera sitio-específica, celular-específica y temporalmente controlada, es una herramienta fundamental que continúa impulsando descubrimientos en neurociencia, permitiéndonos comprender la complejidad del cerebro a un nivel de detalle sin precedentes.

Preguntas Frecuentes sobre Cre-LoxP en Neurociencia
¿Qué significa que un gen esté "floxed"?
Un gen "floxed" (del inglés "flanked by loxP") es un gen que ha sido modificado genéticamente para estar flanqueado en ambos extremos por secuencias de ADN llamadas sitios loxP. Esto prepara el gen para ser reconocido y eliminado por la Cre recombinasa.
¿Por qué usar un knockout condicional en lugar de un knockout total?
Un knockout total elimina un gen en todas las células del organismo desde el principio del desarrollo. Esto a menudo es útil para entender la función general del gen, pero si el gen es esencial para el desarrollo embrionario o para funciones básicas de supervivencia, el knockout total puede ser letal. Un knockout condicional permite que el gen sea eliminado solo en tipos celulares específicos o en momentos específicos de la vida del organismo (usando Cre inducible), evitando la letalidad temprana y permitiendo el estudio de la función del gen en el contexto de un organismo vivo en etapas posteriores o en tejidos particulares.
¿La Cre recombinasa solo actúa en los sitios loxP que yo introduzco?
La Cre recombinasa tiene una alta especificidad por los sitios loxP. Sin embargo, en algunos casos, puede reconocer secuencias que se asemejan a los sitios loxP en el genoma del huésped (sitios crípticos), lo que puede llevar a recombinaciones no deseadas o "fuera de objetivo". Aunque raro, es una consideración importante al diseñar experimentos y analizar resultados.
¿Cómo puedo controlar cuándo se activa la Cre recombinasa?
Para controlar el momento de la activación de Cre, se utilizan versiones inducibles de la enzima, como la CreER. Esta enzima está fusionada a un dominio que responde a un ligando externo, como el tamoxifeno. La enzima solo se vuelve activa y puede entrar en el núcleo cuando se administra el ligando, permitiendo al investigador decidir el momento preciso de la manipulación genética.
¿El marcaje de linaje con Cre-LoxP es permanente?
Sí, la eliminación del casete de parada flanqueado por loxP que activa la expresión de la proteína reportera es un evento de recombinación permanente en el ADN. Una vez que ocurre en una célula, esa célula y todas sus células descendientes (progenie) continuarán expresando la proteína reportera, incluso si la Cre recombinasa ya no está presente.
¿Se puede usar Cre-LoxP para activar la expresión de un gen en lugar de inactivarla?
Sí. Además de la inactivación (deleción) de genes y el marcaje de linaje (activación de reporteros), el sistema Cre-LoxP puede ser diseñado para activar la expresión de un gen de interés. Esto se puede lograr colocando el gen de interés después de un casete de parada flanqueado por loxP. Cuando Cre está presente, el casete de parada se elimina, permitiendo la expresión del gen de interés solo en esas células. También puede usarse para intercambiar secuencias de ADN (recombinase-mediated cassette exchange) usando variantes de sitios loxP.
Si quieres conocer otros artículos parecidos a Cre-LoxP en Neurociencia: Una Herramienta Clave puedes visitar la categoría Neurociencia.
