El cerebro humano es la estructura más compleja que conocemos, una red intrincada de miles de millones de neuronas interconectadas que orquestan desde nuestros pensamientos más profundos hasta las funciones corporales más básicas. Comprender cómo se forma, cómo procesa la información y cómo cambia a lo largo de la vida es el objetivo central de la neurociencia. En este viaje exploratorio, desvelaremos algunos de sus secretos mejor guardados, desde el preciso momento en que una neurona 'nace' y encuentra su lugar, pasando por la intrigante idea de si existe una célula dedicada a recordar a una persona específica, hasta la sorprendente capacidad de nuestro cerebro para generar nuevas células incluso en la vejez.
Estas preguntas no son meras curiosidades filosóficas, sino áreas activas de investigación que emplean técnicas sofisticadas para mapear, rastrear y comprender el funcionamiento neuronal. Acompáñanos a explorar el 'nacimiento neuronal', el controvertido concepto de la 'célula de la abuela' y la asombrosa realidad de la neurogénesis adulta.
El Nacimiento Neuronal: Un Momento Clave en el Desarrollo Cerebral
El desarrollo del cerebro, particularmente la formación de la corteza cerebral, es un proceso extraordinariamente orquestado. La corteza cerebral, la capa externa y plegada responsable de funciones cognitivas superiores, tiene una estructura de múltiples capas distintiva. Esta organización no es aleatoria; se establece mediante un gradiente 'de dentro hacia fuera'. Las neuronas que nacen primero migran a las capas más internas de la corteza en desarrollo, mientras que las neuronas que nacen más tarde se desplazan a las capas más superficiales.
Pero, ¿qué significa exactamente el 'nacimiento neuronal'? En el contexto del desarrollo embrionario, particularmente en la zona ventricular (ZV), existen células progenitoras multipotentes. Estas células se dividen. Un evento de división celular de una célula progenitora que da lugar a una célula hija comprometida con un destino neuronal se conoce como el nacimiento neuronal de esa célula hija. Una vez que la neurona está 'nacida' y comprometida, generalmente abandona el ciclo celular y comienza su migración hacia la placa cortical (PC) para ocupar su posición final en la corteza cerebral en desarrollo.
Las células progenitoras parecen adquirir propiedades específicas de capa en el momento de este nacimiento neuronal, lo que influye en el lugar al que migrará la neurona hija. Sin embargo, los mecanismos moleculares precisos por los cuales las células progenitoras adquieren estos destinos de capa aún no están completamente claros. La dificultad radica en identificar cohortes de células progenitoras que comparten una fecha de nacimiento neuronal específica para estudiarlas aisladamente.
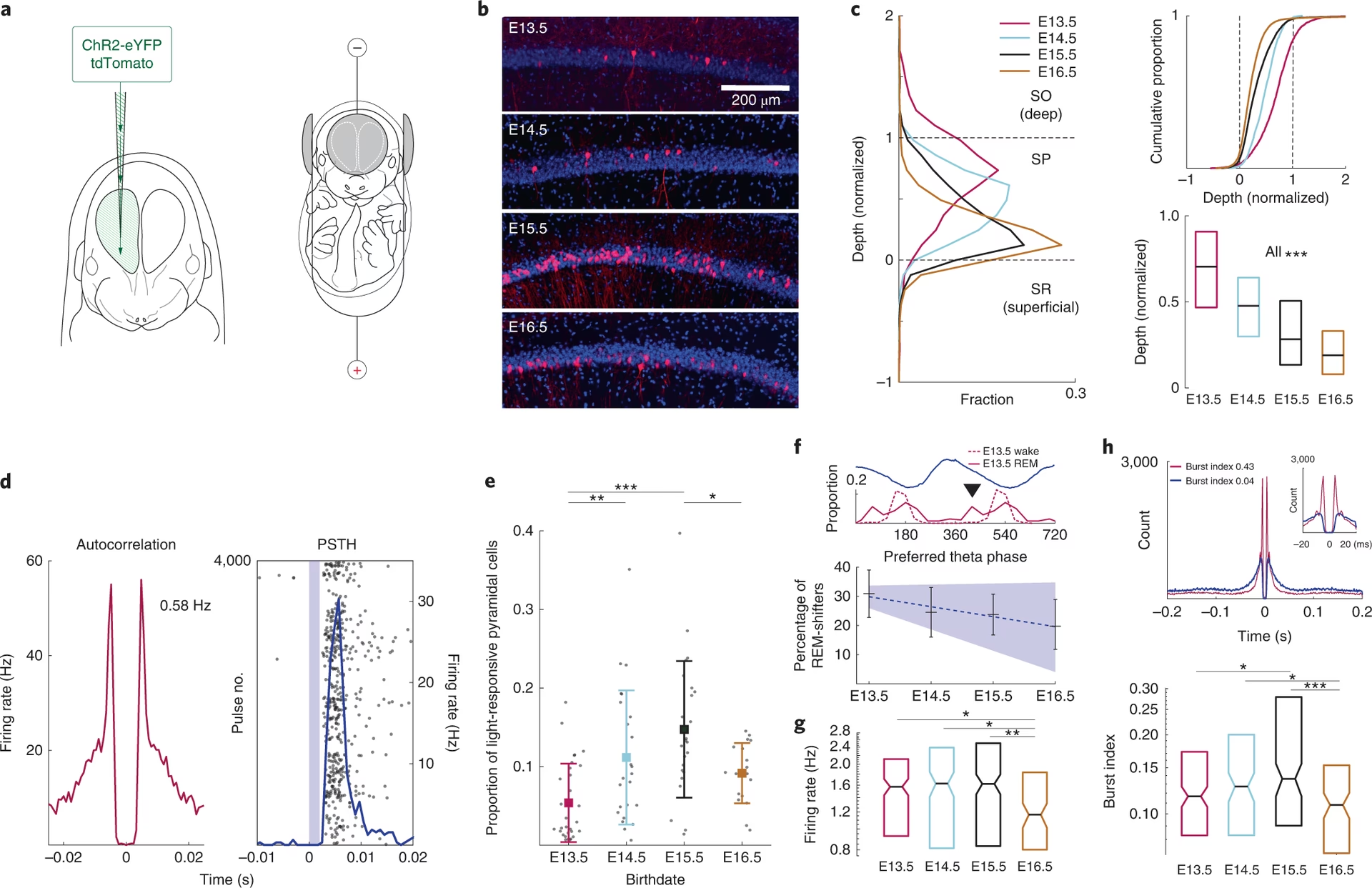
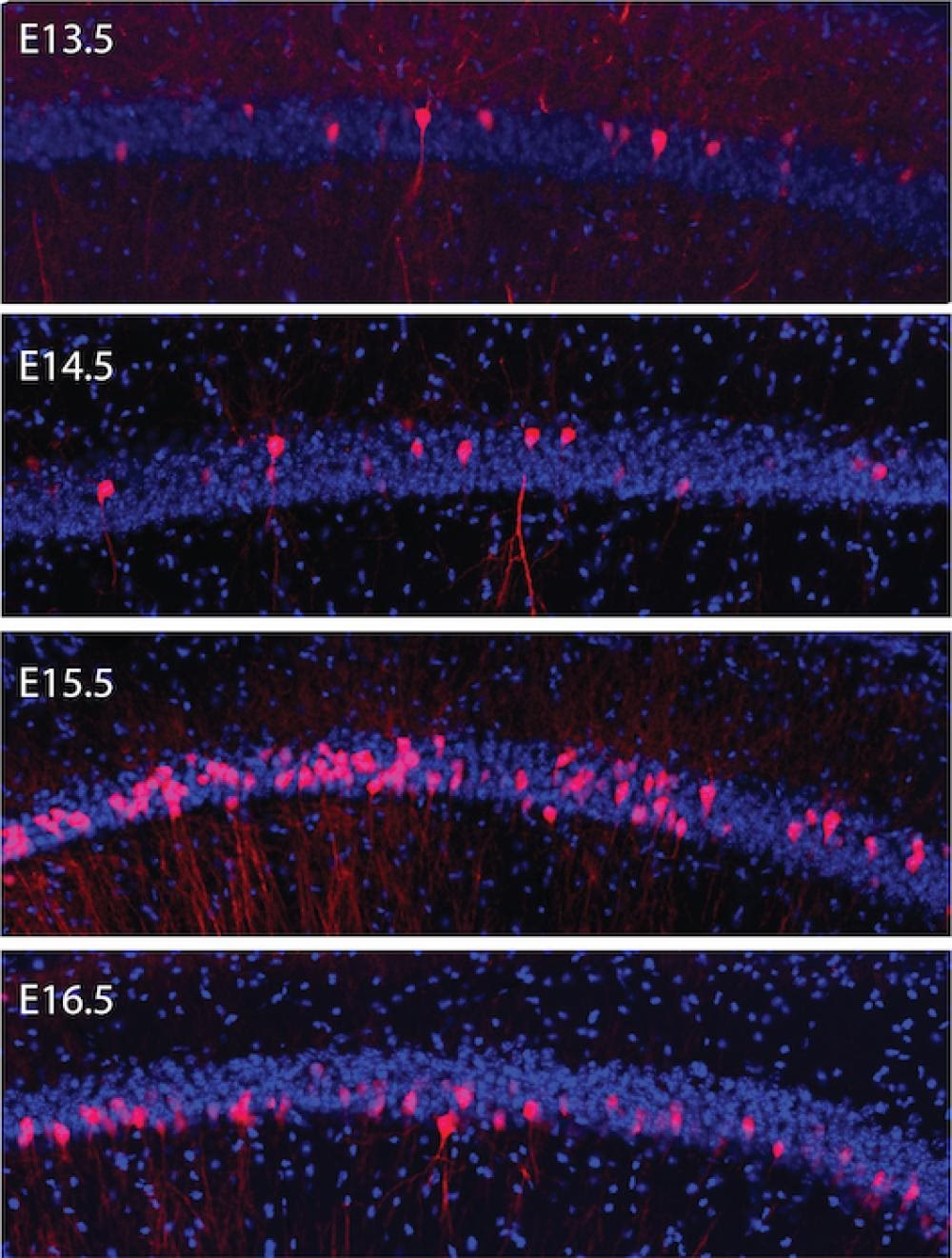
Para abordar este desafío, los investigadores han desarrollado técnicas ingeniosas. Una de ellas, descrita en la información proporcionada, utiliza vectores adenovirales defectuosos en replicación para realizar una 'transferencia génica pulsada' en las células progenitoras de una manera específica a la fecha de nacimiento neuronal. Al inyectar estos vectores (que contienen un gen marcador) en el ventrículo del mesencéfalo de embriones de ratón en diferentes momentos (por ejemplo, entre el día embrionario 10.5 y 14.5), los investigadores pueden etiquetar cohortes específicas de células progenitoras que estaban en división en ese momento preciso.
Lo notable de esta técnica es que los vectores adenovirales introducen el gen en un subconjunto de células progenitoras que comparten la misma fecha de nacimiento neuronal. Estas células progenitoras etiquetadas se diferencian normalmente en neuronas corticales y forman las capas corticales canónicas de manera 'de dentro hacia fuera', tal como lo hacen las neuronas no infectadas. Esta capacidad permite a los científicos distinguir y estudiar poblaciones de células progenitoras relacionadas con fechas de nacimiento específicas e incluso introducir genes para manipular o rastrear estas poblaciones.
Estudios más avanzados, como el realizado utilizando ratones transgénicos Z/AP junto con vectores adenovirales que expresan la enzima Cre recombinasa, han permitido rastrear el linaje de las células progenitoras infectadas. En estos ratones Z/AP, la expresión de un gen marcador (LacZ) puede ser cambiada por otro (hAP) en presencia de Cre. Al inyectar el vector Cre en un momento específico (por ejemplo, E11.5), se etiquetan las células progenitoras activas en ese momento. Los resultados de estos experimentos sugieren que las células progenitoras infectadas con vectores adenovirales pueden generar progresivamente descendencia que abarca muchas capas corticales, lo que indica que la infección viral no parece afectar su multipotencia inicial.
Sin embargo, la distribución final de las células marcadas en la corteza adulta depende del momento de la inyección, lo que refuerza la idea de que las propiedades intrínsecas de las células progenitoras cambian con el tiempo. Estos cambios intrínsecos parecen regular su compromiso con fenotipos laminares específicos, aunque los mecanismos moleculares exactos que median la generación secuencial de diversos fenotipos laminares a partir de una población de células progenitoras multipotentes aún no están completamente dilucidados.
La técnica de transferencia génica mediada por adenovirus abre la puerta a examinar las propiedades moleculares de subconjuntos de células progenitoras que comparten la misma fecha de nacimiento neuronal. Esto es crucial para comprender los mecanismos de la neurogénesis cortical y cómo se forman las estructuras laminares del cerebro.
La Célula de la Abuela: ¿Una Neurona Para Cada Concepto?
Dentro del vasto campo de la neurociencia cognitiva, una de las ideas más intrigantes y debatidas es la de la 'célula de la abuela'. Este concepto surge en el contexto de las teorías localistas de codificación neuronal, que postulan que una sola neurona, o un pequeño grupo de neuronas, podría representar un objeto, persona o concepto específico y complejo.
La definición estricta de una célula de la abuela es una neurona que representa un concepto específico y complejo (no meramente una percepción simple) de una manera multimodal e invariante. Esto significa que la neurona respondería a ese concepto particular sin importar cómo se presente el estímulo: visualmente (una foto), textualmente (el nombre escrito) o auditivamente (el nombre hablado). La idea central es codificar un concepto complejo en una sola célula de forma invariante.
El término fue introducido por Jerry Lettvin en 1969, aunque el concepto ya había sido predicho por Jerzy Konorski en 1967, quien las llamó neuronas 'gnósticas'. Konorski las describió como neuronas individuales que responden a estímulos complejos como caras, manos, objetos, etc.
La noción de la célula de la abuela es altamente controvertida. Mientras que algunos neurocientíficos, como Barlow y Bowers, han argumentado a favor de su existencia y la consideran una característica plausible de la codificación cerebral para objetos y conceptos, otros, como Plaut y McClelland o Quian Quiroga y colaboradores, han expresado un fuerte escepticismo o propuesto modelos de codificación más distribuidos.
Sin embargo, en los últimos años, la evidencia neurofisiológica ha aportado nuevos datos a este debate. Estudios, particularmente en el lóbulo temporal medial (LTM) de humanos (incluyendo el hipocampo y la corteza entorrinal), han encontrado neuronas con propiedades sorprendentemente cercanas a las de las células de la abuela. En estos experimentos, se presentan a los sujetos diversos estímulos (imágenes, texto, sonidos) mientras se registra la actividad de neuronas individuales.
Los hallazgos clave incluyen:
- Neuronas en el LTM que disparan selectivamente a múltiples imágenes de una persona específica (como Oprah Winfrey o Saddam Hussein).
- La misma neurona responde no solo a las imágenes, sino también al nombre escrito y hablado de esa persona. Esto demuestra la invariancia multimodal y la representación de un concepto abstracto ('Oprah Winfrey') independientemente de la modalidad sensorial.
- Casos aún más llamativos, como una neurona que responde a la actriz Halle Berry incluso cuando está enmascarada como Catwoman, lo que sugiere una representación que va más allá de la apariencia visual y se acerca a la abstracción del concepto.
- Respuestas similares se han observado para objetos icónicos, como la Ópera de Sídney, donde una neurona responde a imágenes desde diferentes ángulos, en color o blanco y negro, e incluso a las palabras 'Sydney Opera'.
Estos estudios sugieren que algunas neuronas del LTM codifican una representación abstracta del concepto desencadenado por el estímulo. Se estima que hasta el 40% de las células del LTM podrían estar sintonizadas a este tipo de representación explícita.
Aunque el debate continúa y es posible que la representación de conceptos complejos implique tanto células altamente selectivas como redes distribuidas, la evidencia de neuronas en el LTM con propiedades de invariancia multimodal y selectividad para conceptos específicos proporciona un soporte empírico significativo a la noción de la célula de la abuela, al menos como un tipo especial de célula localista.
Neurogénesis Adulta: ¿Seguimos Creando Neuronas Toda la Vida?
Durante mucho tiempo, el dogma central en neurociencia sostenía que nacíamos con un número fijo de neuronas y que, una vez alcanzada la madurez, la producción de nuevas células cerebrales cesaba. Sin embargo, en las últimas décadas, esta visión ha sido desafiada y, finalmente, refutada por una creciente evidencia.
Hoy sabemos que el cerebro adulto, al menos en ciertas regiones, tiene la capacidad de generar nuevas neuronas a través de un proceso llamado neurogénesis adulta. La región más estudiada y donde la neurogénesis adulta es más prominente en mamíferos, incluidos los humanos, es el hipocampo, una estructura cerebral fundamental para la memoria y las emociones.
Investigaciones recientes, como un estudio publicado en Nature Medicine que analizó cerebros de personas fallecidas de entre 43 y 97 años, han proporcionado pruebas convincentes de que la neurogénesis ocurre a lo largo de toda la vida humana, incluso en edades avanzadas (hasta los 97 años en ese estudio). Los investigadores fueron capaces de identificar neuronas inmaduras, las recién llegadas al circuito, en el hipocampo de estos cerebros.
Los hallazgos de este estudio revelaron:
| Característica | Cerebro Sano (43-97 años) | Cerebro con Alzheimer Temprano |
|---|---|---|
| Neurogénesis (producción de nuevas neuronas) | Presente, con ligera disminución con la edad. | Reducción drástica (aprox. 30%) en las primeras etapas. |
| Número de neuronas nuevas (aprox.) | Hasta 30,000 por milímetro cúbico en edades más jóvenes. | Cae a 20,000 por milímetro cúbico en etapas tempranas. |
| Implicación | Soporta el aprendizaje continuo a lo largo de la vida. | Podría ser un indicador temprano de la enfermedad o un factor contribuyente. |
Este descubrimiento es revolucionario porque confirma que nuestro cerebro no es una estructura estática una vez que llegamos a adultos. La capacidad de generar nuevas neuronas en el hipocampo sugiere que esta neurogénesis adulta podría desempeñar un papel vital en funciones cognitivas como el aprendizaje y la formación de nuevas memorias, procesos que continúan a lo largo de nuestra existencia.
La Dra. Maria Llorens-Martin, una de las investigadoras principales de este estudio, sugiere que seguimos generando nuevas neuronas mientras necesitemos aprender cosas nuevas, lo cual ocurre constantemente en nuestras vidas.
Además de confirmar la neurogénesis en la vejez, el estudio arrojó luz sobre su relación con enfermedades neurodegenerativas como el Alzheimer. La observación de una reducción significativa en la producción de nuevas neuronas en las primeras etapas de la enfermedad de Alzheimer, incluso antes de la acumulación masiva de placas de beta-amiloide (una característica distintiva del Alzheimer) y probablemente antes de la aparición de síntomas clínicos evidentes, es particularmente importante.
Este hallazgo sugiere que la disminución de la neurogénesis podría ser uno de los eventos más tempranos en la patología del Alzheimer. Comprender por qué ocurre esta disminución podría abrir nuevas vías para el desarrollo de tratamientos, enfocándose no solo en eliminar las placas de beta-amiloide, sino también en preservar o estimular la producción de nuevas neuronas.
La investigación sobre neurogénesis adulta es un campo dinámico que sigue explorando sus funciones exactas, cómo se regula y cómo se ve afectada por el envejecimiento, el estilo de vida (ejercicio, dieta) y las enfermedades. La confirmación de que podemos seguir produciendo nuevas células cerebrales incluso en la novena década de vida subraya la plasticidad y la capacidad de adaptación del cerebro a lo largo de todo el ciclo vital.
Preguntas Frecuentes sobre el Cerebro
A continuación, abordamos algunas preguntas comunes que surgen al explorar estos fascinantes temas:
¿Qué determina la posición de una neurona en la corteza cerebral?
La posición final de una neurona en las capas de la corteza cerebral está fuertemente influenciada por su fecha de nacimiento neuronal. Las neuronas que nacen primero migran a las capas internas, mientras que las nacidas más tarde se dirigen a las capas más externas, estableciendo el patrón 'de dentro hacia fuera'.
¿Son las células progenitoras completamente predeterminadas para una sola capa desde el principio?
La evidencia sugiere que las células progenitoras tempranas son multipotentes y pueden dar lugar a descendencia que abarca múltiples capas. Sin embargo, a medida que avanza el desarrollo y las células progenitoras continúan dividiéndose, sus propiedades intrínsecas cambian, lo que las compromete progresivamente a generar neuronas destinadas a capas específicas en función de la fecha de nacimiento.
Si existe una 'célula de la abuela', ¿significa que perdemos un recuerdo si esa célula muere?
Este es uno de los argumentos en contra de una codificación puramente localista. Es probable que la representación de conceptos complejos implique tanto células altamente selectivas como una red neuronal más distribuida. Si bien una célula individual puede ser muy selectiva, la robustez de la memoria y el conocimiento probablemente dependa de la actividad coordinada de conjuntos de neuronas.
¿La neurogénesis adulta ocurre en todo el cerebro?
Aunque la neurogénesis adulta ha sido confirmada de manera robusta en el hipocampo y otras regiones como la zona subventricular, su extensión a otras áreas del cerebro adulto humano sigue siendo un tema de investigación activa y debate.
¿Podría estimular la neurogénesis ayudar a tratar el Alzheimer?
La drástica reducción de la neurogénesis en las primeras etapas del Alzheimer sugiere que la promoción de la generación de nuevas neuronas podría ser una estrategia terapéutica potencial. Sin embargo, esto requiere más investigación para entender cómo estimular la neurogénesis de manera segura y efectiva, y si estas nuevas neuronas pueden integrarse funcionalmente para mitigar los efectos de la enfermedad.
Explorar el nacimiento de las neuronas, cómo codifican la información y su capacidad de renovación a lo largo de la vida nos recuerda la asombrosa plasticidad y complejidad del cerebro. Cada descubrimiento nos acerca un paso más a desentrañar los misterios de la mente humana y abre nuevas avenidas para comprender y tratar las enfermedades neurológicas.
Si quieres conocer otros artículos parecidos a Secretos del Cerebro: Nacimiento y Memoria puedes visitar la categoría Neurociencia.
