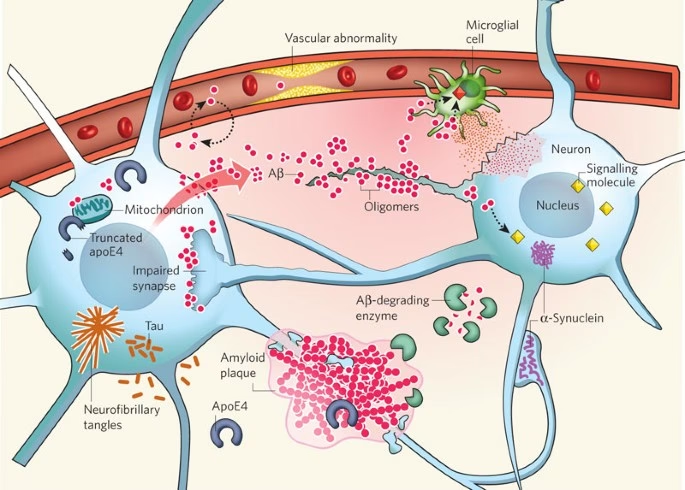
La enfermedad de Alzheimer (EA) representa el desafío neurodegenerativo más común de nuestro tiempo, manifestándose como una progresiva pérdida de la capacidad cognitiva y la memoria. A pesar de los avances, aún no contamos con un tratamiento que detenga su avance de raíz; las terapias actuales se centran principalmente en aliviar los síntomas. Comprender los mecanismos subyacentes es crucial para encontrar curas efectivas, y la investigación actual apunta a una interacción compleja entre factores genéticos y la función de células cerebrales clave, como la microglía y una proteína llamada TREM2.

Durante mucho tiempo, la pregunta de si el Alzheimer es una cuestión de 'naturaleza' (genética) o 'crianza' (ambiente/estilo de vida) ha intrigado tanto a la comunidad científica como al público. La respuesta, como suele ocurrir en biología, no es simple. Si bien los genes juegan un papel innegable, no son la única pieza del rompecabezas. Factores ambientales y celulares también contribuyen de manera significativa a la probabilidad de desarrollar la enfermedad.
- El Rol Clave de TREM2 en la Microglía
- La Genética del Alzheimer: ¿Naturaleza o Algo Más?
- Variantes Genéticas: Riesgo vs. Causa Directa
- El Gen APOE: Un Jugador Principal en el Riesgo
- Genes Causales Raros y Alzheimer de Inicio Temprano
- Factores Ambientales y Estilo de Vida: Más Allá de los Genes
- Pruebas Genéticas para el Alzheimer
- La Importancia de la Diversidad en la Investigación Genética
- Preguntas Frecuentes sobre Genética y TREM2 en Alzheimer
El Rol Clave de TREM2 en la Microglía
Estudios recientes han puesto el foco en el receptor activador expresado en células mieloides 2, conocido como TREM2. Esta proteína se encuentra predominantemente en la microglía, las células inmunes residentes del sistema nervioso central (SNC). La microglía actúa como el sistema de limpieza y defensa del cerebro, patrullando constantemente para detectar y eliminar desechos, patógenos y células dañadas. TREM2 es fundamental para que la microglía pueda llevar a cabo estas funciones vitales.
Se ha observado que TREM2 participa activamente en procesos microgliales como la proliferación (aumento del número de células), la supervivencia, la migración hacia áreas de daño y, crucialmente, la fagocitosis. La fagocitosis es el proceso por el cual las células engullen y digieren partículas extrañas o desechos celulares. En el contexto del Alzheimer, esto incluye la eliminación de sustancias neurotóxicas y proteínas anormales, como las que forman las placas amiloides, una característica distintiva de la enfermedad.
La visión académica predominante sugiere que TREM2 y las moléculas a las que se une (sus ligandos) ejercen efectos protectores en el SNC frente al Alzheimer. Al regular la función de la microglía, TREM2 ayuda a mantener el cerebro limpio y a mitigar el daño. Además de la fagocitosis, TREM2 también está implicado en la regulación de la respuesta inflamatoria y diversas vías de señalización celular, modulando así la respuesta inmune y el papel regulador de la microglía en el microambiente cerebral.
A pesar de la extensa investigación, el mecanismo de acción específico de TREM2 en el Alzheimer aún no se comprende completamente. Sin embargo, su papel central en la función microglial y la limpieza de agregados tóxicos lo convierte en un objetivo terapéutico potencial fascinante. Apuntar a TREM2 podría ofrecer una estrategia para potenciar la capacidad de la microglía para combatir la patología del Alzheimer, aunque aún existen limitaciones y desafíos para trasladar este conocimiento a tratamientos efectivos.
La Genética del Alzheimer: ¿Naturaleza o Algo Más?
La pregunta de si el Alzheimer se hereda es compleja. Si bien la mayoría de los casos no tienen una única causa genética directa, la genética sí influye significativamente en el riesgo de desarrollarlo. Nuestros genes, segmentos de ADN empaquetados en cromosomas dentro de cada célula, contienen las instrucciones para todas las funciones celulares, incluida la salud cerebral.
Pequeñas variaciones o cambios permanentes en estos genes, llamadas variantes genéticas, pueden afectar la probabilidad de desarrollar una enfermedad como el Alzheimer. La mayoría de las variantes son comunes y no causan enfermedades, pero algunas sí. En casos raros, heredar una variante en un gen específico casi garantiza el desarrollo de la enfermedad (como en algunas formas de Alzheimer de inicio temprano). Sin embargo, lo más común es que las variantes genéticas simplemente aumenten o, incluso, disminuyan el riesgo de padecer la enfermedad, sin ser una sentencia definitiva.
La investigación genética es un componente clave de la medicina de precisión, un enfoque emergente que considera la variabilidad individual en genes, entorno y estilo de vida para predecir qué estrategias de tratamiento y prevención serán más efectivas para grupos específicos de personas.
Variantes Genéticas: Riesgo vs. Causa Directa
En la mayoría de los casos, el Alzheimer es una enfermedad compleja influenciada por la combinación de múltiples genes, factores de estilo de vida y el entorno. Esto significa que una persona puede heredar varias variantes genéticas que, juntas, modifican su riesgo. Es importante destacar que no todas las personas que desarrollan Alzheimer tienen antecedentes familiares de la enfermedad. Sin embargo, tener un padre o hermano con Alzheimer sí aumenta el riesgo en comparación con aquellos sin esa conexión familiar.
Gracias a la investigación, hemos pasado de conocer solo 10 áreas genéticas asociadas al Alzheimer en 2010 a identificar al menos 80 hoy en día. Comprender qué genes están involucrados y cuál es su función es crucial para desarrollar métodos de prevención, retraso o tratamiento de la demencia.
El Gen APOE: Un Jugador Principal en el Riesgo
Uno de los genes más conocidos que influyen en el riesgo de Alzheimer es el gen de la apolipoproteína E (APOE). Este gen produce una proteína que ayuda a transportar el colesterol y otros tipos de grasa en el torrente sanguíneo. Se cree que los problemas en este proceso contribuyen al desarrollo del Alzheimer. El gen APOE se presenta en varias formas, llamadas alelos (por ejemplo, ε2, ε3, ε4).
Cada persona hereda dos alelos APOE, uno de cada progenitor biológico, lo que da lugar a seis combinaciones posibles: 2/2, 2/3, 2/4, 3/3, 3/4 y 4/4.
| Alelo APOE | Efecto sobre el Riesgo de Alzheimer | Prevalencia Aproximada |
|---|---|---|
| APOE ε2 | Puede ofrecer cierta protección. El Alzheimer, si ocurre, suele desarrollarse más tarde. | 5% - 10% |
| APOE ε3 | Considerado neutro; ni aumenta ni disminuye el riesgo. Es el más común. | Mayoría de la población |
| APOE ε4 | Aumenta el riesgo de Alzheimer y se asocia con una edad de inicio más temprana en algunas poblaciones. | 15% - 25% (una copia); 2% - 5% (dos copias) |
Tener dos copias de APOE ε4 confiere un riesgo mayor que tener una sola copia. Sin embargo, heredar un alelo APOE ε4 no significa que la persona desarrollará Alzheimer; muchas personas con este alelo nunca padecen la enfermedad.

Genes Causales Raros y Alzheimer de Inicio Temprano
Además de las variantes que aumentan el riesgo, existen tres variantes genéticas raras en genes específicos que se sabe que causan directamente el Alzheimer. Estas variantes, cuando se heredan, tienen una probabilidad muy alta de causar la enfermedad, a menudo antes de los 65 años (conocido como Alzheimer de inicio temprano). Menos del 10% de todos los casos de Alzheimer son de inicio temprano, y de estos, solo el 10%-15% se deben a cambios en estos tres genes:
- Proteína Precursora Amiloide (APP) en el cromosoma 21
- Presenilina 1 (PSEN1) en el cromosoma 14
- Presenilina 2 (PSEN2) en el cromosoma 1
Un niño con un progenitor que porta una variante en uno de estos genes tiene un 50% de probabilidad de heredarla. Estas mutaciones conducen a la producción de proteínas anormales que contribuyen a la acumulación de fragmentos amiloides pegajosos que forman las placas amiloides en el cerebro, una característica fundamental del Alzheimer.
Además, las personas con síndrome de Down tienen una copia extra del cromosoma 21, que contiene el gen APP, lo que les confiere un mayor riesgo de desarrollar Alzheimer de inicio temprano. Se estima que el 50% o más de las personas con síndrome de Down desarrollarán Alzheimer, generalmente en sus 50 o 60 años.
Factores Ambientales y Estilo de Vida: Más Allá de los Genes
La influencia del entorno y el estilo de vida es un área de investigación creciente. Factores como el ejercicio, la dieta, la exposición a ciertas sustancias químicas o el tabaquismo pueden tener efectos positivos o negativos al alterar la forma en que ciertos genes funcionan. El campo de la epigenética estudia cómo estos factores externos pueden modificar el ADN de una célula de maneras que afectan la actividad génica sin cambiar la secuencia del ADN en sí.
Esto subraya que el Alzheimer no es puramente una cuestión de herencia. Es una enfermedad compleja donde la predisposición genética interactúa con una multitud de otros factores a lo largo de la vida.
Pruebas Genéticas para el Alzheimer
Actualmente, las pruebas genéticas no se utilizan de forma rutinaria en la práctica clínica para diagnosticar o predecir el riesgo de Alzheimer en la población general. Sin embargo, en algunos casos específicos, si una persona presenta síntomas a una edad temprana y tiene un historial familiar muy fuerte de Alzheimer, un neurólogo puede solicitar una prueba para los genes causales raros (APP, PSEN1, PSEN2).
Aunque también existe la prueba para el gen APOE, sus resultados no pueden predecir con certeza quién desarrollará la enfermedad. Principalmente se utiliza en entornos de investigación para identificar participantes con mayor riesgo y estudiar los cambios tempranos en el cerebro o la efectividad de tratamientos potenciales en diferentes perfiles genéticos. Algunas personas acceden a su estado APOE a través de pruebas genéticas de consumo directo al público, pero es recomendable discutir estos resultados con un médico o asesor genético para comprender mejor sus implicaciones.
La Importancia de la Diversidad en la Investigación Genética
La investigación muestra que las tasas de demencia varían entre diferentes grupos raciales y étnicos. Si bien 'raza' y 'etnia' son construcciones sociales, estas definiciones pueden ayudar a los investigadores a examinar factores de riesgo, tanto externos (entorno, educación, ingresos) como biológicos (genética). Estudiar la ascendencia genética, la región geográfica de la que una persona desciende biológicamente, es crucial para identificar factores únicos vinculados a la ascendencia que pueden afectar el riesgo de Alzheimer en diferentes poblaciones. La investigación en poblaciones diversas es fundamental para desarrollar estrategias de prevención, diagnóstico y tratamiento que funcionen para todas las personas.
Los objetivos de la investigación genética en Alzheimer incluyen:
- Responder preguntas básicas sobre el inicio del proceso de la enfermedad.
- Determinar cómo los factores genéticos de riesgo y protección interactúan con otros genes y con las influencias del estilo de vida o el entorno.
- Identificar a las personas con alto riesgo para que puedan beneficiarse tempranamente de nuevas intervenciones.
- Explicar las diferencias en el riesgo entre distintos grupos y entre hombres y mujeres.
- Utilizar los descubrimientos genéticos para desarrollar terapias potenciales.
Preguntas Frecuentes sobre Genética y TREM2 en Alzheimer
¿El Alzheimer es siempre hereditario?
No, la mayoría de los casos de Alzheimer no son causados por un único gen heredado que garantice la enfermedad. La mayoría son de inicio tardío y resultan de una combinación compleja de múltiples genes de riesgo, estilo de vida y factores ambientales.
¿Qué es TREM2 y por qué es importante?
TREM2 es una proteína que se encuentra principalmente en las células inmunes del cerebro llamadas microglía. Es importante porque ayuda a la microglía a realizar funciones vitales como limpiar desechos y proteínas anormales, lo cual es crucial para mantener la salud cerebral y combatir la patología del Alzheimer.
¿Puedo saber mi riesgo genético de Alzheimer?
Se pueden realizar pruebas genéticas para el gen APOE, que es un factor de riesgo común. Sin embargo, el resultado de esta prueba no predice con certeza si desarrollarás Alzheimer. Para las formas raras de inicio temprano causadas por genes específicos, las pruebas son más predictivas pero solo se recomiendan en casos con síntomas tempranos y fuerte historial familiar.
¿Cómo interactúan los genes y el estilo de vida en el Alzheimer?
Los factores de estilo de vida y ambientales pueden influir en cómo se expresan ciertos genes, afectando el riesgo de la enfermedad. La investigación en epigenética explora estas interacciones, sugiriendo que un estilo de vida saludable puede mitigar el riesgo incluso si hay una predisposición genética.
¿TREM2 es un objetivo para el tratamiento del Alzheimer?
Sí, dada su función en la microglía y la eliminación de la patología amiloide, TREM2 se considera un objetivo terapéutico prometedor. La investigación busca formas de modular la actividad de TREM2 para potenciar la capacidad de la microglía para proteger el cerebro.
Si quieres conocer otros artículos parecidos a Alzheimer: Genética, TREM2 y Microglía puedes visitar la categoría Neurociencia.