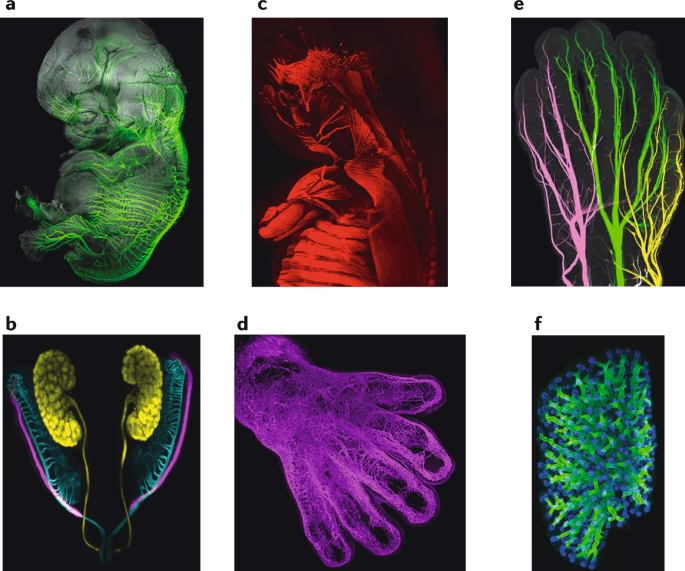
Durante mucho tiempo, para estudiar la intrincada estructura interna de los tejidos biológicos, los científicos dependían de cortar muestras en rebanadas extremadamente finas. Estas secciones, a menudo de solo unas pocas micras de grosor, se montaban en portaobjetos y se examinaban bajo un microscopio. Si bien esta técnica ha sido fundamental para la histología y la patología durante más de un siglo, presenta limitaciones significativas, especialmente cuando se trata de comprender la organización espacial compleja de órganos enteros o redes neuronales. La reconstrucción tridimensional a partir de innumerables secciones finas es laboriosa, propensa a errores y puede perder información crucial sobre las conexiones a larga distancia. Aquí es donde entra en juego el aclaramiento de tejidos, una colección de técnicas innovadoras diseñadas para hacer que las muestras biológicas, incluso órganos completos o pequeños organismos, sean transparentes para su examen en tres dimensiones.
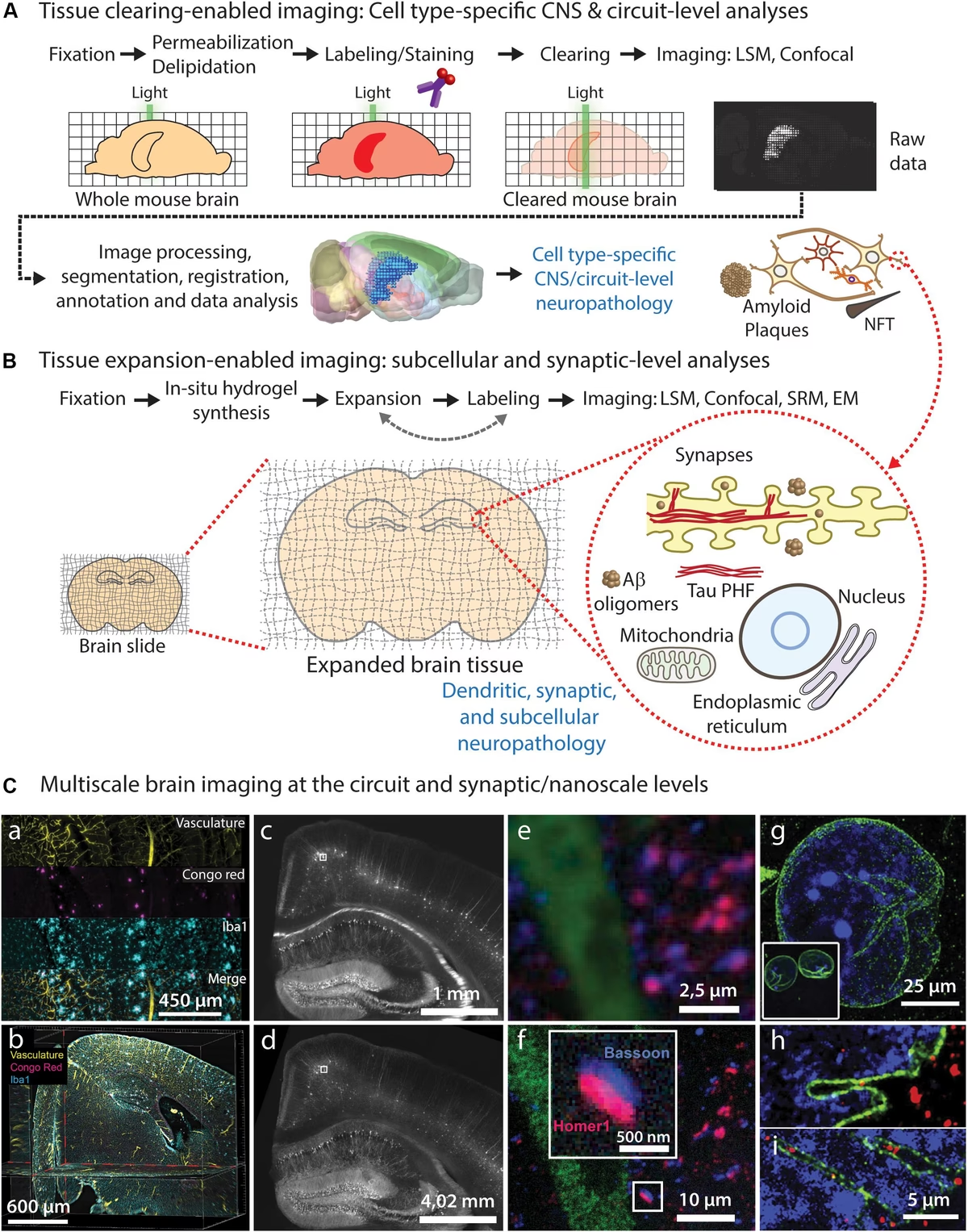
El principio fundamental detrás del aclaramiento de tejidos es simple pero ingenioso: igualar el índice de refracción de los diferentes componentes dentro de la muestra biológica. Los tejidos vivos son opacos principalmente porque la luz se dispersa al pasar a través de diversas estructuras (agua, lípidos, proteínas) que tienen diferentes índices de refracción. Piénsalo como intentar ver a través de un cubo lleno de cubitos de hielo; la luz se dispersa en cada interfaz hielo-agua. El aclaramiento de tejidos busca eliminar o reemplazar los componentes que causan esta dispersión (principalmente agua y lípidos) con medios que tienen un índice de refracción similar al de las proteínas restantes, haciendo que la luz viaje en línea recta a través de la muestra.
¿Por Qué Aclarar Tejidos? La Necesidad de la Visualización 3D
La opacidad inherente de los tejidos ha sido un obstáculo importante para la visualización tridimensional a gran escala. Las técnicas microscópicas tradicionales, como la microscopía confocal, tienen una penetración de luz limitada en muestras gruesas debido a la dispersión. Esto obliga a los investigadores a seccionar las muestras en finas láminas. Sin embargo, muchas estructuras biológicas importantes, como los vasos sanguíneos, los axones neuronales que se extienden por grandes distancias, o las redes celulares dentro de un órgano, existen en tres dimensiones y sus relaciones espaciales son vitales para comprender su función.
El aclaramiento de tejidos, combinado con técnicas de microscopía avanzadas como la microscopía de hoja de luz (light-sheet microscopy), permite obtener imágenes de muestras intactas de hasta varios centímetros de grosor con resolución celular. Esto significa que se pueden estudiar circuitos neuronales completos, la vasculatura de un órgano o la distribución de células inmunes en un tumor sin destruirlos mediante el seccionamiento. Los beneficios son claros: un flujo de trabajo más rápido, menos artefactos de corte, una mejor comprensión de la arquitectura global y la posibilidad de cuantificar y mapear estructuras en su contexto natural.
Principios Químicos de las Técnicas de Aclaramiento
Existen diversas metodologías de aclaramiento, cada una con sus propias ventajas y limitaciones, basadas en diferentes principios químicos para lograr la transparencia. Se pueden categorizar ampliamente en:
Métodos basados en disolventes orgánicos
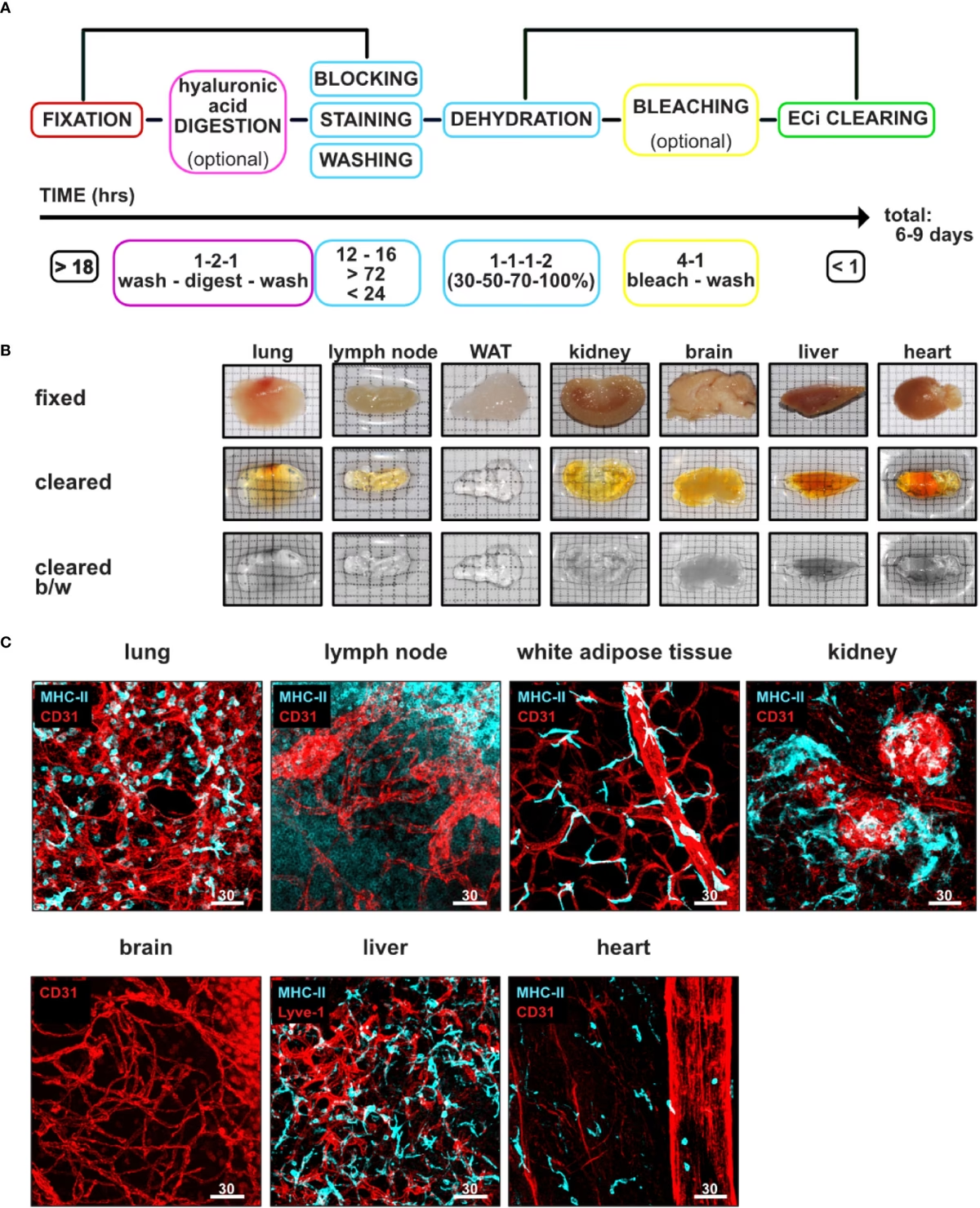
Estos métodos funcionan deshidratando la muestra (reemplazando el agua con alcoholes) y luego sumergiéndola en disolventes orgánicos que eliminan los lípidos y tienen un alto índice de refracción (~1.55), cercano al de las proteínas. Son generalmente muy rápidos y efectivos para lograr una alta transparencia. Sin embargo, la deshidratación y la exposición a disolventes a menudo provocan la pérdida de la fluorescencia de las proteínas fluorescentes endógenas (como GFP) y pueden causar contracción del tejido. Técnicas como 3DISCO (3D imaging of solvent-cleared organs) e iDISCO (immunolabeling-enabled 3D imaging of solvent-cleared organs) han sido desarrolladas para mitigar la pérdida de fluorescencia y permitir la inmunotinción.
Métodos basados en soluciones acuosas
Estos métodos sumergen la muestra en soluciones concentradas de compuestos con alto índice de refracción, como azúcares (sacarosa, fructosa) o alcoholes hidrófilos (glicerol, 2,2'-tiodietanol - TDE). Al ser acuosos, son más compatibles con la fluorescencia endógena y permiten la tinción de lípidos. Su protocolo suele ser más sencillo. Sin embargo, pueden ser lentos, especialmente para muestras grandes, y las soluciones concentradas pueden ser muy viscosas, dificultando el manejo y la penetración de sondas moleculares. Ejemplos incluyen SeeDB, TDE y la familia Scale (como ScaleS).
Métodos basados en hidrogeles
Una limitación de los métodos anteriores es la pérdida de componentes moleculares (como proteínas o ARN) durante el proceso. Los métodos basados en hidrogeles abordan esto estabilizando la muestra mediante la incrustación en un hidrogel poroso. Las macromoléculas se retienen dentro de la red del hidrogel al unirse a él (por ejemplo, mediante reticulación), mientras que los lípidos se eliminan mediante detergentes. El tejido incrustado en hidrogel es luego sumergido en una solución de alto índice de refracción. Estos métodos preservan muy bien la estructura tisular y permiten múltiples rondas de tinción y destinción. CLARITY (Clear Lipid-exchanged Acrylamide-hybridized Rigid Imaging / Embedding and Staining Hydrogel-based) fue una técnica pionera, seguida por variantes mejoradas como PACT, PARS, ACT-PRESTO y SWITCH. Una variante notable es CUBIC (clear unobstructed brain imaging cocktails and computational analysis), que utiliza cócteles químicos para la delipidación e igualación del índice de refracción, y que también puede preservar la fluorescencia endógena y permitir la inmunotinción.
Métodos de hiperhidratación
Estos métodos combinan el uso de detergentes para eliminar lípidos con la hidratación mediada por urea u otros agentes para bajar el índice de refracción. Intentan mantener un ambiente acuoso para preservar la fluorescencia. Un ejemplo es la familia Scale, que ha evolucionado para ser más rápida y evitar la expansión tisular.
La elección del método de aclaramiento depende de varios factores, incluyendo el tipo de tejido, el tamaño de la muestra, el tipo de marcador (fluorescencia endógena vs. inmunotinción), la necesidad de preservar lípidos y la velocidad requerida.
| Método Principal | Mecanismo Principal | Rapidez | Preservación de Fluorescencia Endógena | Manejo de Lípidos | Índice de Refracción Final (aprox.) |
|---|---|---|---|---|---|
| Basado en Disolventes | Deshidratación, Eliminación de Lípidos | Alta | Baja (requiere inmunotinción) | Eliminación efectiva | 1.55 |
| Basado en Soluciones Acuosas | Inmersión en Medio de Alto IR | Baja a Moderada | Alta | Preservación (permite tinción) | 1.44 - 1.52 |
| Basado en Hidrogeles | Estabilización con Hidrogel, Eliminación/Intercambio de Lípidos | Moderada (electr. rápida) | Alta | Eliminación o Intercambio | 1.38 - 1.45 |
| Hiperhidratación (ej. Scale) | Delipidación, Hidratación/Igualación IR | Moderada | Alta | Eliminación | 1.38 - 1.48 |
Aplicaciones Clave en Neurociencia y Más Allá
El aclaramiento de tejidos ha abierto nuevas puertas en la investigación, especialmente en neurociencia, donde la complejidad de las redes neuronales requiere una comprensión tridimensional. Algunas aplicaciones destacadas incluyen:
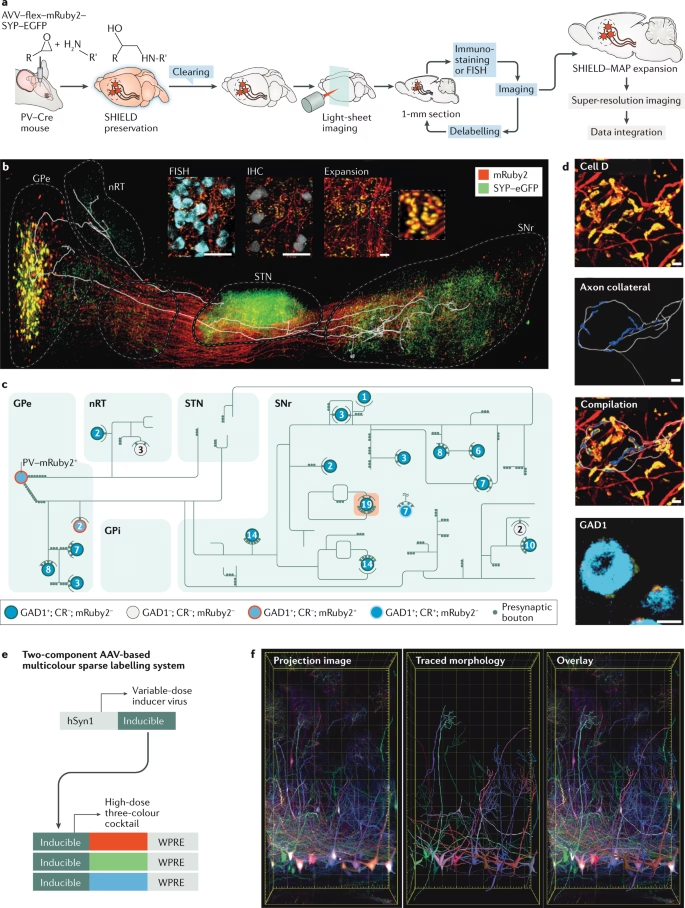
- Mapeo de Circuitos Neuronales: Permite visualizar y rastrear proyecciones neuronales a larga distancia a través del cerebro completo, identificando tipos celulares específicos y su conectividad. Esto es crucial para entender cómo funcionan los diferentes módulos cerebrales y cómo interactúan.
- Visualización de Vasculatura: Permite obtener imágenes detalladas de la red vascular en órganos enteros, revelando su organización y posibles anomalías en enfermedades.
- Estudio de Enfermedades Neurológicas: Facilita la visualización de patologías como la acumulación de agregados proteicos (característica del Alzheimer o Parkinson) o la inflamación en 3D dentro del contexto tisular intacto.
- Análisis de Metástasis de Cáncer: Permite rastrear la propagación de células cancerosas a través de órganos y el cuerpo entero en modelos animales, con resolución celular.
- Imagen de Órganos Enteros: Desde cerebros, riñones, pulmones, hasta órganos reproductores, el aclaramiento permite estudiar su morfología, distribución celular y patologías en su totalidad.
- Investigación en Organoides y Esferoides: Facilita la caracterización tridimensional de estos modelos in vitro que imitan órganos.
- Estudio de Otros Organismos: Se ha aplicado con éxito en modelos como peces cebra, moscas Drosophila, e incluso en plantas, permitiendo la visualización de estructuras complejas en 3D.
Más allá de la neurociencia, el aclaramiento se utiliza para estudiar la arquitectura de tumores, la distribución de fármacos o nanopartículas en tejidos, la estructura del sistema inmune en órganos linfoides y la microvasculatura en diversos tejidos.
Combinando Aclaramiento con Otras Tecnologías
El verdadero poder del aclaramiento reside en su combinación con otras tecnologías de vanguardia:
- Microscopía de Hoja de Luz (Light-Sheet Microscopy): Es el compañero ideal para las muestras aclaradas. Ilumina la muestra con una fina hoja de luz, lo que reduce el fotoblanqueo y la fototoxicidad, permitiendo la adquisición rápida de grandes volúmenes de datos con alta resolución.
- Inmunotinción y Sondas Moleculares: Las muestras aclaradas pueden ser inmunoteñidas para visualizar proteínas específicas o hibridadas con sondas para detectar ARN (FISH, HCR), permitiendo el fenotipado molecular de células dentro de su contexto 3D. La penetración de anticuerpos en tejidos gruesos puede ser un desafío, y se han desarrollado métodos para mejorarla (ej. electroforesis en CLARITY, o métodos como FLASH o magnetohidrodinámica).
- Microscopía de Expansión (Expansion Microscopy): Esta técnica expande físicamente la muestra tisular incrustándola en un polímero hidrofílico que se hincha. Combinada con el aclaramiento, permite lograr una resolución casi super-resolución en muestras 3D grandes, superando las limitaciones de difracción de la luz.
- Análisis Computacional y Atlas: Los enormes conjuntos de datos generados por la imagen 3D de muestras aclaradas requieren herramientas computacionales avanzadas para su procesamiento, segmentación (identificación de células o vasos) y mapeo. La alineación de estos datos con atlas de referencia 3D (cerebro de ratón, cerebro humano) permite comparar resultados entre diferentes experimentos y laboratorios.
Es importante notar que el término 'clearing' también se usa en histopatología tradicional (como se menciona en una de las referencias proporcionadas) para describir el paso de eliminar el alcohol después de la deshidratación y antes de la infiltración con parafina, generalmente usando xileno o sustitutos. Este 'clearing' tradicional tiene el propósito de preparar el tejido para el corte en secciones finas y el montaje en portaobjetos, no para la visualización 3D de muestras gruesas. Aunque comparten el nombre y el objetivo de alterar las propiedades ópticas del tejido, son técnicas distintas con aplicaciones y protocolos diferentes.
Desafíos y Consideraciones
A pesar de sus avances, el aclaramiento de tejidos presenta desafíos. La preservación de la fluorescencia endógena es variable entre métodos. La penetración uniforme de anticuerpos o sondas en muestras muy grandes puede ser difícil. Algunos métodos pueden causar distorsión (expansión o contracción) del tejido. El manejo de los grandes volúmenes de datos de imagen generados es computacionalmente intensivo. Además, algunos reactivos de aclaramiento pueden ser tóxicos (como el xileno en el contexto tradicional) o costosos.
Preguntas Frecuentes
¿Cuál es el objetivo principal del aclaramiento de tejidos?
El objetivo principal es hacer que las muestras biológicas, como órganos o tejidos gruesos, sean transparentes para permitir su visualización en tres dimensiones utilizando microscopía, sin necesidad de cortarlos en secciones finas.
¿En qué se diferencia el aclaramiento moderno de la histopatología tradicional?
En la histopatología tradicional, el 'clearing' prepara el tejido para la incrustación en parafina y el corte en secciones finas. El aclaramiento moderno, para visualización 3D, hace que las muestras gruesas o enteras sean transparentes para la microscopía volumétrica.
¿Por qué son opacos los tejidos biológicos?
Son opacos principalmente debido a la dispersión de la luz causada por las diferencias en el índice de refracción entre sus componentes, como el agua, los lípidos y las proteínas.
¿Qué tipos de tejidos u órganos se pueden aclarar?
Se pueden aclarar una amplia variedad de tejidos y órganos, incluyendo cerebros completos, riñones, pulmones, corazón, tumores, embriones, organoides e incluso organismos pequeños como peces cebra o insectos.
¿El aclaramiento de tejidos daña la muestra?
Los métodos de aclaramiento están diseñados para preservar la estructura tisular lo mejor posible, pero algunos pueden causar cierta contracción, expansión o pérdida de moléculas, dependiendo de la química utilizada.
¿Se puede combinar el aclaramiento con la tinción de células o estructuras específicas?
Sí, la mayoría de los métodos de aclaramiento son compatibles con la inmunotinción (para detectar proteínas) y la hibridación in situ (para detectar ARN), permitiendo visualizar células o moléculas específicas en 3D.
Conclusión
El aclaramiento de tejidos ha transformado la forma en que estudiamos la biología a nivel de sistemas y órganos. Al superar la barrera de la opacidad, estas técnicas nos permiten explorar la compleja arquitectura tridimensional de la vida con un detalle sin precedentes. Combinado con los avances en microscopía, tinción y análisis computacional, el aclaramiento continúa impulsando descubrimientos en neurociencia, biología del desarrollo, investigación del cáncer y muchas otras áreas, proporcionando una ventana clara hacia la intrincada organización de las estructuras biológicas.
Si quieres conocer otros artículos parecidos a Aclaramiento de Tejidos: Ventana a la 3D puedes visitar la categoría Neurociencia.