En el intrincado universo de nuestro cerebro, existe una diminuta pero poderosa estructura que actúa como la orquesta maestra de nuestros ritmos internos: el Núcleo Supraquiasmático (NSQ). Situado estratégicamente en el hipotálamo, este par de núcleos es el epicentro de nuestro sistema de tiempo circadiano, dictando el compás de la mayoría de los procesos biológicos que se repiten aproximadamente cada 24 horas. Desde cuándo sentimos sueño hasta la liberación de hormonas cruciales, el NSQ mantiene nuestro cuerpo sincronizado con el ciclo de luz y oscuridad del mundo exterior. Comprender su funcionamiento no solo revela los mecanismos detrás de nuestro reloj interno, sino que también arroja luz sobre por qué los desajustes circadianos pueden tener profundas repercusiones en nuestra salud física y mental.

- ¿Qué es el Núcleo Supraquiasmático (NSQ)?
- Estructura y Componentes del NSQ
- Cómo el NSQ Recibe Información: Las Vías Aferentes
- Cómo el NSQ Envía Señales: Las Vías Eferentes
- La Relación Fundamental con la Melatonina
- Variaciones Fisiológicas del NSQ
- Importancia Clínica: Cuando el Reloj se Desajusta
- ¿Qué Sucede si el NSQ Sufre Daño?
- Preguntas Frecuentes sobre el NSQ
- Tabla Comparativa: Núcleo Central vs. Corteza del NSQ
¿Qué es el Núcleo Supraquiasmático (NSQ)?
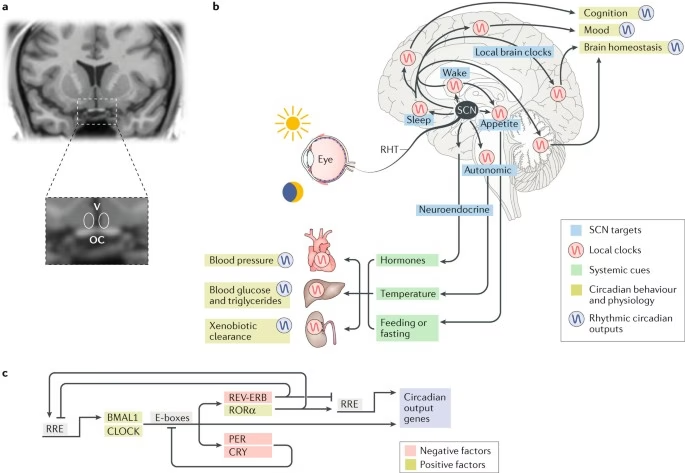
El Núcleo Supraquiasmático, o NSQ, es una estructura bilateral que se encuentra en la parte anterior del hipotálamo. Es reconocido como el marcapasos central del sistema de sincronización circadiana, regulando la mayoría de los ritmos circadianos en el cuerpo. Su ubicación es precisa: directamente encima del quiasma óptico, una encrucijada donde se cruzan los nervios ópticos. Esta proximidad no es casual, ya que el NSQ recibe su señal más importante, la luz, directamente desde la retina.

Estructura y Componentes del NSQ
El NSQ está compuesto por dos núcleos, cada uno con aproximadamente 10,000 neuronas, situados a ambos lados del tercer ventrículo, justo por encima del quiasma óptico. Esta estructura se divide funcionalmente en dos subregiones principales: el 'núcleo central' (core) y la 'corteza' o 'envoltura' (shell). El núcleo central, que recibe las proyecciones de la retina, es rico en péptido intestinal vasoactivo (VIP) y péptido liberador de gastrina (GRP). Por otro lado, la corteza contiene neuronas que expresan arginina vasopresina (AVP).
La distribución y expresión de estos neuropéptidos (VIP, GRP y AVP) son consistentes en muchas especies de mamíferos, lo que subraya su importancia evolutiva para mantener el ritmo circadiano. En el núcleo central, los niveles de VIP aumentan durante el período oscuro, mientras que el GRP aumenta durante el período de luz y es específicamente activado por las entradas directas de las células ganglionares fotosensibles de la retina a través del tracto retinohipotalámico (TRH). Estudios en animales han demostrado que los niveles de GRP aumentan por la mañana y alcanzan su pico alrededor del mediodía. El VIP y su receptor, VPAC2, forman una vía de señalización clave en el NSQ que controla los ritmos circadianos diarios y mantiene la sincronización interna del núcleo.
Las neuronas de AVP en la corteza proyectan hacia el núcleo paraventricular (NPV), coordinando los ritmos de alimentación circadianos y ayudando a sincronizar los horarios de comida con el ritmo circadiano. Las neuronas de AVP también proyectan hacia neuronas que controlan la sed en el órgano vasculoso de la lámina terminal (OVLT). Se ha observado que los ratones aumentan su ingesta de agua antes de dormir, lo que se correlaciona con el aumento de la actividad eléctrica de las neuronas de AVP hacia el OVLT durante este período.
Cómo el NSQ Recibe Información: Las Vías Aferentes
El NSQ no opera en aislamiento; recibe información de diversas regiones del cerebro. Las proyecciones neuronales aferentes al NSQ son múltiples. Su tracto principal es el retinohipotalámico (TRH), que se origina en las células ganglionares fotosensibles de la retina. Estas células contienen melanopsina y responden directamente a la luz ambiental, proporcionando al NSQ información crucial sobre la intensidad y duración del día.
Aunque inicialmente se describieron unas 40 regiones con proyecciones monosimpáticas al NSQ, la investigación reciente se ha centrado en cuatro entradas aferentes principales:
- Tracto Retinohipotalámico (TRH): Proviene de las células ganglionares de la retina. Secreta glutamato y polipéptido activador de la adenilato ciclasa hipofisaria (PACAP) en las regiones del núcleo central ricas en VIP. Media la regulación fótica de la ritmicidad circadiana. El PACAP potencia la acción del glutamato.
- Tracto Geniculohipotalámico (TGH): Proviene de la lámina intergeniculada (LIG). Proporciona una entrada fótica indirecta mediada tanto por estímulos fóticos como no fóticos (como la actividad motora o conductual). Utiliza neurotransmisores como neuropéptido Y (NPY), GABA y encefalina (ENK). El NPY es el principal neurotransmisor del TGH y actúa directamente sobre las neuronas marcapasos del NSQ.
- Núcleos del Rafe Mediano: Ubicados en el mesencéfalo, liberan serotonina en las regiones del NSQ que reciben información de la retina (ricas en VIP). Su papel principal es modular la respuesta del marcapasos a la luz. La serotonina puede potenciar (de día) o inhibir (de noche) la entrada de glutamato.
- Núcleos Tegmentales (Pedunculopontino, Parabigeminal, Laterodorsal): Estas proyecciones transportan neurotransmisores colinérgicos al NSQ.
La mayoría de estas entradas monosimpáticas se concentran más densamente en el núcleo central del NSQ, con una dispersión menor en la corteza. La interacción de estos neurotransmisores y vías permite que el NSQ integre información sobre la luz, el nivel de actividad y el estado interno para mantener un ritmo circadiano preciso.
Cómo el NSQ Envía Señales: Las Vías Eferentes
Las neuronas del NSQ envían proyecciones (eferentes) para comunicar el tiempo circadiano a otras partes del cerebro y del cuerpo. La mayoría de las proyecciones monosimpáticas terminan en núcleos cercanos del hipotálamo y el tálamo. En el hipotálamo, las proyecciones eferentes del NSQ alcanzan el núcleo preóptico medial, la zona subparaventricular, el núcleo ventromedial, el núcleo dorsomedial, el núcleo geniculado lateral ventral y el núcleo septal lateral.
La principal vía eferente polisimpática del NSQ proyecta hacia la glándula pineal. Durante la noche, estas fibras liberan norepinefrina, que estimula los receptores adrenérgicos beta-1 y alfa-1 en los pinealocitos, desencadenando la producción de melatonina. La melatonina actúa como una señal humoral que varía en intensidad a medida que las noches se alargan o acortan a lo largo del año. Por lo tanto, la producción de melatonina se prolonga en invierno (noches más largas) y se acorta en verano (noches más cortas).

Como el oscilador maestro, el NSQ utiliza tanto entradas humorales como neuronales para coordinar los relojes circadianos periféricos. Órganos periféricos como el pulmón, el hígado, el riñón, el corazón y los músculos también exhiben expresión de genes circadianos, que se basa en la combinación de la entrada fótica al NSQ y la entrada no fótica, como el momento de la ingesta de alimentos o la actividad motora. Los principales neurotransmisores involucrados en las proyecciones eferentes del NSQ son AVP y VIP.
La Relación Fundamental con la Melatonina
La melatonina juega un papel crucial en la sincronización de los eventos biológicos internos con las señales ambientales externas. Su secreción rítmica por la glándula pineal está regulada directamente por el NSQ. El ciclo luz-oscuridad es el principal sincronizador. La secreción de melatonina es estimulada por la oscuridad e inhibida por la luz. En coordinación con el NSQ, la melatonina está centralmente involucrada en mantener la ritmicidad circadiana y regular el sueño.
El NSQ regula el momento exacto de la liberación de melatonina, mientras que la melatonina retroalimenta al NSQ para disminuir la actividad neuronal del NSQ. Este proceso está controlado por dos receptores de melatonina de alta afinidad (MT1 y MT2) ubicados en el NSQ. La activación del receptor MT1 suprime la tasa de disparo neuronal en el NSQ, mientras que el MT2 actúa principalmente induciendo cambios de fase en el ritmo circadiano.
La capacidad de la melatonina para arrastrar o sincronizar el reloj circadiano mediante su acción directa en el NSQ ha llevado a investigar su uso terapéutico para tratar trastornos del ritmo circadiano, como el jet lag, el trastorno por trabajo en turnos y ciertos tipos de insomnio. Sin embargo, los resultados sobre su efectividad no siempre son concluyentes. Algunos agonistas de los receptores de melatonina, como el ramelteon, están aprobados para el tratamiento del insomnio.
Durante el período de vigilia, las señales de alerta del NSQ son dominantes, alcanzando un pico unas 2-3 horas antes de la hora habitual de acostarse. Estas señales contrarrestan la acumulación homeostática de la necesidad de sueño. Por la noche, esta señal de alerta disminuye, en parte, debido al aumento de los niveles de melatonina, lo que finalmente permite que ocurra el sueño. La melatonina no solo comunica el ciclo ambiental de luz-oscuridad al marcapasos circadiano, sino que también puede mediar entre el marcapasos circadiano y la conducta de sueño-vigilia.
Variaciones Fisiológicas del NSQ
El NSQ y los ritmos que regula no son estáticos; pueden variar fisiológicamente a lo largo del tiempo y en respuesta a las estaciones.
Cambios Estacionales: Los neurotransmisores involucrados en la actividad circadiana del NSQ también afectan otros procesos estacionales. Por ejemplo, en invierno, los ritmos de melatonina se retrasan aproximadamente 90 minutos en comparación con los del verano. Los niveles de serotonina alcanzan su pico entre octubre y noviembre antes de disminuir y tocar fondo entre diciembre y enero. Las reducciones en las concentraciones de serotonina durante los meses de invierno coinciden con una mayor prevalencia del trastorno afectivo estacional (TAS) durante este período.
Cambios Relacionados con la Edad: La creciente alteración del ciclo sueño-vigilia es un fenómeno esperado del envejecimiento normal. Aproximadamente el 40% al 70% de los ancianos experimentan trastornos crónicos del sueño. Estudios han encontrado una actividad eléctrica de menor amplitud en el NSQ de ratones envejecidos, así como una disminución en las proyecciones neuronales eferentes del NSQ a la zona subparaventricular del hipotálamo. Tratar los ritmos circadianos alterados a nivel del NSQ podría potencialmente mejorar las alteraciones del sueño nocturno y la fatiga diurna que a menudo reportan los adultos mayores.
Importancia Clínica: Cuando el Reloj se Desajusta
Un conocimiento detallado del NSQ, sus vías y neurotransmisores es esencial para comprender los mecanismos del reloj circadiano maestro y sugerir objetivos de intervención para abordar los trastornos del sueño del ritmo circadiano. Además, tiene implicaciones en la cronofarmacología, donde la eficacia de los medicamentos puede variar según el momento de administración dentro del ciclo circadiano.
Trastornos del Estado de Ánimo: La investigación ha relacionado la alteración de la ritmicidad circadiana con trastornos del estado de ánimo, como el trastorno bipolar, el trastorno afectivo estacional (TAS) y otros trastornos depresivos. Los pacientes con trastorno depresivo mayor, por ejemplo, a menudo reportan despertares tempranos e insomnio. Se postula que los ritmos circadianos están retrasados en el trastorno depresivo mayor. Los enfoques de tratamiento incluyen inhibidores selectivos de la recaptación de serotonina (ISRS) que aceleran los ritmos circadianos y la terapia de luz matutina para inducir avances de fase.
El trastorno afectivo estacional se cree que es causado por vías serotoninérgicas disfuncionales desde los núcleos del rafe. Los tratamientos exitosos han incluido medicamentos que alteran la neurotransmisión serotoninérgica. Las personas con trastorno bipolar a menudo reportan reducción del sueño durante los episodios maníacos. Se ha observado que la expresión de genes reloj se adelanta durante los episodios maníacos y se retrasa durante los episodios depresivos.
Trastornos del Sueño del Ritmo Circadiano: Estos trastornos afectan millones de personas y tienen efectos adversos en la salud y la calidad de vida. Dos de los más comunes son:
- Trastorno de Fase del Sueño Avanzada (TAS Avanzada) y Trastorno de Fase del Sueño Retrasada (TAS Retrasada): En el TAS Avanzada, las personas se duermen a una hora normal pero se despiertan varias horas antes de lo habitual (ej. 2:00-5:00 AM). Afecta aproximadamente al 1% de los adultos de mediana edad y mayores. En el TAS Retrasada, las personas se duermen pasada la medianoche y se despiertan tarde por la mañana o por la tarde. Tiene una prevalencia del 7-16% entre adolescentes y adultos jóvenes y a menudo tiene un componente familiar.
- Trastorno del Sueño por Trabajo en Turnos: Afecta a adultos con horarios de trabajo no estándar que alteran los ciclos normales de sueño-vigilia de 24 horas. Con la edad, la adaptación circadiana al trabajo en turnos disminuye. Estas personas experimentan alteración en el ritmo de melatonina.
- Trastorno del Ritmo Sueño-Vigilia Irregular (RSVI): En este trastorno, el ciclo sueño-vigilia pierde su ritmo circadiano normal. A menudo asociado con discapacidad intelectual en niños y demencia en ancianos, especialmente con comorbilidades psiquiátricas y médicas. Se cree que está relacionado con daño estructural en el NSQ. En pacientes con demencia, los niveles nocturnos de melatonina pueden estar reducidos, lo que resulta en una mayor expresión de la vigilia generada por el NSQ por la noche. Curiosamente, la melatonina exógena no siempre ha demostrado ser efectiva para tratar el RSVI. Tratamientos combinados con mayor exposición a la luz diurna y caminatas diarias han mostrado mejoras significativas.
¿Qué Sucede si el NSQ Sufre Daño?
Dado su papel central como marcapasos, el daño al NSQ tiene consecuencias significativas. Estudios en animales han demostrado que la ablación completa del NSQ resulta en un ciclo de melatonina anormal y ritmos irregulares de descanso/actividad. En humanos, la destrucción del NSQ también ha demostrado patrones alterados de temperatura corporal y función conductual. La pérdida de la señal temporal coherente lleva a que los diferentes ritmos biológicos del cuerpo se desincronicen entre sí y con el ambiente externo, lo que puede manifestarse en problemas graves de sueño, estado de ánimo y otras funciones fisiológicas.
Preguntas Frecuentes sobre el NSQ
¿El NSQ aumenta o disminuye la melatonina?
El NSQ no produce melatonina, sino que *regula* su liberación. La oscuridad estimula una vía neuronal que, pasando por el NSQ, finalmente lleva a que la glándula pineal produzca y libere melatonina. La luz inhibe esta vía. La melatonina, a su vez, retroalimenta al NSQ, generalmente *disminuyendo* su actividad neuronal, lo que ayuda a reforzar la señal de oscuridad y promover el sueño.
¿Qué pasa si el NSQ está dañado?
El daño al NSQ interrumpe la capacidad del cerebro para mantener ritmos circadianos estables. Esto puede llevar a graves trastornos del sueño (como el ritmo sueño-vigilia irregular), alteraciones en la temperatura corporal, problemas en la regulación hormonal y una mayor susceptibilidad a trastornos del estado de ánimo, ya que el cuerpo pierde su sincronización interna y con el ambiente.
Tabla Comparativa: Núcleo Central vs. Corteza del NSQ
| Característica | Núcleo Central (Core) | Corteza (Shell) |
|---|---|---|
| Ubicación Principal | Central, recibe entradas directas del TRH | Periférica, rodea el núcleo central |
| Principales Neuropéptidos | VIP, GRP | AVP |
| Entradas Primarias | Tracto Retinohipotalámico (TRH) | Entradas menos directas (recibe procesamiento del core) |
| Función Clave | Procesamiento de la señal fótica, sincronización interna del NSQ | Proyecciones eferentes a otras áreas del cerebro, coordinación con ritmos conductuales (ej. alimentación, sed) |
En resumen, el Núcleo Supraquiasmático es una estructura cerebral fundamental que actúa como nuestro reloj biológico maestro. Su capacidad para recibir señales de luz y coordinar una vasta red de ritmos circadianos es esencial para nuestra salud y bienestar. Los desajustes en este sistema pueden tener amplias repercusiones, subrayando la importancia de mantener la salud circadiana a través de hábitos adecuados de sueño y exposición a la luz. La investigación continua sobre el NSQ sigue revelando nuevas formas en que nuestro ritmo interno moldea quiénes somos.
Si quieres conocer otros artículos parecidos a El NSQ: Reloj Maestro del Cerebro puedes visitar la categoría Neurociencia.
