La Proteína Quinasa A (PKA), también conocida como proteína quinasa dependiente de AMP cíclico, es una enzima clave en la señalización celular que desempeña múltiples roles esenciales en diversos tipos de células, incluidas las neuronas. Su capacidad para responder a los niveles intracelulares del segundo mensajero AMP cíclico (cAMP) la posiciona como un nodo central en cascadas de señalización iniciadas por una variedad de estímulos, como hormonas y neurotransmisores.
Descubierta por Edmond H. Fischer y Edwin G. Krebs en 1968, quienes fueron galardonados con el Premio Nobel por su trabajo en la fosforilación, la PKA es una de las quinasas de proteínas más estudiadas. En mamíferos, la PKA existe típicamente como un tetrámero inactivo compuesto por dos subunidades reguladoras y dos subunidades catalíticas. Las subunidades reguladoras contienen dominios de unión a cAMP y un dominio que interactúa con las subunidades catalíticas, así como un dominio auto-inhibitorio. Las subunidades catalíticas, por su parte, albergan el sitio activo para la unión y hidrólisis de ATP, necesario para la fosforilación.
Existen al menos dos tipos principales de PKA en células de mamífero: Tipo I y Tipo II. Mientras que la PKA Tipo I se encuentra predominantemente en el citosol, la PKA Tipo II está anclada a diversas estructuras subcelulares a través de sus subunidades reguladoras y proteínas ancla específicas. Esta localización precisa es fundamental para dirigir la actividad de la PKA hacia sustratos específicos en compartimentos celulares definidos, permitiendo respuestas localizadas a las señales.
- Activación y Mecanismo de Acción de PKA
- La PKA en el Contexto Neuronal: Localización Crítica
- MAP2: El Ancla Dominante en Neuronas
- Translocación Dinámica a las Espinas tras la Activación
- Importancia Funcional de la Localización Dinámica
- Tabla Comparativa: PKA Tipo II en Neuronas
- Preguntas Frecuentes (FAQ)
- ¿Qué es PKA en el contexto de las neuronas?
- ¿Dónde se localiza la PKA en una neurona en estado de reposo?
- ¿Cómo se mantiene la PKA en los ejes dendríticos?
- ¿Qué sucede con la PKA cuando una neurona se activa (por ejemplo, por neuromoduladores)?
- ¿Por qué es importante que la PKA se mueva a las espinas dendríticas?
Activación y Mecanismo de Acción de PKA
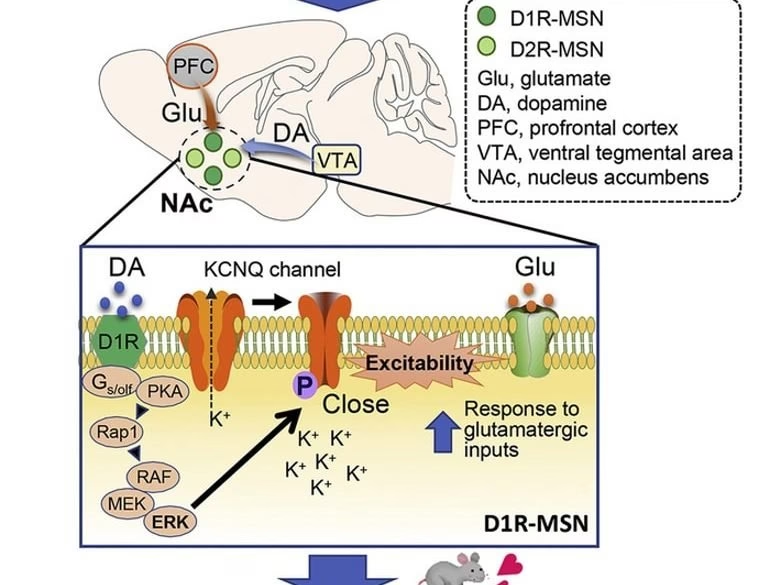
La activación clásica de la PKA ocurre cuando los niveles intracelulares de cAMP aumentan en respuesta a una señal. Por ejemplo, en las neuronas, la activación de receptores acoplados a proteínas G (GPCRs) por neuromoduladores como la norepinefrina o la dopamina puede estimular la adenilil ciclasa a través de la proteína Gs, lo que cataliza la conversión de ATP a cAMP. Cuatro moléculas de cAMP se unen a las dos subunidades reguladoras del tetrámero de PKA. Esta unión induce un cambio conformacional en las subunidades reguladoras, provocando su disociación de las subunidades catalíticas. Las subunidades catalíticas libres son ahora activas y pueden migrar a diferentes ubicaciones dentro de la célula para fosforilar sus proteínas sustrato.
Una vez liberadas, las subunidades catalíticas activas transfieren un grupo fosfato del ATP a residuos de serina o treonina específicos en las proteínas diana, en un contexto mínimo de Arg-Arg-X-Ser/Thr. Esta fosforilación puede alterar la actividad, localización o interacción de la proteína sustrato, lo que a su vez modula diversas funciones celulares. La PKA puede afectar las células de dos maneras principales: mediante fosforilación directa de proteínas existentes o afectando la síntesis de nuevas proteínas. En el segundo caso, la PKA puede fosforilar factores de transcripción como CREB (elemento de respuesta a cAMP), que luego se une a secuencias de ADN específicas (elementos de respuesta a cAMP o CRE) para alterar la expresión génica. Este último mecanismo es más lento y puede tardar horas o días.
La inactivación de PKA se regula mediante varios mecanismos. Uno importante es la hidrólisis de cAMP a AMP por enzimas fosfodiesterasas (PDEs). Muchas PDEs son a su vez sustratos de PKA, creando un circuito de retroalimentación negativa donde la PKA activada promueve la degradación del cAMP que la activó. Además, la actividad de la subunidad catalítica puede ser regulada por fosforilación o por la unión a inhibidores específicos, como el inhibidor de PKA termoestable (PKI).

La PKA en el Contexto Neuronal: Localización Crítica
En el ámbito de la neurociencia, la PKA es fundamental para procesos como la plasticidad sináptica, la memoria y el aprendizaje. Sin embargo, para llevar a cabo sus diversas funciones de manera efectiva en la compleja estructura de una neurona, la PKA no puede estar distribuida uniformemente. Su localización subcelular y su capacidad para ser dirigida a sitios de acción específicos son cruciales.
Investigaciones utilizando microscopía de fluorescencia en neuronas piramidales del hipocampo y la corteza han revelado que la distribución de la PKA Tipo II no es homogénea. En estado de reposo, la PKA Tipo II se encuentra concentrada predominantemente en los ejes dendríticos (dendritic shafts), en comparación con el soma, los axones y las espinas dendríticas. Esta observación inicial, realizada tanto con PKA marcada con fluorescencia como con la PKA endógena detectada por inmunocitoquímica, sugiere un mecanismo activo que mantiene la enzima alejada de las espinas en condiciones basales.
Esta distribución espacial diferencial está controlada en gran medida por las Proteínas Ancla de Quinasa A (AKAPs). Las AKAPs son proteínas que se unen a las subunidades reguladoras de la PKA, anclándola a ubicaciones específicas dentro de la célula. Estas AKAPs a menudo actúan como centros de señalización, reuniendo a la PKA con sus sustratos, otras quinasas, fosfatasas y enzimas que regulan el cAMP, como las adenilil ciclasas y las fosfodiesterasas.
MAP2: El Ancla Dominante en Neuronas
Para identificar qué AKAP es responsable de anclar la PKA Tipo II en las dendritas, se realizaron estudios funcionales y de deleción. Se observó que la distribución de la PKA Tipo II se asemeja a la de la proteína de unión a microtúbulos MAP2 (Microtubule-Associated Protein 2), que fue una de las primeras AKAPs identificadas. Experimentos demostraron que el dominio de unión a AKAPs en las subunidades reguladoras RIIβ es esencial para esta exclusión de las espinas y concentración en el eje dendrítico.
Aún más convincente, la eliminación genética del sitio de unión a PKA en MAP2 en ratones resultó en una alteración significativa de la localización de la PKA Tipo II. En neuronas con esta deleción de MAP2, la PKA Tipo II ya no estaba restringida a los ejes dendríticos e incluso mostró una ligera tendencia a enriquecerse en las espinas. Estos resultados indican firmemente que MAP2 es la AKAP dominante en las neuronas piramidales que ancla la PKA Tipo II a los ejes dendríticos en estado de reposo.
Translocación Dinámica a las Espinas tras la Activación
La localización de la PKA no es estática. Es un proceso dinámico que cambia con la actividad neuronal. Un hallazgo crucial es que, tras la elevación de los niveles intracelulares de cAMP (por ejemplo, mediante la aplicación de activadores de adenilil ciclasa como forskolin/IBMX, o neuromoduladores endógenos como norepinefrina o dopamina), la subunidad catalítica de la PKA experimenta una rápida translocación.

Las subunidades catalíticas, que inicialmente están tethered a las subunidades reguladoras ancladas en el eje dendrítico por MAP2, se disocian al unirse el cAMP. Una vez libres, estas subunidades catalíticas se mueven rápidamente y se enriquecen en las espinas dendríticas cercanas. Mientras tanto, las subunidades reguladoras permanecen ancladas en los ejes dendríticos. Este movimiento de la subunidad catalítica hacia las espinas sugiere que allí se encuentran sustratos de PKA abundantes esperando ser fosforilados tras la activación.
Las mediciones de movilidad mediante proteínas fluorescentes fotoactivables confirmaron este modelo. La movilidad de la subunidad catalítica en los ejes dendríticos aumentó significativamente tras la elevación de cAMP, lo que es consistente con su liberación de un complejo anclado. Curiosamente, la movilidad de la subunidad catalítica en las espinas no cambió significativamente tras la activación, lo que podría indicar que una vez que entra en la espina, se une rápidamente a sus sustratos o a otros componentes que restringen su difusión.
Importancia Funcional de la Localización Dinámica
La distribución espacial y la translocación dependiente de la actividad de la PKA Tipo II no son meras curiosidades bioquímicas; son determinantes críticos de la función de la PKA en las neuronas. La investigación ha demostrado que el gradiente espacial de PKA Tipo II entre los ejes dendríticos y las espinas es esencial para la regulación de la fuerza sináptica y la potenciación a largo plazo (LTP).
La LTP es un mecanismo celular considerado clave para el aprendizaje y la memoria, que implica un fortalecimiento duradero de la comunicación entre neuronas en sinapsis específicas. La capacidad de la PKA activada para translocarse a las espinas, donde residen muchos componentes cruciales de la sinapsis, le permite fosforilar objetivos locales y modular la eficacia sináptica de manera precisa. Por lo tanto, no solo la cantidad total de PKA activa, sino también dónde y cuándo se activa y se mueve, es fundamental para la plasticidad sináptica y, en última instancia, para la función cerebral.
La intrincada regulación de la localización de PKA mediante AKAPs como MAP2 en los ejes dendríticos, y la posterior translocación de su subunidad catalítica a las espinas tras la activación, representa un mecanismo sofisticado que permite a las neuronas dirigir la señalización de PKA a compartimentos subcelulares específicos. Esto asegura que las respuestas celulares a las señales extracelulares sean localizadas, eficientes y apropiadas para la función neuronal, especialmente en el contexto de la plasticidad sináptica.
Tabla Comparativa: PKA Tipo II en Neuronas
| Característica | PKA Tipo II en Reposo (Bajo cAMP) | PKA Tipo II Activada (Alto cAMP) |
|---|---|---|
| Estructura y Estado | Tetrámero (2 Subunidades Reguladoras + 2 Catalíticas). Principalmente asociado a AKAPs (MAP2). | Subunidad Catalítica (C) libre. Subunidades Reguladoras (R) permanecen ancladas. |
| Ubicación Principal | Concentrada en Ejes Dendríticos. Excluida de Espinas Dendríticas. | La Subunidad Catalítica se transloca y enriquece en Espinas Dendríticas. Las Subunidades Reguladoras permanecen en Ejes Dendríticos. |
| Movilidad de la Subunidad Catalítica | Menor (anclada). | Mayor (liberada en el eje dendrítico). |
| Rol Funcional Implicado | Mantenimiento del estado basal. | Modulación de la Fuerza Sináptica, Potenciación a Largo Plazo (LTP). |
| Principal Ancla | MAP2. | Las subunidades catalíticas libres no están ancladas. |
Preguntas Frecuentes (FAQ)
¿Qué es PKA en el contexto de las neuronas?
En las neuronas, la PKA es una enzima clave que responde al aumento de cAMP, un segundo mensajero. Regula diversas funciones neuronales mediante la fosforilación de proteínas, siendo crucial para la plasticidad sináptica y la comunicación entre neuronas.

¿Dónde se localiza la PKA en una neurona en estado de reposo?
En reposo, la PKA Tipo II se encuentra principalmente concentrada en los ejes (shafts) de las dendritas, siendo relativamente excluida de las espinas dendríticas.
¿Cómo se mantiene la PKA en los ejes dendríticos?
La PKA Tipo II es anclada en los ejes dendríticos por proteínas específicas llamadas AKAPs (Proteínas Ancla de Quinasa A). La investigación sugiere que MAP2 es la AKAP dominante responsable de este anclaje en las neuronas piramidales.
¿Qué sucede con la PKA cuando una neurona se activa (por ejemplo, por neuromoduladores)?
Cuando los niveles de cAMP aumentan debido a la activación neuronal, la subunidad catalítica de la PKA se disocia de las subunidades reguladoras ancladas. La subunidad catalítica libre se mueve rápidamente hacia las espinas dendríticas.
¿Por qué es importante que la PKA se mueva a las espinas dendríticas?
Las espinas dendríticas son los principales sitios de contacto sináptico y contienen muchos sustratos clave de la PKA. La translocación de la PKA activada a las espinas permite la fosforilación localizada de estas proteínas, lo cual es esencial para modificar la fuerza de las sinapsis y procesos como la potenciación a largo plazo (LTP).
En resumen, la PKA es una enzima vital en el sistema nervioso, cuya función está íntimamente ligada a su localización subcelular dinámica. El anclaje de la PKA Tipo II a los ejes dendríticos mediante MAP2 y su capacidad para translocarse a las espinas dendríticas tras la activación por cAMP son mecanismos fundamentales que permiten a las neuronas regular la fuerza sináptica y la plasticidad, sentando las bases para procesos cognitivos complejos.
Si quieres conocer otros artículos parecidos a PKA en Neuronas: Anclaje y Translocación puedes visitar la categoría Neurociencia.
