Para adentrarnos en el estudio del intrincado universo que compone nuestros órganos y tejidos, necesitamos herramientas que nos permitan observar estructuras invisibles a simple vista. La histología, la ciencia que estudia los tejidos biológicos, utiliza un conjunto fundamental de procedimientos conocido como técnica histológica. Este proceso meticuloso prepara las muestras biológicas para que puedan ser examinadas bajo el microscopio, revelando detalles celulares y arquitecturas tisulares cruciales para la investigación y el diagnóstico.

La técnica histológica es, en esencia, una serie de operaciones cuidadosamente orquestadas aplicadas a una muestra de tejido biológico. Su objetivo principal es preservar la estructura del tejido tal como estaba en el organismo vivo, hacerlo lo suficientemente rígido para cortarlo en secciones extremadamente finas y, finalmente, colorearlo para que las diferentes estructuras sean visibles y distinguibles al microscopio. A lo largo de los años, esta técnica ha evolucionado, pero sus pasos fundamentales permanecen como la base de la histología.
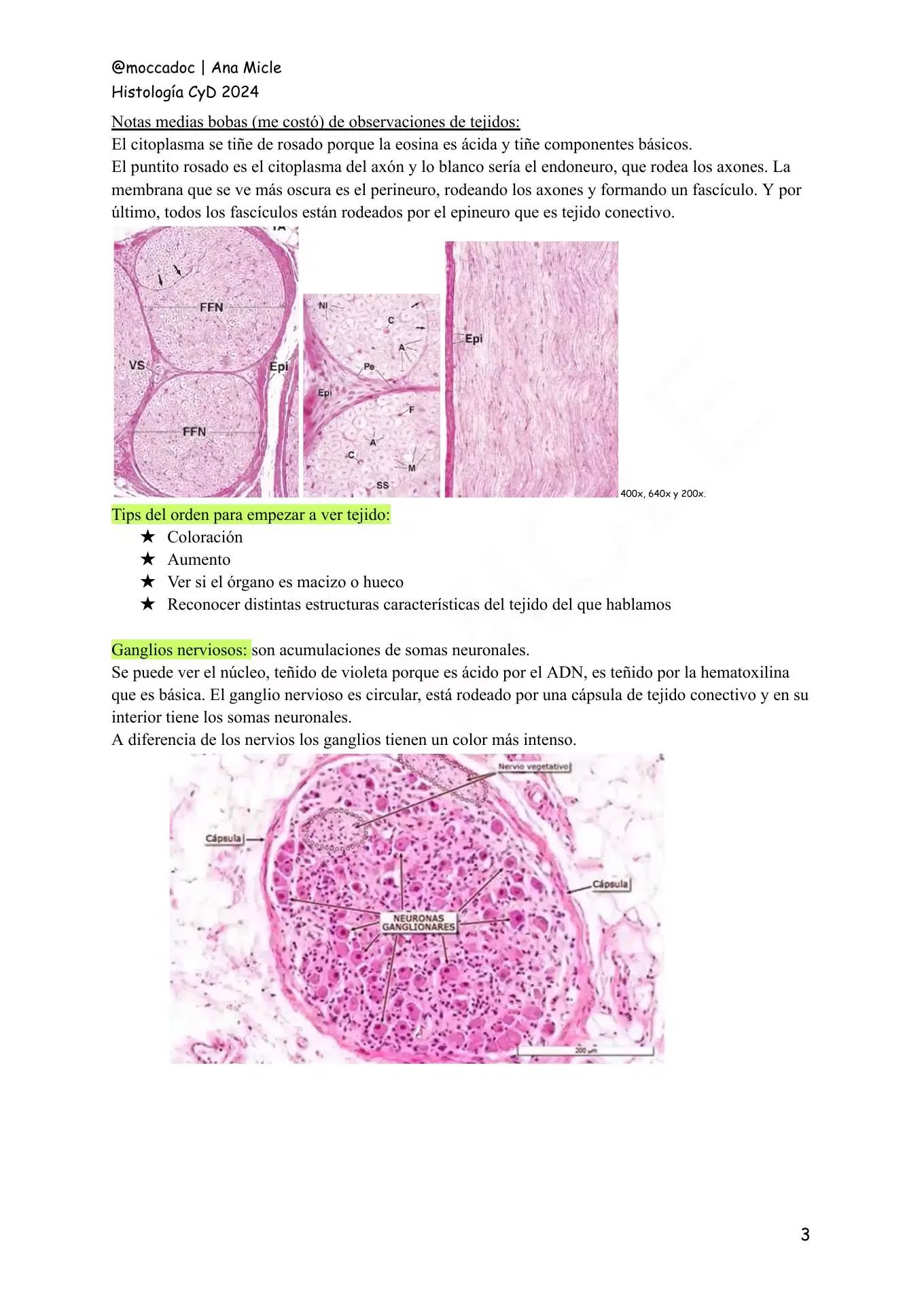
Aunque la forma exacta de enumerar los pasos puede variar ligeramente entre laboratorios o autores, la secuencia general busca llevar el tejido desde su estado fresco a una preparación microscópica permanente y teñida. Algunas fuentes enumeran hasta diez pasos, mientras que otras agrupan ciertos procedimientos. La observación final al microscopio, aunque el objetivo de todo el proceso, a menudo no se considera un paso técnico per se, sino el fin último al que sirve la técnica.
El primer eslabón en esta cadena es la obtención del material histológico. Sin una muestra adecuada, no hay estudio posible. Los tejidos pueden obtenerse de diversas maneras, dependiendo de si provienen de un individuo vivo o de un cadáver, y del tipo de tejido o lesión que se necesita estudiar. Las muestras de individuos vivos se obtienen mediante biopsias. Existen varios tipos de biopsias, adaptadas a diferentes situaciones: la biopsia excisional, donde se extrae la lesión completa; la biopsia incisional, donde solo se toma una sección de la lesión; la biopsia endoscópica, colposcópica, la punción aspiración con aguja fina (PAAF) para tejidos líquidos o semilíquidos, y la punción con aguja gruesa (Tru-cut o PAAG) para tejidos más densos como la médula ósea. Cuando la muestra se obtiene de un cadáver, el procedimiento se denomina necropsia o autopsia.
Una vez obtenida la muestra, el tiempo es crucial. El tejido comienza a degradarse inmediatamente después de ser separado del organismo vivo mediante procesos de autólisis (autodigestión por enzimas celulares) y putrefacción (degradación por microorganismos). Para detener estos procesos y conservar la morfología original, se aplica la fijación. Este paso consiste en sumergir el tejido en una sustancia fijadora, usualmente líquida. La fijación no solo previene la degradación, sino que también endurece el tejido, facilitando los pasos posteriores, mejora la captación de los colorantes y tiene acción antiséptica. El fijador más común para la microscopía de campo claro es el formol al 10% (formal formaldehído al 4%). Para estudios más detallados, como la microscopía electrónica, se requieren fijadores específicos como paraformaldehído, glutaraldehído y tetróxido de osmio. Es vital que el fijador penetre bien en el tejido, por lo que el tamaño de la muestra influye en el tiempo de fijación. Una fijación inadecuada puede comprometer todo el proceso.
Tras la fijación, el tejido debe someterse a lavados. El propósito de este paso es eliminar el exceso de fijador químico. Si el fijador residual permanece en el tejido, puede interferir con los pasos subsiguientes, especialmente la infiltración y el corte. Generalmente, se utiliza agua destilada para este lavado.
Los siguientes pasos preparan el tejido para ser incluido en un medio sólido que permita cortes muy finos. El medio de inclusión más común es la parafina, que es una sustancia hidrófoba (no se mezcla con agua). Sin embargo, el tejido, después de la fijación (generalmente en soluciones acuosas como el formol) y los lavados, está lleno de agua. Por lo tanto, es necesario eliminar el agua del tejido mediante un proceso llamado deshidratación. Esto se logra pasando la muestra por una serie de soluciones de alcohol en concentraciones crecientes (por ejemplo, de 50% a 100% alcohol puro). A medida que la concentración de alcohol aumenta, el agua es gradualmente reemplazada por alcohol.
Una vez que el tejido está completamente deshidratado e impregnado de alcohol puro, este alcohol debe ser eliminado, ya que tampoco es miscible con la parafina. Aquí interviene el paso de aclaramiento. Se sustituye el alcohol por una sustancia que sea miscible tanto con el alcohol como con la parafina. El disolvente orgánico más utilizado para este propósito es el xilol (xileno), aunque pueden usarse otros como el benceno. Al pasar el tejido por varios baños de xilol, el alcohol es gradualmente reemplazado. Durante este proceso, el tejido a menudo pierde su color, de ahí el término "aclaramiento". El xilol penetra profundamente en el tejido, preparándolo para el siguiente paso.

Con el tejido completamente impregnado de xilol, se procede a la infiltración. La muestra se sumerge en parafina histológica que ha sido calentada por encima de su punto de fusión para que esté en estado líquido. Dado que el xilol es un disolvente de la parafina, la parafina líquida caliente puede penetrar en el tejido, reemplazando gradualmente el xilol. Esto se realiza generalmente en varios baños de parafina para asegurar una completa impregnación. La deshidratación, el aclaramiento y la infiltración, que históricamente se hacían manualmente, hoy en día se realizan de manera eficiente y automática en máquinas procesadoras de tejidos, optimizando el tiempo y la calidad del proceso.
Después de la infiltración, el tejido lleno de parafina líquida necesita solidificarse para formar un bloque que pueda ser cortado. Este paso se denomina inclusión o confección de bloques. La muestra infiltrada se coloca en un molde, que se rellena con parafina líquida fresca. A menudo, se utiliza una parte del casete de plástico donde se procesó la muestra para crear un soporte en el bloque solidificado. El molde con la parafina y el tejido se enfría rápidamente (por ejemplo, en una placa fría a 4°C) para que la parafina solidifique, formando un bloque sólido y homogéneo con el tejido embebido en su interior. Es fundamental orientar correctamente el tejido dentro del molde antes de que la parafina solidifique, especialmente si se necesita un corte específico (horizontal, vertical, transversal) para evaluar estructuras particulares o márgenes de resección.
Con el bloque de parafina listo, el siguiente paso es la microtomía, que es el proceso de obtener cortes extremadamente delgados del tejido incluido. Se utiliza un instrumento de precisión llamado micrótomo, equipado con una cuchilla muy afilada. El bloque de parafina se sujeta firmemente en el micrótomo, y la cuchilla corta secciones de tejido de unos pocos micrómetros de grosor, generalmente entre 3 y 10 micras. Para que la luz del microscopio pueda atravesar fácilmente el tejido y permitir una buena visualización celular, un grosor ideal es de 3-5 micras. Los cortes obtenidos se colocan cuidadosamente en un baño de flotación con agua tibia (aproximadamente 35-45°C). El calor del agua ayuda a que las secciones de parafina, que tienden a arrugarse al ser cortadas, se estiren y queden planas. Una vez estirados, los cortes se "pescan" cuidadosamente con un portaobjetos de vidrio. El portaobjetos se marca con la identificación de la muestra y la fecha, listo para los pasos siguientes.
Los tejidos en sí mismos son en gran parte transparentes y carecen de coloración intrínseca que permita distinguir fácilmente las diferentes estructuras celulares y tisulares. Por lo tanto, es imprescindible aplicar tinción para visualizar la morfología. La tinción utiliza colorantes que tienen afinidad por diferentes componentes celulares y tisulares, tiñéndolos de colores contrastantes. Antes de la tinción, la parafina debe ser eliminada del portaobjetos, ya que la mayoría de los colorantes son acuosos y no penetrarían la parafina hidrófoba. Esto se logra calentando los portaobjetos en una estufa para derretir la parafina y luego pasándolos por una serie de alcoholes en concentración decreciente para rehidratar el tejido.
La tinción más utilizada y considerada de rutina es la de Hematoxilina y Eosina (H&E). Es una tinción bicrómica que proporciona una excelente visión general de la arquitectura tisular. La Hematoxilina es un colorante básico que tiñe las estructuras ácidas, como los núcleos celulares (debido a la presencia de ADN) y el retículo endoplasmático rugoso, de un color azul purpúreo a negro. La Eosina es un colorante ácido que tiñe las estructuras básicas, como el citoplasma celular y las fibras de colágeno, de color rosado a rojo. Además de la H&E, existen numerosas otras tinciones especiales (tricrómico de Masson, PAS, Perls, Plata metenamina, Ziehl-Neelsen, Van Gieson, Azul Alcian, Sudán III, Rojo Congo, etc.) que se utilizan para poner en evidencia estructuras o sustancias específicas (como fibras de colágeno, mucopolisacáridos, hierro, hongos, bacterias, fibras elásticas, etc.) que no se visualizan adecuadamente con la tinción de rutina.
Después de la tinción, para que la preparación sea permanente y pueda ser observada al microscopio de manera óptima, se realiza el montaje. Esto implica colocar un cubreobjetos sobre el corte de tejido teñido, utilizando un medio de montaje. La mayoría de los medios de montaje son resinas sintéticas que son miscibles con disolventes orgánicos como el xileno, pero no con agua. Por lo tanto, antes de aplicar el medio de montaje, el tejido rehidratado y teñido debe ser nuevamente deshidratado (pasando por alcoholes de concentración creciente) y aclarado (con xileno) para que el medio de montaje pueda penetrar correctamente. El medio de montaje sella el tejido entre el portaobjetos y el cubreobjetos, protegiéndolo y preservándolo para su observación a largo plazo.
El paso final, aunque a menudo no se cuenta como parte de la técnica preparatoria, es la observación al microscopio. La laminilla con el tejido teñido y montado se examina bajo un microscopio (generalmente de campo claro) a diferentes aumentos. El patólogo o investigador observa las células, su morfología, la arquitectura del tejido y cualquier alteración presente para llegar a un diagnóstico o para realizar un estudio detallado. Es aquí donde se interpreta toda la información revelada por la técnica histológica.

La técnica histológica es una herramienta indispensable en medicina y biología. Permite el diagnóstico de una amplia gama de enfermedades, desde infecciones hasta cáncer, al permitir la evaluación detallada de las alteraciones celulares y tisulares. Es la base de la anatomía patológica y una técnica fundamental en la investigación científica para comprender la estructura y función de los organismos a nivel microscópico.
| Paso (Lista 1) | Paso (Lista 2) | Descripción/Propósito |
|---|---|---|
| Obtención del material histológico | Recogida de la muestra | Adquirir el tejido de interés (biopsia, necropsia). |
| Proceso de fijación | Fijación | Conservar la estructura, prevenir degradación, endurecer. |
| Lavados | (Implícito en Inclusión/Deshidratación) | Eliminar exceso de fijador. |
| Deshidratación | (Parte de Inclusión) | Eliminar agua del tejido (con alcoholes). |
| Aclaramiento | (Parte de Inclusión) | Sustituir alcohol por sustancia miscible con parafina (xilol). |
| Infiltración | (Parte de Inclusión) | Impregnar el tejido con parafina líquida. |
| Inclusión | Inclusión / Confección de los bloques | Embeber el tejido en parafina sólida para formar un bloque. |
| Microtomía | Corte histológico – Microtomía | Cortar el bloque en secciones muy finas. |
| Tinción | Tinción de los cortes histológicos | Colorear las estructuras tisulares y celulares para visualizarlas. |
| (No considerado por algunos) Observación | Observación al microscopio y diagnóstico | Examinar la preparación teñida bajo el microscopio. |
| (No mencionado como paso separado) | Recepción y registro de la muestra | Identificar y documentar la muestra al llegar al laboratorio. |
| (No mencionado como paso separado) | Descripción macroscópica y corte | Examinar la muestra a simple vista y seleccionar/cortar áreas para procesar. |
| (No mencionado como paso separado) | Montaje de la preparación histológica | Colocar cubreobjetos con medio de montaje para preservar la muestra. |
Como se puede observar, las listas de pasos pueden variar ligeramente en su granularidad o denominación, pero el proceso fundamental de preparar un tejido para su observación microscópica sigue una lógica secuencial para preservar, endurecer, cortar y colorear la muestra.
Preguntas Frecuentes sobre la Técnica Histológica:
¿Cuántos pasos tiene la técnica histológica?
El número exacto de pasos puede variar según cómo se agrupen los procesos. Generalmente, se describen entre 8 y 10 pasos principales, desde la obtención de la muestra hasta la tinción y montaje. La observación final es el objetivo, no siempre contado como un paso técnico.
¿Por qué es necesaria la fijación?
La fijación es crucial para detener la degradación del tejido después de su extracción (autólisis y putrefacción), preservar su estructura lo más fielmente posible a su estado original en el organismo vivo, endurecerlo para facilitar el corte y mejorar la afinidad por los colorantes.
¿Qué es la deshidratación y por qué se hace?
La deshidratación es la eliminación del agua del tejido, generalmente usando alcoholes de concentración creciente. Se hace porque el medio de inclusión más común (parafina) es hidrófobo y no se mezclará con el agua presente en el tejido después de la fijación y lavado.
¿Qué es el aclaramiento?
Es el paso donde el alcohol utilizado para la deshidratación es reemplazado por una sustancia (como el xilol) que es miscible tanto con el alcohol como con la parafina. Esto prepara el tejido para la infiltración con parafina y a menudo hace que el tejido se vuelva translúcido.
¿Por qué se incluye el tejido en parafina?
La inclusión en parafina proporciona al tejido un soporte sólido y homogéneo. La parafina endurece el tejido de manera uniforme, permitiendo que se puedan obtener cortes muy finos (de micras de grosor) con el micrótomo, algo que sería imposible de hacer con el tejido blando.
¿Qué es la microtomía?
Es el proceso de cortar las secciones muy finas (histológicas) del bloque de tejido incluido en parafina, utilizando un instrumento llamado micrótomo.
¿Por qué se tiñen los tejidos?
Los tejidos en estado natural son mayormente transparentes y sin coloración distintiva. La tinción utiliza colorantes que se unen selectivamente a diferentes componentes celulares y tisulares, haciéndolos visibles y permitiendo diferenciar estructuras como núcleos, citoplasma, fibras, etc., bajo el microscopio.
¿Qué es la tinción de Hematoxilina y Eosina (H&E)?
Es la tinción de rutina más común. La Hematoxilina tiñe las estructuras ácidas (como los núcleos) de azul-púrpura, y la Eosina tiñe las estructuras básicas (como el citoplasma) de rosa-rojo, proporcionando una visión general de la morfología tisular.
¿Qué es el montaje de la preparación?
Es el paso final donde se coloca un cubreobjetos sobre el corte de tejido teñido, utilizando un medio de montaje. Esto sella la muestra, la protege, la preserva para su estudio a largo plazo y optimiza su visualización al microscopio.
En resumen, la técnica histológica es un pilar fundamental en la biología y la medicina, un proceso complejo pero estandarizado que nos permite transformar una diminuta muestra de tejido en una valiosa fuente de información para el diagnóstico, la comprensión de las enfermedades y el avance del conocimiento científico.
Si quieres conocer otros artículos parecidos a El Viaje del Tejido: Técnica Histológica puedes visitar la categoría Neurociencia.
