La optogenética representa un avance extraordinario en la neurociencia, ofreciendo una herramienta poderosa para investigar y potencialmente tratar trastornos neurológicos. Esta técnica innovadora combina métodos genéticos y ópticos para lograr un control preciso, tanto temporal como espacial, sobre eventos definidos en células específicas dentro de tejido vivo. Durante mucho tiempo, la neurociencia se enfrentó a una disyuntiva entre la especificidad temporal y la espacial al intentar manipular la actividad neuronal. La optogenética, al permitir la estimulación de células con luz, parece resolver este problema, abriendo nuevas vías para comprender el funcionamiento del cerebro y controlar el comportamiento. Aunque hasta ahora su aplicación principal ha sido en investigación animal, su potencial para la investigación y terapia en humanos es inmenso.

La idea de utilizar la luz para controlar células no es nueva. Ya en 1979, Francis Crick, un visionario en el campo, anticipó la dificultad de la neurociencia para dirigirse a células individuales in vivo sin afectar a otras, sugiriendo la luz como una posible solución. Por esa época, se descubrió que ciertos microorganismos poseen proteínas que responden a la luz. Un hito crucial fue el descubrimiento de la bacteriorrodopsina por Oesterhelt y Stoeckenius en 1971, una bomba de iones activada por fotones de luz. Pronto se identificaron otros miembros de esta familia, como la halorrodopsina (Matsuno-Yagi y Mukohata, 1977) y la canalrodopsina (Nagel et al., 2002). El verdadero punto de inflexión llegó en 2005, cuando investigadores del laboratorio de Karl Deisseroth demostraron por primera vez un sistema optogenético de un solo componente (Boyden et al., 2005). Al año siguiente, en 2006, nació oficialmente el término “optogenética”.
¿Cómo Funciona la Optogenética? El Proceso Paso a Paso
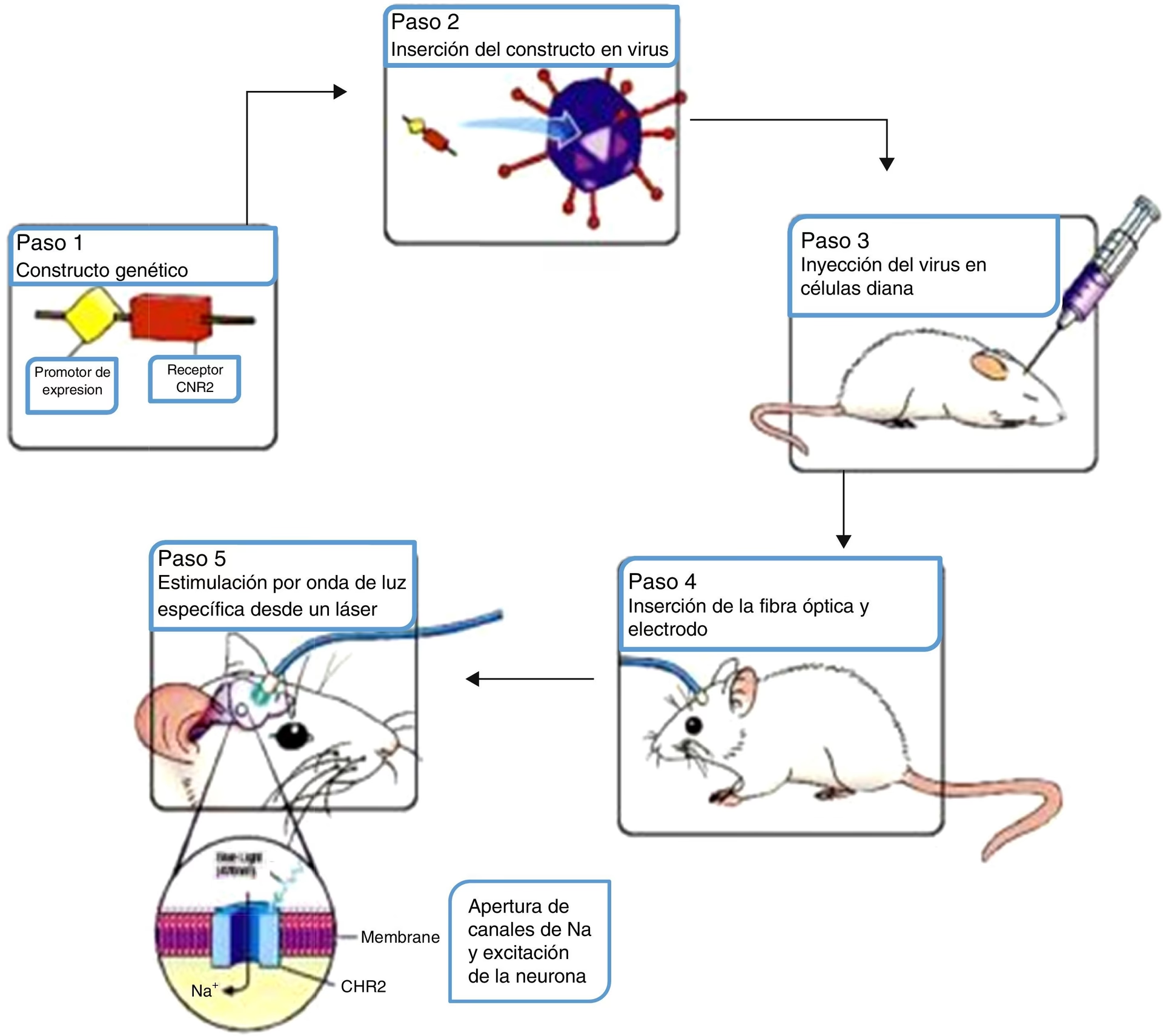
Estrictamente hablando, la optogenética implica la combinación de manipulación genética y óptica. Se ha aplicado con éxito en diversos modelos animales, incluyendo C. elegans, mosca, pez cebra, ratón, rata y primates. El objetivo final, particularmente en neurociencia cognitiva, es controlar el comportamiento de mamíferos en movimiento libre mediante la administración de luz. Para lograr esto, se siguen varios pasos fundamentales:
1. Especificación de Opsinass: El primer paso es seleccionar las proteínas sensibles a la luz, llamadas opsinas. Existen dos superfamilias principales: las opsinas microbianas (tipo I) y las opsinas animales (tipo II). Ambas requieren retinal (un cofactor orgánico relacionado con la vitamina A) para convertir la luz en energía, y la unión de retinal las convierte en rodopsinas. Diversos tipos de opsinas microbianas han demostrado ser adecuadas para el control optogenético, reaccionando de manera diferente a la estimulación lumínica de longitudes de onda particulares. Por ejemplo, la luz azul hace que la canalrodopsina-2 (ChR2) despolarice rápidamente una neurona, activándola. Las opsinas utilizadas varían en sus propiedades de conductancia iónica, actuando en escalas de tiempo que van desde milisegundos hasta decenas de minutos. Ejemplos avanzados incluyen ChETAs, que permiten un control ultrarrápido, y opsinas de función escalonada (step-function opsins - SFOs), diseñadas para mostrar actividad prolongada después de terminar el estímulo lumínico. Para la inhibición neuronal, se utilizan bombas activadas por luz, como la Halorrodopsina de Natronomonas pharaonis (NpHR), que hiperpolariza la neurona en reacción a la luz amarilla. El control bioquímico se puede lograr utilizando opsinas animales de tipo II modificadas, llamadas optoXRs, que permiten la señalización intracelular mediada por receptores en respuesta a la luz verde.
2. Introducción de Genes de Opsinas: Para que las células de mamíferos expresen opsinas microbianas (ya que simplemente administrar la proteína no funciona), es necesario introducir un gen que codifique la opsina deseada en células específicas. Una técnica común es inyectar un virus (generalmente inofensivo) que transporte el gen de la opsina al cerebro del mamífero. La principal desventaja de los sistemas de expresión viral es que no pueden transportar grandes cantidades de material genético, pero tienen la ventaja de lograr altos niveles de expresión de la opsina. Otra opción es usar animales transgénicos (knock-in) que posean las opsinas desde el nacimiento, lo que permite estudiar el desarrollo del sistema, aunque los niveles de expresión suelen ser más bajos. Otras estrategias incluyen el uso de animales Cre-driver, virus Cre-dependientes o electroporación in utero. También es posible dirigirse a circuitos mediante la estimulación de axones en lugar del soma ("projection targeting") o usar virus que se transducen a lo largo de las terminales axónicas. A menudo se utilizan estrategias combinadas para optimizar la especificidad y la expresión.
3. Administración de Luz: Finalmente, la luz debe ser entregada al tejido objetivo. Esto se logra típicamente mediante una fibra óptica insertada directamente en el cerebro a través de una cánula implantada crónicamente y fijada al cráneo. La luz láser o de un LED se puede canalizar a través de esta fibra óptica para estimular las células que expresan la opsina. Para estudios in vitro, un láser o LED se puede acoplar directamente al trayecto de luz del microscopio. Para estructuras cerebrales más profundas, las fibras ópticas son esenciales, ya que la intensidad de la luz disminuye drásticamente al penetrar el tejido (aproximadamente un 1% por mm de profundidad). Se están desarrollando sistemas inalámbricos y opsinas activadas por longitudes de onda más largas (rojo o infrarrojo cercano), que dispersan menos la luz, para reducir la invasividad y mejorar la penetración.
Las opsinas microbianas se han centrado principalmente en acoplar directamente la luz al transporte rápido de iones (activación o inhibición neuronal rápida), mientras que las opsinas animales modificadas se utilizan para el control bioquímico mediado por receptores.

Aplicaciones de la Optogenética en Neurociencia Cognitiva
La optogenética ha revolucionado la neurociencia al permitir a los investigadores abordar preguntas fundamentales sobre las bases moleculares, celulares y circuitales del comportamiento, superando la limitación de la especificidad temporal y espacial. A diferencia de la estimulación eléctrica, que tiene alta resolución temporal pero baja especificidad espacial (afecta a muchas neuronas a la vez), o las manipulaciones farmacológicas y genéticas, que pueden ser más específicas para tipos de células pero carecen de precisión temporal, la optogenética combina una alta especificidad temporal con precisión celular.
Esta técnica se ha aplicado con éxito en una amplia gama de áreas relevantes para la neurociencia cognitiva:
- Neuromodulación y Recompensa: Se ha utilizado para aclarar la relación entre la actividad de las neuronas dopaminérgicas (DA) y el refuerzo positivo. Estudios han demostrado que la estimulación óptica de neuronas DA en el área tegmental ventral puede inducir auto-estimulación intracraneal y que la actividad dopaminérgica fásica es suficiente para mediar el condicionamiento conductual. La optogenética también ha revelado roles opuestos de las neuronas D1+ y D2+ en el núcleo accumbens en el procesamiento de la recompensa de cocaína. Incluso, se ha demostrado cómo la modulación de la actividad de neuronas individuales en las vías directa e indirecta de los ganglios basales puede afectar los síntomas del Parkinson.
- Sueño y Sistemas Neuromoduladores: La optogenética ha sido crucial para investigar los mecanismos neuronales del sueño y las interacciones entre sistemas neuromoduladores como la hipocretina (Hcrt) y el sistema locus coeruleus/norepinefrina. La estimulación de neuronas productoras de Hcrt en ratones en movimiento libre, por ejemplo, aumenta la probabilidad de despertar. Dada la asociación de la deficiencia de Hcrt con la narcolepsia, este enfoque podría proporcionar información valiosa sobre este trastorno.
- Depresión: La estimulación optogenética de la corteza prefrontal medial (mPFC) ha demostrado iniciar respuestas rápidas similares a antidepresivos en ratones, abriendo vías para comprender mejor los circuitos implicados en la depresión.
- Comportamiento Social y Trastornos Psiquiátricos: La optogenética está mejorando nuestra comprensión del comportamiento social y las deficiencias psiquiátricas. La hipótesis del equilibrio Excitación/Inhibición (E/I) postula que un desequilibrio en los patrones de E/I dentro de los circuitos neuronales está implicado en enfermedades psiquiátricas como el autismo y la esquizofrenia. Estudios optogenéticos han demostrado que elevaciones en el equilibrio E/I celular en el mPFC se correlacionan con un aumento de la actividad de alta frecuencia y deficiencias conductuales.
- Oscilaciones Corticales: La optogenética ha ayudado a demostrar el papel causal de clases específicas de interneuronas inhibitorias en la generación de oscilaciones gamma, importantes para la comunicación neuronal y asociadas a procesos cognitivos y condiciones psiquiátricas.
- Memoria y Miedo: Se han investigado intensamente los circuitos neuronales subyacentes al condicionamiento del miedo y la formación de la memoria. La inhibición optogenética de neuronas CA1 del hipocampo puede revertir el recuerdo de la memoria de miedo contextual, incluso semanas después del entrenamiento. Estos hallazgos son vitales no solo para entender la memoria, sino también para trastornos de ansiedad y estrés postraumático.
- Combinación con Neuroimagen: Una aplicación prometedora es la combinación de optogenética con resonancia magnética funcional (fMRI), conocida como opto-fMRI. Aunque presenta desafíos, esta técnica única permite observar cómo los cambios funcionales en el cerebro son resultado directo de la manipulación optogenética.
Optogenética como Potencial Terapéutico para Enfermedades Neurológicas
La optogenética no solo es una herramienta de investigación fundamental, sino que también posee un gran potencial como estrategia terapéutica para diversas enfermedades neurológicas. La clave reside en su capacidad para proporcionar un control espacial y temporal preciso sobre las neuronas, algo que las terapias actuales como la estimulación cerebral profunda (DBS) y la farmacoterapia a menudo no logran simultáneamente, lo que limita su eficacia y aumenta los efectos secundarios.
Aunque la traslación de la optogenética a la clínica enfrenta desafíos (invasividad de la entrega del gen y la fibra óptica, posible daño por calor), su potencial para tratar enfermedades complejas del sistema nervioso con la precisión necesaria es considerable. Se ha explorado su aplicación en modelos de varias enfermedades:
- Lesión de la Médula Espinal (LME): La LME es devastadora debido a la incapacidad de regeneración axonal en el sistema nervioso central adulto. La optogenética surge como un posible tratamiento. Se sabe que el aumento del calcio intracelular es importante para la regeneración axonal después de una lesión. La optogenética, utilizando opsinas como ChR2 que inducen despolarización y la entrada de calcio, podría aumentar esta señalización para promover la regeneración. Además, se ha demostrado que la estimulación optogenética intermitente de neuronas motoras remanentes puede inducir neuroplasticidad y recuperación funcional en modelos de LME cervical. También se ha aplicado con éxito en modelos de accidente cerebrovascular, que comparte similitudes con la LME (muerte neuronal, tejido cicatricial), mostrando aumento de la neuroplasticidad y recuperación motora. El potencial de la optogenética para la LME radica en aumentar el calcio intracelular para activar mecanismos intrínsecos de regeneración, mejorar la neuroplasticidad de axones preservados, promover la mielinización y restaurar circuitos neuronales.
- Esclerosis Múltiple (EM): Esta enfermedad se caracteriza por la desmielinización. Las terapias actuales son parcialmente efectivas y tienen efectos secundarios. Aumentar la actividad neuronal se ha mostrado beneficioso para aumentar la mielinización y la proliferación de oligodendrocitos. Usando estimulación optogenética en la corteza premotora de ratones, se demostró que la mejora de la actividad neuronal aumentaba el grosor de la mielina axonal y la proliferación de oligodendrocitos, estableciendo un objetivo potencial para el tratamiento de la EM.
- Epilepsia: Caracterizada por la hiperexcitabilidad neuronal y convulsiones recurrentes. Los tratamientos actuales tienen limitaciones y efectos secundarios significativos. La optogenética, con su alta resolución temporal y espacial, podría ser una alternativa superior. Se ha demostrado su eficacia en modelos in vitro e in vivo de diversos tipos de epilepsia (neocortical, talamocortical, lóbulo temporal, crisis de ausencia), utilizando tanto la inhibición (NpHR) como la activación (ChR2) de poblaciones neuronales específicas para reducir la actividad convulsiva. La optogenética también ha sido invaluable para descifrar los circuitos patológicos responsables de diferentes tipos de crisis, como las crisis de ausencia generalizadas, e identificar los mecanismos de tratamientos existentes como la DBS de baja frecuencia.
- Enfermedad de Alzheimer (EA): Esta neurodegeneración progresiva se caracteriza por el deterioro cognitivo. La investigación reciente sugiere que los déficits de memoria tempranos en la EA podrían deberse a una disfunción en la recuperación de la memoria, no en su almacenamiento. Estudios optogenéticos han activado "células engrama" (neuronas que almacenan rastros de memoria) en el giro dentado de ratones modelo de EA, restaurando la densidad de espinas dendríticas y mejorando la memoria a largo plazo. Esto no solo valida la optogenética como herramienta para estudiar la memoria, sino que también sugiere que la estimulación neuronal dirigida podría ser una estrategia terapéutica para la EA. La optogenética también ha ayudado a establecer una relación causal entre la plasticidad sináptica (LTD y LTP) y la codificación de la memoria, demostrando que la memoria puede ser inactivada y reactivada ópticamente.
En resumen, la optogenética es una herramienta fundamental para la investigación básica, permitiendo una comprensión sin precedentes de los circuitos neuronales y los procesos fisiológicos subyacentes al comportamiento y la cognición. Además, su potencial traslacional como terapia para enfermedades neurológicas es innegable, ofreciendo la posibilidad de tratamientos más precisos y con menos efectos secundarios que las opciones actuales.
Comparativa de Técnicas de Neuromodulación
Para entender mejor el avance que representa la optogenética, es útil compararla con otras técnicas de neuromodulación:
| Característica | Optogenética | Estimulación Eléctrica | Farmacología | Manipulación Genética Clásica |
|---|---|---|---|---|
| Especificidad Temporal | Alta (milisegundos) | Alta (milisegundos) | Baja (minutos a horas) | Muy Baja (desarrollo, días) |
| Especificidad Espacial/Celular | Alta (tipos de células específicas) | Baja (afecta a muchas neuronas) | Media (ciertos tipos de receptores/neurotransmisores) | Alta (ciertos tipos de células/vías) |
| Invasividad (en vivo) | Media-Alta (implante de fibra/virus) | Alta (implante de electrodo) | Variable (sistémica vs local) | Variable (transgénesis vs local) |
| Control de Excitación/Inhibición | Preciso (usando diferentes opsinas) | Menos preciso (depende de la configuración) | Depende del fármaco y receptor | Generalmente pérdida o ganancia de función constitutiva |
Preguntas Frecuentes (FAQ)
- ¿Se utiliza actualmente la optogenética en humanos?
- Actualmente, la optogenética se encuentra principalmente en fases de investigación preclínica en modelos animales. La traslación a humanos enfrenta desafíos significativos, como la entrega segura y eficiente de los genes de opsina y la administración de luz a regiones profundas del cerebro sin causar daño. Sin embargo, hay investigaciones explorando su potencial para restaurar la visión en personas con ciertas cegueras.
- ¿Qué son las opsinas y por qué son importantes?
- Las opsinas son proteínas sensibles a la luz, encontradas originalmente en microorganismos. Son cruciales para la optogenética porque, al ser introducidas en neuronas o otras células, permiten que estas respondan a la luz. Dependiendo del tipo de opsina, la luz puede activar o inhibir la actividad celular, proporcionando un control directo sobre su función.
- ¿Cómo permite la optogenética controlar neuronas con tanta precisión?
- La precisión se deriva de dos factores principales: la especificidad genética y el control óptico. Los métodos genéticos permiten expresar las opsinas solo en tipos celulares o circuitos neuronales específicos. La luz se puede dirigir con precisión espacial (a través de fibras ópticas o LEDs implantados) y temporal (pulsos cortos de luz a milisegundos), activando o inhibiendo solo las células modificadas en el momento exacto deseado.
- ¿Qué enfermedades neurológicas podrían beneficiarse de la optogenética?
- La investigación preclínica sugiere un potencial terapéutico para una amplia gama de trastornos, incluyendo la enfermedad de Parkinson, la epilepsia, la enfermedad de Alzheimer, la esclerosis múltiple, la lesión de la médula espinal, trastornos de ansiedad y depresión. La idea es utilizar la optogenética para corregir la actividad anormal de circuitos neuronales específicos subyacentes a estas enfermedades.
- ¿Cuáles son los principales desafíos para llevar la optogenética a la clínica?
- Los desafíos clave incluyen la seguridad y eficiencia de la entrega de genes en el cerebro humano (por ejemplo, usando virus), la necesidad de implantar dispositivos para la administración de luz (fibras ópticas), el riesgo de daño por calor debido a la luz, y la necesidad de demostrar la eficacia y seguridad a largo plazo en ensayos clínicos. Sin embargo, los avances continuos en la ingeniería de opsinas y los métodos de entrega de luz están ayudando a superar estas barreras.
En conclusión, la optogenética se ha consolidado como una de las herramientas más poderosas en la caja de la neurociencia moderna. Su capacidad para manipular la actividad neuronal con una especificidad sin precedentes está desentrañando los complejos circuitos que gobiernan el comportamiento y la cognición. Más allá de la investigación básica, el potencial terapéutico de la optogenética para tratar enfermedades neurológicas devastadoras es una realidad cada vez más cercana, ofreciendo una luz de esperanza para millones de pacientes.
Si quieres conocer otros artículos parecidos a Optogenética: Luz para Entender el Cerebro puedes visitar la categoría Neurociencia.