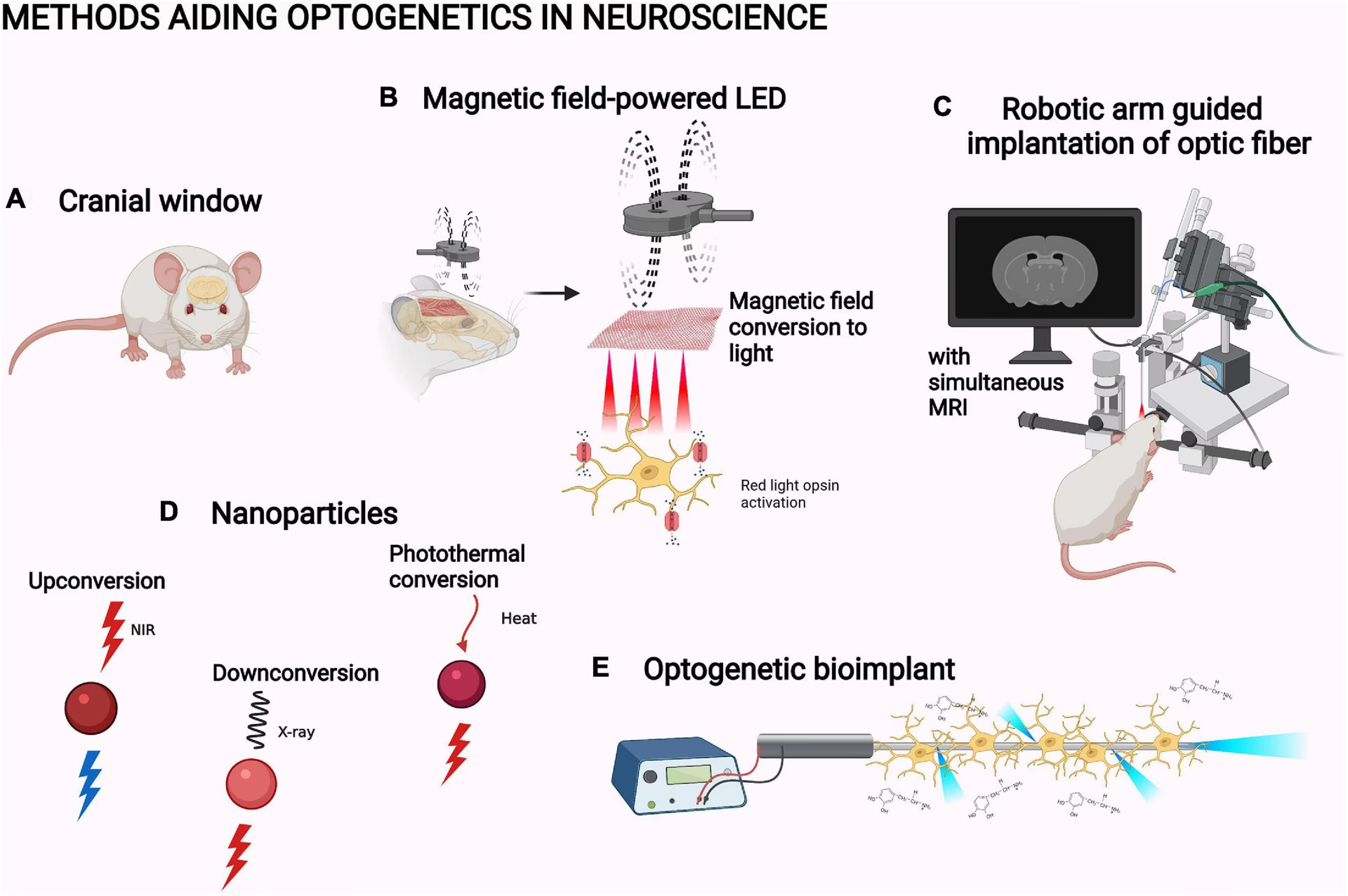
La neurociencia busca incansablemente herramientas que permitan comprender la compleja actividad de las células nerviosas y los circuitos cerebrales. Tradicionalmente, las técnicas disponibles ofrecían un compromiso difícil entre la precisión fisiológica y la capacidad de analizar un gran número de experimentos. Sin embargo, avances recientes han dado paso a una tecnología revolucionaria: la optogenética. Esta técnica, que combina la óptica y la genética, permite controlar la actividad de células, principalmente neuronas, utilizando la luz, abriendo nuevas e inexploradas vías tanto en la investigación básica como en el descubrimiento de fármacos.

La optogenética, reconocida como el "Método del Año" por Nature Methods en 2010 y destacada como un "Avance de la Década" por Science, se basa en la introducción de proteínas sensibles a la luz (opsinas) en células específicas. Una vez expresadas, estas proteínas actúan como interruptores que responden a la iluminación, permitiendo excitar o inhibir la actividad celular con una precisión temporal y espacial sin precedentes. La idea de usar la luz para controlar la actividad neuronal se remonta a sugerencias de Francis Crick en 1979, pero no fue hasta el descubrimiento y la aplicación de opsinas microbianas como la canalrodopsina-2 (ChR2) que la técnica se hizo ampliamente viable en neuronas de mamíferos.
- ¿Qué es la Optogenética?
- Impacto en la Investigación Básica en Neurociencia
- Optogenética en el Descubrimiento de Fármacos
- Optogenética en Humanos: Desafíos Clínicos
- Desafíos Pendientes y Direcciones Futuras
- Glosario
- Tabla Comparativa: Cribado Tradicional vs. Optogenético
- Preguntas Frecuentes
- ¿Qué es exactamente la optogenética en neurociencia?
- ¿Por qué la optogenética fue considerada un gran avance?
- ¿Cómo se utiliza la optogenética en el descubrimiento de fármacos?
- ¿Se puede aplicar la optogenética en humanos?
- ¿Cuáles son los principales desafíos para la optogenética?
- ¿La optogenética podría llevar a tratamientos personalizados?
¿Qué es la Optogenética?
En esencia, la optogenética implica la alteración óptica de procesos fisiológicos y su posterior medición óptica. La clave reside en la expresión de proteínas fotosensibles, principalmente canales iónicos, bombas o enzimas activadas por la luz, dentro de las células objetivo. Estas herramientas optogenéticas, en particular las diseñadas para electrofisiología totalmente óptica, ofrecen una capacidad sin precedentes para investigar modelos celulares de enfermedades con un alto rendimiento y contenido de información.
Las herramientas optogenéticas se dividen principalmente en dos categorías:
- Actuadores Optogenéticos: Proteínas que, al ser iluminadas con una longitud de onda específica, modifican el estado fisiológico de la célula. Los ejemplos más comunes incluyen las canalrodopsinas (ChR2, CheRiff) que permiten la entrada de cationes para despolarizar y excitar neuronas, las halorodopsinas o arquerodopsinas que bombean iones para hiperpolarizar e inhibir, o incluso enzimas activadas por luz que modifican cascadas de señalización intracelular (como bPAC para el cAMP).
- Sensores o Reporteros Optogenéticos: Proteínas fluorescentes que cambian su brillo o color en respuesta a cambios en el estado fisiológico de la célula, como el potencial de membrana (QuasAr, BeRST1) o la concentración de iones (GCaMP, RCaMP para calcio). Estos permiten monitorizar la actividad celular ópticamente.
La combinación de actuadores y reporteros, a menudo espectralmente compatibles (evitando la interferencia entre la luz de activación y la de medición), permite la electrofisiología totalmente óptica, donde tanto la estimulación como el registro de la actividad neuronal se realizan exclusivamente con luz.
Impacto en la Investigación Básica en Neurociencia
La optogenética ha transformado radicalmente la forma en que los neurocientíficos estudian los circuitos cerebrales. La capacidad de activar o inactivar poblaciones neuronales genéticamente definidas con precisión de milisegundos en animales vivos y en comportamiento permite establecer relaciones causales directas entre la actividad de neuronas específicas y funciones cerebrales o comportamientos complejos. Esto contrasta con técnicas anteriores que a menudo solo permitían correlaciones o manipulaciones con menor precisión temporal o espacial.
Se ha utilizado para investigar la contribución de circuitos neuronales específicos en una amplia gama de funciones, incluyendo la toma de decisiones, el aprendizaje, la memoria del miedo, el apareamiento, la adicción, la alimentación y la locomoción. Al manipular la actividad de neuronas etiquetadas genéticamente con luz y registrar la actividad de otras células o regiones cerebrales (usando electrofisiología o imágenes), los investigadores pueden mapear la conectividad funcional del cerebro.
Optogenética en el Descubrimiento de Fármacos
Uno de los campos donde la optogenética tiene un potencial transformador es el descubrimiento de fármacos, especialmente para trastornos neurológicos. El desafío fundamental en el desarrollo de fármacos es encontrar compuestos que modulen procesos fisiológicos específicos en subconjuntos particulares de células. Los ensayos de alto rendimiento (HTS) a menudo carecen de relevancia fisiológica, mientras que los ensayos fenotípicos más ricos son lentos y costosos. La optogenética ofrece una forma de mejorar este compromiso.
Mejorando el Equilibrio entre Rendimiento y Realismo
La esencia del descubrimiento de fármacos es identificar moléculas que alteren un proceso fisiológico. Los ensayos de HTS tradicionales, si bien son rápidos, a menudo simplifican drásticamente el contexto fisiológico. La optogenética, al permitir la estimulación y medición de la actividad celular en un contexto más realista (como células que expresan múltiples canales iónicos o en cultivos neuronales complejos), aumenta la relevancia fisiológica de los ensayos de alto rendimiento.
Aplicaciones en Cribado de Alto Rendimiento (HTS)
La optogenética permite realizar cribados de alto rendimiento que antes eran inviables. Se pueden diseñar ensayos para:
- Cribados Basados en Dianas (Targets): Modular la actividad de un canal iónico o una vía de señalización específica usando luz y medir el efecto de los compuestos. Por ejemplo, se han desarrollado ensayos totalmente ópticos para canales de sodio (NaV), canales de calcio (CaV) y canales activados por nucleótidos cíclicos (CNG) en células HEK modificadas para generar potenciales de acción o cambios de voltaje lentos controlados por luz. Esto permite estudiar la farmacología dependiente del estado del canal de forma masiva.
- Cribados Fenotípicos: Medir el efecto de los compuestos en fenotipos funcionales complejos, como la excitabilidad neuronal o la transmisión sináptica, independientemente de la diana molecular.
Las ventajas de usar la luz en HTS incluyen:
- Precisión Temporal y Espacial: Permite activar poblaciones celulares o subcelulares específicas con gran control.
- Control In-Well: Es posible mezclar células con diferentes actuadores/sensores o variar la intensidad de la luz dentro de un mismo pocillo para realizar controles internos o curvas dosis-respuesta.
- Bajo Costo Potencial: Una vez establecidos los sistemas, el costo por ensayo puede ser bajo.
Ejemplos específicos mencionados incluyen el cribado de canales NaV1.7 en células HEK que disparan potenciales de acción inducidos ópticamente (Optopatch), permitiendo identificar bloqueadores dependientes del uso. Otro ejemplo es el uso de una adenilil ciclasa fotoactivada (bPAC) para modular canales CNG mediante cAMP inducido por luz.
Cribado Fenotípico Detallado
El cribado fenotípico con optogenética se centra en medir las consecuencias funcionales de la modulación farmacológica en células o circuitos. La excitabilidad neuronal, que integra la actividad de múltiples canales iónicos y factores metabólicos, es un fenotipo poderoso para modelar enfermedades y descubrir fármacos.

Las mediciones optogenéticas de la excitabilidad neuronal pueden aplicarse en varios contextos:
- Identificación de Dianas: Usar perturbaciones genéticas (como CRISPR) junto con mediciones de excitabilidad para identificar genes que la modulan.
- Cribados Basados en Dianas: Comparar el efecto de un fármaco en la excitabilidad de neuronas con o sin una diana específica para distinguir mecanismos de acción.
- Cribados Selectivos por Tipo Celular: Identificar compuestos que afectan selectivamente la excitabilidad de ciertos tipos de neuronas (ej. excitatorias vs. inhibitorias) en un cultivo mixto.
- Estratificación de Pacientes: Medir el efecto de fármacos en neuronas derivadas de células madre pluripotentes inducidas (iPSC) de pacientes para predecir la respuesta clínica o estratificar pacientes para ensayos.
La transmisión sináptica, implicada en muchas enfermedades neuropsiquiátricas, también puede investigarse optogenéticamente. Se están desarrollando herramientas para medir la entrada de calcio presináptico, la fusión de vesículas, la liberación de neurotransmisores (como glutamato con iGluSnfr) y los potenciales postsinápticos (usando Optopatch entre células presinápticas y postsinápticas). Aunque desafiantes debido a la complejidad sináptica y la variabilidad, estos ensayos prometen identificar moduladores de la función sináptica.
Mediciones en Tejido y In Vivo
La complejidad de los circuitos neuronales hace que la validación de hallazgos de cribado en tejido intacto sea crucial. La optogenética permite estudiar la función neuronal en rodajas de cerebro agudas o en animales vivos. Se pueden mapear los efectos de los compuestos en la excitabilidad de microcircuitos específicos, o inducir comportamientos relevantes para enfermedades en modelos animales (miedo, agresión, dolor) mediante estimulación optogenética para evaluar la eficacia de los fármacos. La baja tasa de procesamiento (throughput) limita estas aplicaciones principalmente a la validación de dianas y la priorización de candidatos a fármacos.
Seguridad y Toxicología
La optogenética también se aplica en farmacología de seguridad. Las mediciones funcionales en cardiomiocitos derivados de iPSC humanas (hiPSC-CM) usando luz para controlar el voltaje o el calcio, y para marcar el paso (pacing) óptico, proporcionan un fenotipo rico para evaluar el riesgo de cardiotoxicidad de los compuestos. De manera similar, los métodos electrofisiológicos totalmente ópticos pueden usarse para estudios de neurotoxicidad, evaluando el efecto de los compuestos en la excitabilidad intrínseca de las neuronas y la transmisión sináptica.
Optogenética en Humanos: Desafíos Clínicos
La aplicación de la optogenética en humanos, especialmente en el cerebro, presenta desafíos significativos pero también un potencial enorme para tratar una variedad de trastornos neurológicos y psiquiátricos. Si bien los primeros ensayos clínicos se centran en el sistema visual (retinitis pigmentosa), la aplicación en el cerebro es un objetivo a largo plazo.
Obstáculos para la Translación Clínica
Llevar la optogenética al cerebro humano requiere superar varios obstáculos:
- Entrega del Gen: Se necesitan vectores virales (como AAV) para introducir el gen de la opsina en las células objetivo. Esto implica un procedimiento neuroquirúrgico invasivo. La expresión debe ser duradera a partir de una única inyección.
- Entrega de Luz: Se requieren dispositivos médicos implantables para proporcionar la estimulación óptica necesaria. La luz penetra poco el tejido cerebral, especialmente las longitudes de onda azul/verde a las que responden muchas opsinas actuales. Esto requiere un dispositivo implantado cerca de la diana. La elección de opsinas que responden a luz roja (que penetra mejor) o el desarrollo de nuevas herramientas son cruciales.
- Seguridad a Largo Plazo: Se desconocen los efectos a largo plazo de la expresión de proteínas no humanas, la exposición crónica a la luz y la presencia de dispositivos implantados en el cerebro.
A pesar de estos desafíos, varios grupos están trabajando hacia los primeros ensayos en humanos, y se espera que ocurran en la próxima década.
Diseño de Ensayos Clínicos
Los ensayos clínicos de optogenética en el cerebro son complejos porque combinan una terapia génica (producto medicinal) y un dispositivo médico implantable. Esto plantea preguntas regulatorias sobre su clasificación y diseño.
A diferencia de los ensayos de fase 1 de fármacos tradicionales (que usan dosis bajas en voluntarios sanos para probar la seguridad), un ensayo optogenético cerebral no puede usar este enfoque. La introducción de un gen permanente y un dispositivo implantable en el cerebro implica riesgos significativos que solo pueden justificarse si hay una expectativa de beneficio para el paciente. Por lo tanto, los primeros ensayos probablemente se realizarán en pacientes con la enfermedad objetivo, utilizando una dosis (expresión de opsina y estimulación lumínica) que se espera sea eficaz.
Consideraciones de Seguridad
La seguridad es primordial. Los riesgos potenciales de la terapia génica incluyen la mutagénesis insercional (riesgo teórico de tumores, aunque bajo con AAV), respuesta inmune al vector o la opsina, y toxicidad celular. Los riesgos del dispositivo incluyen daño tisular por implantación, respuesta inmune, formación de glía y degradación del dispositivo. La monitorización es difícil en el cerebro. La incompatibilidad con RMN (MRI) de los dispositivos implantados puede limitar las opciones de imagen para monitorizar el cerebro.

Estrategias para Ensayos Clínicos
Para abordar los desafíos, se proponen estrategias como:
- Realizar ensayos en pacientes que ya van a someterse a cirugía cerebral (ej. por epilepsia focal), lo que permitiría la posible remoción y análisis del tejido y el dispositivo si surgen problemas o al final del estudio.
- Diseñar estudios de duración suficiente para evaluar no solo la seguridad inicial, sino también la durabilidad de la expresión de la opsina, la respuesta del tejido a la estimulación crónica y los posibles cambios en la eficacia a largo plazo (que pueden tardar en manifestarse en algunas enfermedades).
- Involucrar a pacientes y cuidadores en el diseño del ensayo para asegurar que los criterios de valoración reflejen mejoras significativas en la calidad de vida, no solo métricas fisiológicas.
- Planificar seguimientos a largo plazo para monitorizar la seguridad de la terapia génica permanente y el dispositivo.
Desafíos Pendientes y Direcciones Futuras
Aunque la optogenética ha avanzado enormemente, persisten desafíos técnicos:
- Herramientas Moleculares: Necesidad de más opsinas y reporteros con espectros de acción compatibles (especialmente en el rojo lejano/infrarrojo) para evitar la interferencia entre estimulación y medición. Desarrollo de reporteros para otros analitos importantes como neurotransmisores (GABA, glicina, dopamina, serotonina, acetilcolina).
- Cuantificación: Dificultad para obtener mediciones absolutas precisas de voltaje o concentración debido a la variabilidad en la expresión de las proteínas y la distribución de la luz. Se necesitan métodos de calibración y diseño experimental robusto.
- Instrumentación y Software: Los sistemas de cribado de alto rendimiento actuales a menudo carecen de la capacidad de iluminación espacial y temporalmente compleja y la resolución y velocidad necesarias para medir la actividad neuronal rápida a nivel unicelular. Se requiere el desarrollo de nueva instrumentación comercial. La gran cantidad de datos generados también exige pipelines de software avanzados para procesamiento y análisis.
A pesar de estos desafíos, el potencial de la optogenética para acelerar el descubrimiento de fármacos, particularmente para enfermedades de la excitabilidad celular, es inmenso. Al permitir probar compuestos directamente en modelos funcionales más cercanos a la biología de la enfermedad (incluyendo neuronas derivadas de pacientes), se espera reducir la alta tasa de fracaso que ha afectado tradicionalmente el desarrollo de fármacos neurológicos. La integración exitosa de la optogenética en el descubrimiento y la clínica podría marcar el comienzo de una nueva era para el tratamiento de trastornos cerebrales.
Glosario
| Término | Definición |
|---|---|
| Bouton | Engrosamiento en el axón neuronal que contiene vesículas sinápticas. Una sinapsis comprende una unión de un bouton presináptico y una espina dendrítica postsináptica. |
| Canalrodopsina | Clase de proteínas transmembrana que transportan cationes a través de la membrana plasmática en respuesta a la estimulación lumínica. |
| CheRiff | Tipo de canalrodopsina que muestra buena sensibilidad a la iluminación con luz azul y cinética de apertura y cierre rápida. |
| Despolarización | En el estado de reposo de la mayoría de las células, el interior de la célula es eléctricamente negativo en relación con el exterior ("polarizado"). La despolarización se refiere a un cambio hacia un voltaje menos negativo, a menudo causado por un flujo de iones positivos hacia la célula. |
| Fluorescent Imaging Plate Reader (FLIPR) | Instrumento comercialmente disponible que monitoriza la dinámica de fluorescencia simultánea de cada pocillo en una placa de múltiples pocillos. Este instrumento es ampliamente utilizado para cribado de alto rendimiento para identificar moduladores de dianas GPCR y canales iónicos. |
| GCaMP | Clase de indicadores de calcio basados en proteínas que emiten fluorescencia verde. El brillo de estos reporteros es altamente sensible a la concentración local de Ca2+. |
| Canal Kir | Canal de potasio rectificador de entrada. Estos canales iónicos tienen mayor conductancia para el potasio en potenciales negativos que en potenciales positivos. Los canales Kir no muestran comportamiento dependiente del voltaje, es decir, la corriente es solo una función del voltaje instantáneo en lugar de depender también de voltajes pasados. En neuronas y cardiomiocitos, los canales Kir son críticos para estabilizar un potencial de membrana en reposo negativo, cercano al potencial de reversión del potasio. |
| Canales NaV | Canales de sodio dependientes del voltaje. Cuando son activados por un cambio despolarizante en el voltaje de membrana, estos canales iónicos se abren y conducen iones sodio hacia la célula. Esta corriente de entrada conduce a una mayor despolarización, creando una retroalimentación positiva que produce un pico en el voltaje de membrana. La mayoría de los canales NaV se cierran espontáneamente después de un corto tiempo, por lo que la activación de NaV solo produce un breve pico en el voltaje de membrana. Los canales NaV producen el ascenso del potencial de acción en neuronas y cardiomiocitos. |
| QuasAr | Reportero de proteína fluorescente de infrarrojo cercano del voltaje de membrana. Esta proteína responde a los cambios en el voltaje de membrana de forma rápida y sensible, pero es muy tenue. |
| RCaMP | Clase de indicadores de calcio basados en proteínas que emiten fluorescencia roja. El espectro desplazado hacia el rojo de estos reporteros facilita su emparejamiento con canalrodopsinas activadas por luz azul. |
| Potencial de Reversión | El valor del potencial de membrana en el que un ion no fluirá ni hacia adentro ni hacia afuera de una célula. El potencial de reversión para cada ion depende de sus concentraciones dentro y fuera de la célula, según la ecuación de Nernst. |
Tabla Comparativa: Cribado Tradicional vs. Optogenético
| Característica | Cribado Tradicional (Basado en Fluorescencia) | Cribado Optogenético |
|---|---|---|
| Relevancia Fisiológica | A menudo baja (ensayos minimalistas) | Potencialmente alta (ensayos celulares funcionales) |
| Rendimiento (Throughput) | Alto | Potencialmente alto (con instrumentación adecuada) |
| Contenido de Información | Limitado (principalmente flujos iónicos o cambios de voltaje estáticos) | Rico (dinámica de voltaje/calcio dependiente del tiempo, selectividad celular) |
| Control del Estímulo | Generalmente estático o químico | Preciso temporal y espacialmente (con luz) |
| Selectividad por Tipo Celular | Limitada (requiere separación física o tinción) | Alta (mediante direccionamiento genético) |
| Costo | Moderado a alto (depende del sistema) | Potencialmente bajo (una vez establecida la plataforma) |
Preguntas Frecuentes
¿Qué es exactamente la optogenética en neurociencia?
La optogenética es una técnica biológica que permite controlar la actividad de neuronas u otros tipos celulares utilizando la luz. Esto se logra introduciendo genes que codifican proteínas fotosensibles (opsinas) en las células objetivo, lo que las hace responder a la iluminación con cambios en su actividad eléctrica o bioquímica.
¿Por qué la optogenética fue considerada un gran avance?
La optogenética fue un gran avance porque proporcionó por primera vez una herramienta para controlar la actividad neuronal con una precisión temporal (milisegundos) y espacial (tipos celulares específicos) sin precedentes. Esto permitió a los investigadores establecer relaciones causales entre la actividad de neuronas o circuitos definidos y el comportamiento o la función cerebral, superando las limitaciones de técnicas anteriores.
¿Cómo se utiliza la optogenética en el descubrimiento de fármacos?
La optogenética se utiliza en el descubrimiento de fármacos para crear ensayos celulares más fisiológicamente relevantes y de alto rendimiento. Permite cribar grandes bibliotecas de compuestos midiendo su efecto sobre la excitabilidad neuronal, la transmisión sináptica o vías de señalización específicas, controladas por luz. Esto puede ayudar a identificar nuevas dianas terapéuticas y a evaluar la eficacia y selectividad de los candidatos a fármacos.
¿Se puede aplicar la optogenética en humanos?
Sí, la aplicación de la optogenética en humanos ya ha comenzado en ensayos clínicos, principalmente para restaurar parcialmente la visión en pacientes con retinitis pigmentosa mediante la sensibilización de las células ganglionares a la luz. La aplicación en el cerebro humano es un objetivo futuro con potencial para tratar trastornos neurológicos, aunque presenta desafíos significativos relacionados con la entrega segura de los genes, la implantación de dispositivos lumínicos y la seguridad a largo plazo.
¿Cuáles son los principales desafíos para la optogenética?
Los desafíos incluyen el desarrollo de herramientas moleculares mejoradas (opsinas y reporteros con espectros de luz compatibles, reporteros para más moléculas señalizadoras), lograr una cuantificación precisa de las respuestas celulares, mejorar la instrumentación para permitir cribados de alto rendimiento con estimulación y medición complejas, y desarrollar pipelines de software para manejar la gran cantidad de datos generados. En la clínica, los desafíos incluyen la entrega segura de genes, la miniaturización y biocompatibilidad de los dispositivos implantables y la evaluación de la seguridad a largo plazo.
¿La optogenética podría llevar a tratamientos personalizados?
Sí, uno de los potenciales futuros de la optogenética es su uso en medicina de precisión. Al estudiar la respuesta a fármacos de neuronas derivadas de iPSC de pacientes individuales, la optogenética podría ayudar a predecir la respuesta de un paciente a una terapia específica o a estratificar pacientes para ensayos clínicos, abriendo la puerta a tratamientos más personalizados para trastornos neurológicos.
Si quieres conocer otros artículos parecidos a Optogenética: Controlando el Cerebro con Luz puedes visitar la categoría Neurociencia.