La enfermedad de Alzheimer (EA) representa uno de los desafíos más complejos de la neurociencia moderna. Su naturaleza progresiva y el impacto devastador en la memoria y la cognición hacen que la búsqueda de tratamientos efectivos sea una prioridad global. Sin embargo, estudiar esta enfermedad en humanos es inherentemente difícil, lo que impulsa la necesidad de desarrollar modelos experimentales que capturen sus características clave. Tradicionalmente, se han utilizado modelos animales (principalmente ratones) y cultivos celulares in vitro, pero estos a menudo fallan en replicar completamente los aspectos específicos de la patología humana.

Uno de los principales obstáculos es que las células neuronales en cultivo carecen del entorno tridimensional y las interacciones complejas que existen en el cerebro vivo. Además, los modelos animales no siempre replican fielmente las características moleculares humanas de la EA, como las isoformas específicas de la proteína Tau.
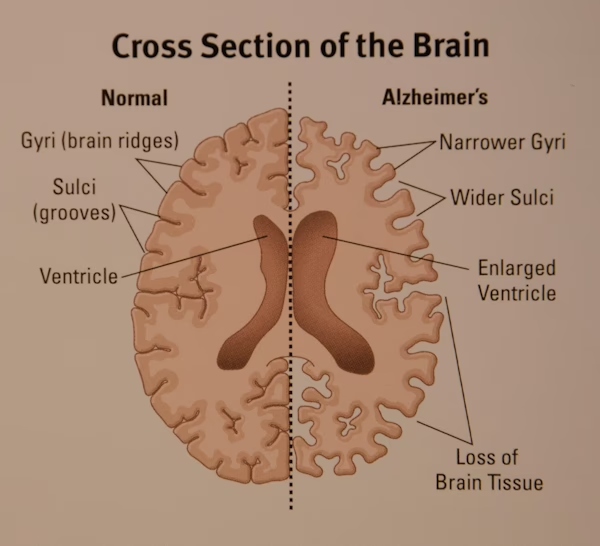
El Desafío de Modelar la Patología Humana
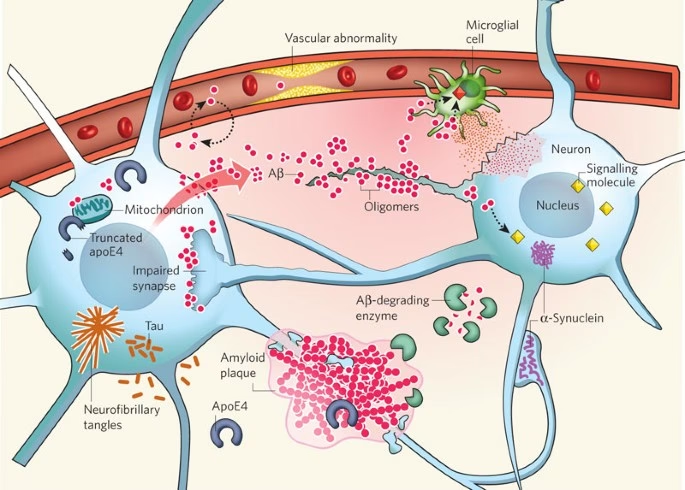
La enfermedad de Alzheimer se caracteriza por la acumulación anormal de dos proteínas clave en el cerebro: la proteína beta-amiloide, que forma placas extracelulares, y la proteína Tau, que forma ovillos neurofibrilares intracelulares. Si bien ambas patologías son cruciales, la proteína Tau juega un papel directo en la disfunción neuronal y la neurodegeneración.
En humanos, la proteína Tau existe en varias isoformas, destacando las que contienen 3 o 4 repeticiones de la secuencia de unión a microtúbulos (conocidas como 3R y 4R Tau). El equilibrio entre estas isoformas y su procesamiento adecuado son vitales para la función neuronal normal. Sin embargo, en la EA, Tau se vuelve hiperfosforilada y cambia su conformación, perdiendo su capacidad para estabilizar los microtúbulos y agregándose en los ovillos. Muchos modelos animales tradicionales no expresan las isoformas humanas de Tau o no replican fielmente su patología.
Un Enfoque Innovador: El Modelo Quimérico
Para superar estas limitaciones, la investigación ha explorado el uso de células madre pluripotentes humanas (PSC). Estas células tienen la capacidad única de diferenciarse en cualquier tipo celular, incluidas las neuronas, y pueden derivarse de individuos con diferentes fondos genéticos, lo que permite estudiar el impacto de mutaciones asociadas a la EA.
Un avance significativo es la creación de modelos quiméricos, donde neuronas derivadas de PSC humanas se trasplantan en el cerebro de modelos animales de EA. Este enfoque combina la ventaja de tener células neuronales humanas con el entorno tridimensional y complejo de un cerebro vivo. Recientemente, se ha desarrollado un modelo de este tipo trasplantando precursores neuronales corticales derivados de PSC humanas en el cerebro de un modelo murino de EA.
Descubriendo las Señales Neuronales del Alzheimer en el Modelo Quimérico
Este modelo quimérico ha permitido observar cómo se comportan las neuronas humanas en un entorno patológico relevante para la EA. Los resultados han sido esclarecedores, revelando la manifestación de importantes hallmarks neuronales de la enfermedad:
Integración y Diferenciación
Tras el trasplante, los precursores neuronales humanos lograron diferenciarse e integrarse exitosamente en el tejido cerebral del ratón huésped. Esto es crucial, ya que demuestra la viabilidad de este enfoque para estudiar neuronas humanas funcionales en un contexto más natural que un cultivo 2D.
Patología de la Proteína Tau
Las neuronas humanas trasplantadas mostraron la expresión de las isoformas humanas 3R y 4R de la proteína Tau. Más importante aún, exhibieron cambios patológicos en Tau, incluyendo fosforilación anormal y alteraciones conformacionales. Estos son pasos tempranos y críticos en el desarrollo de la patología de Tau en la EA, que preceden a la formación de los ovillos neurofibrilares maduros. La observación de estas anomalías en un entorno cerebral vivo ofrece una ventana única para estudiar los mecanismos subyacentes.
Neurodegeneración
Uno de los hallazgos más relevantes fue que las neuronas humanas trasplantadas experimentaron neurodegeneración, es decir, muerte celular. La pérdida de neuronas es una característica central y devastadora del Alzheimer, directamente relacionada con el declive cognitivo. Observar este proceso en neuronas humanas dentro de un cerebro huésped proporciona un modelo valioso para investigar las causas y progresiones de la muerte neuronal en la EA.
Un Hallazgo Sorprendente: Disociación entre Muerte Celular y Ovillos Neurofibrilares
Intrínsecamente ligado a la patología de Tau y la neurodegeneración, el estudio reveló un hallazgo notable en este modelo: la muerte celular estaba disociada de la formación de ovillos neurofibrilares maduros. Esto significa que las neuronas estaban muriendo sin necesariamente haber acumulado grandes ovillos de Tau. Este descubrimiento es significativo porque sugiere que las formas tóxicas de Tau (como la Tau hiperfosforilada o conformacionalmente alterada, o incluso agregados más pequeños como oligómeros) podrían ser responsables de la muerte neuronal independientemente o antes de la formación de los grandes e insolubles ovillos. Esto refuerza la idea de que atacar las formas tempranas y solubles de Tau podría ser una estrategia terapéutica más efectiva que centrarse únicamente en la eliminación de los ovillos.
Cambios en la Expresión Génica
El análisis de la expresión génica a nivel genómico en las neuronas humanas trasplantadas proporcionó más pistas sobre los procesos afectados en la EA. Se observó una regulación positiva (aumento) de genes involucrados en la mielinización. Aunque la razón exacta de este aumento no está clara en el contexto de la patología neuronal intrínseca, podría reflejar una compleja interacción con las células gliales del huésped o un intento de compensación.
Más directamente relacionados con los síntomas de la EA, se observó una regulación negativa (disminución) de genes cruciales para la memoria y la cognición, la transmisión sináptica y la proyección neuronal. Estos cambios genéticos reflejan el deterioro funcional de las neuronas: la reducción de la actividad sináptica, la retracción de las conexiones neuronales y, en última instancia, la base molecular de los déficits cognitivos característicos de la enfermedad.
Implicaciones del Modelo Quimérico
Este novedoso modelo quimérico presenta varias ventajas para la investigación de la EA:
- Permite el estudio de características patológicas específicas de humanos, como la expresión de isoformas de Tau.
- Proporciona un entorno tridimensional más natural y complejo que los cultivos celulares in vitro.
- Facilita el análisis de diferentes fondos genéticos y mutaciones asociadas a la EA, trasplantando neuronas derivadas de PSC de pacientes.
- Posibilita el seguimiento de la progresión de la enfermedad y la manifestación de los hallmarks a lo largo del tiempo en neuronas humanas vivas.
- Ofrece una plataforma potencial para probar la eficacia de nuevas terapias dirigidas a la patología de Tau o la neurodegeneración en un contexto más relevante para humanos.
Aunque es un modelo animal, la presencia de neuronas humanas que replican aspectos clave de la patología de Tau y la neurodegeneración lo convierte en una herramienta poderosa para desentrañar los complejos mecanismos de la EA y desarrollar estrategias terapéuticas más efectivas.
Comparación de Modelos de Alzheimer
| Tipo de Modelo | Entorno | Especificidad Humana | Hallmarks Clave (Observados en este contexto) |
|---|---|---|---|
| Cultivos Celulares 2D (In vitro) | Artificial, 2D | Alta (si son células humanas) | Patología de Tau (variable), Acumulación de Beta-Amiloide (variable). Falta entorno 3D. |
| Modelos Murinos Tradicionales | Cerebro vivo (3D) | Baja (proteínas murinas) | Placas de Beta-Amiloide, Patología de Tau (a menudo requiere sobreexpresión humana, no siempre replica fielmente). |
| Modelo Quimérico (PSC Humanas en Ratón) | Cerebro vivo (3D) | Alta (neuronas humanas) | Patología de Tau humana (isoformas 3R/4R, fosforilación, conformación), Neurodegeneración, Cambios Genéticos relevantes. Posible disociación Tau/muerte celular. |
Preguntas Frecuentes (FAQ)
¿Qué es la proteína Tau y por qué es importante en el Alzheimer?
La proteína Tau es una proteína que normalmente ayuda a estabilizar los microtúbulos dentro de las neuronas, estructuras esenciales para el transporte y la forma celular. En el Alzheimer, Tau se modifica (hiperfosforilación) y se agrega en ovillos, lo que interrumpe la función neuronal y contribuye a la muerte celular.
¿Qué son los ovillos neurofibrilares?
Son agregados anormales de proteína Tau hiperfosforilada y mal plegada que se acumulan dentro de las neuronas en el cerebro de pacientes con Alzheimer y otras tauopatías.
¿Este modelo quimérico significa que el Alzheimer se puede curar pronto?
No directamente. Este modelo es una herramienta de investigación para entender mejor los mecanismos de la enfermedad y probar posibles terapias. No es un tratamiento en sí mismo, pero acelera la investigación al permitir estudiar aspectos humanos de la EA.
¿Por qué es importante que la muerte celular esté disociada de la formación de ovillos en este modelo?
Sugiere que las formas tóxicas de Tau que causan la muerte neuronal podrían ser agregados más pequeños o formas modificadas de la proteína, y no necesariamente los grandes ovillos maduros. Esto podría redirigir los esfuerzos terapéuticos hacia etapas más tempranas o formas específicas de la patología de Tau.
¿Qué significa usar células madre pluripotentes humanas (PSC)?
Significa usar células que pueden dar lugar a cualquier tipo de célula del cuerpo. En este caso, se dirigen a que se conviertan en neuronas para estudiar cómo se ven afectadas por la enfermedad de Alzheimer.
Conclusión
El desarrollo y la aplicación de modelos quiméricos utilizando neuronas derivadas de células madre pluripotentes humanas representan un avance significativo en la investigación de la enfermedad de Alzheimer. Este enfoque permite estudiar hallmarks neuronales clave, como las anomalías de la proteína Tau (incluyendo fosforilación y cambios conformacionales) y la neurodegeneración, en un entorno que se asemeja más al cerebro humano vivo que los modelos in vitro. El sorprendente hallazgo de la disociación entre la muerte celular y la formación de ovillos subraya la complejidad de la patología de Tau y abre nuevas vías para la investigación terapéutica. Al permitir el estudio de aspectos específicos de la patología humana y los efectos de diferentes fondos genéticos, estos modelos están allanando el camino para una comprensión más profunda de la EA y el desarrollo de intervenciones más efectivas contra esta devastadora enfermedad.
Si quieres conocer otros artículos parecidos a Neurociencia: Hallmarks Clave del Alzheimer puedes visitar la categoría Neurociencia.