¿Qué pasa en el cerebro cuando sufrimos depresión? La depresión mayor, un trastorno que afecta a millones a nivel mundial, ha sido tradicionalmente abordada desde la hipótesis de las monoaminas. Sin embargo, la limitada eficacia de los tratamientos actuales y la diversidad de síntomas sugieren una complejidad mucho mayor. La investigación reciente apunta a que la depresión es, fundamentalmente, un trastorno de los circuitos neuronales, una disfunción en la comunicación entre diferentes áreas del cerebro. Entender esta complejidad a nivel molecular, celular y de red es crucial para desarrollar terapias más efectivas.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
Durante décadas, la teoría predominante sobre la depresión se centró en desbalances de neurotransmisores como la serotonina, la noradrenalina y la dopamina. Aunque importantes, los tratamientos basados únicamente en esta hipótesis logran la remisión completa en menos del 50% de los pacientes y tardan semanas o meses en hacer efecto. Esto ha impulsado a la neurociencia a buscar explicaciones más profundas, revelando que la patofisiología de la depresión involucra una intrincada red de sistemas interconectados en el cerebro.
Mecanismos Moleculares Implicados
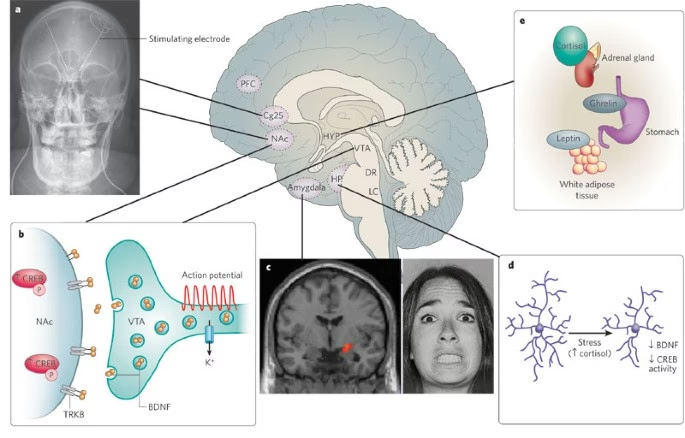
A nivel molecular, numerosos procesos se ven alterados en la depresión. Un actor clave es el factor neurotrófico derivado del cerebro (BDNF), esencial para la supervivencia, crecimiento y plasticidad neuronal. Curiosamente, su papel varía según la región cerebral. En el centro de recompensa (circuito VTA-Núcleo Accumbens), un aumento de BDNF puede asociarse a conductas depresivas, mientras que en el hipocampo y la corteza prefrontal, niveles bajos de BDNF se vinculan a la depresión y los antidepresivos tienden a aumentarlos. El estrés crónico también modula los niveles de BDNF de forma dependiente del tiempo y la región.
La señalización del glutamato, el principal neurotransmisor excitatorio, es fundamental. Antagonistas del receptor NMDA, como la Ketamina, han mostrado efectos antidepresivos rápidos y duraderos. El mecanismo propuesto implica que el bloqueo del NMDA desactiva la CaMKII, lo que lleva a una desfosforilación del factor de elongación eEF2, permitiendo una rápida síntesis de BDNF en el hipocampo. Esto, a su vez, aumenta la expresión de receptores AMPA en la superficie neuronal y potencia las respuestas sinápticas, promoviendo la plasticidad.
La vía de señalización mTOR (Diana de Rapamicina en Mamíferos) es otro componente crucial. Regula la síntesis de proteínas y el desarrollo dendrítico, y está implicada en la plasticidad sináptica. La disfunción en la señalización de mTOR, posiblemente influenciada por BDNF y NMDA, se ha relacionado con cambios en la plasticidad sináptica que contribuyen a la depresión. Se cree que el estrés prolongado puede inducir atrofia neuronal y depresión sináptica en la corteza prefrontal (CPF) y el hipocampo, mientras que causa hipertrofia y potenciación en la amígdala y el Núcleo Accumbens. Esta respuesta opuesta en diferentes regiones subraya la complejidad del trastorno.
El eje hipotalámico-pituitario-adrenal (eje HPA), que controla la respuesta al estrés, está frecuentemente alterado en la depresión. El estrés crónico lleva a una liberación excesiva de cortisol y CRH, que tienen efectos neurotóxicos y pueden suprimir el BDNF, afectando la neurogénesis y la plasticidad. Los glucocorticoides influyen en la señalización intracelular y la plasticidad sináptica, y la exposición al estrés temprano puede dejar una huella duradera en la reactividad molecular a futuros estresores.
La Epigenética en la Depresión
La epigenética se refiere a cambios heredables en la expresión génica que no implican alteraciones en la secuencia del ADN. Factores ambientales como el estrés pueden modificar la expresión génica a través de mecanismos epigenéticos, como la modificación de histonas (acetilación, metilación) y la metilación del ADN. Estos cambios pueden alterar la estructura de la cromatina, afectando qué genes se activan o silencian.
La investigación en modelos animales y humanos ha encontrado alteraciones epigenéticas específicas en la depresión. Por ejemplo, se han observado cambios en la acetilación y metilación de histonas en el Núcleo Accumbens y el hipocampo tras el estrés crónico. Inhibidores de las histonas deacetilasas (HDAC) han mostrado efectos antidepresivos en modelos animales. La metilación del promotor de BDNF también ha sido relacionada con la depresión en humanos, disminuyendo con el tratamiento antidepresivo.
El estrés temprano en la vida, como la separación materna en roedores, puede inducir cambios epigenéticos duraderos en regiones cerebrales clave, aumentando la vulnerabilidad a la depresión en la adultez. Sorprendentemente, se ha encontrado evidencia de transmisión de vulnerabilidad al estrés a través de mecanismos epigenéticos en las células germinales en modelos animales, aunque la complejidad de esta transmisión y el papel de los factores conductuales aún se investigan.
Neurogénesis y Plasticidad Sináptica
La hipótesis de la neurogénesis propone que el aumento de la formación de nuevas neuronas en el hipocampo adulto contribuye a los efectos terapéuticos de los antidepresivos clásicos, explicando parcialmente su latencia de acción. El estrés crónico, que induce conductas depresivas y ansiosas, generalmente deteriora la neurogénesis hipocampal. El exceso de cortisol, neurotóxico, suprime el BDNF, un factor clave para la neurogénesis, lo que podría relacionarse con la reducción del volumen del hipocampo observada en algunos pacientes deprimidos.
Los antidepresivos pueden revertir la supresión de la proliferación celular inducida por el estrés o el cortisol en modelos animales. Sin embargo, la relación entre neurogénesis y depresión no es simple ni universal. Existen estudios contradictorios donde el estrés no afectó la neurogénesis, o donde los antidepresivos fueron efectivos en poblaciones (como los ancianos) con neurogénesis limitada. Algunos estudios sugieren que los antidepresivos podrían más bien promover la “desmaduración” de neuronas existentes, haciéndolas más plásticas, en lugar de crear activamente nuevas neuronas. La complejidad se incrementa al considerar las diferencias de sexo y las condiciones específicas del estrés.
La Depresión como Trastorno de Circuitos Neuronales
La evidencia más convincente de que la depresión es un trastorno de circuitos proviene de estudios con Estimulación Cerebral Profunda (DBS). La DBS, dirigida a regiones específicas del cerebro, puede aliviar rápidamente los síntomas en pacientes resistentes al tratamiento, sugiriendo que la modulación de la actividad en redes neuronales disfuncionales es terapéutica.
El Circuito Mesolímbico Dopaminérgico
Este circuito, compuesto por neuronas de Dopamina del Área Tegmental Ventral (VTA) que proyectan al Núcleo Accumbens (NAc), es crucial para la recompensa y la motivación. En modelos de depresión, la actividad de las neuronas dopaminérgicas del VTA puede estar alterada. Estudios optogenéticos (usando luz para controlar neuronas) han demostrado que modular la actividad fásica de las neuronas VTA-NAc puede inducir o aliviar conductas depresivas, aunque con resultados que dependen del contexto del estrés, sugiriendo poblaciones de neuronas dopaminérgicas con funciones distintas.
La Habénula Lateral y el Núcleo del Rafe Dorsal
La Habénula Lateral (LHb) integra información del prosencéfalo y el mesencéfalo, jugando un papel en las conductas motivadas y la aversión. La hiperactividad de la LHb se ha asociado con la depresión en modelos animales. El Núcleo del Rafe Dorsal (DRN) es la principal fuente de Serotonina (5-HT) en el cerebro y tiene proyecciones recíprocas con la LHb y otras regiones implicadas en el estado de ánimo. La LHb puede influir en la actividad del DRN, y se ha observado una mayor excitabilidad de las interneuronas GABAérgicas en el DRN de ratones susceptibles al estrés, lo que lleva a una disminución de la actividad serotoninérgica.
El Locus Coeruleus y el Sistema Noradrenérgico
El Locus Coeruleus (LC) es el principal núcleo Noradrenalinaérgico y un componente vital de la respuesta al estrés, aumentando su actividad en modelos de estrés. Recibe proyecciones glutamatérgicas del CPF y la LHb. La disfunción en la interacción glutamatérgica-noradrenérgica en el LC podría contribuir a la depresión. Circuitos como el LH (orexina)-LC (noradrenalina)-Amígdala, implicados en el aprendizaje del miedo, también podrían jugar un papel.
Amígdala y Circuitos del Miedo/Recompensa
La Amígdala, especialmente la basolateral (BLA), está implicada en el procesamiento del miedo y el estrés. Se ha identificado poblaciones de neuronas en la BLA que proyectan al NAc (asociadas a la recompensa) y otras que proyectan a la amígdala central (CeM, asociadas a la aversión). El estrés puede alterar el equilibrio entre las entradas corticales y talámicas a la BLA, posiblemente desplazando el procesamiento hacia vías subcorticales rápidas, que, en un estado crónico, podrían volverse desadaptativas.
Núcleo Accumbens: Recompensa y Motivación
El Núcleo Accumbens (NAc) juega un papel crítico en la sintomatología depresiva, incluyendo la anhedonia (pérdida de interés/placer) y la reducción de la motivación. Las neuronas espinosas medianas (MSNs) del NAc, enriquecidas en receptores D1 o D2 de dopamina, proyectan a diferentes estructuras. Un desbalance entre la actividad de las MSNs D1 (asociadas a recompensa/conducta positiva) y D2 (asociadas a aversión/conducta negativa) puede promover estados motivacionales disfuncionales. Modelos de depresión muestran una disminución de la fuerza sináptica excitatoria en las MSNs D1. La modulación crónica de la actividad de estas subpoblaciones puede inducir conductas depresivas. La plasticidad de las espinas dendríticas en el NAc, regulada por vías como IKK/NFkB y BDNF, es crucial y se ve alterada en la depresión.
Adaptaciones Homeostáticas
El cerebro posee mecanismos de homeostasis para estabilizar la actividad neuronal frente a perturbaciones. En modelos de depresión, se ha observado hiperactividad de las neuronas dopaminérgicas del VTA, asociada a un aumento de la corriente Ih (una fuerza excitatoria). Curiosamente, en los animales resilientes al estrés, aunque también pueden mostrar un aumento de Ih, este se acompaña de un aumento compensatorio en corrientes de potasio (K+) que estabilizan la actividad. Esta adaptación homeostática en las neuronas VTA-NAc podría ser clave para la resiliencia natural al estrés, sugiriendo nuevas estrategias terapéuticas enfocadas en potenciar estos mecanismos.
El Rol del Sistema Inmune
Existe una creciente evidencia que vincula los procesos inflamatorios con la patofisiología de la depresión. Se han encontrado niveles elevados de citoquinas pro-inflamatorias en el cerebro de pacientes deprimidos post-mortem y en modelos animales de estrés crónico. La administración de citoquinas o inductores de inflamación puede causar conductas depresivas. Estudios recientes sugieren que el estado inflamatorio, medido por citoquinas periféricas como la IL-6, podría ser un predictor de vulnerabilidad al estrés. Sin embargo, la relación es compleja, ya que fármacos antiinflamatorios atenuaron los efectos antidepresivos de la DBS en un estudio, lo que requiere más investigación.
Ritmos Circadianos, Sueño y Depresión
Las alteraciones en los ritmos circadianos y del sueño son síntomas comunes en la depresión. La teoría del "Social Zeitgeber" propone que eventos estresantes que alteran los horarios de sueño/vigilia pueden desincronizar los ritmos moleculares y celulares en individuos vulnerables, precipitando la depresión. La Terapia de Privación del Sueño (SDT) puede aliviar rápidamente los síntomas depresivos en muchos pacientes, aunque el efecto suele ser transitorio tras recuperar el sueño, sugiriendo que podría estar "reseteando" un reloj circadiano aberrante.
Se han identificado alteraciones en la expresión de genes reloj circadianos (como Per1 y Per2) en pacientes deprimidos y modelos animales. La manipulación de estos genes en el VTA puede modular tanto los ritmos circadianos como las conductas depresivas. Estos hallazgos revelan una conexión molecular entre el sistema circadiano y la regulación del estado de ánimo, ofreciendo posibles dianas terapéuticas.
Preguntas Frecuentes
¿Es la depresión simplemente un desbalance químico?
No, la investigación actual sugiere que es un trastorno mucho más complejo que implica disfunciones en múltiples niveles, desde moléculas y genes hasta la comunicación y la plasticidad de los circuitos neuronales. Si bien los neurotransmisores son importantes, no son la única causa.
¿Por qué los antidepresivos tardan tanto en hacer efecto?
La latencia de semanas o meses sugiere que su acción no es solo inmediata sobre los neurotransmisores, sino que implica cambios más lentos y duraderos en el cerebro, como la plasticidad sináptica, la señalización molecular a largo plazo o posiblemente, aunque debatido, la neurogénesis.
¿El estrés temprano en la vida puede aumentar el riesgo de depresión?
Sí, hay fuerte evidencia que sugiere que la exposición a estrés significativo en etapas tempranas del desarrollo puede inducir cambios epigenéticos y estructurales en el cerebro que aumentan la vulnerabilidad a trastornos del estado de ánimo en la adultez.
¿Qué implican los hallazgos sobre los circuitos cerebrales para los tratamientos futuros?
Sugieren que las terapias más efectivas podrían no solo dirigirse a neurotransmisores específicos, sino a modular la actividad de redes neuronales disfuncionales (como la DBS), o a corregir las alteraciones moleculares, epigenéticas o de plasticidad que subyacen a estas disfunciones.
¿Cómo afecta el sueño a la depresión?
Existe una estrecha relación. La desregulación de los ritmos circadianos y del ciclo sueño-vigilia es un síntoma común y se cree que contribuye a la patología. La privación de sueño puede aliviar temporalmente los síntomas, sugiriendo que restaurar los ritmos normales es terapéutico.
Conclusión
La depresión mayor es una enfermedad heterogénea cuya complejidad se refleja en la diversidad de síntomas y la respuesta variable a los tratamientos. La neurociencia moderna, superando la visión simplista del desbalance químico, la entiende cada vez más como un trastorno de la compleja red de circuitos cerebrales. La disfunción en la plasticidad sináptica, las alteraciones epigenéticas inducidas por el ambiente, los cambios en la neurogénesis y las fallas en los mecanismos de homeostasis contribuyen a la patofisiología.
La investigación continua, utilizando herramientas avanzadas para estudiar moléculas, genes y circuitos, es fundamental para desentrañar completamente los mecanismos subyacentes a la depresión. Solo así podremos desarrollar tratamientos más precisos, rápidos y efectivos que aborden la raíz de las disfunciones neuronales que caracterizan este devastador trastorno.
Si quieres conocer otros artículos parecidos a La Depresión: Un Trastorno de Circuitos puedes visitar la categoría Neurociencia.

