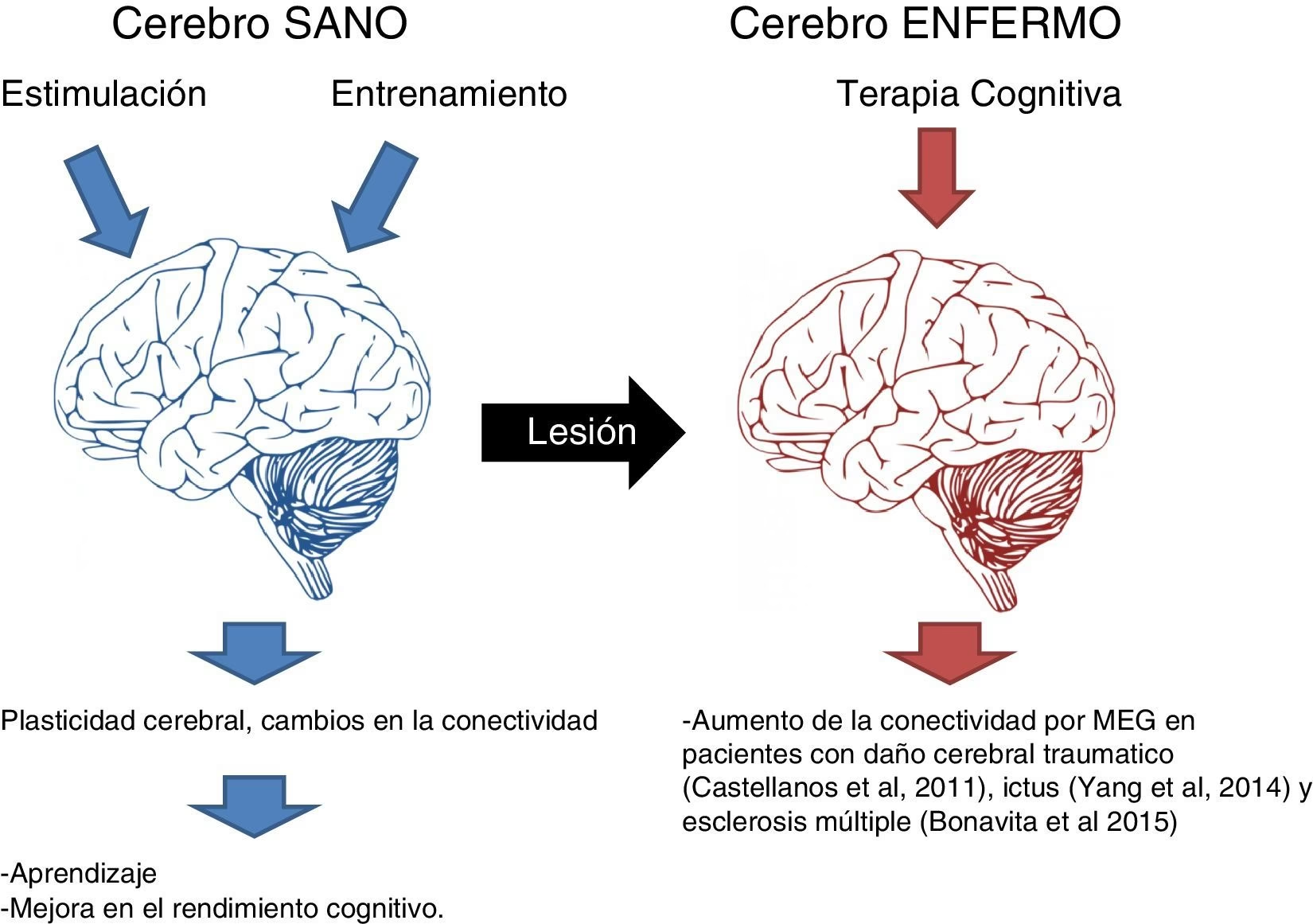
Durante mucho tiempo se sostuvo la creencia de que el desarrollo y la capacidad de recuperación del cerebro se detenían una vez alcanzada la edad adulta. Sin embargo, los avances en las técnicas modernas de neuroimagen cerebral han revolucionado nuestra comprensión, permitiendo reconceptualizar la dinámica y el funcionamiento del sistema nervioso central. Existe una creciente evidencia que demuestra que el encéfalo posee una notable capacidad para cambiar y adaptarse a diversas circunstancias, no solo en las etapas tempranas de la vida como la infancia y la adolescencia, sino también a lo largo de la edad adulta e incluso en escenarios de lesión cerebral. Esta flexibilidad y modificabilidad del cerebro se conoce como neuroplasticidad.

El objetivo de este artículo es explorar en profundidad este fascinante concepto. Realizaremos una revisión de sus principales aspectos históricos, definiciones clave, así como los complejos procesos genéticos, bioquímicos y fisiológicos que lo sustentan. La comprensión de la neuroplasticidad es fundamental, ya que constituye la base de muchas técnicas de recuperación neurológica y neuropsicológica empleadas en campos como la rehabilitación. Al final, se definen algunos términos esenciales para una mejor comprensión del tema.
Aspectos Históricos de la Neuroplasticidad
La historia de la neurociencia moderna está marcada por debates fundamentales sobre la organización cerebral. En 1861, Pierre Paul Broca publicó un artículo que localizaba la función del lenguaje articulado en el giro frontal inferior izquierdo. Años más tarde, en 1874, Carl Wernicke identificó otra área crucial para la comprensión del lenguaje en el giro temporal superior izquierdo. Estos trabajos sentaron las bases de la corriente localizacionista, que postula que funciones específicas tienen ubicaciones precisas en el cerebro.
Paralelamente, surgió un debate sobre la estructura fundamental del tejido nervioso. En 1888, Santiago Ramón y Cajal propuso que el cerebro estaba compuesto por unidades discretas llamadas neuronas, una idea conocida como la teoría neuronal. En contraposición, Camilo Golgi defendió la teoría reticular, visualizando el cerebro como un gran sincitio interconectado, sin unidades individuales claras.
Estas teorías, localizacionista (Broca y Wernicke), neuronal (Ramón y Cajal) y reticular (Golgi), formaron el núcleo de la neurociencia naciente entre 1860 y 1890. Más recientemente, la corriente conexionista, impulsada por Donald Hebb, describió el funcionamiento cerebral a través de vastas redes neuronales distribuidas e interconectadas, conciliando en cierta medida las visiones anteriores.
La autoría original del término neuroplasticidad es objeto de discusión. Se atribuye a Ernesto Lugaro, en 1906, el uso del término plasticidad cortical para referirse a la idea de que el paso del impulso nervioso podría dejar una huella física o química en la neurona. En 1938, Margaret Kennard realizó experimentos con monos, mostrando que las lesiones cerebrales en edades tempranas resultaban en déficits motores menos severos que en adultos. Este hallazgo dio origen al Principio de Kennard, que sugiere una mayor capacidad de recuperación en cerebros jóvenes debido a una plasticidad más pronunciada. En 1947, Donald Hebb, basándose en las ideas de Lugaro, propuso que la experiencia conducía a una remodelación sináptica.
Entre las décadas de 1960 y 1970, estudios que utilizaban técnicas avanzadas como la ultraestructura sináptica, el análisis de factores de crecimiento neuronal y la investigación sobre la potenciación a largo plazo en las sinapsis, transformaron radicalmente la visión científica del cerebro. Se pasó de considerar el tejido nervioso como una estructura rígida e inmutable a entenderlo como una estructura dinámica, adaptable y plástica.
Aunque los primeros trabajos de Broca sobre el deterioro del lenguaje tras una lesión generaron una percepción inicial de limitada recuperación cerebral, la década de 1970 trajo consigo trabajos experimentales clave que validaron los conceptos de neuroplasticidad en el ámbito clínico. Los estudios de Merzenich et al. mostraron cambios en los mapas somatosensoriales de monos adultos tras una amputación digital. Kaas, Merzenich y Killackey observaron la reorganización de la corteza somatosensorial después de daño nervioso periférico en mamíferos adultos. Wall y Egger demostraron la formación de nuevas conexiones en cerebros de ratones adultos tras una deaferentización parcial. Estos estudios demostraron cambios estructurales en el sistema nervioso central de animales adultos, que se traducían en mejorías adaptativas bajo entrenamiento específico tras una lesión inducida.
Entre 1990 y 2010, los principales avances se centraron en terapias basadas en células madre neuronales, el uso de factores de crecimiento nervioso y el papel de las enzimas en el sistema nervioso central, consolidando la relevancia clínica de la neuroplasticidad.
Conceptos Generales de Neuroplasticidad
La neuroplasticidad puede definirse como la capacidad intrínseca del sistema nervioso para modificar su reactividad como resultado de activaciones sucesivas. Esta capacidad permite que el tejido nervioso experimente cambios adaptativos o reorganizacionales, tanto en un estado fisiológico normal como tras una alteración. Otros autores la definen de manera más amplia como cualquier respuesta cerebral que surge ante cambios internos o externos, manifestándose en modificaciones reorganizacionales en la percepción y la cognición.
Estas definiciones posicionan la neuroplasticidad como uno de los pilares fundamentales que sustentan procesos de gran complejidad, como las funciones cognitivas superiores, entendiéndolas desde una perspectiva conexionista más que estrictamente localizacionista.
En 1982, PubMed adoptó la definición de plasticidad neuronal como término clave (MeSH), describiéndola como la capacidad del sistema nervioso para cambiar su reactividad como resultado de activaciones sucesivas, categorizándola como un proceso fisiológico.
Un aspecto relevante de la plasticidad es la neurogénesis, el proceso de producción, diferenciación y supervivencia de neuronas nuevas. Aunque no todas las neuronas generadas en etapas inmaduras son funcionales, la neurogénesis es un proceso plástico regulado por la experiencia que persiste en ciertas regiones cerebrales adultas, como el hipocampo, la mucosa olfatoria y la zona periventricular.
Una forma tangible en que se manifiesta la neuroplasticidad es a través de la corteza cerebral, lo que se conoce como plasticidad cortical. Esta se subdivide en plasticidad cortical fisiológica, que es el sustrato del aprendizaje y la memoria, así como del neurodesarrollo, y plasticidad cortical patológica, que puede ser adaptativa (favoreciendo la recuperación funcional tras una lesión) o mal adaptativa (contribuyendo a déficits o condiciones crónicas).
La neuroplasticidad es el fundamento de los procesos de neurorehabilitación. En 2006, se la definió como un proceso continuo de remodelación de mapas neurosinápticos a corto, mediano y largo plazo, que optimiza el funcionamiento de las redes cerebrales durante la filogenia, la ontogenia y después de daños en el sistema nervioso.
La plasticidad que ocurre durante el desarrollo (ontogenia) para crear nuevos circuitos de aprendizaje y mantener redes neuronales en adultos y ancianos se denomina plasticidad natural. Cuando los cambios ocurren después de lesiones periféricas o centrales y contribuyen a la recuperación clínica, se habla de plasticidad post-lesional.
Bruce Dobkin clasifica los mecanismos plásticos en dos grandes grupos: plasticidad de redes neuronales y plasticidad en las sinapsis. La plasticidad del sistema nervioso central abarca mecanismos como la neurogénesis, la apoptosis (muerte celular programada), el crecimiento de brotes dendríticos y axónicos, la potenciación a largo término (PLT), la depresión a largo término (DLT), y el reclutamiento de corteza adyacente o del hemisferio contralateral.
La complejidad de la neuroplasticidad es tal que su comprensión requiere un enfoque de biología de sistemas, modelos computacionales y neuroinformática. Se reconocen mecanismos como la plasticidad sináptica y la plasticidad de la excitabilidad neuronal intrínseca.
Aquí se presenta una tabla que resume algunos de los mecanismos plásticos principales mencionados en el texto, categorizados según la división propuesta por Bruce Dobkin:
| Tipo de Plasticidad (según Dobkin) | Mecanismos Implicados (según el texto) |
|---|---|
| Plasticidad de redes neuronales | Neurogénesis, Apoptosis, Brotes dendríticos y axónicos, Reclutamiento de corteza adyacente, Reclutamiento del hemisferio contralateral |
| Plasticidad en las sinapsis | Potenciación a largo término (PLT), Depresión a largo término (DLT), Desenmascaramiento sináptico |
Procesos Genéticos, Bioquímicos y Fisiológicos
La capacidad de respuesta de una neurona a las señales no está siempre preprogramada de forma rígida. Esto es posible gracias a complejos procesos biomoleculares que incluyen aspectos neurobioquímicos, neurogenómicos y neuroproteómicos.
Genética y expresión protéica en la plasticidad cerebral
La era postgenómica ha revelado la implicación de genes y sus productos en la plasticidad sináptica. Genes como FOX, Homer1a y NACC-1, así como factores de crecimiento como el factor neurotrófico cerebral (BDNF), el factor de crecimiento endotelial vascular (VEGF) y el factor de crecimiento derivado de insulina (IGF), junto con las apoproteínas E, desempeñan roles cruciales en los cambios neuroplásticos.
La homeostasis neuroplástica, en gran medida mediada por el IGF, y los mecanismos moleculares de la plasticidad sináptica son esenciales para regular procesos neurogénicos, incluyendo el nacimiento, promoción, maduración y mantenimiento de las neuronas.
El gen FOXP2 es uno de los más estudiados en relación con la neuroplasticidad, particularmente por su vínculo con el lenguaje. Se expresa en circuitos motores implicados en el habla y el lenguaje (ganglios basales, tálamo, cerebelo) y mutaciones en este gen se asocian con dificultades en su aprendizaje y adquisición.
Ciertos alelos de las apoproteínas E (ε2 y ε3) también parecen estar relacionados con una mayor capacidad de reparación sináptica, favoreciendo la neuroplasticidad.
Neurobioquímica y fisiología de algunos procesos de plasticidad cerebral
La neuroplasticidad es un continuo de mecanismos eléctricos, genéticos, estructurales, bioquímicos y funcionales. A nivel molecular, dos rutas biomoleculares clave para la potenciación a largo término (PLT) y la depresión a largo término (DLT), procesos fundamentales para la memoria y el olvido, respectivamente, son la excitabilidad intrínseca (cambios en canales iónicos) y la plasticidad sináptica (cambios en la fuerza de la sinapsis).
Un punto crucial en los fenómenos neuroplásticos mediados por PLT o DLT es el manejo celular del calcio (Ca2+). La PLT suele depender de receptores como NMDA, AMPA y kainato. La DLT requiere canales L de Ca2+, receptores NMDA y metabotrópicos de glutamato (RmGlu).
La liberación presináptica de glutamato y la despolarización postsináptica aumentan el Ca2+. Según el tipo de neurona, esto activa receptores NMDA, RmGlu o canales de Ca2+ dependientes de voltaje (CCDV).
Tras la activación de receptores transmembrana, se desencadenan cascadas de señalización mediadas por proteínas kinasas y fosfatasas que modulan la plasticidad sináptica. Los receptores AMPA están implicados; por ejemplo, el Ca2+ activa la proteína kinasa 2 dependiente de calmodulina-Ca2+ (PKDCAL2), que fosforila una subunidad de AMPAR, aumentando su número funcional.
Neurotransmisores como dopamina, noradrenalina o adenosina, a través de receptores acoplados a proteínas G, pueden activar la adenilato ciclasa, induciendo PLT. El AMP cíclico resultante activa la proteína kinasa A, que también fosforila subunidades de AMPAR.
Para una plasticidad sináptica estable, se activan vías que involucran receptores tirosina kinasas, modulando la transcripción genética y la transducción proteica. Las señales sinápticas y la actividad neuronal activan redes bioquímicas que llevan a la fosforilación de AMPAR, transcripción génica y síntesis proteica, impulsando así la plasticidad.
Esta dinámica de la plasticidad sináptica actúa como un engranaje molecular que conecta el ambiente externo, lleno de sensaciones, con la realidad cerebral interna. Como señala Tansey, el sistema nervioso es increíblemente sutil y complejo, y sus conexiones no son meramente binarias, sino moduladas con muchos estados de activación o desactivación.
La capacidad de producir PLT varía según la red neuronal. En el hipocampo y la neocorteza, requiere PKDCAL2. El hipocampo necesita además RmGlu para consolidar la memoria. En el striatum, se requiere proteína kinasa A, y en el cerebelo, proteína kinasa C. Esto subraya que, aunque la neuroplasticidad es un proceso general, sus mecanismos específicos varían según la estructura encefálica.
Plasticidad extraneuronal
La plasticidad no es exclusiva de las neuronas. La neuroglia, que incluye astrocitos, oligodendrocitos y microglía, juega un papel crucial. La glía participa en la neovascularización, regulación energética y metabólica, modulación astrocítica del calcio para la sinaptogénesis y señalización neuronal. Existen, por tanto, importantes procesos neuroplásticos de orden extraneuronal.
Componentes de la matriz extracelular, como los glicanos (cadenas de monosacáridos), también son esenciales. El ácido polisiálico (APS), asociado a moléculas de adhesión celular neuronal (NCAM), interviene en la migración celular, crecimiento neurítico, formación sináptica y eficiencia sináptica. Se ha identificado su expresión en regiones plásticas como el hipocampo y parece ejercer funciones en la regeneración de axones y dendritas tras una lesión.
Las integrinas, moléculas estructurales de la matriz extracelular, y sus receptores, también realizan funciones reguladoras neuronales en procesos fisiológicos como la memoria y en condiciones patológicas como la inflamación o la cicatrización. Tienen la capacidad de modular canales iónicos como los NMDA y AMPA, disminuyendo corrientes citotóxicas de glutamato.
Otras moléculas de la matriz extracelular, las neurotrofinas, controlan la supervivencia, diferenciación y reparación neuronal, trabajando estrechamente con el factor de crecimiento nervioso (FCN) y el BDNF. También influyen en la neurotransmisión y la reorganización sináptica.
Neuroplasticidad y Aprendizaje
Como se mencionó anteriormente, la plasticidad cortical fisiológica es considerada el sustrato fundamental del aprendizaje y la memoria humana. La capacidad del cerebro para formar nuevas conexiones sinápticas, fortalecer las existentes (como en la potenciación a largo término) o debilitarlas (como en la depresión a largo término) es directamente el mecanismo biológico subyacente a la adquisición de nuevas habilidades, conocimientos y la consolidación de recuerdos. Cada vez que aprendemos algo nuevo, ya sea un idioma, una habilidad motora o un concepto abstracto, se están produciendo cambios a nivel sináptico y de redes neuronales. La repetición y la práctica refuerzan estas conexiones, haciendo que el aprendizaje sea más robusto y el recuerdo más accesible. Por lo tanto, la neuroplasticidad no es solo un fenómeno de recuperación tras una lesión, sino un proceso continuo y esencial para el aprendizaje a lo largo de toda la vida.
Preguntas Frecuentes sobre Neuroplasticidad
- ¿Qué es exactamente la neuroplasticidad?
- Es la capacidad del sistema nervioso para cambiar su estructura y función en respuesta a la experiencia, el aprendizaje o una lesión. Permite que el cerebro se adapte y se reorganice.
- ¿El cerebro solo es plástico en la infancia?
- No. Aunque la plasticidad es más pronunciada en etapas tempranas, el cerebro mantiene su capacidad de cambio a lo largo de toda la vida adulta e incluso en la vejez, aunque los mecanismos pueden variar.
- ¿Quiénes fueron figuras clave en el estudio temprano del cerebro?
- Pioneros incluyen a Broca y Wernicke (localizacionismo), Ramón y Cajal (teoría neuronal), Golgi (teoría reticular) y Hebb (conexionismo), quienes sentaron las bases para entender la organización y el funcionamiento cerebral.
- ¿Qué tipos de neuroplasticidad existen?
- Se puede clasificar de diversas maneras: plasticidad cortical (fisiológica y patológica), plasticidad natural (desarrollo y aprendizaje continuo) y post-lesional (recuperación tras daño). También se divide en plasticidad de redes neuronales y plasticidad en las sinapsis.
- ¿Cómo funcionan los mecanismos plásticos a nivel molecular?
- Involucran cambios en la expresión genética, la síntesis de proteínas, la liberación de factores de crecimiento y, crucialmente, la modulación de la fuerza sináptica a través de la regulación del calcio y la actividad de receptores (como NMDA y AMPA) y proteínas kinasas.
- ¿La plasticidad cerebral solo ocurre en las neuronas?
- No. La glía (astrocitos, etc.) y los componentes de la matriz extracelular también desempeñan roles activos en la plasticidad, regulando el entorno neuronal, la formación de sinapsis y la regeneración.
- ¿Qué tiene que ver la neuroplasticidad con el aprendizaje y la memoria?
- La plasticidad sináptica, especialmente la potenciación a largo término y la depresión a largo término, es el mecanismo biológico fundamental que subyace al aprendizaje y la formación de la memoria. El cerebro cambia físicamente a medida que aprendemos.
- ¿Por qué es importante la neuroplasticidad en la rehabilitación?
- La neuroplasticidad post-lesional es la base de la recuperación funcional. Las terapias de rehabilitación buscan aprovechar esta capacidad del cerebro para reorganizar circuitos y compensar las áreas dañadas, facilitando la recuperación de funciones perdidas.
Conclusiones
El tejido nervioso ya no se considera una estructura estática, sino un sistema notablemente dinámico, adaptable y plástico. La neuroplasticidad es una propiedad intrínseca del sistema nervioso que integra las visiones localizacionistas y conexionistas en la comprensión moderna del funcionamiento cerebral.
Este proceso es múltiple y generalizado en la biología cerebral, pero a la vez particular de cada red neuronal específica. Su complejidad requiere un enfoque que involucre la bioquímica, la genómica y la proteómica, ya que no se limita a simples modificaciones estructurales de las dendritas, sino que implica adaptaciones intra y extra-celulares mediadas por diversas rutas de señalización biomolecular.
Los procesos biomoleculares aseguran que la respuesta neuronal no esté rígidamente predeterminada. La neuroplasticidad es, por tanto, un proceso continuo de remodelación de mapas neurosinápticos que ocurre tanto en la ausencia como en la presencia de daño cerebral.
El conocimiento profundo de la neuroplasticidad abre vías para futuros blancos farmacológicos y terapéuticos en la prevención, tratamiento y rehabilitación de enfermedades neurológicas. Redefine la biología cerebral desde una perspectiva evolutiva, básica y clínica.
Para los profesionales de la salud involucrados en la neuro-rehabilitación, ya sea farmacológica o no farmacológica, comprender el sustrato neurofisiológico y neuroquímico de los fenómenos plásticos cerebrales es una herramienta invaluable. Permite diseñar planes de rehabilitación dirigidos, controlados, replicables e intensivos, maximizando el potencial de recuperación del paciente basado en la capacidad innata del cerebro para cambiar y adaptarse.
Si quieres conocer otros artículos parecidos a Neuroplasticidad: El Cerebro Dinámico puedes visitar la categoría Neurociencia.