En la era moderna, los cambios drásticos en nuestro entorno y estilo de vida plantean serias amenazas para la salud humana. Entre los principales desafíos globales se encuentra un aumento sin precedentes en una amplia gama de trastornos neurológicos. Durante la última década, ha quedado claro que la microbiota intestinal tiene un papel potencial en la función cerebral, mediando vías de señalización a través de metabolitos microbianos. En la intersección de la neurociencia y la microbiología, estudios innovadores han revelado relaciones activas entre los animales y las poblaciones microbianas que viven en su interior, apoyando el desarrollo y funcionamiento de los sistemas neurológicos. Estas interacciones, que involucran comunicación inmunológica, neural y química, son complejas pero vitales para la salud de los individuos y nuestra comprensión de los trastornos neurológicos.

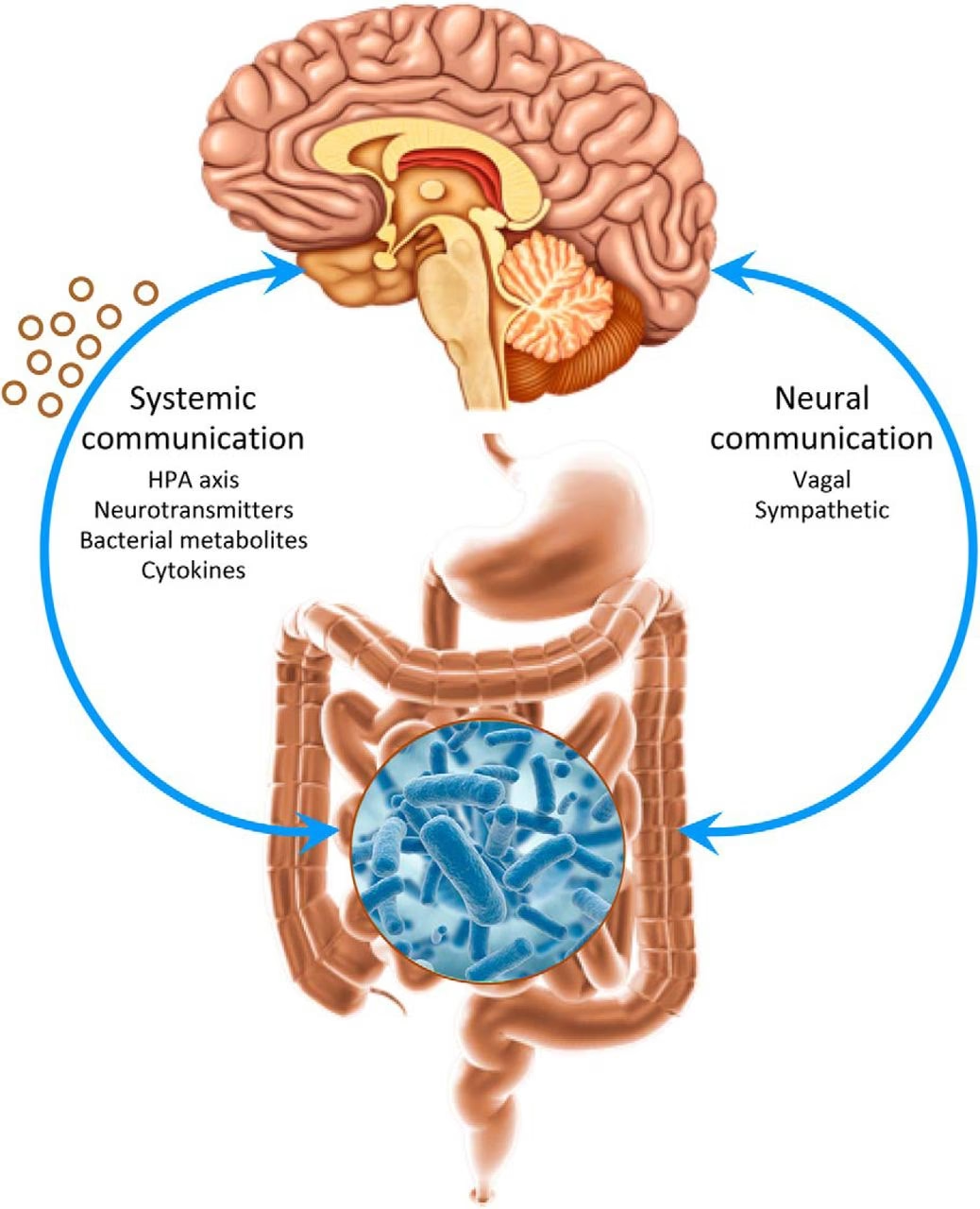
La microbiota intestinal, que reside en el tracto gastrointestinal, desempeña un papel importante en el estado de salud del huésped al regular células en órganos locales y distantes, incluido el cerebro. La transmisión bidireccional ocurre en el eje intestino-cerebro en forma de un mecanismo de comunicación bidireccional entre el intestino y el sistema neurológico del huésped. Esta información puede transferirse a través de redes cerebrales, hormonas y el sistema inmunológico, lo que facilita la microbiota intestinal. La transmisión bidireccional en el eje intestino-cerebro regula mecánicamente la disfunción cerebral, mantiene una asociación mutualista con el huésped y regula los sistemas inmunológicos innato y adaptativo. Este eje involucra diferentes vías, como el sistema nervioso autónomo y entérico, el sistema endocrino, el eje hipotalámico-pituitario-suprarrenal (HPA), el sistema inmunológico y la microbiota y sus metabolitos.
Una microbiota intestinal sana beneficia al huésped produciendo metabolitos microbianos y neurotransmisores para la comunicación con las células del huésped, como las células epiteliales intestinales y las células inmunes. Las alteraciones en la microbiota intestinal y la producción de metabolitos microbianos se han relacionado con una amplia gama de trastornos neurológicos relacionados con el sistema inmune, incluidos trastornos del desarrollo, neurodegeneración y desregulación emocional. El tracto digestivo es el hábitat de más del 98% de las bacterias en nuestros cuerpos. El término "microbiota intestinal" se refiere a los microorganismos particulares que están presentes y residen en el intestino.
El desarrollo de técnicas ómicas ha contribuido a la comprensión de la microbiota intestinal como uno de los reguladores clave de las interacciones entre el intestino y el cerebro. La investigación en animales y humanos ha proporcionado evidencia de que la microbiota intestinal podría influir en el comportamiento cerebral y el desarrollo cognitivo produciendo hormonas, factores inmunológicos y metabolitos, lo que también sugiere que cambiar el microbioma intestinal puede mejorar o potencialmente tratar trastornos cerebrales. Las señales del cerebro pueden afectar las funciones sensomotoras y secretoras del estómago a través de intrincadas redes neurohumorales, y de manera similar, las señales aferentes viscerales que llegan al tracto gastrointestinal pueden afectar la función cerebral. El eje intestino-cerebro ha surgido recientemente como un participante clave en la regulación del funcionamiento cerebral normal en condiciones fisiológicas normales, así como en el desarrollo de enfermedades neuropatológicas como factor o condición de riesgo.
El Fascinante Eje Intestino-Cerebro
El microbioma intestinal está compuesto por bacterias, arqueas, virus y microbios eucariotas que colonizan el tracto digestivo. La microbiota intestinal, que comprende aproximadamente 100 a 150 veces más genes que el genoma humano, se encuentra en los intestinos humanos e incluye aproximadamente 1,000 especies y 7,000 tipos de bacterias. Los Firmicutes grampositivos o gramnegativos (incluidas las especies Lactobacillus, Eubacterium y Clostridium) y los Bacteroidetes gramnegativos forman la mayoría de las bacterias (que contienen Bacteroides y Prevotella). Los siguientes cinco filos constituyen la mayoría de la comunidad microbiana intestinal: Bacteroidetes, Firmicutes, Actinobacteria, Proteobacteria y Verrucomicrobia. La dieta, la edad, el género, el entorno y los genes de los individuos tienen un impacto en la composición de su microbiota intestinal. La disbiosis del microbioma intestinal humano se ha asociado con diversas patologías.
La disbiosis intestinal, manifestada por variaciones en la diversidad y frecuencia de la comunidad microbiana (taxones y especies en general) que componen la flora intestinal, se ha relacionado en estudios tanto en animales como en humanos con agregación anormal de proteínas cerebrales, inflamación, desregulación inmune y reducción de la actividad neuronal y sináptica en estudios de Enfermedad de Alzheimer. La capacidad de la microbiota intestinal para afectar las actividades relacionadas con el cerebro sugiere que desencadena la producción de factores inmunes que actúan tanto en el sistema nervioso central (SNC) como en el sistema nervioso entérico (SNE), como citoquinas y mediadores inflamatorios.
El sistema nervioso autónomo, un componente del sistema nervioso periférico, regula procesos fisiológicos no sujetos a control consciente. Controla funciones viscerales vitales coordinando respuestas complementarias entre los sistemas nerviosos simpático y parasimpático. La comprensión de la comunicación bidireccional entre el SNC y el tracto digestivo avanzó enormemente con el descubrimiento del SNE, una rama del sistema nervioso autónomo. El SNE, a veces conocido como el "segundo cerebro del cuerpo", se mantiene en un estado saludable gracias a la cooperación de las neuronas entéricas y las conexiones con el SNC. El SNE está compuesto por millones de neuronas que se encuentran en la mucosa del tracto digestivo. Estas neuronas son responsables de mantener el equilibrio de las actividades intestinales. La ruta de comunicación más directa entre el intestino y el cerebro es el nervio vago.
Una comprensión más profunda de la conexión intestino-cerebro mostró una compleja vía de comunicación que no solo mantiene la salud del sistema gastrointestinal, sino que también es probable que tenga una variedad de consecuencias sobre cómo funciona el cerebro en general, incluida la función cognitiva superior y la motivación. El eje intestino-cerebro (EIC), que es una sofisticada red de comunicación bidireccional entre el intestino y el SNC, es donde ocurre la comunicación entre el SNC y el intestino. Las rutas de comunicación incluyen el sistema nervioso autónomo (por ejemplo, el sistema nervioso entérico (SNE) y el nervio vago), el sistema neuroendocrino, el eje hipotalámico-pituitario-suprarrenal (HPA), el sistema inmunológico y las vías metabólicas. Varios neurotransmisores y metabolitos, incluidos los ácidos grasos de cadena corta, los ácidos biliares secundarios, las vitaminas vitales y los aminoácidos, modulan muchas vías del sistema inmunológico, que a su vez afectan la cognición, el comportamiento, el aprendizaje, el movimiento y las enfermedades neurodegenerativas. El eje intestino-cerebro ha sido denominado eje MGI (Microbiota-Gut-Brain) ya que parece regular el sistema inmunológico, el tracto digestivo, el comportamiento, la respuesta al estrés y los procesos del SNC.
Cómo la Microbiota Intestinal Afecta el Cerebro
El SNC y el SNE se comunican entre sí utilizando una serie de mecanismos de señalización química, incluidas vías neuronales directas, inmunes y endocrinas. El eje intestino-cerebro es una red de conexiones que involucra múltiples sistemas biológicos que facilita la comunicación bidireccional entre las bacterias intestinales y el cerebro, y es vital para mantener los sistemas gastrointestinal, neurológico y microbiano de los animales. Además del sistema neurológico, la microbiota intestinal también afecta el cerebro a través de los sistemas endocrino, inmunológico y metabólico (la vía neuroanatómica intestino-cerebro). En el eje microbiota intestinal-cerebro, se pone más énfasis en la participación de las bacterias porque la microbiota intestinal puede usarse como variable independiente y modificarse intencionalmente. Los microbios pueden afectar la forma en que se desarrolla, madura, envejece y mantiene la homeostasis el sistema nervioso, por ejemplo, alterando la forma en que se expresan los factores neurotróficos y las subunidades del receptor N-metil D-aspartato (NMDA) en el hipocampo.
Las principales formas en que la microbiota puede influir en el desarrollo y la función del sistema nervioso son las redes biológicas, incluida la transmisión directa e indirecta a través de transmisores químicos, el sistema inmunológico, las vías neuronales y las vías endocrinas. La respuesta del eje HPA implica neuronas del hipotálamo que liberan hormonas como la hormona liberadora de corticotropina (CRH) en la circulación portal o el cerebro, causando la liberación de la hormona adrenocorticotrópica (ACTH), que inicia la producción y liberación de cortisol. Las reacciones de señalización neuroinmune son reguladas por el cortisol.
Microbiota y Neurotransmisores
Los microbios intestinales pueden ayudar a regular las funciones corporales y alterar el comportamiento en su huésped animal a través de interacciones químicas con el sistema nervioso, incluida la comunicación "directa" e "indirecta". Los microorganismos tienen la capacidad de sintetizar algunos de los compuestos neuroactivos ellos mismos, así como de estimular la producción de otros metabolitos y neurotransmisores por parte del huésped que regulan la señalización intestino-cerebro. La microbiota también es necesaria para la maduración, activación y desarrollo normal de la microglia, que son células inmunes innatas en el cerebro. Parece que la programación inmune por la microglia está regulada por señales del metabolismo microbiano, ya que la administración de ácidos grasos de cadena corta (AGCC) derivados de bacterias a ratones libres de gérmenes restaura la forma y función microglial. Moléculas derivadas de microbios que señalizan al cerebro. Neurotransmisores como la dopamina, la serotonina, la norepinefrina, la glicina y el ácido gamma-aminobutírico son producidos por la microbiota intestinal, y cada uno tiene un impacto específico en el cerebro. Los desequilibrios en estos neurotransmisores pueden llevar a trastornos como la Enfermedad de Alzheimer, la Enfermedad de Parkinson, el trastorno del espectro autista, los trastornos de ansiedad y los trastornos depresivos.
Por ejemplo, Bifidobacterium infantis aumenta los niveles plasmáticos de triptófano, lo que afecta la transmisión central de serotonina; el GABA puede ser producido por Lactobacillus y Bifidobacterium; la noradrenalina puede ser producida por especies de Escherichia, Bacillus y Saccharomyces; la serotonina puede ser producida por especies de Streptococcus, Candida, Escherichia y Enterococcus; la dopamina puede ser producida por bacterias; y la acetilcolina puede ser producida por Lactobacillus. Los AGCC, un tipo de señalización directa, son lípidos generados por microbios intestinales a través de la fermentación de fibra dietética que tienen la capacidad de influir en el sistema inmunológico, la epigenética y la neuroplasticidad en el SNC. El cerebro, el equilibrio energético y el metabolismo se ven afectados por los AGCC, que incluyen butirato, propionato y acetato, y son subproductos metabólicos vitales de la actividad microbiana intestinal. Además, los AGCC sirven como ligandos endógenos para los receptores acoplados a proteínas G (GPCR) huérfanos, y los AGCC intracelulares regulan la expresión génica al prevenir las deacetilasas de histonas. Además, los AGCC interactúan con los aferentes vagales, lo que afecta la inflamación y la regulación hormonal. Las interacciones de los AGCC con sistemas celulares particulares y vías de señalización intestino-cerebro apoyan la idea de que los AGCC pueden desempeñar un papel significativo en la comunicación MGI.
A través de la comunicación química indirecta, la microbiota también afecta el sistema neurológico y el comportamiento, como lo demuestra la regulación microbiana del sistema neuroendocrino. La microbiota intestinal puede afectar el apetito y los patrones de alimentación de su huésped cambiando las señales endocrinas producidas por las células enteroendocrinas (EEC) en el epitelio intestinal, lo que implica la producción de la hormona péptido similar al glucagón 1 (GLP1). La microbiota en el intestino puede producir neurotransmisores por sí sola y también puede estimular la creación de estas sustancias en sus huéspedes animales. Por ejemplo, se sabe que varios microbios, incluidas las especies de Escherichia, Bacteroides, Bifidobacterium y sus especies, generan el neurotransmisor GABA. Se ha demostrado que las bacterias son esenciales para la producción del neurotransmisor serotonina 5-hidroxitriptamina (5-HT) en sistemas modelo de ratones animales. Los metabolitos microbianos como el indol, los AGCC, los ácidos biliares secundarios, el α-tocoferol, el p-aminobenzoato y la tiramina tienen un impacto en la generación y secreción de 5-HT por las células enteroendocrinas (EEC). Los microbios intestinales sintetizan AGCC, 5-HT, dopamina, ácido butírico, aminoácidos gamma y aminoácidos gamma, y estas sustancias son accesibles entre las células microbianas. El intestino, particularmente las células intestinales, puede sintetizar grandes cantidades de 5-HT, lo que afecta el cerebro. Además, las enzimas microbianas pueden fabricar neurotoxinas como el ácido D-láctico y el amoníaco. Estos metabolitos neuroactivos, como los neurotransmisores GABA, dopamina, noradrenalina y serotonina, aminoácidos (por ejemplo, triptófano y tiramina), lipopolisacárido (LPS), ácidos grasos de cadena corta (AGCC), trimetilamina-N-óxido (TMAO) y polisacárido A (PSA), inducen directa o indirectamente la migración de células inmunes periféricas al cerebro y se cree que causan neuroinflamación e influyen en las funciones del SNC.
Los patrones moleculares asociados a microbios (MAMPs), que se liberan, también conectan el SNC con la microbiota. Los MAMPs son moléculas producidas por microbios intestinales, como ARN de doble cadena, lipopolisacáridos y lipoproteínas, que son identificadas por una variedad de receptores, especialmente los receptores tipo Toll. Sin embargo, las concentraciones de 5-HT y su precursor metabólico triptófano en el hipocampo disminuyeron en ratones libres de gérmenes, lo que indica un posible papel de la microbiota intestinal en la regulación de las vías de señalización de 5-HT en el SNC. De hecho, es difícil evaluar cuánto afecta directamente el metabolismo microbiano a la actividad del SNC, en parte porque no entendemos completamente la tasa promedio de transporte de numerosos metabolitos microbianos al cerebro.
Vía Endocrina
Los AGCC pueden alterar la función del eje intestino-cerebro regulando la producción de hormonas intestinales. La activación de los receptores acoplados a proteínas G (GPCR) por los AGCC en el colon es el mecanismo subyacente a la producción de estas hormonas intestinales, lo que mejora la liberación del péptido YY (PYY) y el péptido similar al glucagón 1 (GLP1) de las células L enteroendocrinas. Estas hormonas a su vez tienen el poder de afectar el estado de ánimo, la memoria y el aprendizaje. Mediante el uso de receptores de ácidos grasos libres (FFARs), los AGCC pueden señalizar al cerebro activando directamente los aferentes vagales. El GLP1 tiene muchos receptores en todo el cuerpo y puede afectar las funciones cerebrales a través de rutas tanto humorales como neuronales, incluido el SNC y el SNP, así como el corazón, los pulmones, los intestinos y el páncreas. El GLP1 está involucrado en la mejora de la memoria y el aprendizaje en ratones, la mejora de la neuroplasticidad y la neuroprotección en el hipocampo, en modelos animales de Enfermedad de Alzheimer, y en la reducción de las placas β-amiloides y la activación microglial. Otro neuropéptido anoréxico, el PYY, reduce el apetito y previene la motilidad gástrica. Además de ser secretado por las células L del tracto gastrointestinal distal (colon e íleon), el hipotálamo y la glándula pituitaria tienen los niveles más altos de expresión de PYY en el cerebro humano, que se expresa en todo el cerebro. La forma más común de PYY circulante es PYY3–36, una forma truncada de la proteína que interactúa preferentemente con el receptor Y2 del neuropéptido Y. Según investigaciones realizadas en animales, el PYY afecta tanto el apetito como la actividad cerebral mediante mecanismos que cruzan la barrera hematoencefálica (BHE) o activando vías aferentes vagales que se conectan con la lámina propia y el plexo mientérico de la pared intestinal y transmiten al tronco encefálico. Otras hormonas metabólicas que afectan la función cerebral y que están influenciadas por los AGCC incluyen la grelina, la leptina y la insulina; sin embargo, la investigación sobre estas hormonas ha sido menos focalizada que la de PYY y GLP1. La leptina es una hormona que induce la pérdida de peso que es producida principalmente por las células adiposas, y es bien conocida por regular el equilibrio energético del cuerpo activando sus receptores hipotalámicos para expresar neuropéptidos orexigénicos y anoréxicos como el neuropéptido Y y la hormona α-melanocito estimulante, lo que reduce el apetito.
Vía Inmune
El sistema inmunológico es influenciado y afectado directamente tanto por el SNC como por el microbioma intestinal. La microbiota intestinal tiene un impacto significativo en el desarrollo y la función del sistema inmunológico periférico. La microbiota es necesaria para el desarrollo y la activación de las células inmunes innatas en el cerebro. La fisiopatología de los trastornos psiquiátricos puede involucrar respuestas inmunes e inflamación. Las interacciones citoquina-SNC afectan las funciones cerebrales y tienen un efecto en los neurocircuitos que regulan la motivación, la actividad motora y el estado de ánimo. Además, a través del sistema inmunológico sistémico y las citoquinas circulantes, la microbiota intestinal y el cerebro se comunican. Las células inmunes penetran directamente la BHE y llegan al SNC, o pueden producir citoquinas y quimiocinas en el cerebro. Las citoquinas son sustancias producidas en el intestino que pueden viajar a través del torrente sanguíneo y, bajo ciertas condiciones, tener un efecto en el hipotálamo y otras áreas del cerebro.
La BHE es una barrera física que separa el microambiente cerebral del resto del cuerpo. Está compuesta por proteínas de unión estrecha que conectan las células endoteliales murales y microvasculares. La BHE regula el movimiento de moléculas entre el torrente sanguíneo y el líquido cefalorraquídeo del SNC. La permeabilidad de la BHE está influenciada por la microbiota intestinal, ya que algunos informes muestran que los ratones libres de gérmenes tienen una mayor permeabilidad de la BHE en relación con los ratones control, debido en parte a la reducción de la expresión de proteínas de unión estrecha como la ocludina y la claudina 5. La BHE es importante porque protege el cerebro contra patógenos y respuestas inmunes desfavorables que podrían dañar las neuronas y las conexiones entre ellas. Muchos trastornos psiquiátricos, como la depresión mayor, la esquizofrenia, el trastorno del espectro autista y el trastorno obsesivo-compulsivo, se han relacionado con la desregulación microglial. Los AGCC tienen un impacto directo en las células inmunes y los moduladores inmunológicos para mantener la homeostasis. La influencia de los AGCC en la inmunidad de la mucosa intestinal está bien descrita. Sin embargo, los AGCC también pueden tener un impacto en el sistema inmunológico periférico, modulando la actividad cerebral. Al aumentar la barrera intestinal e inhibir la transferencia de bacterias y metabolitos bacterianos o por contacto directo entre los AGCC y las células inmunes, lo que podría disminuir la neuroinflamación en el cerebro, la inflamación sistémica puede reducirse. Los AGCC regulan la maduración y activación de linfocitos T, macrófagos, células dendríticas (CD) y neutrófilos. Los neutrófilos, el tipo de granulocito más prevalente, son una parte esencial del sistema inmunológico innato y se producen en la médula ósea. Son los primeros en aparecer en el sitio de la inflamación y explotan la producción de citoquinas para atraer a otras células, como los macrófagos. Los AGCC tienen un efecto inmediato en los neutrófilos regulando la producción de citoquinas proinflamatorias como el factor de necrosis tumoral (TNF), posiblemente a través de la inhibición de la deacetilasa de histonas (HDAC).
Vías Neuronales para las Interacciones Intestino-Cerebro
El intestino y el cerebro están físicamente conectados a través de conexiones neurológicas. La más significativa de estas redes neuronales es el nervio vago, que emerge del tronco encefálico e inerva el tracto gastrointestinal y el SNE. El vínculo más directo y mejor estudiado entre el intestino y el SNC, el nervio vago, es otra vía a través de la cual los microbios intestinales se comunican con el cerebro. Casi todo el sistema digestivo está inervado por el nervio vago, que tiene un 80% de fibras aferentes y un 20% de fibras eferentes. Las terminales nerviosas aferentes vagales inervan múltiples capas de la pared digestiva, mientras que las aferentes mucosas terminan dentro de la lámina propia de la mucosa intestinal. Los receptores vagales detectan sustancias químicas inflamatorias, elementos dietéticos, metabolitos bacterianos y péptidos reguladores intestinales para transferir señales al sistema nervioso central.
Sin embargo, hay alguna evidencia de que las bacterias en el intestino pueden activar directamente las neuronas. Los receptores tipo Toll 3 y 7, que detectan ARN viral, así como los receptores tipo Toll 2 y 4, que detectan peptidoglicano y lipopolisacárido, están presentes en los sistemas nerviosos entéricos tanto de ratones como de humanos. Se ha demostrado que Bacteroides fragilis, Lactobacillus rhamnosus (JB-1) y el polisacárido A aislado de B. fragilis estimulan las neuronas aferentes intestinales ex vivo. El tratamiento crónico con Bifidobacterium longum NCC3001 redujo los síntomas de ansiedad inducidos por la inflamación intestinal persistente. Los efectos observados en estos ensayos se eliminaron cuando la integridad del nervio vago se vio comprometida a través de la vagotomía. Además, los metabolitos microbianos tienen la capacidad de activar directamente las neuronas. Los receptores FXR y TGR5 se expresan en las neuronas cerebrales, aunque los individuos sanos tienen concentraciones bajas o indetectables de ácidos biliares en estos órganos. Varios estudios han identificado el ganglio cervical superior como la ubicación de los receptores GPR41 y FFAR3, los ganglios prevertebrales, las neuronas ganglionares submucosas y mientéricas, los ganglios simpáticos de los troncos simpáticos torácico y lumbar, y el ganglio vagal, lo que sugiere la activación neuronal por los AGCC derivados de microbios. La inervación neuronal del epitelio colónico se reduce en ratones libres de gérmenes y se restaura mediante la colonización microbiana. Las bacterias intestinales también ayudan en el desarrollo de células gliales entéricas en ratones, que son esenciales para mantener las redes neuronales y controlar la homeostasis intestinal. La actividad de las neuronas entéricas puede ser influenciada por la microbiota intestinal a través de la comunicación química, según un estudio reciente que muestra que la activación de los receptores de aril hidrocarburo en ratones adultos puede afectar la motilidad intestinal afectando el SNE.
Disbiosis Intestinal y Trastornos Neurológicos
Los trastornos neurológicos y neuropsiquiátricos están asociados con cambios en la composición de la microbiota intestinal. Los trastornos neurológicos son afecciones del sistema nervioso central y periférico que pueden dañar el cerebro, la médula espinal, los nervios craneales y periféricos, el sistema nervioso autónomo, las raíces nerviosas y la placa neuromuscular. Numerosas afecciones pueden provocar hemorragias cerebrales, incluidas enfermedades de los vasos sanguíneos, trastornos causados por problemas en el desarrollo del sistema nervioso, lesiones en la médula espinal o el cerebro, y tumores cerebrales. Una amplia variedad de enfermedades neurológicas están relacionadas con la disbiosis del microbioma intestinal humano. En contraste, los pacientes con enfermedades neurológicas y los controles sanos tienen composiciones de microbiota dramáticamente diferentes.
Es importante destacar que la comunicación a lo largo del eje microbiota intestinal-cerebro ocurre a lo largo de la vida, como se observa en enfermedades del neurodesarrollo (por ejemplo, TEA), neurodegeneración (por ejemplo, EP y EA) y comportamiento (por ejemplo, depresión y ansiedad). Según algunos estudios recientes en animales y humanos, la mayoría de los cuales fueron estudios de asociación, las modificaciones en la diversidad microbiana están relacionadas con resultados de salud negativos y pueden causar alteraciones en el SNC; estas alteraciones están asociadas con TEA, depresión y ansiedad. Otros estudios han reportado vínculos adicionales entre la composición de la microbiota y la depresión, la ansiedad y el TEA. Por lo tanto, la composición de la microbiota, que evoluciona con el tiempo, puede tener implicaciones en la función cerebral. A continuación, revisamos los avances recientes en el campo de la neuromicrobiología, particularmente los vínculos entre la microbiota intestinal y las enfermedades neurológicas. Al explorar el papel que desempeñan los microbios intestinales en los trastornos neurológicos, nos centramos específicamente en el TEA, la EA, la EP, la depresión y los trastornos de ansiedad.
Enfermedad de Alzheimer y la Microbiota
La Enfermedad de Alzheimer (EA) afecta a aproximadamente 50 millones de personas en todo el mundo y es la causa más frecuente de enfermedad neurológica progresiva crónica e irreversible y el tipo más común de demencia en individuos mayores. A medida que la condición progresa, los síntomas que afectan el pensamiento y la memoria pueden comprometer seriamente incluso las actividades diarias más básicas. La pérdida de neuronas y la disfunción sináptica progresivamente empeorante son síntomas de la EA. La EA es causada por la formación de agregados de formas polimerizadas de proteína precursora de β-amiloide (Aβ) en depósitos de amiloide solubles multimerizados y/o insolubles en el cerebro que desencadenan una cascada de eventos patológicos que conducen a ovillos neurofibrilares, agregados de proteínas tau hiperfosforiladas, formación de lesiones neurofibrilares y, en última instancia, demencia. El inflamasoma y sus productos se han relacionado con la patogénesis de la EA, ya que se ha observado una mayor expresión de IL-1β e IL-18 en la microglia, los astrocitos y las neuronas que rodean las placas de Aβ o en el plasma de pacientes con EA.

Las células mononucleares de sangre periférica de pacientes con EA también mostraron una mayor expresión de NLRP3, ASC, caspasa-1, caspasa-5, IL-1β e IL-18. Los pacientes con tauopatías, que son enfermedades neurodegenerativas caracterizadas por la acumulación de proteína tau aberrante en el cerebro, típicamente exhiben niveles aumentados de caspasa-1 escindida y ASC, así como IL-1β madura en la corteza. Evidencia importante vincula la neuroinflamación causada por el inflamasoma NLRP3 con el desarrollo y la progresión de la EA. La patogénesis de la EA se ha asociado con una serie de causas microbiológicas. En comparación con los controles, las muestras de heces de pacientes con EA mostraron niveles más altos de Bacteroidetes y niveles más bajos de Firmicutes y Actinobacteria. Ruminococcaceae, Turicibacteraceae y Clostridiaceae fueron todas familias de Firmicutes donde los pacientes con EA tuvieron menores abundancias. Según varios estudios, puede haber vínculos mecanísticos entre la fisiopatología de la EA y otros microbios, como espiroquetas, hongos y Chlamydia pneumoniae.
En estudios recientes, la microbiota intestinal también se ha relacionado con la etiología de la EA. Una proteína derivada de metabolitos de la microbiota encontrada en el líquido cefalorraquídeo de pacientes con EA y conectada con dos biomarcadores relacionados con la enfermedad (tau fosforilada y tau fosforilada/Aβ42) plantea la posibilidad de que el microbioma intestinal desempeñe un papel en la etiología de la EA. Al comparar los microbiomas fecales y los AGCC fecales entre ratones afectados por EA y ratones de tipo salvaje a diversas edades, se observaron aumentos dramáticos en Proteobacteria y Verrucomicrobia y disminuciones marcadas en Butyricicoccus y Ruminococcus en ratones con EA, lo que indica una composición y diversidad de microbiota alteradas. El nivel disminuido de AGCC indica además alteraciones en muchas vías metabólicas. Se demostró que, en comparación con ratones de tipo salvaje no transgénicos, la diversidad de la microbiota intestinal de los ratones transgénicos dobles APP/PS1 de uso común, que producen una proteína precursora de amiloide (APP) quimérica de ratón/humano y una presenilina 1 (PS1) humana mutante, estaba marcadamente cambiada. Además, en comparación con ratones control sanos con microbiota intestinal, los animales transgénicos APP/PS1 libres de gérmenes muestran una reducción sorprendente en el grado de patología cerebral de β-amiloide. Otros estudios reportaron hallazgos similares sobre el cambio en la composición de la microbiota en el modelo de ratón transgénico APP/PS1, que muestra un aumento en el número de la familia inflamatoria Erysipelotrichaceae, estrechamente relacionada. Además, los ratones APP/PS1 libres de gérmenes mostraron una disminución de la patología amiloide en comparación con los ratones convencionales.
Enfermedad de Parkinson y el Intestino
La Enfermedad de Parkinson (EP), que afecta a más del 1% de la población anciana y al 0,3% de la población general en todo el mundo, es la segunda enfermedad neurodegenerativa más prevalente después de la EA. La EP es un trastorno neurodegenerativo progresivo caracterizado por la incapacidad de controlar los movimientos voluntarios como resultado de alteraciones severas en la función de la sustancia negra y el estriado. La degradación de las neuronas dopaminérgicas, la acumulación de versiones fosforiladas de la proteína neuronal α-sinucleína (αSyn), el mal funcionamiento mitocondrial, un exceso de especies reactivas de oxígeno y un aumento en la activación microglial son algunas de estas alteraciones. La inflamación y el plegamiento incorrecto de la α-sinucleína son mecanismos patológicos clave subyacentes a las α-sinucleinopatías como la EP. La patogénesis de la EP depende en gran medida de la acumulación de α-sinucleína. Los síntomas de la EP incluyen temblores, dificultad para caminar, postura encorvada y rigidez muscular. Los problemas gastrointestinales, más frecuentemente el estreñimiento, pueden afectar hasta al 80% de los pacientes con Enfermedad de Parkinson y pueden preceder a los diagnósticos de EP por muchos años.
La creciente evidencia sugiere que la disbiosis intestinal contribuye al inicio, desarrollo y progresión de la EP. Al comparar pacientes con EP prodrómica y/o clínicamente diagnosticada con sujetos de control, encontramos que estos pacientes tenían disbiosis de la microbiota intestinal. La organización general y la composición de la microbiota intestinal asociada con la EP se han examinado utilizando técnicas de secuenciación de alto rendimiento independientes del cultivo, y se han encontrado características de los perfiles de microbiota alterados en pacientes con EP. Numerosos estudios anteriores encontraron que los pacientes con EP tenían una α-diversidad mayor, pero menor diversidad bacteriana que las personas sanas. Además, un estudio reveló que había diferencias en la β-diversidad (entre muestras) entre pacientes con EP y controles. Se ha establecido una conexión entre las características clínicas de la EP y la disminución de la diversidad bacteriana, que se evalúa principalmente utilizando índices de α-diversidad como Shannon y Simpson.
Según un estudio reciente, ciertos síntomas de la EP pueden estar particularmente relacionados con el microbioma prodrómico, incluido el estreñimiento, el posible trastorno del comportamiento del sueño REM (RBD), la inactividad física, el tabaquismo, los niveles de urato y el parkinsonismo subumbral. Contrariamente al sexo, la inactividad, el RBD sospechado, el estreñimiento y el tabaquismo, que estaban todos relacionados con la β-diversidad, estaban el estreñimiento, la exposición ocupacional a solventes y las tres variables mencionadas anteriormente. La edad y los medicamentos que reducen el urato estaban relacionados tanto con la α como con la β-diversidad. Sin embargo, una investigación reveló que la α-diversidad del microbioma intestinal no es un biomarcador de la EP. La permeabilidad intestinal y la inflamación causadas por la disbiosis intestinal asociada con la EP, como el aumento de Akkermansia y la disminución de bacterias productoras de AGCC, pueden facilitar la exposición del plexo neural intestinal a toxinas como el lipopolisacárido (LPS) y los pesticidas, lo que puede causar agregación anormal de fibrillas de α-sinucleína y el desarrollo de cuerpos de Lewy. A pesar de las personas con otras enfermedades, las personas con EP tienen una composición de microbioma diferente a la de las personas sanas o con otros trastornos neurológicos.
La flora intestinal en pacientes con EP carece de bacterias que producen AGCC (principalmente butirato), como taxones de la familia Lachnospiraceae y Faecalibacterium prausnitzii, que tienen propiedades antiinflamatorias conocidas. Además, ciertas especies bacterianas, como Proteus mirabilis, que causa deficiencias motoras en ratones, pueden ser la causa de la enfermedad similar a la EP. Se requieren investigaciones longitudinales prospectivas a largo plazo sobre el microbioma para rastrear el desarrollo de la enfermedad y caracterizar los cambios en la composición taxonómica del microbioma que contribuyeron o pueden haber definido el estado de la enfermedad. Persiste la incertidumbre sobre la forma precisa en que el microbioma intestinal puede afectar los síntomas relacionados con la EP.
Esclerosis Múltiple y el Microbioma Intestinal
La Esclerosis Múltiple (EM) es una condición neurológica e inflamatoria que afecta a más de dos millones de individuos en todo el mundo. Los principales síntomas de esta condición incluyen desmielinización, pérdida axonal, infiltración de linfocitos en el SNC y neuroinflamación. Algunos de los signos clínicos de la EM incluyen ataxia, mala coordinación, hiperreflexia, rigidez, deterioro visual y sensorial, fatiga y déficits cognitivos. La mayoría de los pacientes sufren un tipo de enfermedad conocido como remitente-recurrente, que se caracteriza por un deterioro gradual pero significativo de la función neurológica y una reaparición progresiva de los síntomas. La mayoría de los pacientes tienen lesiones cerebrales o lesiones en el cerebro y la médula espinal; sin embargo, algunas personas solo tienen lesiones en la médula espinal. Los microbios (y las sustancias que secretan o las toxinas que producen) son un contribuyente significativo a la fisiopatología de la EM entre las variables ambientales. Los pacientes con EM tienen una composición de microbioma diferente a la de los individuos sanos.
Es interesante notar que incluso los pacientes con EM activa tienen un microbioma diferente al de aquellos que están en remisión, cuya microbiota es más comparable a la de los controles sanos. Una mayor abundancia de Firmicutes y la ausencia de Fusobacteria en pacientes pediátricos con EM se asociaron con un tiempo más corto hasta la recaída. En comparación con las personas sanas, las muestras fecales de personas con EM muestran alteraciones en la riqueza de las especies Mycoplana, Dorea, Pseudomonas, Blautia y Akkermansia. La enfermedad similar a la esclerosis múltiple atenuada aparece en modelos preclínicos en ratones libres de gérmenes, y los ratones que recibieron la microbiota intestinal de pacientes con EM experimentaron una encefalomielitis autoinmune experimental más severa y tuvieron menores proporciones de células T reguladoras antiinflamatorias que los ratones que recibieron el microbioma de individuos sanos. El hallazgo notable fue que trasplantar los microbios intestinales de gemelos con EM a animales libres de gérmenes, que están genéticamente predispuestos a desarrollar encefalomielitis autoinmune experimental (EAE), fue suficiente para promover la enfermedad in vivo con una incidencia significativamente mayor que trasplantar los microbios de gemelos sanos. Curiosamente, las células inmunes de ratones que recibieron muestras derivadas de EM produjeron menos IL-10 que las células de animales que tuvieron su microbiota de gemelos sanos. La neutralización de IL-10, una de las principales citoquinas reguladoras, aumentó la incidencia de la enfermedad en ratones inoculados con muestras fecales sanas. Este importante hallazgo demostró cómo el microbioma humano puede producir cambios particulares en el sistema inmunológico que pueden ser la causa o la consecuencia del inicio de la EM. Persiste la incertidumbre sobre si este papel desempeña una parte crucial en el inicio y desarrollo de la enfermedad. A la luz de esto, hay un considerable interés en las variaciones en la microbiota de pacientes con EM en comparación con controles sanos.
Trastorno del Espectro Autista y Bacterias Intestinales
Los Trastornos del Espectro Autista (TEA) son un conjunto de cambios en el desarrollo neurológico marcados por dificultades en la interacción social y la comunicación, así como por conductas estereotipadas y repetitivas. El estreñimiento, la diarrea, el dolor abdominal, la flatulencia y los gases intestinales son comunes entre las personas con problemas de TEA (23-70%) y con frecuencia son comórbidos con enfermedades gastrointestinales. La microbiota intestinal media los niveles de transmisores químicos como GABA, glutamato, oxitocina y serotonina 5-HT compleja en el TEA. Debido a la inflamación de bajo grado que experimentan los pacientes con TEA, las influencias microbianas en el sistema inmunológico también pueden ser muy importantes para determinar las respuestas neuroinmunes en el TEA. Se están aplicando nuevas tecnologías en este campo de investigación en rápida expansión a medida que se hace evidente cuánto afectan los metabolitos microbianos, incluidos la taurina, los metabolitos de ácidos biliares, los AGCC y el ácido 5-aminovalérico, a los síntomas del TEA.
Hay pocos estudios sobre TEA y generalmente inconsistentes que destaquen el papel del microbioma en la patogénesis. Sin embargo, hay algunos que resaltan las diferencias en bacterias como Firmicutes, Clostridiales, Prevotella, Bifidobacterium y Clostridium perfringens, especies que se observan entre pacientes con TEA y controles. Esto resulta en un cambio en la composición de la microbiota intestinal, una reducción en la calidad de la dieta y una deficiencia en nutrientes. Los datos de la literatura científica generalmente muestran una reducción de Bacteroides con una proporción (% niños con TEA/% niños control) igual a 0,71; una reducción de Bifidobacterium con una proporción (% niños con TEA/% niños control) igual a 0,52; una reducción de Escherichia coli con una proporción (%) igual a 0,3; un aumento en Faecalibacterium con una proporción (%) igual a 1,32; y un aumento en Lactobacillus. Clostridium todavía está presente en una cantidad en gran medida sin cambios. Es evidente que estos trastornos neurológicos van acompañados de cantidades reducidas de bacterias beneficiosas y niveles mayores de bacterias mortales, aunque no se puede decir que ciertas bacterias sean compatibles y estén relacionadas con el inicio del TEA. La microbiota intestinal y sus metabolitos pueden ser crucialmente significativos en la fisiopatología del TEA.
Ansiedad y Depresión: ¿Un Vínculo Microbiano?
La ansiedad y la depresión son trastornos mentales y neurológicos que afectan al 25% de la población mundial. Estas dos condiciones patológicas parecen estar íntimamente relacionadas: de hecho, el 85% de las personas con depresión y el 90% de las personas con trastornos de ansiedad experimentan ansiedad considerable. Las etapas tempranas y tardías de estas patologías tienen signos clínicos significativamente diferentes. Las muertes por suicidio en adolescentes han aumentado en las últimas décadas como resultado del aumento de los síntomas depresivos. La relación entre la ansiedad y la depresión y los cambios en la estabilidad y composición de la microbiota intestinal ha sido investigada a fondo. Numerosos estudios se han centrado recientemente en la relación entre la microbiota intestinal y las personas que sufren de trastornos de ansiedad y del estado de ánimo. En particular, la evidencia de la investigación en humanos ha demostrado que, al tener en cuenta la diversidad microbiana y las composiciones taxonómicas, con frecuencia hay alguna variación en la microbiota fecal entre pacientes y controles sanos. Además, se reveló que ciertas bacterias estaban relacionadas con rasgos clínicos y perfiles metabólicos o inflamatorios.
Ha habido algunos estudios sobre la diversidad microbiana humana, pero la mayoría de ellos no han podido demostrar una conexión entre la baja diversidad microbiana y los trastornos depresivos. A pesar de que solo un estudio encontró que los individuos con trastorno depresivo mayor (TDM) tenían una mayor diversidad alfa de la microbiota intestinal que los sujetos sanos, la diversidad alfa es el número de especies que se pueden detectar en un ecosistema microbiano. Al comparar pacientes con TDM con respondedores a medicamentos con controles sanos, los pacientes con TDM mostraron una mayor diversidad alfa fecal (niveles más altos de Enterobacteriaceae y Alistipes pero niveles más bajos de Faecalibacterium). Debido a esto, los autores reportaron un vínculo negativo entre Faecalibacterium y la intensidad de los síntomas de depresión. También se han encontrado cambios interesantes en la microbiota fecal en pacientes con trastornos de ansiedad. Observaron que los pacientes con trastorno de ansiedad generalizada (TAG) tenían niveles más bajos de diversidad y riqueza microbiana, lo que se correlacionaba con niveles más bajos de productores de ácidos grasos de cadena corta como Eubacterium rectale y Fecalibacterium y niveles más altos de Ruminococcus, Escherichia, Shigella y Fusobacterium. Según otro estudio, los probióticos (Bifidobacterium bifidum, Lactobacillus acidophilus y Lactobacillus casei) administrados a pacientes con TDM redujeron drásticamente los síntomas de depresión en comparación con un placebo. El potencial de las bacterias para producir ácido 3,4-dihidroxifenilacético, un metabolito de la dopamina, se correlaciona favorablemente con la salud mental según los datos metagenómicos fecales, lo que plantea la posibilidad de que los microbios desempeñen un papel en la producción de diferentes moléculas neuroactivas durante la depresión que en condiciones normales. Lactobacillus rhamnosus libera GABA y activa los receptores GABA en el cerebro (es decir, receptores GABA Aα2 y GABA B1b) y se ha demostrado que atenúa los comportamientos similares a la depresión y la ansiedad en ratones.
Accidente Cerebrovascular y la Microbiota Intestinal
El accidente cerebrovascular es la segunda causa principal de muerte en todo el mundo. La morbilidad y mortalidad del accidente cerebrovascular aumentan en muchos países, contribuyendo a la carga financiera y la pérdida de calidad de vida, disminuyendo así el índice de felicidad nacional. Aproximadamente 15 millones de personas en todo el mundo son víctimas de un accidente cerebrovascular cada año. Pueden ocurrir debido a modificaciones en diversas enfermedades, como enfermedad cerebrovascular, aterosclerosis, dislipidemia, diabetes e hipertensión arterial. Sin embargo, hasta la fecha, pocos estudios se han centrado en explorar la correlación entre el accidente cerebrovascular hemorrágico y la microbiota intestinal. La microflora de la microbiota intestinal puede estar involucrada en el desarrollo del accidente cerebrovascular y/o las lesiones cerebrales. Estudios han informado que el accidente cerebrovascular isquémico representa aproximadamente el 80% de todos los accidentes cerebrovasculares, y la microbiota intestinal juega un papel esencial en la patogénesis y el pronóstico del accidente cerebrovascular isquémico. Múltiples estudios han demostrado que el accidente cerebrovascular isquémico cambia significativamente la composición de la microbiota intestinal. Se ha encontrado que los pacientes que sufren de accidente isquémico transitorio o accidente cerebrovascular tienen patógenos oportunistas como Desulfovibrio, Enterobacter, Megasphaera y Osicillibacter, así como menos patógenos beneficiosos o comensales como Bacteroides, Fecalibacterium y Prevotella. La abundancia de Peptococcaceae y Prevotellaceae está relacionada con la gravedad del accidente cerebrovascular.
Recientemente, un estudio preclínico también sugirió que las alteraciones en la microbiota intestinal estaban asociadas con la transformación hemorrágica (TH). La abundancia relativa de Proteobacteria y Actinobacteria aumentó significativamente en ratas con TH después de un accidente cerebrovascular experimental, lo que indica que la microbiota intestinal está involucrada en la progresión del accidente cerebrovascular isquémico. El papel y mecanismo precisos de la microbiota intestinal en el inicio y la progresión del accidente cerebrovascular y la lesión cerebral siguen siendo desconocidos. Aunque los modelos animales han arrojado resultados fascinantes, se necesita más investigación clínica para dilucidar completamente el potencial de tales modalidades terapéuticas microbianas.
Tabla Comparativa: Microbiota Intestinal y Trastornos Neurológicos Seleccionados
| Trastorno Neurológico | Alteraciones Típicas de la Microbiota | Posibles Mecanismos de Vínculo |
|---|---|---|
| Enfermedad de Alzheimer | Aumento de Bacteroidetes; Disminución de Firmicutes, Actinobacteria, Butyricicoccus, Ruminococcus | Neuroinflamación, metabolitos (TMAO, AGCC), agregación de Aβ y Tau, permeabilidad intestinal |
| Enfermedad de Parkinson | Aumento de Akkermansia; Disminución de bacterias productoras de AGCC (Lachnospiraceae, F. prausnitzii), Proteus mirabilis | Agregación de α-sinucleína, neuroinflamación, AGCC, permeabilidad intestinal, problemas GI (estreñimiento) |
| Esclerosis Múltiple | Variaciones en Firmicutes, Fusobacteria, Mycoplana, Dorea, Pseudomonas, Blautia, Akkermansia | Inflamación, células T reguladoras, permeabilidad intestinal |
| Trastorno del Espectro Autista | Variaciones en Firmicutes, Clostridiales, Prevotella, Bifidobacterium, Clostridium perfringens, Bacteroides, E. coli, Faecalibacterium, Lactobacillus | Inflamación, metabolitos (AGCC, ácidos biliares), neurotransmisores (GABA, serotonina), problemas GI |
| Ansiedad y Depresión | Variaciones en Enterobacteriaceae, Alistipes, Faecalibacterium, Ruminococcus, Escherichia, Shigella, Fusobacterium, Lactobacillus, Bifidobacterium | Neurotransmisores (Serotonina, GABA, Dopamina), AGCC, inflamación, eje HPA |
| Accidente Cerebrovascular | Aumento de Desulfovibrio, Enterobacter, Megasphaera, Osicillibacter, Proteobacteria, Actinobacteria; Disminución de Bacteroides, Fecalibacterium, Prevotella, Peptococcaceae, Prevotellaceae | Inflamación, metabolitos, permeabilidad intestinal, aterosclerosis |
Preguntas Frecuentes sobre la Microbiota Intestinal y el Cerebro
¿Qué es el eje intestino-cerebro?
Es una red de comunicación bidireccional compleja que conecta el sistema nervioso central (cerebro) con el sistema nervioso entérico (intestino). Involucra vías neuronales (como el nervio vago), endocrinas, inmunes y metabólicas, permitiendo que el intestino y su microbiota influyan en la función cerebral y viceversa.
¿Cómo afectan exactamente las bacterias intestinales a mi cerebro?
Las bacterias intestinales influyen en el cerebro de varias maneras. Producen metabolitos como ácidos grasos de cadena corta (AGCC) y neurotransmisores (serotonina, GABA, dopamina) que pueden señalizar al cerebro directamente o a través de otras vías. También modulan el sistema inmunológico, afectando la inflamación sistémica y cerebral, e influyen en la integridad de la barrera hematoencefálica.
¿Pueden los probióticos ayudar a tratar trastornos neurológicos?
La investigación preclínica y algunos estudios clínicos sugieren que la modulación de la microbiota intestinal, por ejemplo, mediante suplementos probióticos, podría tener potencial terapéutico para algunos trastornos neurológicos al influir en el eje intestino-cerebro. Sin embargo, se necesita mucha más investigación para comprender los mecanismos precisos y confirmar su eficacia clínica en humanos.
Conclusión y Direcciones Futuras
El microbioma intestinal es importante para la salud y los estados de enfermedad del huésped, y la mayor parte de la investigación sobre este tema hasta la fecha solo ha revelado asociaciones entre ciertos trastornos clínicos y perfiles bacterianos. La microbiota intestinal tiene un impacto sustancial tanto en la fisiología como en la fisiopatología del cerebro debido a la interacción bidireccional entre el intestino y el sistema neurológico. Esta comunicación tiene lugar a través de una variedad de vías e involucra el nervio vago, los sistemas neuroendocrinos, los neurotransmisores del SNC y las sustancias inflamatorias. La evidencia discutida se acumula a partir de estudios preclínicos y clínicos sobre la microbiota intestinal, su disbiosis y su asociación con el desarrollo y la progresión de trastornos neurológicos, desde anomalías del neurodesarrollo hasta la depresión y la enfermedad de Parkinson, aunque determinar su modo de acción exacto requiere más investigación.
Las terapias de suplementos probióticos son herramientas efectivas con considerable potencial terapéutico para los trastornos neurológicos, aunque determinar sus mecanismos de acción precisos requiere más investigación. Futuros estudios en este campo pueden proporcionar información sobre la conexión entre la microbiota y el SNC y los avances en el tratamiento de los trastornos neurológicos. Los campos de la microbiología y la neurociencia, así como otras disciplinas, deben seguir trabajando juntos para desarrollar métodos exhaustivos y pertinentes que permitan determinar los mecanismos de acción para resultados que actualmente son observacionales, junto con esfuerzos responsables para traducir estos descubrimientos en mejoras para la salud humana. Las principales poblaciones del mundo sufren trastornos neurológicos, que se espera que aumenten en un 13% para 2030. Por lo tanto, existe una urgencia por desarrollar biomarcadores más fiables y opciones terapéuticas viables en vista de la patogenicidad de las enfermedades.
Múltiples estudios han demostrado que la microbiota intestinal es fundamental para el desarrollo y la función cerebral. En varios estudios de investigación preclínica y clínica, el microbioma del tracto gastrointestinal en el EIC ha sido revisado por su asociación con múltiples trastornos neurológicos, como la EA, la EM, la EP, el TEA, la epilepsia, el accidente cerebrovascular y la lesión cerebral. Sin embargo, se necesita una investigación más profunda para comprender el mecanismo de acción y la función de la microbiota intestinal en la patogénesis de la enfermedad y su aplicabilidad futura con fines terapéuticos o pronósticos. No obstante, el impacto en la microbiota intestinal y la composición de sus especies beneficiosas en el EIC aún deben dilucidarse en futuros estudios. Dado que muchos pacientes reciben múltiples medicamentos, se necesita más investigación para aclarar cualquier posible interacción entre la microbiota intestinal y los medicamentos. La microbiota intestinal es una nueva línea que separa la salud humana de una variedad de trastornos, y la futura investigación neuroterapéutica proporcionará información crítica sobre este tema. A pesar de los desarrollos recientes en nuestra comprensión del EIC, se requiere más investigación para determinar si este conocimiento puede ser útil en un entorno clínico. Los estudios futuros deben aclarar los vínculos subyacentes entre la microbiota intestinal y diversas enfermedades neurológicas y determinar si tratar la microbiota es un curso de tratamiento seguro y efectivo. Podría ser posible desarrollar técnicas que apunten a la microbiota intestinal para ofrecer opciones de terapia innovadoras, seguras y eficientes para los trastornos neurodegenerativos si los trastornos cerebrales tradicionales se ven de manera integral y ahora como condiciones completas con un papel significativo para el tracto gastrointestinal.
Si quieres conocer otros artículos parecidos a El Eje Intestino-Cerebro y Trastornos Neurológicos puedes visitar la categoría Neurociencia.

