El cerebro humano es una red intrincada de estructuras que trabajan en armonía para controlar todo, desde el pensamiento abstracto hasta el simple acto de mover un dedo. Dentro de esta red, los ganglios basales desempeñan un papel crucial en la coordinación y el control del movimiento, la cognición y las emociones. Una parte esencial de los ganglios basales es el globus pallidus (GP), que se divide en dos segmentos: el globus pallidus externo (GPe) y el globus pallidus interno (GPi). Mientras que el GPe actúa como un núcleo intrínseco dentro de la red, el GPi es particularmente importante porque sirve como el principal núcleo de salida de los ganglios basales, modulando directamente la información que llega a otras áreas cerebrales clave, como el tálamo.
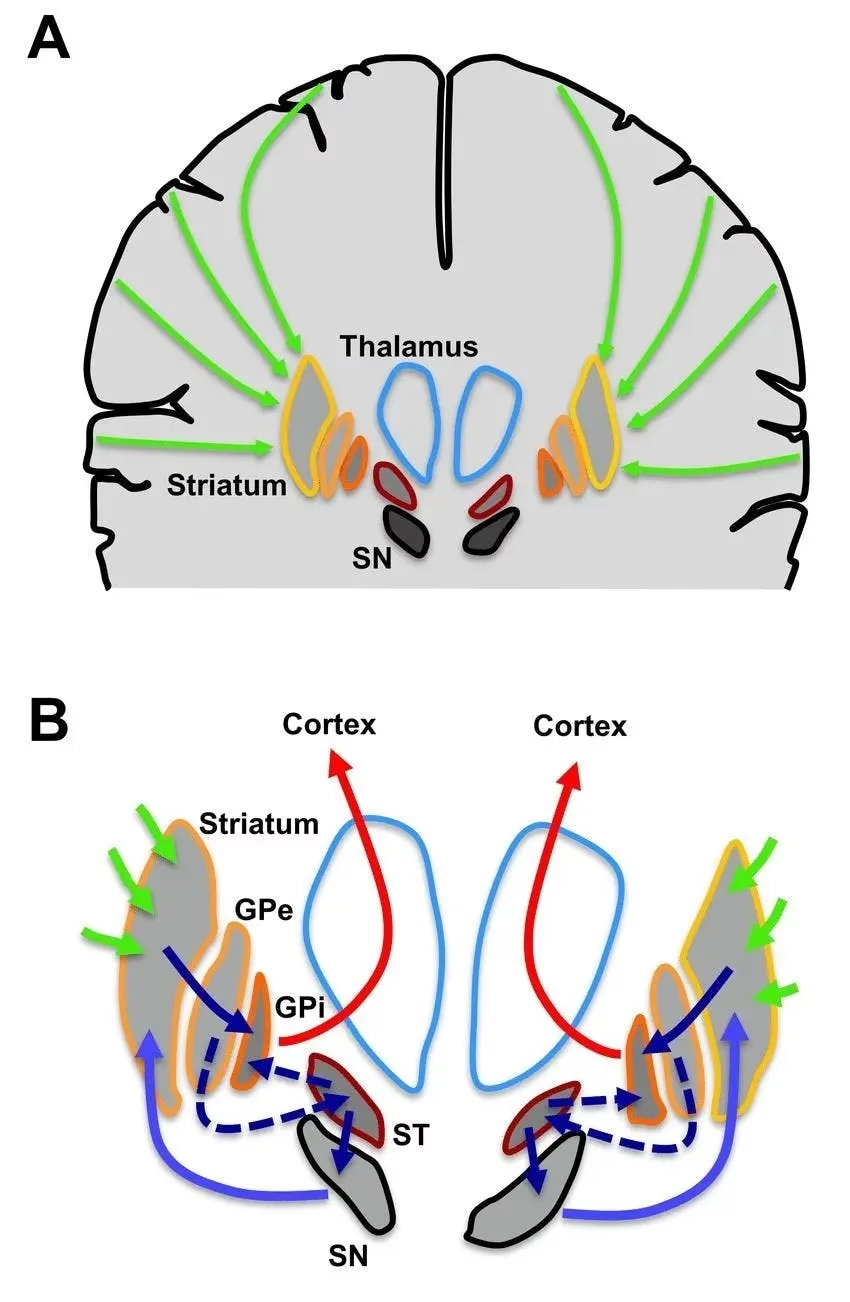
Comprender la función y las conexiones del GPi es fundamental para desentrañar los mecanismos que subyacen al movimiento normal y a los trastornos neurológicos que afectan a los ganglios basales. Este artículo explorará en detalle qué es el GPi, su estructura, sus intrincadas conexiones dentro de los circuitos de los ganglios basales y su relevancia clínica en diversas condiciones neurológicas.
- Estructura y Ubicación del Globus Pallidus Internus (GPi)
- El GPi como Núcleo de Salida Clave de los Ganglios Basales
- Circuitos Funcionales: Vías Directa e Indirecta
- Conexiones del GPi con el Tálamo
- Desarrollo Embrionario
- Suministro de Sangre y Drenaje Venoso
- Rol en Funciones Cognitivas Superiores
- Variantes Fisiológicas
- Consideraciones Quirúrgicas: El GPi como Diana Terapéutica
- Relevancia Clínica: El GPi en Diversos Trastornos
- Preguntas Frecuentes sobre el GPi
- Conclusión
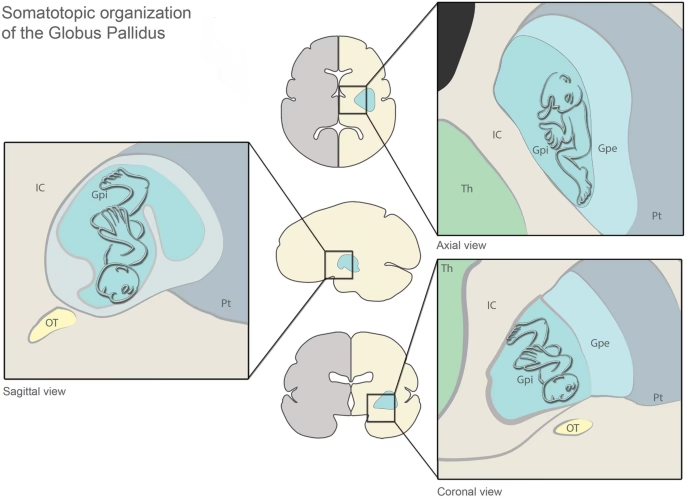
Estructura y Ubicación del Globus Pallidus Internus (GPi)
El globus pallidus (GP) es una estructura subcortical del cerebro, con una forma aproximadamente triangular, situada medial al putamen. Su nombre, que proviene del latín 'globo pálido', se debe a su apariencia más clara en comparación con las estructuras vecinas (putamen y estriado) en secciones cerebrales. Esta palidez es el resultado de una alta concentración de axones mielinizados que atraviesan la estructura, contrastando con la relativa falta de mielina en el estriado adyacente.
Una lámina medular medial de sustancia blanca divide el GP en dos segmentos distintos: el globus pallidus interno (GPi) y el globus pallidus externo (GPe). El GPi es la subdivisión medial, mientras que el GPe es la subdivisión lateral. El GPe es generalmente más grande que el GPi y se localiza caudomedialmente al cuerpo estriado. El globus pallidus, junto con el putamen, forma colectivamente el núcleo lentiforme (o lenticular), que se encuentra debajo de la ínsula. El núcleo caudado y el putamen, por su parte, constituyen el corpus striatum (cuerpo estriado), otra parte vital de los ganglios basales.
La relación anatómica entre estas estructuras es íntima y compleja. El núcleo caudado se sitúa directamente lateral y se anida dentro del contorno cóncavo del ventrículo lateral. El putamen se encuentra inferior y dentro de la concavidad de la cabeza y el cuerpo del núcleo caudado. El globus pallidus, a su vez, se localiza en el aspecto medial del putamen, bordeado más medialmente por la curva de la cápsula interna, una importante vía de sustancia blanca que transporta fibras nerviosas entre la corteza y las estructuras subcorticales. Esta ubicación estratégica permite al GPi interactuar extensamente con otras partes del cerebro.
El GPi como Núcleo de Salida Clave de los Ganglios Basales
La función principal del globus pallidus en general es controlar los movimientos conscientes y propioceptivos. Sin embargo, dentro del GP, el GPi tiene un rol particularmente destacado como el principal núcleo de salida de todo el sistema de los ganglios basales. Esto significa que la información procesada por los ganglios basales, a través de complejas interacciones entre sus diversos núcleos, converge en gran medida en el GPi antes de ser enviada a otras áreas cerebrales, principalmente el tálamo.
El GPi actúa como el punto final para las dos vías principales a través de las cuales los ganglios basales regulan el movimiento: la vía directa y la vía indirecta. Al ser el núcleo de salida, el GPi modula la actividad de estructuras receptoras, influyendo así en la planificación y ejecución de comportamientos orientados a objetivos. Esta modulación es posible gracias a sus extensas conexiones con otras partes del cerebro, recibiendo información de múltiples fuentes y proyectándola hacia el exterior del sistema de ganglios basales.
Circuitos Funcionales: Vías Directa e Indirecta
Los ganglios basales procesan la información a través de circuitos paralelos que involucran vías directas e indirectas. Estas vías, aunque simplificadas en los modelos clásicos, explican cómo los ganglios basales equilibran la promoción e inhibición del movimiento. El GPi es un actor central en ambas.
La Vía Directa: Promoviendo el Movimiento
La vía directa se considera que promueve el movimiento. Se inicia con la llegada de señales excitatorias (glutamatérgicas) desde la corteza cerebral al estriado. Las neuronas del estriado que participan en la vía directa expresan receptores D1 de dopamina y son excitadas por la dopamina liberada por la substantia nigra pars compacta (SNpc) a través de las proyecciones nigroestriatales. Cuando estas neuronas estriatales se activan, envían señales inhibitorias (GABAérgicas) directamente al GPi (y a la substantia nigra pars reticularis, SNpr).
El GPi, en su estado tónico normal, ejerce una fuerte inhibición sobre los núcleos talámicos (particularmente los núcleos ventral anterior y ventral lateral del tálamo). Al recibir señales inhibitorias de la vía directa, la actividad del GPi disminuye. Esta reducción de la actividad del GPi resulta en una menor inhibición sobre el tálamo. Es decir, el tálamo es "desinhibido". El tálamo desinhibido, a su vez, envía señales excitatorias (glutamatérgicas) a la corteza motora, lo que facilita la iniciación y ejecución del movimiento.
En resumen, la vía directa es un circuito que, al activarse, conduce a la desinhibición del tálamo por parte del GPi, lo que resulta en una mayor excitación de la corteza motora y, por lo tanto, facilita el movimiento deseado. Es interesante notar que se ha sugerido que el GPi secreta una sustancia opiácea llamada sustancia P, que podría tener un papel en la regulación de la vía nigroestriatal.
La Vía Indirecta: Limitando el Movimiento
La vía indirecta, por otro lado, tiende a limitar o refinar el movimiento, ayudando a prevenir movimientos excesivos o no deseados. Al igual que la vía directa, se inicia con señales corticales excitatorias al estriado.
Las neuronas estriatales involucradas en la vía indirecta expresan receptores D2 de dopamina y son inhibidas por la dopamina de la SNpc. Cuando estas neuronas estriatales se activan (menos por la dopamina), envían señales inhibitorias (GABAérgicas) al GPe (globus pallidus externo).
El GPe, que también ejerce una inhibición tónica sobre el núcleo subtalámico (NST), ve su actividad reducida por la inhibición del estriado. Una menor actividad del GPe significa una menor inhibición sobre el NST. En consecuencia, el NST se vuelve más activo. El NST es una estructura excitatoria (glutamatérgica) que proyecta hacia el GPi y la SNpr.
El NST activado envía señales excitatorias al GPi. Esto aumenta la actividad del GPi. Un GPi más activo aumenta su inhibición tónica sobre los núcleos talámicos (ventral anterior y ventral lateral). Esta mayor inhibición del tálamo reduce su capacidad para excitar la corteza motora, suprimiendo o limitando así el movimiento.
En resumen, la vía indirecta es un circuito más complejo que, al activarse, conduce a un aumento de la actividad del GPi, lo que resulta en una mayor inhibición del tálamo y, por lo tanto, limita el movimiento. Se ha descubierto que el GPe secreta una sustancia opiácea llamada encefalina, que también podría modular la vía nigroestriatal.
La interacción dinámica y el equilibrio entre estas dos vías, que convergen en el GPi como su salida final, son fundamentales para la coordinación precisa y el control fluido del movimiento. La disfunción en cualquiera de estas vías, o en el equilibrio entre ellas, puede llevar a trastornos del movimiento característicos.
Tabla Comparativa: Vía Directa vs. Vía Indirecta
| Característica | Vía Directa | Vía Indirecta |
|---|---|---|
| Efecto en el Movimiento | Promueve/Facilita | Limita/Suprime |
| Receptor de Dopamina Estriatal | D1 (Excitatorio por Dopamina) | D2 (Inhibitorio por Dopamina) |
| Proyección Estriatal Principal | GPi/SNpr (Inhibitoria) | GPe (Inhibitoria) |
| Involucra al GPe | No directamente (recibe modulación) | Sí (es inhibido por el estriado D2) |
| Involucra al Núcleo Subtalámico (NST) | No directamente | Sí (es desinhibido por el GPe) |
| Efecto en el GPi/SNpr | Inhibición (disminuye actividad) | Excitación (aumenta actividad) |
| Efecto en el Tálamo | Desinhibición (aumenta actividad) | Inhibición (disminuye actividad) |
| Efecto en la Corteza Motora | Excitación (facilita movimiento) | Inhibición (limita movimiento) |
Conexiones del GPi con el Tálamo
Como se mencionó, el GPi es el principal núcleo de salida de los ganglios basales y proyecta principalmente hacia el tálamo. Las fibras eferentes del GPi forman haces conocidos como el ansa lenticularis y el fasciculus lenticularis. Estos haces atraviesan la cápsula interna y alcanzan la región ventrolateral del tálamo, dirigiéndose específicamente a los núcleos ventral lateral (VL) y ventral anterior (VA). El GPi ejerce una influencia tónica, es decir, constante en condiciones normales, sobre estos núcleos talámicos.
La naturaleza de esta influencia es inhibitoria. El GPi utiliza el neurotransmisor GABA (ácido gamma-aminobutírico), que es el principal neurotransmisor inhibitorio en el cerebro, para reducir la actividad de las neuronas en los núcleos VA y VL del tálamo. Dado que estos núcleos talámicos son cruciales para retransmitir información hacia la corteza motora y premotora, esta inhibición tónica por parte del GPi restringe la iniciación del movimiento y ayuda a prevenir movimientos no deseados o erráticos.
La modulación de esta inhibición tónica por las vías directa e indirecta es lo que permite el control fino del movimiento. Cuando la vía directa se activa, inhibe al GPi, reduciendo su freno sobre el tálamo. Esto "libera" al tálamo para que excite la corteza motora, permitiendo el movimiento. Cuando la vía indirecta se activa, excita al GPi, aumentando su freno sobre el tálamo, lo que suprime el movimiento. Esta interacción es un ejemplo clásico de cómo la desinhibición juega un papel fundamental en los circuitos neuronales.
Desarrollo Embrionario
El desarrollo del cerebro humano es un proceso complejo que comienza en las primeras semanas de gestación. Los ganglios basales, incluido el globus pallidus, tienen orígenes específicos durante este desarrollo. En la quinta semana de gestación, el prosencéfalo (cerebro anterior) se diferencia en telencéfalo y diencéfalo. El telencéfalo da origen a la mayoría de los componentes de los ganglios basales, como el núcleo caudado y el putamen.
Sin embargo, el globus pallidus tiene un origen ligeramente diferente. Se desarrolla a partir de neuroblastos en la pared del tercer ventrículo, una estructura que deriva del diencéfalo. Esta distinción embrionaria subraya las diferencias funcionales y de conectividad entre el GP y otras partes del estriado, a pesar de su estrecha relación anatómica y funcional en el cerebro maduro.
Suministro de Sangre y Drenaje Venoso
Como estructura cerebral vital, el GPi requiere un suministro constante y adecuado de sangre. Recibe su irrigación sanguínea de varias arterias cerebrales principales: la arteria coroidea anterior (AChA), la arteria cerebral media (ACM) y la arteria cerebral anterior (ACA).
La mayor parte del suministro sanguíneo al globus pallidus proviene de la ACM. Ramas perforantes de la ACA irrigan las porciones anterior e inferior del GP. Las arterias perforantes de la ACM irrigan la mayoría de las porciones superiores y posteriores del segmento lateral del GP (principalmente GPe). La arteria de Heubner, que puede surgir del segmento A1 o A2 de la ACA o en la unión de la ACA con la arteria comunicante anterior, también suministra una pequeña porción del segmento lateral del GP. La AChA perfunde la porción medial del GP, que incluye el GPi.

El drenaje venoso del GP se realiza a través de venas que drenan los ganglios basales adyacentes, especialmente el núcleo caudado y el putamen. Este sistema venoso se forma a partir de grupos de venas profundas y ventriculares. El grupo profundo incluye las venas estriadas inferiores que drenan el putamen y el núcleo caudado, uniéndose a las venas cerebrales medias profundas y basales. El grupo ventricular drena el núcleo caudado y se une a las venas cerebrales internas y basales. Las venas basales y cerebrales internas se unen para formar la gran vena de Galeno, que luego drena en el seno recto.
En cuanto al drenaje linfático, el sistema linfático del cerebro, incluyendo los ganglios basales, se ha descrito recientemente como un sistema perivascular, de líquido cefalorraquídeo (LCR), vías de drenaje olfatorio y vasos linfáticos meníngeos. Aunque se ha señalado que los espacios perivasculares en los ganglios basales y la corteza cerebral pueden ser estructuralmente diferentes, lo que contribuye a diferencias en la composición del fluido entre ambas áreas.
Rol en Funciones Cognitivas Superiores
Aunque el GPi es conocido principalmente por su papel en el control motor, los ganglios basales en su conjunto, y por extensión el GPi, también participan en funciones cognitivas superiores. Esto incluye procesos como el refuerzo, la formación de hábitos, la toma de decisiones y la memoria.
Los núcleos de los ganglios basales, incluido el GP, se interconectan con áreas corticales a través de circuitos de bucle paralelos e independientes. Las cortezas de asociación y límbicas proyectan a dominios específicos del estriado, que a su vez proyectan de regreso a las áreas corticales correspondientes a través del globus pallidus y el tálamo. Estos bucles funcionales permiten que los ganglios basales influyan en procesos no motores al integrar información de áreas cerebrales involucradas en la cognición y las emociones. Se ha sugerido que la ubicación del GP y la substantia nigra facilita la transmisión de información desde el sistema límbico al sistema asociativo, integrando así aspectos motivacionales y emocionales con la planificación y ejecución de acciones.
Variantes Fisiológicas
Estudios de neuroimagen han revelado variaciones fisiológicas en el volumen de las estructuras de los ganglios basales, incluyendo el globus pallidus, basadas en el género y la lateralidad (hemisferio cerebral). Al igual que con las estructuras corticales, existen diferencias volumétricas entre hombres y mujeres en las estructuras subcorticales.
Específicamente para el globus pallidus, los estudios de imagen han demostrado que es más grande en volumen en los hombres en comparación con las mujeres, incluso después de ajustar por el tamaño cortical general. Esta tendencia es opuesta a la observada en el núcleo caudado, que tiende a ser más grande en mujeres. En general, la tendencia de los estudios de imagen sugiere que las mujeres tienden a tener volúmenes subcorticales ligeramente mayores que los hombres, aunque el GP parece ser una excepción notable.
Además de las diferencias de género, también parece haber variabilidad interindividual y entre hemisferios en el volumen del globus pallidus. Algunos estudios de neuroimagen han encontrado que el volumen del GPi (y GPe) es significativamente mayor en el hemisferio izquierdo en comparación con el hemisferio derecho. Estas variantes fisiológicas son importantes para considerar en la investigación y en la interpretación de hallazgos clínicos.
Consideraciones Quirúrgicas: El GPi como Diana Terapéutica
Dada su posición crítica como núcleo de salida en los circuitos de los ganglios basales, el GPi ha sido un objetivo importante para diversas intervenciones quirúrgicas destinadas a tratar trastornos neurológicos, particularmente aquellos que involucran el movimiento.
Una de las aplicaciones quirúrgicas más relevantes del GPi es como blanco para la Estimulación Cerebral Profunda (ECP). La ECP del GPi bilateral ha demostrado ser un tratamiento eficaz para ciertas formas de distonía, incluyendo la asociada a la enfermedad de Wilson y mutaciones genéticas específicas (como la mutación GNAL), especialmente en pacientes que no responden adecuadamente a la medicación o a la toxina botulínica. La ECP implica implantar electrodos en el GPi que emiten impulsos eléctricos para modular su actividad, ayudando a aliviar los síntomas de distonía, que se caracterizan por contracciones musculares involuntarias y posturas anormales.
En el contexto de la enfermedad de Parkinson (EP), una enfermedad neurodegenerativa caracterizada por síntomas motores como temblor, rigidez y bradicinesia, la ECP también es un tratamiento establecido. Sin embargo, el blanco más común para la ECP en la EP es el núcleo subtalámico (NST). Se ha investigado si la ECP dirigida al GPi podría tener ventajas, particularmente en relación con los síntomas no motores como la depresión, que es común en la EP. Una revisión de la evidencia no encontró un beneficio claro de apuntar al GPi sobre el NST para los efectos en el estado de ánimo en pacientes con EP, aunque ambos blancos son efectivos para los síntomas motores principales.
Históricamente, el GPi también fue el objetivo de procedimientos quirúrgicos ablativos, como la palidotomía. La palidotomía implicaba la destrucción controlada de una pequeña parte del GPi para aliviar los síntomas de los trastornos del movimiento hipercinéticos (con movimientos excesivos) e hipocinéticos (con movimientos reducidos). La palidotomía se utilizó para tratar la enfermedad de Huntington y la enfermedad de Parkinson. Sin embargo, con el desarrollo de medicamentos más efectivos y, posteriormente, la ECP, la palidotomía fue en gran medida abandonada como tratamiento para la EP a mediados del siglo XX, aunque sigue siendo relevante en algunos casos de distonía severa u otros trastornos hipercinéticos.

La comprensión detallada de la anatomía funcional y las conexiones del GPi es crucial para el éxito de estos procedimientos quirúrgicos, asegurando que el objetivo se localice con precisión para maximizar el beneficio terapéutico y minimizar los riesgos.
Relevancia Clínica: El GPi en Diversos Trastornos
La disfunción del GPi o de los circuitos en los que participa está implicada en una amplia gama de trastornos neurológicos y psiquiátricos, lo que subraya su importancia clínica. Su papel como núcleo de salida lo convierte en un punto crítico en las vías que, al alterarse, pueden generar síntomas.
En la enfermedad de Parkinson, la pérdida de neuronas dopaminérgicas en la substantia nigra pars compacta (SNpc) afecta el equilibrio entre las vías directa e indirecta. La depleción de dopamina reduce la excitación de la vía directa (a través de receptores D1) y aumenta la inhibición de la vía indirecta (a través de receptores D2). Esto conduce a una mayor activación de la vía indirecta y una menor activación de la vía directa, resultando en una mayor excitación del NST y, crucialmente, un aumento excesivo de la actividad neuronal en el GPi. Esta hiperactividad del GPi resulta en una mayor inhibición del tálamo, lo que suprime el movimiento y contribuye a los síntomas motores parkinsonianos como la bradicinesia y la rigidez. Los estudios han demostrado consistentemente un aumento en la tasa de disparo de las neuronas del GPi en modelos de EP y en pacientes con la enfermedad.
En contraste, la enfermedad de Huntington es un trastorno neurodegenerativo caracterizado por movimientos coreicos (movimientos involuntarios, bruscos y fluidos) y deterioro cognitivo. En la enfermedad de Huntington, hay una pérdida significativa de neuronas en el estriado, particularmente las que forman parte de la vía indirecta (neuronas con receptores D2). La pérdida de estas neuronas reduce la inhibición sobre el GPe. Un GPe menos inhibido aumenta su inhibición sobre el NST, lo que reduce la excitación del GPi. La menor actividad del GPi resulta en una menor inhibición del tálamo, lo que lleva a una desinhibición excesiva del tálamo y, en consecuencia, a movimientos involuntarios. Aunque el GP en sí mismo (incluyendo el GPi) puede mostrar una disminución severa de tamaño en etapas avanzadas de la enfermedad de Huntington, los síntomas motores tempranos se relacionan más directamente con la disfunción de los circuitos estriatales que proyectan al GP.
El GPi también está implicado en trastornos con componentes motores y no motores, como el Trastorno Obsesivo-Compulsivo (TOC) y el Síndrome de Tourette. En el TOC, se han observado alteraciones en la conectividad funcional de los circuitos cortico-estriatales, incluyendo una mayor conectividad entre el GPe, el NST y el GPi, lo que sugiere un papel del GPi en la fisiopatología y explica el éxito de la ECP dirigida al GPi en casos severos.
Se ha documentado la disfunción del GP en casos de isquemia, donde otras partes de los ganglios basales como el putamen y el caudado son más vulnerables, pero el GP puede resultar afectado. También existen informes de casos de lesiones bilaterales del GP asociadas con el abuso crónico de alcohol y opiáceos, lo que resulta en diversos problemas cognitivos y motores. La comprensión de cómo estas sustancias afectan el GPi y los circuitos de los ganglios basales es un área activa de investigación.
En resumen, el GPi no es solo un relé pasivo de información, sino un modulador activo cuya actividad es crítica para el control motor fino y participa en funciones cognitivas. Su disfunción, ya sea por degeneración, lesión o desequilibrios neuroquímicos, tiene profundas consecuencias para la salud neurológica, manifestándose en una variedad de trastornos que afectan el movimiento, el pensamiento y el comportamiento.
Preguntas Frecuentes sobre el GPi
¿Qué es el GPi en neurociencia?
En neurociencia, GPi se refiere al Globus Pallidus Internus, que es uno de los dos segmentos principales del globus pallidus, una estructura subcortical que forma parte de los ganglios basales. El GPi es fundamentalmente el núcleo de salida principal de los ganglios basales, lo que significa que es el punto por donde la información procesada por el sistema de ganglios basales abandona esta red para influir en otras áreas del cerebro, principalmente el tálamo. Juega un papel esencial en la regulación y el control del movimiento, así como en funciones cognitivas y emocionales.
¿Qué hace el GPi al tálamo?
El GPi ejerce una influencia inhibitoria tónica (constante) sobre los núcleos talámicos, específicamente los núcleos ventral anterior (VA) y ventral lateral (VL). Estos núcleos talámicos son importantes para retransmitir señales excitatorias a la corteza motora. Al inhibir el tálamo, el GPi restringe la actividad talámica y, por lo tanto, limita la excitación de la corteza motora. Esta inhibición basal es crucial para prevenir movimientos no deseados. La modulación de esta inhibición por las vías directa e indirecta de los ganglios basales permite la desinhibición controlada del tálamo para iniciar movimientos deseados (vía directa) o aumentar la inhibición para suprimir movimientos (vía indirecta).
¿El GPi es inhibitorio o excitatorio?
Las neuronas que constituyen el GPi son inhibitorias. Utilizan principalmente el neurotransmisor GABA para ejercer su efecto. Las proyecciones del GPi a sus principales objetivos, como el tálamo, son de naturaleza inhibitoria, reduciendo la actividad de las neuronas receptoras. Sin embargo, el *efecto neto* de la actividad del GPi en el movimiento depende de cómo es modulado por otras partes de los ganglios basales. Por ejemplo, la inhibición del GPi por la vía directa resulta en un efecto *excitatorio* general sobre la corteza motora (a través de la desinhibición del tálamo), mientras que la excitación del GPi por la vía indirecta resulta en un efecto *inhibitorio* general sobre la corteza motora.
Conclusión
El Globus Pallidus Internus (GPi) es una estructura cerebral de inmensa importancia funcional. Como principal núcleo de salida de los ganglios basales, actúa como un punto de control crucial en la compleja red que regula el movimiento, integrando información de diversas vías y modulando la actividad del tálamo para permitir la ejecución fluida y precisa de acciones deseadas mientras suprime las no deseadas. Su participación en los circuitos directos e indirectos, su intrincada conectividad, su desarrollo embrionario particular y su vulnerabilidad o alteración en diversas condiciones patológicas, desde la enfermedad de Parkinson y Huntington hasta el TOC y la distonía, resaltan su papel central en la neurobiología del movimiento y más allá. La investigación continua sobre el GPi y sus interacciones dentro de los ganglios basales no solo profundiza nuestra comprensión del cerebro en funcionamiento, sino que también abre vías para el desarrollo de tratamientos más efectivos para una variedad de trastornos neurológicos debilitantes.
Si quieres conocer otros artículos parecidos a GPi en Neurociencia: El Núcleo de Salida Clave puedes visitar la categoría Neurociencia.
