Los Receptores Acoplados a Proteínas G, o GPCRs por sus siglas en inglés (G-protein coupled receptors), constituyen una vasta superfamilia de proteínas integrales de membrana que desempeñan roles fundamentales en la biología de todos los organismos eucariotas, desde levaduras hasta humanos. En el complejo entramado del sistema nervioso, los GPCRs son actores esenciales, modulando la función cerebral mediante la transducción de una increíble diversidad de señales, que abarcan desde fotones y iones hasta péptidos, hormonas y, crucialmente, neurotransmisores.
Con casi 800 genes codificadores en el genoma humano, representando más del 3% del total, los GPCRs son las dianas terapéuticas más frecuentes en la farmacología moderna. Su estructura característica, con un extremo amino terminal extracelular, siete dominios transmembrana en alfa hélice y un extremo carboxilo terminal intracelular, les permite atravesar la membrana plasmática y conectar el exterior celular, donde detectan señales, con el interior, donde inician cascadas de señalización.
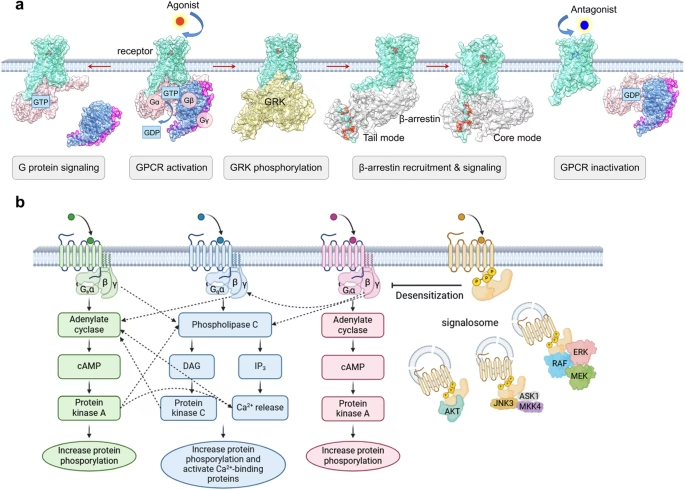
Mecanismo de Señalización de GPCRs: El Ciclo de las Proteínas G
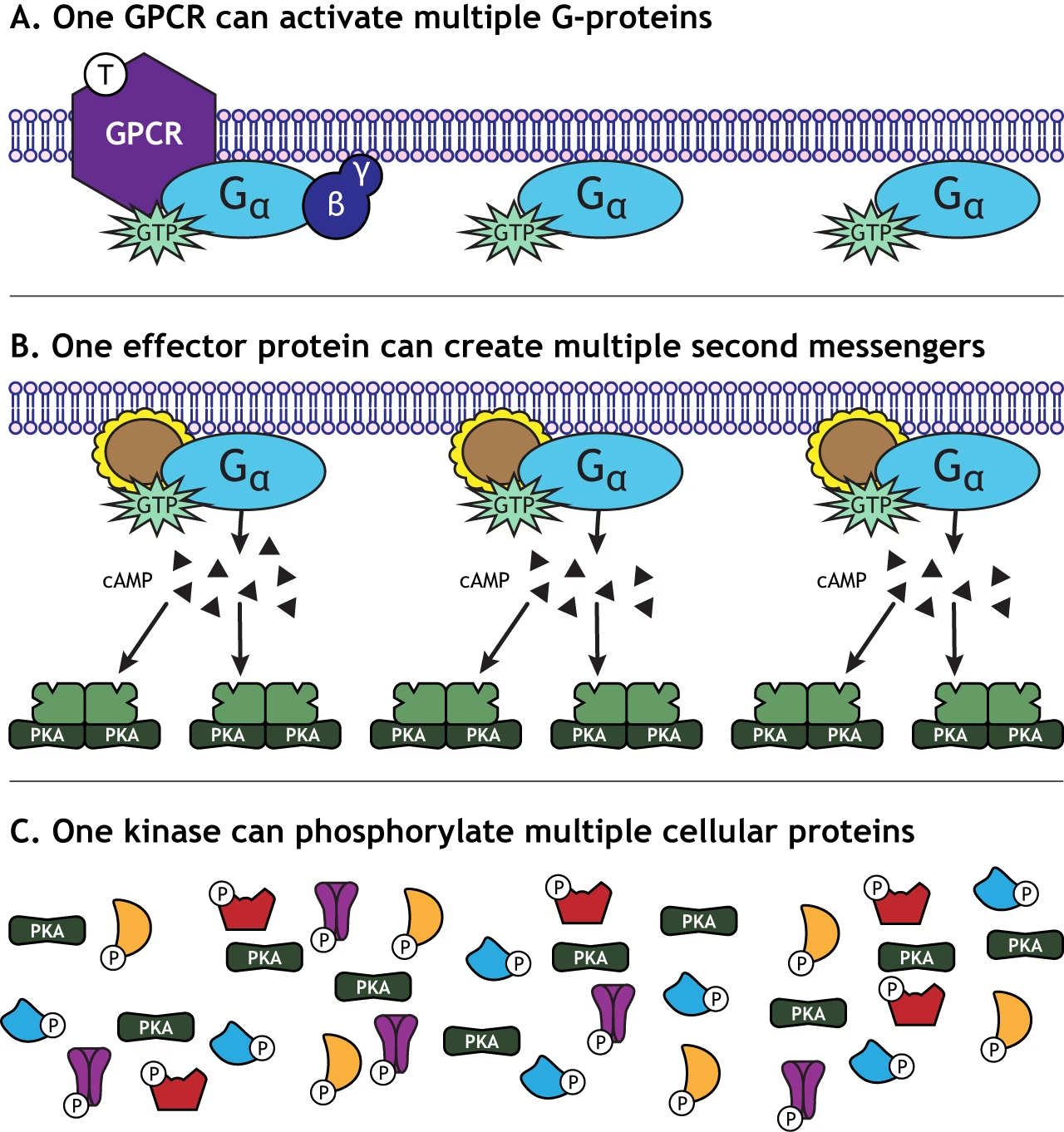
La característica definitoria de los GPCRs es su capacidad para asociarse con proteínas G heterotriméricas (compuestas por subunidades alfa, beta y gamma). Este acoplamiento es el paso inicial en una cascada de señalización intracelular que permite a la célula responder a la señal detectada por el receptor.
En su estado inactivo, la proteína G heterotrimérica se encuentra unida a la membrana plasmática en el lado citoplasmático y la subunidad alfa está ligada a una molécula de guanosín difosfato (GDP). La interacción de un ligando extracelular con el GPCR provoca un cambio conformacional en el receptor. Este cambio permite que el GPCR interactúe con la proteína G inactiva, actuando como un factor de intercambio de nucleótidos de guanina (GEF).
Como GEF, el GPCR activado induce a la subunidad alfa de la proteína G a liberar el GDP y, en su lugar, unirse a una molécula de guanosín trifosfato (GTP) que está disponible en el citosol. Esta unión a GTP provoca un cambio conformacional en la propia proteína G, lo que lleva a su activación. La subunidad alfa unida a GTP se disocia del dímero beta-gamma (Gβγ), y tanto Gα-GTP como Gβγ pueden proceder a interactuar y regular la actividad de diversas proteínas efectoras en la célula, como enzimas o canales iónicos.
La señalización debe ser finamente controlada para evitar respuestas excesivas o prolongadas. La subunidad alfa de la proteína G posee una actividad GTPasa intrínseca, lo que significa que puede hidrolizar lentamente el GTP unido a GDP. Esta hidrólisis inactiva la subunidad alfa, permitiendo que se reasocie con el dímero beta-gamma y que la proteína G vuelva a su estado inactivo, lista para ser activada de nuevo por un receptor. La velocidad de esta hidrólisis de GTP es significativamente aumentada por proteínas reguladoras específicas llamadas Proteínas Reguladoras de Señalización de Proteínas G (RGS), que actúan como proteínas activadoras de GTPasa (GAPs) para las subunidades alfa.
Vías de Señalización Intracelular Mediadas por GPCRs
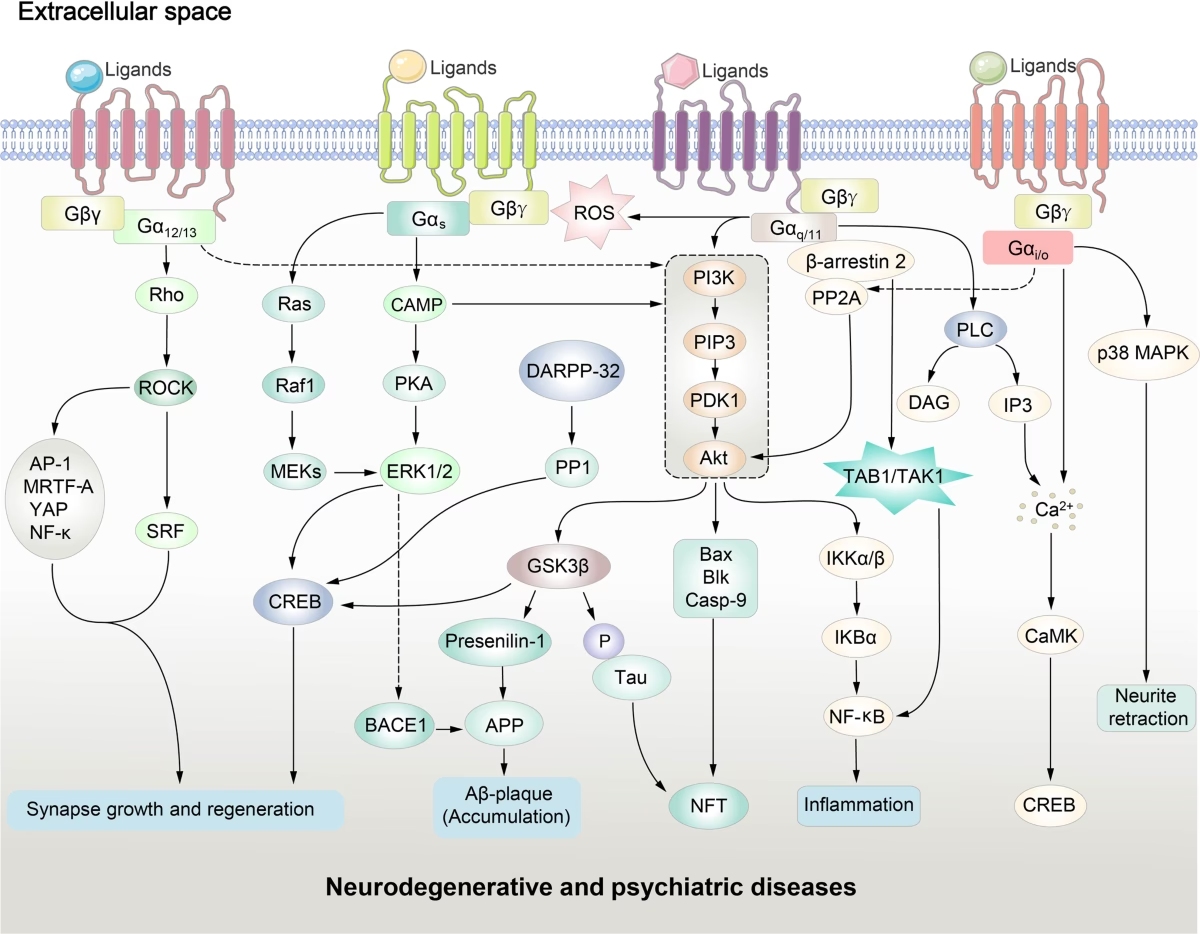
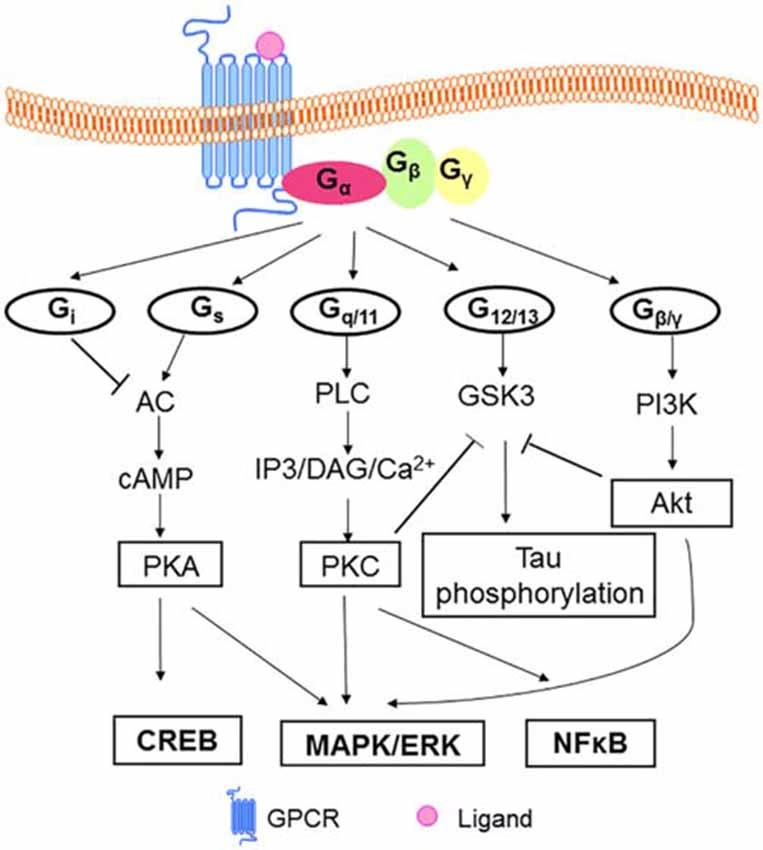
La diversidad funcional de los GPCRs radica en su capacidad para acoplarse a diferentes tipos de proteínas G, principalmente Gs, Gi/o y Gq/11, cada una de las cuales activa distintas cascadas de señalización intracelular:
- Proteínas Gs: La activación de las proteínas Gs estimula la enzima adenilil ciclasa, lo que resulta en un aumento de los niveles intracelulares del segundo mensajero monofosfato de adenosina cíclico (cAMP). El cAMP, a su vez, activa la Proteína Cinasa A (PKA), que fosforila un amplio rango de proteínas diana en residuos de serina/treonina, mediando diversas respuestas celulares.
- Proteínas Gi/o: En contraste, la activación de las proteínas Gi/o inhibe la adenilil ciclasa, lo que lleva a una disminución en los niveles de cAMP. Además, las subunidades beta-gamma liberadas de Gi/o pueden interactuar directamente con ciertos canales iónicos o enzimas, modulando su actividad.
- Proteínas Gq/11: Las proteínas Gq/11 activan la isoforma beta de la enzima Fosfolipasa C (PLCβ). La PLCβ hidroliza un fosfolípido de membrana, el fosfatidilinositol 4,5-bisfosfato (PIP2), generando dos segundos mensajeros: diacilglicerol (DAG) e inositol 1,4,5-trisfosfato (IP3). El IP3 se une a receptores específicos en el retículo endoplasmático, provocando la liberación de iones calcio (Ca2+) al citosol, un mensajero intracelular crucial. El DAG, por su parte, activa la Proteína Cinasa C (PKC), otra cinasa que fosforila proteínas diana y participa en numerosas vías de señalización.
Además de estas vías principales, algunos GPCRs pueden influir directamente en la actividad de canales iónicos en la membrana plasmática o regularlos indirectamente a través de la fosforilación mediada por PKA o PKC.
GPCRs en el Cerebro: Neuromodulación y Circuitos Neuronales
En neurociencia, los GPCRs son fundamentales para la neuromodulación, es decir, la modulación de la actividad neuronal y muscular por parte de neurotransmisores y neuromoduladores. A diferencia de la señalización sináptica rápida mediada por receptores ionotrópicos, los GPCRs a menudo median respuestas más lentas y duraderas que pueden ajustar la excitabilidad de una neurona o la fuerza de una sinapsis a lo largo del tiempo.
Estudios en organismos modelo como C. elegans han revelado aspectos importantes de la señalización GPCR en el sistema nervioso. Se ha demostrado que los neurotransmisores pueden difundir distancias considerables desde su sitio de liberación para activar GPCRs en células distantes, incluso no sinápticas. Esto sugiere que el patrón de señalización mediado por GPCRs no está determinado únicamente por el cableado sináptico anatómico, sino también por los patrones específicos de expresión de los neurotransmisores y sus receptores acoplados a proteína G.
La expresión de GPCRs neuronales tiende a ser muy específica y restringida a conjuntos limitados de células. Esta especificidad permite que cada tipo de receptor ejerza efectos muy concretos en circuitos neuronales individuales y, por ende, en comportamientos específicos. Los estudios genéticos en C. elegans han sido cruciales para identificar nuevos componentes moleculares en las vías de señalización de proteínas G neuronales, incluyendo las proteínas RGS y proteínas como RIC-8.
Un enfoque integrador reciente, utilizando datos de expresión de ARNm de GPCRs del Allen Brain Atlas en cerebros de ratones, macacos y humanos, ha analizado cómo se organizan grandes comunidades (conjuntos) de subtipos de GPCRs en diferentes regiones anatómicas. Aunque la expresión de ARNm de GPCR fue heterogénea en todas las regiones corticales, se encontraron fuertes correlaciones espaciales entre los sistemas acoplados a Gq/11, Gs y Gi/o. La fuerza de estas correlaciones aumentó con la edad, pero disminuyó al eliminar genes aleatoriamente de sus grupos. Estos hallazgos sugieren que los patrones de expresión de los subtipos y familias de receptores GPCR están intrincadamente entrelazados. Las interacciones bien orquestadas por estos conjuntos de GPCRs neuromoduladores podrían ser cruciales para que el cerebro funcione como un sistema complejo altamente integrado.
Regulación y Desensibilización de la Señalización por GPCRs
La atenuación de la señalización por GPCRs tras la exposición prolongada a un agonista es esencial para prevenir la sobreestimulación y mantener la homeostasis celular. Este proceso implica una serie coordinada de eventos, generalmente considerados en tres etapas:
- Desensibilización del Receptor: Comienza a los pocos segundos de la exposición al agonista. Se inicia con la fosforilación del receptor, a menudo por cinasas activadas por segundos mensajeros (como PKA y PKC) o por Cinasa de Receptores Acoplados a Proteínas G (GRKs). La fosforilación en residuos de serina y treonina en las asas citoplasmáticas y la cola C-terminal deteriora la eficiencia del acoplamiento receptor-proteína G, reduciendo la señalización. La desensibilización no implica un cambio detectable en el número de receptores en la superficie y es rápidamente reversible al retirar el agonista.
- Secuestro o Internalización del Receptor: Ocurre más lentamente, en cuestión de minutos. La mayoría de los GPCRs internalizan en vesículas recubiertas de clatrina de manera dependiente de dinamina. La fosforilación por GRKs y la unión de proteínas β-arrestina al receptor facilitan esta endocitosis. Para que un receptor secuestrado se resensibilice, la β-arrestina debe disociarse, el receptor debe ser desfosforilado y el ligando unido debe ser eliminado.
- Regulación a la Baja (Downregulation): La activación prolongada puede llevar a la eliminación de receptores de la membrana plasmática a través de la endocitosis y su posterior degradación en lisosomas. Este proceso, conocido como regulación a la baja, reduce el número total de receptores disponibles en la superficie celular, disminuyendo la capacidad de respuesta de la célula a futuras estimulaciones.
Impacto en la Salud: GPCRs y Enfermedades
Dada su ubicuidad y roles fundamentales, no sorprende que las disfunciones en los GPCRs estén implicadas en una amplia gama de condiciones patofisiológicas. Más de 30 enfermedades y síndromes humanos se asocian potencialmente con la pérdida o ganancia de función de GPCRs causadas por mutaciones.
Las mutaciones activadoras constitutivas, donde el receptor señaliza incluso en ausencia de ligando, pueden contribuir a enfermedades como el hipertiroidismo no autoinmune (mutaciones en el receptor de TSH), la pubertad precoz familiar limitada al varón (mutaciones en el receptor de LHR) o ciertas formas de cáncer (mutaciones en el receptor adrenérgico α1B). La condrodisplasia metafisaria de Jansen, una forma rara de enanismo, es causada por mutaciones activadoras en el receptor de PTH/PTHrP.
Por otro lado, las mutaciones inactivadoras, que resultan en la pérdida de función del receptor, están relacionadas con enfermedades como la diabetes insípida nefrogénica (mutaciones en el receptor de vasopresina V2 o acuaporina 2) y la retinosis pigmentaria (mutaciones en la rodopsina, un GPCR clave en la visión). La retinosis pigmentaria, una enfermedad ocular hereditaria, causa daño en la retina, llevando a visión borrosa y dificultad para ver con poca luz, sin tratamiento curativo conocido.
Además de las mutaciones genéticas, las GPCRs pueden ser blanco de toxinas bacterianas con consecuencias clínicas graves. La toxina del cólera, por ejemplo, modifica la subunidad alfa de las proteínas Gs, impidiendo la hidrólisis de GTP y bloqueándola en un estado activo. Esto resulta en una estimulación constante de la adenilil ciclasa en las células epiteliales intestinales, llevando a una secreción excesiva de iones cloruro y agua en el intestino, causando diarrea severa y deshidratación potencialmente mortal. De manera similar, la toxina de la tosferina modifica las proteínas Gi, impidiendo su interacción con los GPCRs y manteniéndolas inactivas.
GPCRs como Dianas Terapéuticas y Nuevos Horizontes
La relevancia clínica de los GPCRs es inmensa. Representan aproximadamente el 30% de todas las dianas farmacológicas identificadas y siguen siendo objetivos principales para el desarrollo de nuevos medicamentos. Fármacos que actúan sobre GPCRs se utilizan para tratar una vasta gama de afecciones, incluyendo trastornos del sistema nervioso central, enfermedades cardiovasculares, metabólicas, respiratorias y cáncer.
Sin embargo, el desarrollo de fármacos dirigidos a GPCRs presenta desafíos. La falta de conocimiento estructural detallado para muchos receptores y su amplia expresión en diversos tejidos pueden llevar a efectos secundarios no deseados debido a la 'polifarmacología', donde un ligando interactúa con múltiples dianas. Además, aún existen muchos GPCRs 'huérfanos' cuyos ligandos endógenos y funciones se desconocen.
La investigación reciente está explorando conceptos más sofisticados para mejorar la especificidad y eficacia de los fármacos dirigidos a GPCRs:
- Polifarmacología: Aunque a veces es un desafío, entender y diseñar ligandos que interactúen selectivamente con múltiples dianas (como los antipsicóticos atípicos que actúan sobre receptores de dopamina y serotonina) puede ser beneficioso para tratar enfermedades complejas que involucran múltiples vías.
- Señalización Sesgada (Biased Signaling): Los GPCRs activados pueden reclutar diferentes transductores (proteínas G, GRKs, β-arrestinas) y generar respuestas biológicas distintas. Los ligandos sesgados activan preferentemente una vía sobre otra. Por ejemplo, agonistas sesgados hacia la proteína G (y no hacia β-arrestina) en el receptor µ-opioide buscan mantener la analgesia mientras reducen efectos secundarios como la depresión respiratoria. Este concepto ofrece un gran potencial para diseñar fármacos con perfiles de seguridad y eficacia mejorados.
- Modulación Alostérica: Un modulador alostérico se une a un sitio del receptor diferente del sitio ortostérico (donde se une el ligando endógeno), pero altera la respuesta del receptor al ligando ortostérico. Los moduladores alostéricos pueden ser positivos (PAMs, potencian la respuesta) o negativos (NAMs, atenúan la respuesta). Estos moduladores tienen ventajas como la posibilidad de dirigirse a bolsillos menos conservados (mejorando la selectividad) y la capacidad de introducir sesgo de señalización. Aunque su desarrollo es desafiante, varios moduladores alostéricos ya están en el mercado o en ensayos clínicos.
Estos avances en la comprensión de la estructura dinámica, la señalización compleja y la organización en conjuntos de GPCRs están abriendo nuevas vías para el desarrollo de terapias más dirigidas y efectivas para una multitud de enfermedades, muchas de ellas relacionadas con la función del sistema nervioso.
Tabla Comparativa: Vías Principales de Señalización de Proteínas G
A continuación, se presenta una tabla que resume las características principales de las vías de señalización mediadas por los subtipos de proteínas G más relevantes:
| Tipo de Proteína G | Efector Primario | Segundo Mensajero(s) | Efecto Principal | Ejemplos de Diana Aguas Abajo |
|---|---|---|---|---|
| Gs | Adenilil ciclasa | Aumento de cAMP | Estimulación de la actividad celular | Proteína Cinasa A (PKA) |
| Gi/o | Adenilil ciclasa Canales iónicos (directo) | Disminución de cAMP Modulación iónica | Inhibición de la actividad celular Modulación de la excitabilidad | Proteína Cinasa A (PKA) Canales de K+ Canales de Ca2+ |
| Gq/11 | Fosfolipasa C beta (PLCβ) | IP3 y DAG Aumento de Ca2+ intracelular | Diversas respuestas celulares (contracción, secreción, etc.) | Receptores de IP3 (Liberación de Ca2+) Proteína Cinasa C (PKC) |
Preguntas Frecuentes sobre GPCRs en Neurociencia
¿Los GPCRs solo funcionan en las sinapsis?
No, aunque algunos GPCRs se localizan en las sinapsis y responden a neurotransmisores liberados sinápticamente, muchos otros se expresan fuera de las sinapsis. Los neurotransmisores pueden difundir a cierta distancia desde su punto de liberación (señalización extrasináptica) para activar GPCRs en células neuronales o no neuronales distantes. Esto amplía la forma en que los neuromoduladores pueden influir en los circuitos.
¿Cuántos tipos de proteínas G hay?
Existen varios tipos de proteínas G heterotriméricas, clasificadas principalmente por la subunidad alfa. Las más estudiadas y relevantes en neurociencia son las familias Gs, Gi/o y Gq/11. También existen las proteínas G12/13, que activan Rho GTPasas, aunque su papel no se detalló en la información proporcionada.
¿Cómo se detiene la señalización mediada por GPCRs?
La señalización se detiene a través de varios mecanismos. Uno es la hidrólisis del GTP unido a la subunidad alfa por su propia actividad GTPasa, acelerada por proteínas RGS. Otro es la eliminación del ligando del espacio extracelular (por enzimas o transportadores). Además, el propio receptor puede ser inactivado mediante desensibilización (fosforilación que reduce su acoplamiento a la proteína G), internalización (retirada de la membrana plasmática) o regulación a la baja (degradación del receptor).
¿Pueden los GPCRs acoplarse a más de un tipo de proteína G?
Sí, un mismo GPCR puede acoplarse preferentemente a un tipo de proteína G, pero algunos receptores pueden interactuar con múltiples tipos de proteínas G o incluso con otras proteínas como las β-arrestinas de manera diferencial, dependiendo del ligando que se una. Este fenómeno es la base de la señalización sesgada.
¿Por qué son importantes los GPCRs como dianas de fármacos?
Los GPCRs controlan una vasta gama de funciones fisiológicas en todo el cuerpo, incluyendo la neurotransmisión, el metabolismo, la función cardíaca, las respuestas inmunes y sensoriales. Las disfunciones en los GPCRs están implicadas en numerosas enfermedades. Por lo tanto, modular su actividad con fármacos permite influir en estas funciones y tratar enfermedades.
En conclusión, los GPCRs son componentes indispensables de la comunicación celular, especialmente en el sistema nervioso. Su compleja estructura, mecanismos de señalización versátiles y capacidad para integrar diversas señales los convierten en elementos clave para la función cerebral y la homeostasis del organismo. La investigación continua sobre estos receptores, incluyendo su organización en conjuntos y las nuevas modalidades de señalización, promete abrir caminos para terapias más innovadoras y efectivas.
Si quieres conocer otros artículos parecidos a GPCRs: Receptores Clave en Neurociencia puedes visitar la categoría Neurociencia.