Cuando pensamos en el cerebro, la primera célula que viene a la mente es, sin duda, la neurona, famosa por su capacidad de comunicación eléctrica y sináptica. Sin embargo, el tejido nervioso alberga otra población celular fundamental, a menudo subestimada: las células gliales. Durante mucho tiempo, se pensó que estas células simplemente actuaban como un "pegamento" que mantenía unidas a las neuronas. Hoy sabemos que su papel es mucho más activo y crucial para prácticamente todos los aspectos de la función cerebral, desde el desarrollo hasta la respuesta a lesiones y la asombrosa capacidad del cerebro para cambiar y adaptarse.
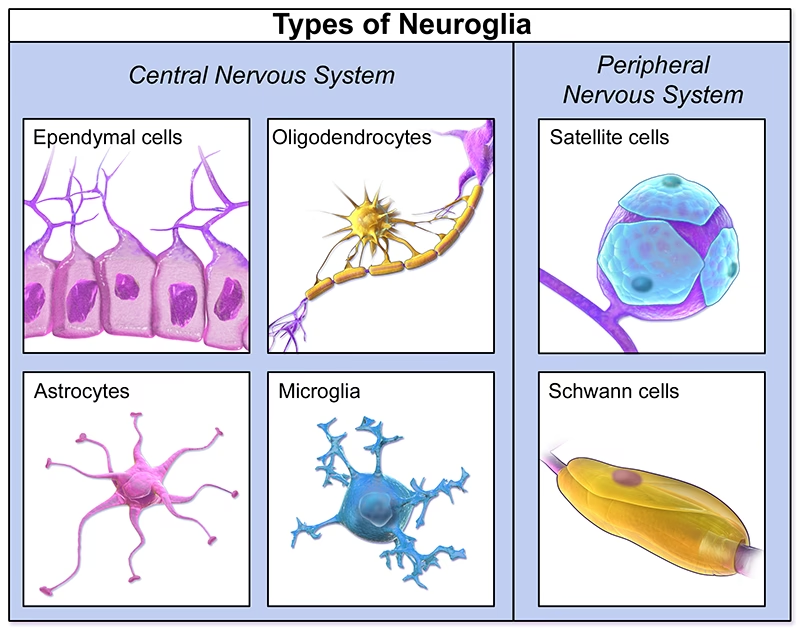
Las células neurogliales, comúnmente llamadas células gliales o simplemente glía, son radicalmente diferentes de las neuronas. La distinción principal radica en que la glía no participa directamente en las interacciones sinápticas ni en la señalización eléctrica, aunque sus funciones de soporte son vitales para definir los contactos sinápticos y mantener la capacidad de señalización de las neuronas. De hecho, son mucho más numerosas que las células nerviosas en el cerebro, superándolas en una proporción que podría ser de 3 a 1. Aunque las células gliales también poseen procesos complejos que se extienden desde sus cuerpos celulares, suelen ser más pequeñas que las neuronas y carecen de axones y dendritas. El término "glía", derivado de la palabra griega que significa "pegamento", refleja esa antigua creencia del siglo XIX de que estas células simplemente mantenían unido el sistema nervioso. A pesar de la falta de evidencia que respalde esta función de unión, el nombre ha perdurado, aunque ahora reconocemos una multitud de roles esenciales.
Funciones Vitales de las Células Gliales
Las funciones bien establecidas de las células gliales son diversas y complejas. Incluyen mantener el entorno iónico adecuado para las células nerviosas, modular la velocidad de propagación de las señales nerviosas, influir en la acción sináptica controlando la recaptación de neurotransmisores, proporcionar un andamiaje esencial para ciertos aspectos del desarrollo neural y desempeñar un papel crucial en la recuperación (o en algunos casos, la prevención de la recuperación) después de una lesión neural.
En el sistema nervioso central (SNC), que comprende el cerebro y la médula espinal, la glía es de suma importancia, ya que regula funciones vitales como el metabolismo, el equilibrio iónico (o equilibrio del pH) y la neurotransmisión. La neurotransmisión se refiere a la forma en que las neuronas se comunican entre sí o con las fibras musculares.
Tipos Principales de Células Gliales
Existen varios tipos de células gliales, cada una con roles especializados. En el sistema nervioso central maduro, encontramos tres tipos principales:
Astrocitos
Los astrocitos, restringidos al cerebro y la médula espinal, son el tipo más abundante de célula glial en el SNC. Poseen elaborados procesos locales que les dan una apariencia estrellada (de ahí el prefijo "astro"). Su función principal es mantener un entorno químico apropiado para la señalización neuronal de diversas maneras. Esto incluye la regulación de neurotransmisores, la formación de la barrera hematoencefálica (una capa protectora crucial), la limpieza de los restos de neuronas muertas y el exceso de iones potasio, el control del flujo sanguíneo al cerebro para asegurar que las regiones activas reciban suficiente sangre, la sincronización de la actividad axonal y la regulación del metabolismo cerebral almacenando glucosa para alimentar a las neuronas. La disfunción de los astrocitos se ha relacionado con afecciones neurológicas como la enfermedad de Alzheimer.
Oligodendrocitos
Los oligodendrocitos, también restringidos al sistema nervioso central, son responsables de formar la mielina, una envoltura laminada rica en lípidos que rodea algunos axones. La mielina es fundamental para la velocidad de conducción del potencial de acción. En el sistema nervioso periférico (SNP), las células que elaboran mielina se llaman Células de Schwann. Los oligodendrocitos desempeñan un papel importante en enfermedades neurológicas como la esclerosis múltiple, donde la vaina de mielina se daña.
Microglía
La microglía son células más pequeñas derivadas de células madre hematopoyéticas (aunque algunas pueden provenir directamente de células madre neurales). Comparten muchas propiedades con los macrófagos tisulares y son principalmente células "limpiadoras" que eliminan los restos celulares de los sitios de lesión o del recambio celular normal. De hecho, algunos neurobiólogos prefieren clasificar la microglía como un tipo de macrófago. Son las células inmunes residentes del cerebro y sirven como primera línea de defensa contra patógenos o agentes causantes de enfermedades. Patrullan constantemente, buscando células atípicas o dañadas. Cuando encuentran algo anómalo, lo envuelven y destruyen mediante fagocitosis. Después de un daño cerebral, el número de microglía en el sitio de la lesión aumenta drásticamente, ya sea por proliferación de la microglía residente o por migración de macrófagos desde la circulación.
Células Ependimarias
Las células ependimarias se desarrollan en los ventrículos y compartimentos llenos de líquido del SNC. Revisten estos espacios y ayudan a formar y transportar el líquido cefalorraquídeo (LCR).
En el sistema nervioso periférico, las Células de Schwann cumplen la función de mielinización equivalente a la de los oligodendrocitos en el SNC.
La Glía y la Neuroplasticidad: Modelando el Cerebro
Tradicionalmente, la neuroplasticidad, la capacidad del tejido nervioso para cambiar, se ha asociado principalmente con las neuronas y la modificación de la fuerza sináptica. Sin embargo, la evidencia emergente subraya que las células gliales desempeñan un papel activo y crucial en la configuración de la neuroplasticidad, permitiendo una regulación altamente flexible de la transmisión sináptica, la excitabilidad neuronal y la sincronización de redes.

El Papel de los Astrocitos en la Plasticidad
Los astrocitos regulan la sinaptogénesis (la formación de nuevas sinapsis), estabilizan la conectividad sináptica y preservan el delicado equilibrio entre excitación e inhibición en las redes neuronales. Sus finos procesos perisinápticos, a menudo llamados "cunas astrocíticas", envuelven las terminales presinápticas y las espinas dendríticas de las sinapsis excitatorias, creando microdominios que facilitan la comunicación local entre el astrocito y la sinapsis. Este concepto ha llevado a la idea de la sinapsis tripartita (neurona pre-sináptica, neurona post-sináptica y astrocito) e incluso tetrapartita (incluyendo la matriz extracelular).
Los astrocitos contribuyen a la estabilidad sináptica produciendo moléculas de adhesión celular como efrinas, integrinas y cadherinas, y promoviendo la expresión de otras moléculas que fortalecen la unión sináptica. También producen proteoglicanos de heparán sulfato como los glicanos, que inducen la formación de sinapsis funcionales y modulan la plasticidad sináptica promoviendo la agrupación de receptores de glutamato. Otras proteínas como las trombospondinas y la hevina, producidas por astrocitos, también regulan la formación y estabilidad sináptica.
A nivel funcional, los astrocitos controlan dinámicamente la concentración de neurotransmisores en el espacio perisináptico. Crean barreras de difusión que limitan la dispersión de neurotransmisores y expresan transportadores de aminoácidos excitatorios (EAATs), como EAAT1 y EAAT2, que median la rápida recaptación de glutamato, dando forma a las respuestas postsinápticas. De manera similar, recaptan GABA a través del transportador GAT3, regulando así tanto la señalización excitatoria como la inhibitoria.
Además de la recaptación, los astrocitos liberan activamente neurotransmisores, un proceso llamado gliotransmisión. Responden a la estimulación neuronal con elevaciones transitorias de calcio intracelular (eventos de Ca2+), que pueden ser locales (microdominios) o extenderse a toda la célula y sus vecinas (ondas de Ca2+). Estos eventos de Ca2+ desencadenan la liberación de gliotransmisores como glutamato, D-serina (que potencia las sinapsis excitatorias) y ATP/adenosina (que puede inducir supresión heterosináptica). La gliotransmisión puede potenciar o inhibir la transmisión sináptica y la excitabilidad neuronal, actuando como un modulador flexible.
Mediante uniones gap, los astrocitos forman redes que pueden regular la sincronización neuronal en una escala de tiempo más lenta que la transmisión sináptica. Los eventos de Ca2+ que viajan a través de estas uniones pueden transferir estímulos excitatorios o inhibitorios entre territorios astrocíticos, contribuyendo al equilibrio excitación-inhibición.
El equilibrio iónico, particularmente el del potasio (K+), es crucial para la excitabilidad neuronal. Durante la actividad neuronal, se acumula K+ extracelular, lo que podría despolarizar y bloquear la actividad. Los astrocitos son fundamentales para amortiguar este exceso de K+ (hasta el 80%) a través de canales Kir4.1, trabajando en concierto con transportadores de glutamato y bombas Na+/K+-ATPasa para mantener la homeostasis iónica. Las condensaciones de matriz extracelular, como las redes perineuronales, también pueden secuestrar iones K+ extracelularmente.
Finalmente, los astrocitos son centrales en la regulación metabólica neuronal. Las neuronas son muy demandantes energéticamente pero dependen de los astrocitos para el suministro de metabolitos. Los astrocitos utilizan glucólisis y producen lactato, que es transportado a las neuronas a través del "transbordador de lactato astrocito-neurona". Las neuronas convierten el lactato de nuevo en piruvato para alimentar su ciclo de Krebs y fosforilación oxidativa. El lactato también puede potenciar las corrientes mediadas por receptores NMDA, esencial para la formación de la memoria a largo plazo. Los astrocitos también participan en el ciclo glutamato-glutamina, convirtiendo el glutamato recaptado en glutamina, que luego es transportada a las neuronas para la síntesis de neurotransmisores (tanto glutamato como GABA). Este ciclo es crítico para la neurotransmisión y la plasticidad sináptica.
La Microglía y el Remodelado Sináptico
La microglía, las células inmunes residentes del cerebro, monitorean continuamente el microambiente y desempeñan un papel activo en el remodelado dinámico de la conectividad sináptica en el cerebro adulto. Eliminan sinapsis, un proceso crucial para afinar los circuitos neurales.
Las sinapsis son eliminadas por la microglía a través de fagocitosis, a menudo mediada por componentes del complemento (C1q y C3) y la exposición de fosfatidilserina o pentraxinas en las membranas presinápticas. Esta eliminación de sinapsis es un mecanismo esencial tanto durante el desarrollo cerebral (para podar sinapsis inmaduras o excesivas) como en el cerebro adulto para remodelar circuitos. Curiosamente, una disfunción en este proceso puede contribuir a la pérdida patológica de sinapsis, como se observa en la enfermedad de Alzheimer.
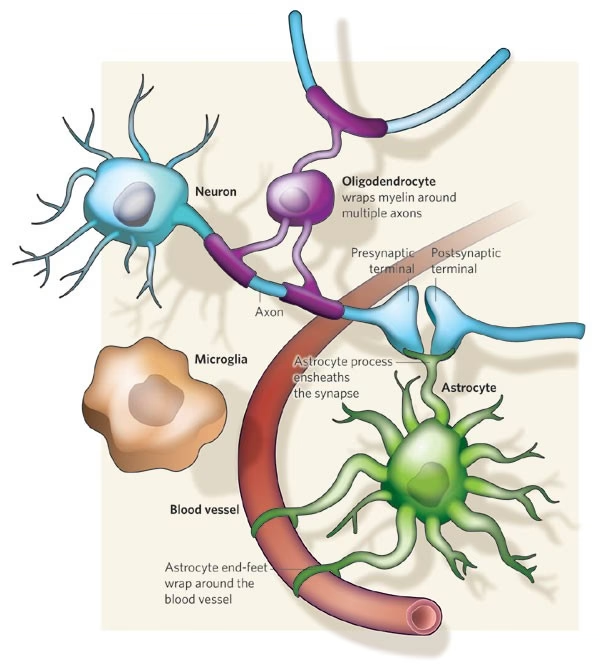
La microglía también puede remodelar localmente la matriz extracelular (ECM) a través de la liberación de metaloproteasas de matriz (MMPs), un proceso que podría estar coordinado con la eliminación de sinapsis.
La actividad neuronal regula la vigilancia y la fagocitosis microglial. Las uniones entre microglía y neuronas, optimizadas para la comunicación purinérgica (ATP/ADP), permiten a la microglía responder rápidamente a los cambios en la actividad neuronal. La microglía también puede eliminar sinapsis mediante mecanismos independientes del complemento, como la trogocitosis.
En conjunto, la glía (especialmente astrocitos y microglía) y la ECM interactúan de manera compleja para mediar la neuroplasticidad, regulando la actividad neuronal, la transmisión sináptica y el remodelado estructural.
La Matriz Extracelular (ECM) en la Plasticidad
La ECM, principalmente compuesta por polisacáridos y proteoglicanos, actúa como un andamio extracelular y crea un entorno regulado para la comunicación intercelular. Modula la plasticidad de varias maneras. En el cerebro maduro, componentes de la ECM como los condroitín sulfato glicosaminoglicanos (CSPGs) y las semaforinas restringen la formación de nuevas sinapsis, ayudando a estabilizar los circuitos establecidos. Las redes perineuronales, condensaciones de ECM, no solo amortiguan K+ sino que también compartimentalizan las superficies neuronales, creando dominios permisivos y restrictivos para la sinaptogénesis. La integridad de la ECM es crucial para mantener el control inhibitorio en las redes neuronales.
Si bien los astrocitos producen una gran parte de los componentes de la ECM, la microglía la remodela durante la neuroinflamación y la vigilancia fisiológica. La degradación local de la ECM por metaloproteasas liberadas por células gliales es probablemente un paso necesario para permitir el remodelado sináptico.
La capacidad de formar nuevas sinapsis, después de la eliminación, también depende de moléculas reguladoras producidas por los astrocitos, como la trombospondina 1 (TSP1) que induce sinapsis estructurales pero funcionalmente silenciosas, y los glicanos 4 y 6 (GPC4/6) y la hevina (SPARC like 1) que promueven sinapsis activas.
Tabla Comparativa de Células Gliales
| Tipo Celular | Ubicación Principal | Funciones Principales |
|---|---|---|
| Astrocitos | SNC (Cerebro, Médula Espinal) | Soporte metabólico, regulación iónica y de neurotransmisores, barrera hematoencefálica, limpieza de desechos, control flujo sanguíneo, plasticidad sináptica. |
| Oligodendrocitos | SNC | Formación de mielina alrededor de axones para acelerar la conducción nerviosa. |
| Microglía | SNC | Células inmunes residentes, fagocitosis (limpieza de desechos y patógenos), remodelado sináptico, respuesta a lesiones. |
| Células Ependimarias | SNC (Ventículos) | Revestimiento de ventrículos, producción y circulación de líquido cefalorraquídeo (LCR). |
| Células de Schwann | SNP (Nervios periféricos) | Formación de mielina alrededor de axones en el SNP. |
Preguntas Frecuentes sobre las Células Gliales
- ¿Qué son las células gliales?
Son un tipo de célula no neuronal en el sistema nervioso que proporciona soporte físico, metabólico e inmune a las neuronas. Son más numerosas que las neuronas. - ¿Cuál es la diferencia principal entre glía y neuronas?
Las neuronas se encargan de la señalización eléctrica y las interacciones sinápticas directas. Las células gliales, aunque esenciales para la función neuronal, no generan potenciales de acción ni participan directamente en la transmisión sináptica eléctrica, sino que modulan y apoyan estos procesos. - ¿Cuántos tipos de células gliales hay?
En el sistema nervioso central maduro, los tipos principales son astrocitos, oligodendrocitos y microglía. También están las células ependimarias. En el sistema nervioso periférico, las células de Schwann son el principal tipo glial responsable de la mielinización. - ¿Cuáles son las funciones más importantes de la glía?
Sus funciones abarcan desde mantener el entorno químico y iónico neuronal, formar la vaina de mielina, eliminar desechos y defender el cerebro (microglía), hasta regular el flujo sanguíneo, proporcionar soporte metabólico y participar activamente en la plasticidad y el remodelado de los circuitos neuronales. - ¿Las células gliales participan en la capacidad del cerebro para cambiar (neuroplasticidad)?
Sí, activamente. Los astrocitos influyen en la formación y estabilidad de las sinapsis, regulan neurotransmisores y proporcionan soporte metabólico. La microglía remodela los circuitos eliminando sinapsis. La matriz extracelular, producida en parte por glía, también modula la plasticidad.
En conclusión, las células gliales son componentes indispensables del sistema nervioso. Lejos de ser meros elementos de soporte pasivo, interactúan dinámicamente con las neuronas y la matriz extracelular, desempeñando roles cruciales en la homeostasis, la señalización y la plasticidad. Su estudio es fundamental para comprender tanto el funcionamiento normal del cerebro como los mecanismos subyacentes a diversas enfermedades neurológicas. La investigación continua revela la complejidad y la importancia de estas células, redefiniendo nuestra comprensión del tejido cerebral.
La intrincada red de comunicación y soporte entre neuronas y glía subraya la naturaleza altamente integrada y cooperativa del cerebro. Comprender cómo estas diferentes poblaciones celulares interactúan es clave para desentrañar los misterios de la cognición, el comportamiento y la salud neurológica. La glía, con su diversidad y múltiples funciones, emerge como un actor principal en la orquesta compleja que es el cerebro humano.
Si quieres conocer otros artículos parecidos a Las Células Gliales: Más que Simple "Pegamento" puedes visitar la categoría Neurociencia.
