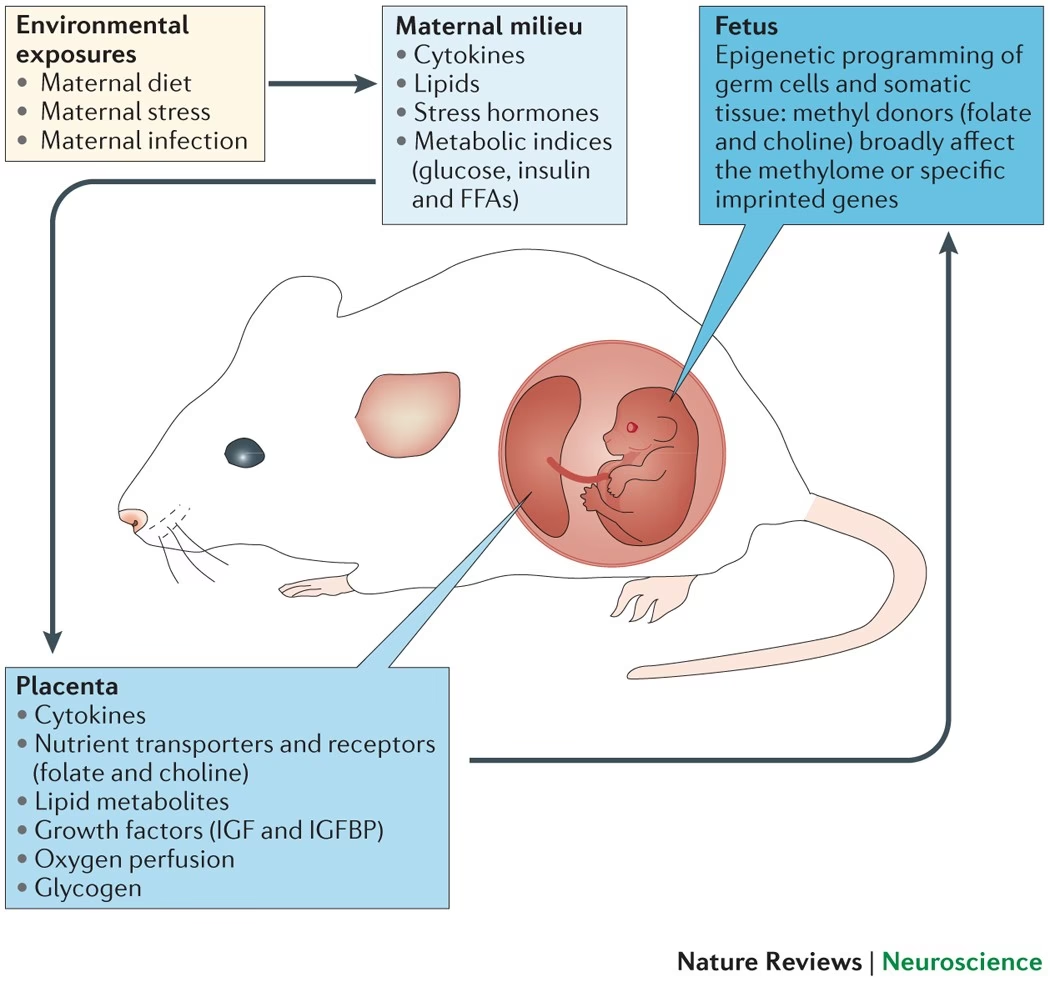
Cuando pensamos en la herencia y la información biológica, nuestra mente suele ir directamente al ADN, esa doble hélice que contiene el código fundamental de la vida. La genética clásica se centra en la secuencia de este código, su replicación fiel y las consecuencias de sus mutaciones. Sin embargo, existe una capa adicional de control, un fascinante campo conocido como epigenética, que va más allá de la secuencia de ADN para regular la expresión de los genes y, en última instancia, la actividad celular.
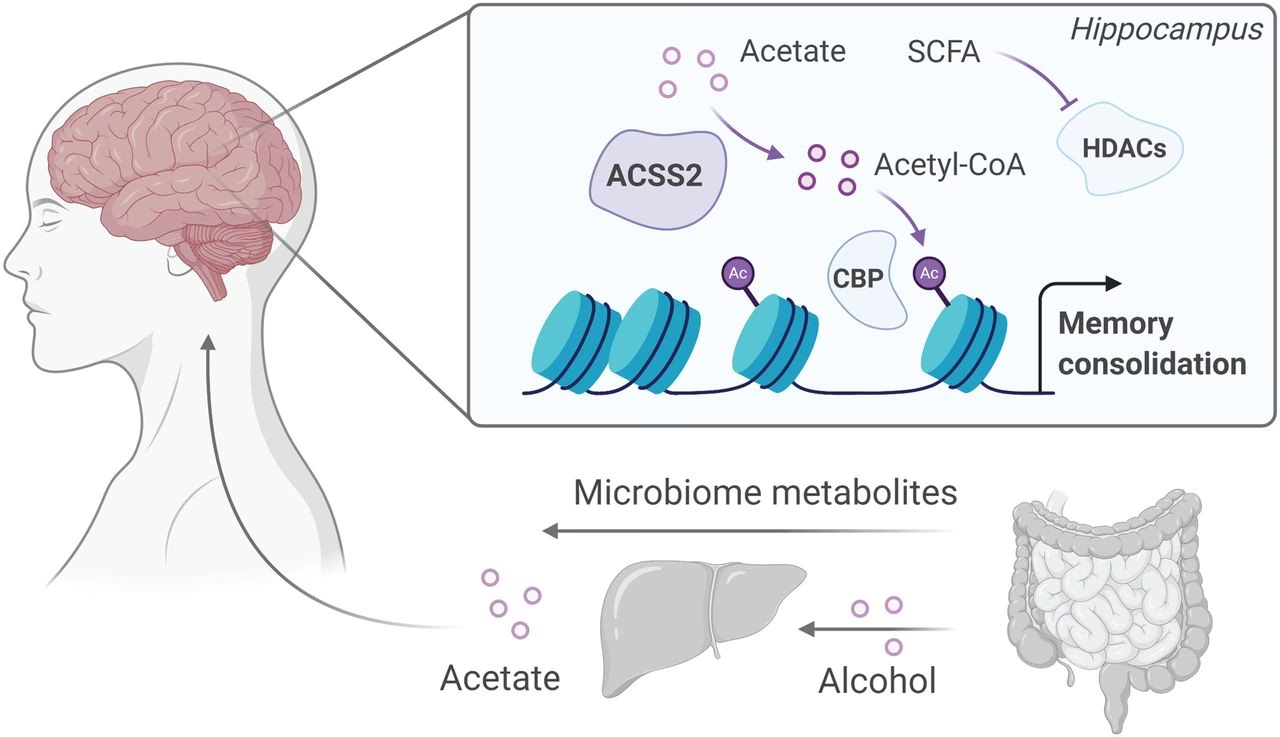
La epigenética se ocupa de los mecanismos regulatorios que, sin modificar la secuencia de ADN subyacente, determinan qué genes se activan (transcriben) y cuáles permanecen silenciados. Esencialmente, el epigenoma es una colección de compuestos químicos que se adhieren y se superponen a la secuencia de ADN, actuando como "instrucciones" adicionales que le dicen al ADN "qué hacer". Estas marcas epigenéticas no alteran la estructura primaria del ADN, pero sí influyen poderosamente en la producción de proteínas, las cuales guían el crecimiento y desarrollo de un organismo, dirigen y mantienen la identidad celular, y permiten la producción de células germinales primordiales (óvulos y espermatozoides).
El término epigenética se atribuye a Conrad Waddington (1942), quien lo describió como una "relación causal entre los genes y sus productos". Posteriormente, Nanney (1958) amplió el concepto para incluir un "conjunto" de mecanismos que dirigían la expresión génica y, de manera crucial, propuso que los patrones de marcas epigenéticas a lo largo del genoma se transmitían a través de las divisiones celulares a las células hijas, junto con la secuencia de ADN.
Con el tiempo, la comprensión de cómo los cambios epigenéticos podían ser heredables, tanto mitóticamente (transmitidos durante la replicación de células somáticas para mantener una línea celular diferenciada) como meióticamente (mantenidos durante la meiosis y capaces de pasar a la descendencia), evolucionó. Esto llevó a la definición contemporánea de epigenética como "mecanismos de herencia que no implican modificaciones de la secuencia de ADN y son reversibles por naturaleza". Comprender estos mecanismos es fundamental, ya que el cuerpo de investigación que asocia la epigenética con diversas enfermedades y funciones normales se expande rápidamente.
- ¿Cómo Regula la Epigenética la Expresión Génica? El Papel de la Cromatina
- Funciones Clave de la Regulación Epigenética Normal
- Los Tres Mecanismos Epigenéticos Principales
- Ejemplos de la Epigenética en Acción
- Tabla Comparativa: Genética vs. Epigenética
- Tabla Comparativa: Eucromatina vs. Heterocromatina
- Preguntas Frecuentes sobre Epigenética
¿Cómo Regula la Epigenética la Expresión Génica? El Papel de la Cromatina
Para entender los mecanismos epigenéticos, es esencial comprender primero el papel de la cromatina en la transcripción génica. Recordemos que el ARN transcribe el código del ADN en el núcleo celular a través del ARN mensajero (ARNm), que luego sale del núcleo para iniciar el proceso de traducción del código de ADN para producir proteínas. La estructura de doble hélice del ADN es demasiado grande para caber en el núcleo celular; por lo tanto, se compacta en una estructura llamada cromatina.
La cromatina, construida a partir de ADN y proteínas (principalmente histonas), es el andamiaje para todo el genoma, conteniendo el material heredable dentro de la célula eucariota. La cromatina existe en dos formas principales:
- Eucromatina: Menos compactada, lo que permite un acceso más fácil a las moléculas necesarias para la transcripción (como las ARN polimerasas). Piensa en ella como una biblioteca con los libros abiertos y accesibles.
- Heterocromatina: Fuertemente compactada y no se transcribe tan fácilmente. Sería como una sección de la biblioteca con los libros cerrados y guardados en cajas, difíciles de acceder.
Los mecanismos epigenéticos están asociados con cambios en la compactación de la cromatina que alteran su accesibilidad para la transcripción. Al modificar la estructura de la cromatina, la célula puede decidir qué genes están disponibles para ser leídos (expresados) y cuáles no.
Funciones Clave de la Regulación Epigenética Normal
En ausencia de enfermedad, los mecanismos regulatorios epigenéticos normales desempeñan varias funciones importantes:
- Dirección y Mantenimiento de la Identidad Celular: Primero, dirigen la diferenciación celular y mantienen una identidad celular específica durante las replicaciones posteriores. Esto asegura que todas las generaciones de células somáticas en una línea particular expresen los genes correctos asociados con la estructura y función de esa célula. Por ejemplo, las células hepáticas maduras continúan dando lugar a células hepáticas que funcionan normalmente, gracias a patrones epigenéticos específicos que se transmiten durante la división celular.
- Producción de Células Germinales Primordiales (CGPs): Segundo, durante la meiosis, la eliminación o modificación de marcas epigenéticas que dirigen la diferenciación celular madura ayuda en el proceso de producción de CGPs totipotentes. Esto implica la 'reprogramación' epigenética de células somáticas para crear óvulos y espermatozoides, células que tienen el potencial de dar origen a cualquier tipo de célula en un nuevo organismo.
Estas funciones destacan la naturaleza dinámica y esencial de la epigenética para el desarrollo y mantenimiento de la vida.
Los Tres Mecanismos Epigenéticos Principales
Los mecanismos subyacentes a estos cambios epigenéticos en el genoma son diversos y complejos, pero se agrupan principalmente en tres áreas principales:
- Modificación de Histonas: Las histonas son las proteínas alrededor de las cuales se enrolla el ADN para formar la cromatina. Las histonas pueden ser modificadas químicamente (por ejemplo, añadiendo grupos acetilo, metilo, fosfato, etc.). Estas modificaciones alteran cómo el ADN se empaqueta alrededor de las histonas, afectando la estructura de la cromatina y, por lo tanto, la accesibilidad del ADN para la transcripción. Las modificaciones en las histonas pueden hacer que la cromatina se afloje (favoreciendo la expresión génica) o se compacte (silenciando los genes).
- Metilación del ADN: Este es quizás el mecanismo epigenético más estudiado. Implica la adición de un grupo metilo a bases de citosina específicas en el ADN, generalmente en regiones donde una citosina está seguida por una guanina (llamadas dinucleótidos CpG). La metilación del ADN en la región promotora de un gen (la secuencia que controla su inicio de transcripción) suele reprimir la expresión génica, ya sea bloqueando directamente la unión de factores de transcripción o reclutando proteínas que promueven una estructura de cromatina compactada.
- ARN No Codificante (ARNnc): Contrariamente a la creencia anterior de que gran parte del genoma era "ADN basura", ahora sabemos que una porción significativa se transcribe en moléculas de ARN que no codifican para proteínas. Estos ARN no codificantes, incluyendo microARN (miARN) y ARN largos no codificantes (ARNlnc), desempeñan roles regulatorios cruciales. Pueden interactuar con el ADN, el ARNm o proteínas (incluyendo las histonas) para influir en la expresión génica. Algunos ARNnc pueden reclutar complejos proteicos que modifican las histonas o metilan el ADN, afectando así la estructura de la cromatina y la transcripción.
Cada uno de estos mecanismos trabaja de manera diferente, a menudo en concierto, para regular la expresión génica, influyendo en el estado de la cromatina y la accesibilidad del ADN.
Ejemplos de la Epigenética en Acción
La epigenética es fundamental en numerosos procesos biológicos. Un ejemplo clásico es la inactivación del cromosoma X en las hembras de mamíferos. Para equilibrar la dosis génica entre sexos (las hembras tienen dos cromosomas X, los machos uno), uno de los cromosomas X en cada célula femenina se inactiva aleatoriamente a través de extensas modificaciones epigenéticas, incluyendo metilación del ADN y modificaciones de histonas que llevan a la formación de heterocromatina.
Otro ejemplo importante se encuentra en los trastornos de impronta genómica, como los síndromes de Angelman y Prader-Willi. La impronta es un proceso epigenético por el cual ciertos genes se expresan solo si se heredan de la madre o del padre, pero no de ambos. Una alteración en la marca epigenética de estos genes (a menudo metilación del ADN) puede llevar a la expresión incorrecta del gen y causar la enfermedad, incluso si la secuencia de ADN subyacente es normal.
Tabla Comparativa: Genética vs. Epigenética
| Aspecto | Genética | Epigenética |
|---|---|---|
| Objeto de estudio principal | Secuencia del ADN | Modificaciones en el ADN y proteínas asociadas (histonas) que regulan la expresión génica |
| Cambio en el ADN | Alteraciones en la secuencia (mutaciones) | No altera la secuencia del ADN |
| Impacto | Define el potencial genético | Controla cuándo y cómo se expresa el potencial genético |
| Reversibilidad | Generalmente no reversible (salvo mutaciones puntuales) | Potencialmente reversible |
| Herencia | Heredada a través de la secuencia de ADN | Puede ser heredada (mitótica y meióticamente) a través de patrones de marcas |
Tabla Comparativa: Eucromatina vs. Heterocromatina
| Característica | Eucromatina | Heterocromatina |
|---|---|---|
| Compactación | Menos compactada | Fuertemente compactada |
| Accesibilidad para transcripción | Alta (permite la expresión génica) | Baja (generalmente reprime la expresión génica) |
| Ubicación típica | Regiones ricas en genes activos | Regiones con genes silenciados, telómeros, centrómeros |
| Apariencia microscópica | Menos densa | Más densa |
Preguntas Frecuentes sobre Epigenética
- ¿La epigenética cambia la secuencia de mi ADN?
- No, la epigenética no altera la secuencia de bases (A, T, C, G) de tu ADN. Lo que cambia son las marcas químicas sobre el ADN o las proteínas asociadas que regulan cómo se lee esa secuencia.
- ¿Pueden los cambios epigenéticos ser heredados?
- Sí, los patrones de marcas epigenéticas pueden transmitirse durante la división celular a las células hijas (herencia mitótica) para mantener la identidad celular. En algunos casos, también pueden transmitirse a través de las células germinales a la siguiente generación (herencia meiótica), aunque este es un campo de investigación activo.
- ¿Es la epigenética reversible?
- A diferencia de las mutaciones genéticas, las marcas epigenéticas son dinámicas y potencialmente reversibles. Esto significa que los patrones epigenéticos pueden cambiar a lo largo de la vida en respuesta a factores internos y externos.
- ¿Cuál es la relación entre la cromatina y la epigenética?
- La cromatina, compuesta por ADN y proteínas (histonas), es la estructura física que empaqueta el ADN en el núcleo. Los mecanismos epigenéticos actúan modificando la cromatina (por ejemplo, alterando las histonas o metilando el ADN) para controlar qué partes del ADN son accesibles para la maquinaria de transcripción, regulando así la expresión génica.
- ¿Cuáles son los tres mecanismos epigenéticos principales?
- Los tres mecanismos principales son la modificación de histonas, la metilación del ADN y la regulación por ARN no codificante. Estos mecanismos trabajan juntos para influir en la estructura de la cromatina y la expresión génica.
En conclusión, la regulación epigenética dirige la expresión de los genes para desarrollar y mantener la identidad celular y para producir CGPs totipotentes a partir de células somáticas maduras durante la meiosis. Mecanismos que incluyen la modificación de histonas, la metilación del ADN, el ARN no codificante y el grado de compactación de la cromatina afectan la accesibilidad de la secuencia de ADN para los propósitos de la expresión génica. Las modificaciones epigenéticas no cambian la estructura del ADN, pero sí cambian su función y son parte integral de la diversidad dentro de las poblaciones y la plasticidad biológica.
Este artículo ha tenido la intención de proporcionar una visión general básica de estos procesos. El conocimiento sobre la epigenética continúa acumulándose rápidamente en la literatura y las áreas clínicas, especialmente en lo que respecta al impacto de las exposiciones ambientales y otros factores relacionados con enfermedades en las alteraciones del epigenoma y los resultados de salud resultantes. Un conocimiento práctico de los mecanismos epigenéticos normales equipará a los profesionales para leer y sintetizar el creciente cuerpo de literatura que describe síntomas y enfermedades con un componente epigenético.
Si quieres conocer otros artículos parecidos a Descubriendo la Epigenética: Más Allá del ADN puedes visitar la categoría Neurociencia.