Nuestro cuerpo realiza una variedad sorprendente de movimientos rítmicos de forma automática: caminar, respirar, tragar. Aunque a menudo pensamos que estos actos requieren un control constante del cerebro superior, gran parte de esta coordinación se orquesta a un nivel más fundamental, gracias a unas estructuras neuronales especializadas conocidas como Generadores de Patrones Centrales, o CPGs por sus siglas en inglés (Central Pattern Generators).

Un CPG es un conjunto de neuronas capaz de producir una salida motora rítmica y coordinada en ausencia de cualquier estímulo externo rítmico. Esto significa que la capacidad de generar el patrón rítmico reside intrínsecamente dentro de la propia red neuronal. La salida de un CPG se caracteriza por un patrón de activación altamente coordinado de diferentes grupos de motoneuronas, lo que permite la ejecución fluida de movimientos complejos.
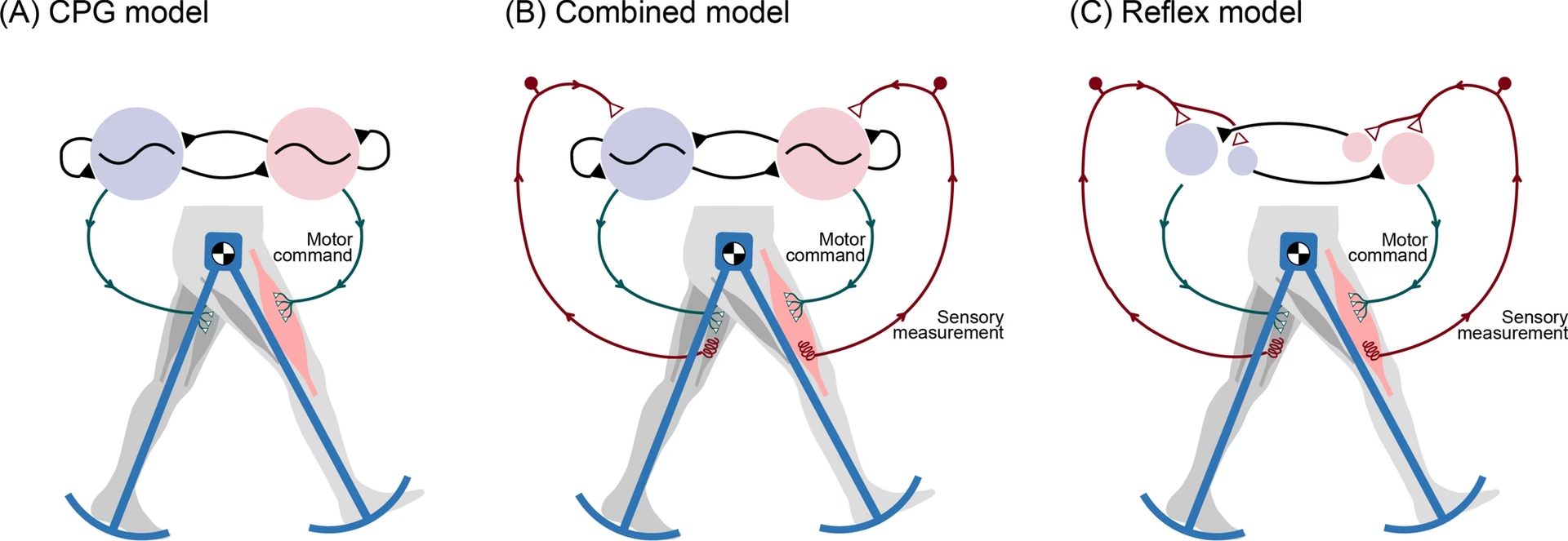
CPGs en la Locomoción: El Origen Espinal del Paso
Décadas de investigación, principalmente en preparaciones animales, han permitido comprender la organización funcional de la red espinal involucrada en la locomoción, identificándola como un CPG locomotor. Este CPG puede generar patrones de activación para caminar incluso cuando está aislado de la entrada rítmica del cerebro o de la periferia.
Una característica impresionante de los CPGs, especialmente en condiciones in vivo, es su habilidad para procesar complejas combinaciones de información sensorial, como la propriocepción (información sobre la posición y movimiento del cuerpo) y el tacto, en tiempo real. Esta capacidad permite que el patrón rítmico se adapte a las condiciones cambiantes del entorno o del cuerpo.
Desarrollo y Conectividad
Se sugiere que el CPG locomotor se desarrolla, al menos parcialmente, siguiendo una estrategia determinista. Un número definido de interneuronas, genéticamente predeterminadas, establecen conexiones específicas dentro de la red desde las etapas embrionarias. Aunque esta compleja y específica conectividad entre los elementos de la red aún no se ha dilucidado por completo, es claro que contribuye a su funcionalidad.
Activación del CPG Locomotor
Incluso cuando la fuente rítmica del patrón está aislada in vitro, y por lo tanto privada de sus entradas descendentes (del cerebro) y aferentes (sensoriales), el patrón rítmico aún puede ser activado por una amplia gama de estímulos. Estos incluyen:
- Estimulación eléctrica.
- Agentes farmacológicos específicos.
- Un aumento en el K+ extracelular, que eleva la excitabilidad general de la red neuronal.
Estos hallazgos refuerzan la idea de que la capacidad rítmica es una propiedad inherente de la red del CPG.
Automaticidad y el Tronco Encefálico
Además del CPG espinal, se ha demostrado otra fuente de automaticidad. La estimulación tónica (constante, no rítmica) en sitios específicos dentro del mesencéfalo (parte del tronco encefálico) puede inducir una marcha cuadrúpeda altamente coordinada en gatos. Esta estimulación no solo puede iniciar el movimiento, sino también facilitar la adaptación a diferentes velocidades en una cinta de correr. Experimentos con gatos despiertos y con electrodos crónicamente implantados mostraron que la estimulación en un punto podía iniciar la marcha, mientras que la estimulación a pocos milímetros de distancia podía detenerla, demostrando que incluso un estímulo tónico simple puede activar patrones motores complejos de postura y locomoción.
Estos resultados sugieren que un alto nivel de automaticidad está integrado dentro de los circuitos locomotores. La combinación de la capacidad de la médula espinal para generar y controlar el rendimiento postural y locomotor, junto con la entrada proprioceptiva y cutánea, indica que un componente neural importante de la automaticidad reside en la médula espinal, que procesa la compleja entrada sensorial y ejecuta los controles de salida motora en tiempo real.
Se ha observado en animales con lesiones medulares parciales que la combinación de entradas proprioceptivas y cutáneas derivadas de las extremidades puede ser la única fuente de control necesaria para coordinar todos los grupos musculares involucrados en movimientos muy complejos, como variar la velocidad y el soporte de peso al caminar en una cinta.
El Sistema Proprioespinal (PSS): Interfaz y Coordinación
El sistema proprioespinal (PSS) es una red de interconexión de neuronas y axones proprioespinales que se extiende a lo largo de toda la médula espinal. Funciona como una interfaz crucial entre las redes neuronales corticales, subcorticales y espinales.
Estructura y Conectividad del PSS
Las neuronas proprioespinales son numéricamente predominantes en la médula espinal y presentan una morfología muy heterogénea. Durante el desarrollo, la formación de sus conexiones parece tener un componente estocástico (aleatorio), facilitado por el simple solapamiento anatómico de axones y dendritas, lo que minimiza la necesidad de señales de guía específicas.
El PSS interconecta múltiples segmentos espinales a lo largo de la médula, desde el cuello hasta la región lumbar, y proporciona proyecciones bilaterales. Funcionalmente, a nivel lumbar, esta red difusa y altamente recurrente interactúa con las neuronas del CPG locomotor.
Actividad y Función del PSS
La actividad del PSS se ha comparado con la de las redes corticales, mostrando un balance entre excitación e inhibición. Su actividad espontánea puede manifestarse como ráfagas irregulares y aisladas que se propagan sin necesidad de un cableado específico, sincronizando conjuntos neuronales dispersos. Esta propagación se ha descrito como una avalancha neuronal.
Experimentalmente, la actividad del PSS se puede registrar en la médula espinal dorsal en forma de ondas eléctricas viajeras. Estas ondas se registran incluso en reposo, sugiriendo que la red proprioespinal produce continuamente un patrón de fondo estable que reverbera la excitación a lo largo de la médula espinal. Esta actividad de fondo representa una fuente continua de entrada facilitadora subumbral que actúa sobre los CPGs espinales.
Esta entrada facilitadora mantiene la excitabilidad del CPG cerca del umbral de activación, haciéndolo más receptivo a las entradas voluntarias para el control locomotor (del cerebro) y a las entradas sensoriales (aferentes), especialmente las proprioceptivas. Esto es crucial para la modulación y el control fino del movimiento.
Funcionalmente, el PSS proporciona un mecanismo para el acoplamiento intersegmental y la coordinación de los grupos musculares dentro y entre múltiples segmentos espinales. En humanos, contribuye a la coordinación rítmica de las extremidades superiores e inferiores durante la locomoción y media algunas respuestas neurológicas entre extremidades.
Además del control directo cortico-motoneuronal, una vía descendente indirecta establece relevos sinápticos dentro del PSS. Cuando se selecciona un movimiento voluntario, estos relevos en el PSS pueden amplificar y prolongar el comando descendente a lo largo de los segmentos lumbosacros de la médula espinal, facilitando la ejecución del movimiento.
PSS y Lesiones Medulares
El PSS presenta un nivel significativo de redundancia y plasticidad. Por esta razón, se ha asociado con la recuperación funcional después de lesiones experimentales graves de la médula espinal, así como con una conectividad intersegmental aberrante a nivel de la lesión. En sujetos con lesiones cervicales crónicas, el PSS podría desempeñar un papel en los reflejos de las extremidades superiores tras la estimulación de nervios en las extremidades inferiores. También genera el mioclono proprioespinal, que son sacudidas musculares espontáneas que se propagan.
Tras una lesión medular, las vías cortico-espinales descendentes pueden quedar comprometidas, reduciendo la capacidad de activar patrones motores voluntarios. Esta desconexión también perturba la influencia descendente sobre el PSS. La arreflexia y la hipotonía muscular características de la fase de shock espinal tras una lesión aguda podrían deberse, en parte, a la pérdida súbita de esta entrada descendente que fisiológicamente modula el PSS. Para compensar esta pérdida, el PSS experimenta reorganizaciones plásticas que pueden alterar aún más su excitabilidad.
Fenómenos como la regresión dendrítica o la reducción en la expresión de genes relacionados con la plasticidad sináptica también pueden afectar al PSS después de una lesión, disminuyendo la eficacia sináptica. Esto puede reducir la ritmicidad basal del PSS y, en consecuencia, la excitabilidad de los CPGs, limitando la posibilidad de que las conexiones descendentes residuales faciliten patrones locomotores.
No obstante, el PSS sobrevive anatómicamente y funcionalmente incluso después de una transección completa de la médula espinal. Por lo tanto, puede soportar la recuperación funcional después de una lesión grave si la excitabilidad de las neuronas proprioespinales se modula hacia valores fisiológicos, permitiendo la explotación de la automaticidad y plasticidad de estas redes.
CPGs en la Deglución: El Programa para Tragar
La deglución (tragar) es otro ejemplo de un movimiento rítmico y secuencial controlado por un CPG. Este CPG se localiza en el tronco encefálico. La deglución puede ser inducida por estimulación mecánica de la faringe o estimulación eléctrica del nervio laríngeo superior, incluso en animales descerebrados, lo que demuestra que el programa generador reside en el tronco encefálico.
Los eventos de la deglución implican contracciones secuenciales en la faringe y el esófago, junto con la relajación coordinada de los esfínteres, de manera similar a una deglución espontánea. Este conjunto programado de impulsos emana del tronco encefálico, a menudo referido como el CPG de la deglución o generador del programa de deglución (SPG).
Núcleos Clave y Neurotransmisores
Los elementos críticos de este CPG incluyen el núcleo del tracto solitario (NTS), la formación reticular adyacente, el núcleo ambiguo y el núcleo dorsomotor del vago. Estos núcleos no están muy bien delimitados y sus neuronas también participan en otras funciones vitales como la respiración y los reflejos cardiovasculares.
Existe una representación topográfica de la entrada sensorial en el NTS, donde las fibras faríngeas y laríngeas se proyectan a subnúcleos específicos, mientras que las aferentes esofágicas se dirigen a otros. El NTS no es una simple estación de relevo; se puede registrar actividad secuencial en sus neuronas tras la estimulación del nervio laríngeo superior.
La microinyección de agonistas de aminoácidos excitatorios (EAA) en el NTS induce eventos motores peristálticos en la faringe y el esófago, que pueden ser bloqueados por antagonistas de EAA. Agonistas y antagonistas de receptores NMDA pueden inducir contracciones rítmicas "similares a la deglución". La modulación con agonistas y antagonistas de GABA-A sugiere que el NTS también ejerce un control inhibitorio tónico sobre las neuronas premotoras.
El reflejo de la deglución es probablemente un reflejo polisimpático a nivel del tronco encefálico, con la participación de varios neurotransmisores en las sinapsis, incluyendo acetilcolina, epinefrina, monoaminas, serotonina, vasopresina, oxitocina, somatostatina, tirotropina y óxido nítrico, entre otros.
CPGs en la Respiración: El Ritmo Vital
La respiración es otro proceso rítmico esencial controlado por un CPG localizado en el tronco encefálico. Este CPG genera el impulso sináptico rítmico para las motoneuronas que controlan los músculos respiratorios.
Ciclo Respiratorio y Tipos Neuronales
El ciclo respiratorio se divide en tres fases principales, basadas en la actividad de los nervios respiratorios:
- Inspiración
- Post-inspiración
- Expiración (fase 2)
Seis tipos básicos de neuronas respiratorias participan en la generación del ritmo respiratorio. Sus patrones de descarga y potencial de membrana están sincronizados con las diferentes fases del ciclo.
Mecanismos de Generación del Ritmo
Las neuronas respiratorias están sujetas a entradas sinápticas excitatorias e inhibitorias y muestran extensas interconexiones, predominantemente inhibitorias en mamíferos adultos.
Existen diferencias en la importancia relativa de los impulsos sinápticos excitatorios e inhibitorios y los neurotransmisores involucrados en la ritmogénesis respiratoria entre neonatos y adultos.
Además de las conexiones sinápticas, las neuronas respiratorias poseen varias corrientes de membrana intrínsecas que podrían participar en la generación del patrón central. Estas incluyen corrientes de calcio, potasio (incluyendo las dependientes de calcio), sodio y corrientes catiónicas mixtas. Se necesita más información cuantitativa sobre la distribución y características de estas corrientes iónicas para comprender completamente la ritmogénesis.
Existen dos teorías principales sobre el origen del ritmo respiratorio: la teoría impulsada por neuronas marcapasos y la teoría impulsada por redes sinápticas. La evidencia experimental apoya ambas teorías, y es posible que el mecanismo subyacente cambie significativamente durante el desarrollo posnatal.
Preguntas Frecuentes sobre los CPGs
- ¿Qué diferencia a un CPG de otros circuitos neuronales?
- La característica definitoria de un CPG es su capacidad para generar un patrón motor rítmico coordinado sin necesidad de una entrada rítmica externa. La fuente del ritmo reside en la propia red neuronal.
- ¿Dónde se encuentran los CPGs?
- Los ejemplos más estudiados se encuentran en la médula espinal (para la locomoción) y en el tronco encefálico (para la deglución y la respiración).
- ¿Pueden los CPGs funcionar sin el cerebro?
- Sí, en preparaciones experimentales, los CPGs espinales y del tronco encefálico pueden generar su patrón rítmico incluso cuando están aislados de las partes superiores del cerebro, aunque la modulación y el control fino en condiciones normales provienen del cerebro y la información sensorial.
- ¿Qué es el Sistema Proprioespinal (PSS)?
- Es una red de interneuronas en la médula espinal que actúa como interfaz entre el cerebro y los circuitos espinales, incluyendo los CPGs. Ayuda a coordinar múltiples segmentos espinales y transmite información descendente.
- ¿Por qué son importantes los CPGs en la recuperación de lesiones?
- Debido a su automaticidad y plasticidad, los CPGs y redes asociadas como el PSS pueden ser cruciales para restaurar alguna función motora rítmica incluso después de lesiones medulares graves, sirviendo como base para terapias de rehabilitación.
En resumen, los Generadores de Patrones Centrales son arquitecturas neurales fundamentales que subyacen a muchos de nuestros movimientos rítmicos automáticos. Desde el simple acto de respirar o tragar hasta la compleja coordinación de la marcha, estas redes demuestran una notable capacidad intrínseca para generar patrones, procesar información sensorial y adaptarse, destacando la sofisticada organización de nuestro sistema nervioso.
Si quieres conocer otros artículos parecidos a Los CPGs: Ritmo Oculto del Movimiento puedes visitar la categoría Neurociencia.
