La cocaína es una sustancia con una doble naturaleza: por un lado, es una droga ilegal de alto potencial adictivo y peligrosidad; por otro, tiene un uso médico muy limitado y estrictamente controlado. Para comprender su impacto, es fundamental adentrarse en su complejo mecanismo de acción dentro del cerebro.

Aunque su uso médico está restringido a la anestesia tópica de ciertas membranas mucosas (oral, laríngea, nasal) y como vasoconstrictor para tratar sangrados nasales (epistaxis), su notoriedad proviene de su potente efecto como estimulante del sistema nervioso central y su capacidad para generar euforia, aumento de energía y sensaciones de competencia y sexualidad. Estos efectos, que duran entre 15 minutos y una hora dependiendo de la dosis y la vía de administración (esnifada, inyectada o fumada como “crack”), están intrínsecamente ligados a su interacción con la compleja maquinaria química del cerebro.

- El Mecanismo Principal: Bloqueo de la Recaptación
- Los Receptores Sigma: Un Blanco Directo y Complejo
- Modulación de Señalización Vía Receptores Sigma
- Efectos Agudos vs. Crónicos: Un Cambio de Rol para los Sigma
- Otros Mecanismos y Efectos Sistémicos
- Toxicidad y sus Manifestaciones
- Manejo de la Toxicidad por Cocaína
- Preguntas Frecuentes sobre la Cocaína y el Cerebro
- Comparativa de Efectos de la Cocaína Vía Receptores Sigma en Exposición Aguda vs Crónica
El Mecanismo Principal: Bloqueo de la Recaptación
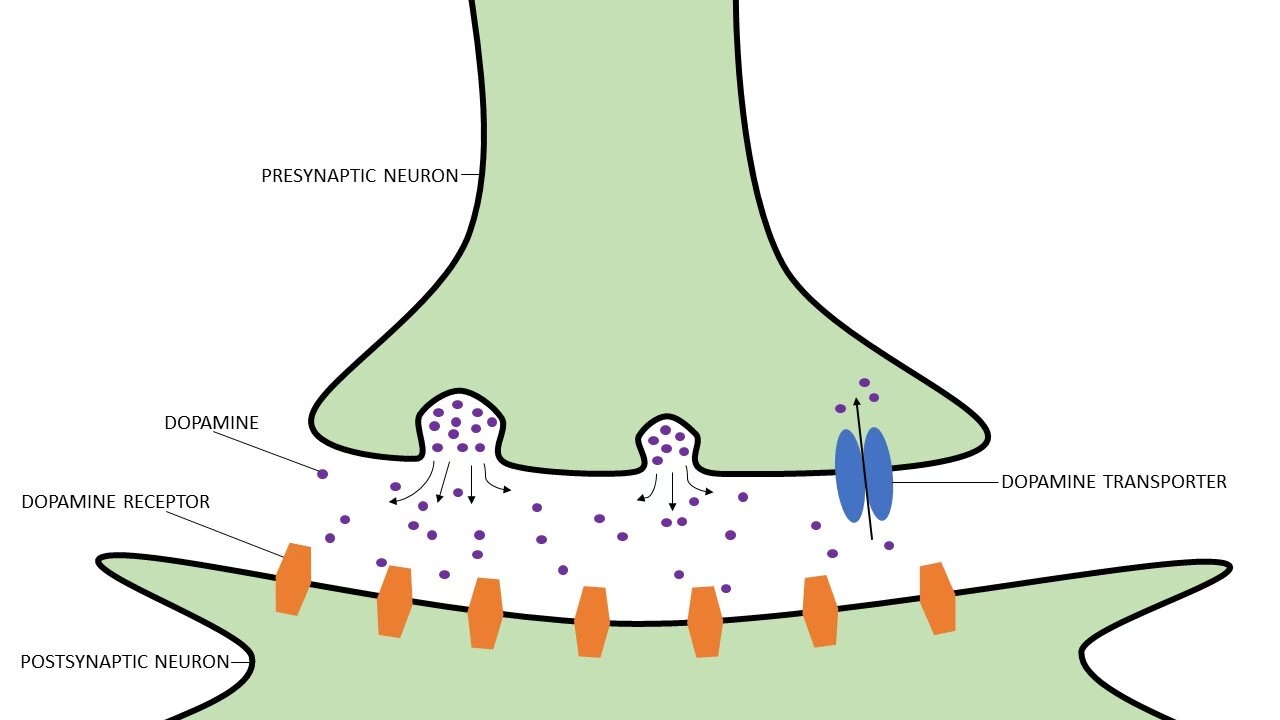
El mecanismo de acción principal y más conocido de la cocaína en el cerebro implica su interacción con los transportadores de monoaminas. En las sinapsis, los neurotransmisores como la dopamina, la norepinefrina, la epinefrina y la serotonina son liberados por una neurona y actúan sobre la siguiente. Después de cumplir su función, estos neurotransmisores son normalmente recaptados por la neurona que los liberó, gracias a proteínas transportadoras específicas en la membrana presináptica. Este proceso de recaptación es crucial para finalizar la señal y mantener el equilibrio en la comunicación neuronal.
La cocaína actúa bloqueando estos transportadores de recaptación. Lo hace con afinidad similar por los transportadores de dopamina (DAT), norepinefrina (NET) y serotonina (SERT). Al impedir que estos neurotransmisores sean retirados de la hendidura sináptica, la cocaína provoca un aumento significativo y prolongado de sus concentraciones extracelulares. Este exceso de monoaminas intensifica la señalización a través de sus receptores postsinápticos.
El efecto más relevante para las propiedades euforizantes y adictivas de la cocaína es el aumento de la dopamina en áreas cerebrales asociadas con el control motor y, crucialmente, con el sistema de recompensa, como el área tegmental ventral (ATV) y los ganglios basales (incluyendo el núcleo accumbens). La activación excesiva de este sistema de recompensa es lo que subyace a la sensación de placer y al fuerte impulso a repetir el consumo, sentando las bases de la adicción.
Los Receptores Sigma: Un Blanco Directo y Complejo
Aunque el bloqueo de la recaptación de monoaminas se consideró durante mucho tiempo el único mecanismo relevante, la investigación más reciente ha proporcionado una fuerte evidencia de que la cocaína ejerce efectos adicionales mediante una interacción directa con los receptores sigma. Existen dos tipos principales, σ1R y σ2R, que, a pesar de su nombre similar, son estructural y funcionalmente distintos. Curiosamente, ambos tienen la capacidad de unirse a la cocaína.
La interacción de la cocaína con los receptores sigma modula la transmisión dopaminérgica de formas complejas. Se ha demostrado que el receptor sigma-1 (σ1R) interactúa con los receptores de dopamina D1 y D2. La unión de la cocaína a σ1R influye en la señalización mediada por estos receptores dopaminérgicos.
Más novedoso es el hallazgo de que el receptor sigma-2 (σ2R) también puede formar complejos con el receptor de dopamina D1 (D1R), aunque no parece interactuar de forma significativa con el receptor D2 (D2R). Lo que complica aún más el panorama es la posibilidad de que D1R, σ1R y σ2R formen complejos heterotriméricos, es decir, estructuras compuestas por las tres proteínas. Dentro de estos trimeros, σ1R parece ser capaz de desplazar a σ2R de su interacción con D1R.
Modulación de Señalización Vía Receptores Sigma
La unión de la cocaína a los receptores sigma modula las vías de señalización intracelular iniciadas por los receptores de dopamina D1 de maneras opuestas, dependiendo de si la interacción es vía σ1R o σ2R:
- Vía σ1R: La cocaína, al unirse a σ1R, parece potenciar la acumulación de AMP cíclico (cAMP) mediada por D1R. Sin embargo, inhibe la señalización de la vía de las MAP quinasas (como ERK1/2).
- Vía σ2R: La cocaína, al unirse a σ2R, bloquea la acumulación de cAMP mediada por D1R. En contraste, potencia la activación de la vía de las MAP quinasas.
Cuando ambos receptores sigma están presentes, el efecto neto de la cocaína sobre la señalización D1R parece ser un equilibrio entre estas modulaciones opuestas, dependiendo de la expresión relativa de σ1R y σ2R y de la formación de los distintos complejos.
Efectos Agudos vs. Crónicos: Un Cambio de Rol para los Sigma
La investigación sugiere que el papel de los receptores sigma en los efectos de la cocaína varía con el tiempo de exposición a la droga. En la exposición aguda a la cocaína, la formación de complejos D1R-σ1R aumenta significativamente. Esto lleva a que la modulación de la señalización D1R esté dominada por σ1R, resultando en una potenciación de las señales de cAMP.
Sin embargo, en condiciones de consumo crónico, la expresión de complejos D1R-σ1R vuelve a niveles basales, pero la expresión de complejos D1R-σ2R aumenta de forma significativa. En esta fase crónica, σ2R se convierte en el actor principal en la modulación de D1R. La potenciación de la vía de las MAP quinasas mediada por el complejo D1R-σ2R en la exposición crónica podría ser un mecanismo clave subyacente a los cambios de plasticidad neuronal a largo plazo que contribuyen al establecimiento de la adicción.
Este cambio en el predominio de σ1R a σ2R en la modulación de D1R entre la exposición aguda y crónica es crucial para entender cómo los efectos de la cocaína evolucionan y cómo la droga induce cambios duraderos en el cerebro que perpetúan la búsqueda y el consumo.
Otros Mecanismos y Efectos Sistémicos
Además de su impacto en las monoaminas y los receptores sigma, la cocaína también puede interactuar con otros receptores, incluyendo receptores muscarínicos de acetilcolina, receptores NMDA y receptores kappa-opioides, aunque el significado funcional completo de estas interacciones sigue siendo objeto de investigación.
A nivel sistémico, la absorción de la cocaína (incluso desde las mucosas en su uso médico) puede tener efectos cardiovasculares significativos debido a la intensificación de la actividad simpática. Esto incluye aumento de la frecuencia cardíaca, la presión arterial y la contractilidad miocárdica, lo que incrementa la demanda de oxígeno del corazón. La cocaína es también un potente vasoconstrictor, y esta constricción puede afectar especialmente a las arterias coronarias, reduciendo el suministro de oxígeno al miocardio. Además, la cocaína puede inducir la activación plaquetaria y la formación de trombos, aumentando el riesgo de eventos cardiovasculares como infartos de miocardio y accidentes cerebrovasculares.

Toxicidad y sus Manifestaciones
La toxicidad de la cocaína puede manifestarse de diversas formas, afectando principalmente al sistema nervioso central y al sistema cardiovascular. Las reacciones del SNC pueden ser bifásicas: inicialmente excitatorias (ansiedad, inquietud, excitación, hiperreflexia, dolor de cabeza, midriasis) y, en casos severos, pueden llevar a convulsiones tónico-clónicas generalizadas. Estas convulsiones a menudo son seguidas por depresión del SNC, que puede ser mortal debido a insuficiencia respiratoria o asfixia si hay vómito concomitante.
Los efectos cardiovasculares de la toxicidad incluyen taquicardia, hipertensión y vasoconstricción arterial que puede desencadenar infarto de miocardio o accidente cerebrovascular. Como potente vasoconstrictor, la cocaína también puede dificultar la disipación del calor, llevando a hipertermia. El contacto accidental con los ojos puede causar daño corneal.
Manejo de la Toxicidad por Cocaína
El tratamiento de la toxicidad aguda por cocaína se basa principalmente en medidas de soporte y el manejo de los síntomas. El uso de benzodiacepinas es la primera línea de tratamiento para la agitación y la toxicidad cardiovascular, ya que disminuyen la actividad simpática del SNC. Para la hipertensión, pueden usarse bloqueadores de canales de calcio no dihidropiridínicos (como diltiazem o verapamilo) o vasodilatadores como nitroglicerina o nitroprusiato, aunque estos últimos conllevan riesgo de taquicardia refleja. El labetalol, un bloqueador mixto beta/alfa, se considera seguro y efectivo para tratar la hipertensión y taquicardia concomitantes.
Para la agitación severa, además de las benzodiacepinas, pueden ser útiles antipsicóticos como haloperidol u olanzapina, a menudo en combinación. Las arritmias ventriculares graves pueden tratarse con lidocaína o emulsión lipídica intravenosa en algunos casos. La hipertermia requiere medidas de enfriamiento externo.
Existe controversia sobre el uso de betabloqueantes puros debido al riesgo teórico de “estimulación alfa no opuesta”, donde el bloqueo de los receptores beta-2 que causan vasodilatación podría empeorar la vasoconstricción mediada por receptores alfa. Sin embargo, evidencia reciente sugiere que este fenómeno es raro y muchos clínicos administran betabloqueantes (especialmente labetalol) cuando la taquicardia incontrolada contribuye a la isquemia miocárdica.
Preguntas Frecuentes sobre la Cocaína y el Cerebro
Aquí respondemos algunas preguntas comunes basadas en la información proporcionada:
¿Cuál es el neurotransmisor más fuertemente ligado a los efectos de la cocaína?
Aunque la cocaína bloquea la recaptación de varios neurotransmisores monoaminérgicos (dopamina, norepinefrina, serotonina), la dopamina es el neurotransmisor más fuertemente ligado a sus efectos de recompensa, euforia y adicción en áreas clave del cerebro como el sistema de recompensa y los ganglios basales.

¿Qué le hace la cocaína a las sinapsis?
La cocaína bloquea las proteínas transportadoras que normalmente eliminan los neurotransmisores monoaminérgicos (como dopamina, norepinefrina y serotonina) de la hendidura sináptica. Esto provoca que estos neurotransmisores se acumulen en el espacio sináptico, intensificando y prolongando su señalización a las neuronas postsinápticas.
¿Tiene la cocaína algún uso médico legítimo?
Sí, la solución tópica de clorhidrato de cocaína al 4% está permitida para la anestesia local de las membranas mucosas de las cavidades oral, laríngea y nasal. También se utiliza por sus propiedades vasoconstrictoras para ayudar a controlar el sangrado nasal (epistaxis) antes de la cauterización o el taponamiento. Sin embargo, no está aprobada por la FDA para otros usos médicos y su disponibilidad es muy restringida.
¿Por qué la cocaína es tan adictiva?
La cocaína es altamente adictiva principalmente porque potencia drásticamente la señalización de dopamina en el sistema de recompensa del cerebro al bloquear su recaptación. Esto genera sensaciones intensas de placer y refuerza fuertemente la conducta de búsqueda de la droga. Con el uso crónico, la interacción con los receptores sigma (especialmente σ2R) parece inducir cambios plásticos a largo plazo en el cerebro que contribuyen a la dependencia y a la perpetuación de la adicción.
¿Cómo afecta la cocaína al corazón?
La cocaína aumenta la frecuencia cardíaca y la presión arterial al potenciar los efectos de la norepinefrina y la epinefrina. Es un potente vasoconstrictor, lo que reduce el flujo sanguíneo, especialmente en las arterias coronarias. También promueve la agregación plaquetaria y la formación de coágulos. Estos efectos combinados aumentan significativamente el riesgo de infarto de miocardio, arritmias graves y accidente cerebrovascular.
Comparativa de Efectos de la Cocaína Vía Receptores Sigma en Exposición Aguda vs Crónica
| Característica | Exposición Aguda | Exposición Crónica |
|---|---|---|
| Complejos D1R-σ1R | Aumentan significativamente | Vuelven a niveles basales |
| Complejos D1R-σ2R | Aumentan ligeramente | Aumentan significativamente |
| Modulación D1R (vía σ1R) - cAMP | Potenciada | Menos relevante |
| Modulación D1R (vía σ2R) - cAMP | Inhibida | Inhibición prevalece |
| Modulación D1R (vía σ1R) - MAP Kinase | Inhibida | Menos relevante |
| Modulación D1R (vía σ2R) - MAP Kinase | Potenciada | Potenciación prevalece |
| Rol en Plasticidad/Adicción | Inicio, predominio σ1R | Establecimiento, predominio σ2R |
En conclusión, el mecanismo de acción de la cocaína es multifacético, centrado en el bloqueo de la recaptación de monoaminas, especialmente la dopamina, pero también modulado de forma compleja por su interacción directa con los receptores sigma. Esta interacción parece desempeñar un papel dinámico y cambiante en el tiempo, contribuyendo a los profundos cambios cerebrales que caracterizan la adicción a esta potente droga.
Si quieres conocer otros artículos parecidos a Cocaína: Mecanismo Cerebral y Adicción puedes visitar la categoría Neurociencia.
