La investigación en neurociencia y biología celular a menudo requiere visualizar estructuras con gran detalle y, al mismo tiempo, comprender su función o identidad molecular. Tradicionalmente, dos técnicas de microscopía han sido fundamentales: la microscopía de fluorescencia (FM) y la microscopía electrónica (EM). Si bien cada una ofrece capacidades únicas, también presentan limitaciones significativas. Aquí es donde entra en juego la Microscopía Correlativa de Luz y Electrones (CLEM), una poderosa metodología que busca combinar lo mejor de ambos mundos para obtener una visión más completa.

Mientras que la microscopía de fluorescencia (FM) y la microscopía electrónica (EM) son técnicas potentes por sí solas, no están exentas de inconvenientes. La microscopía de fluorescencia proporciona información funcional valiosa pero tiene una resolución muy limitada, mientras que la EM, aunque de alta resolución, carece de información funcional específica, lo que significa que identificar células o estructuras basándose únicamente en la morfología de EM puede ser propenso a errores. Ningún modo de imagen por sí solo puede, por lo tanto, proporcionar información completa. Realizar CLEM permite tener lo mejor de ambas técnicas.
Microscopía de Fluorescencia (FM)
La microscopía de fluorescencia debe su popularidad a la inmensa variedad de estrategias de marcaje que se pueden emplear. Las muestras pueden teñirse, inmunomarcaje o etiquetarse utilizando proteínas fluorescentes genéticamente codificadas. Además, gracias a las propiedades espectrales de estas etiquetas fluorescentes, se pueden identificar múltiples marcadores simultáneamente utilizando luz de excitación de diferentes longitudes de onda. De esta manera, diferentes partes de la célula y, por lo tanto, diferentes funciones celulares, pueden ser visualizadas simultáneamente, formando una imagen de fluorescencia multicolor.
La fluorescencia es el fenómeno de la emisión de luz tras la absorción de un fotón. Cuando una molécula en estado fundamental absorbe un fotón, se excita a un estado de mayor energía desde donde puede decaer a estados intermedios de menor energía. Los canales de decaimiento disponibles dependen de la molécula y su entorno. La diferencia de energía entre el estado fundamental y el estado intermedio puede ser liberada como un fotón, cuya emisión se llama fluorescencia. La microscopía de fluorescencia se basa en la imagen de moléculas fluorescentes que se unen selectivamente a diferentes partes de una célula u organismo. La capacidad de etiquetar específicamente objetivos moleculares es una de sus mayores fortalezas, proporcionando información sobre la presencia y localización de proteínas, ácidos nucleicos u otras moléculas de interés.
Microscopía Electrónica (EM)
La microscopía electrónica es un método potente para adquirir información estructural de alta resolución a escala nanométrica. Debido a que la longitud de onda de los electrones acelerados es mucho más corta que la de la luz visible, se puede superar la barrera de difracción de la luz y visualizar características mucho más pequeñas.
Lo que distingue a la microscopía de luz de la microscopía electrónica no es solo la resolución. El tipo de contraste que se mide típicamente en EM es muy distinto de FM. Mientras que en FM solo se pueden detectar macromoléculas específicas que han sido marcadas, en EM se adquiere principalmente información contextual. En otras palabras, se ve todo lo que hay. Ejemplos de aplicaciones útiles de EM en ciencias de la vida incluyen estructuras de membrana como el retículo endoplasmático, el aparato de Golgi y estructuras vesiculares.
La microscopía electrónica, a menudo realizada en un Microscopio Electrónico de Barrido (SEM), enfoca un haz de electrones de alta energía (típicamente hasta 30 keV) sobre la superficie de una muestra. Una serie de procesos de dispersión tienen lugar al interactuar el haz con los átomos del material, resultando en la generación de, entre otros, electrones secundarios de baja energía (SE’s) y electrones retrodispersados de alta energía (BSE’s). Estos son detectados con detectores dedicados. Al escanear el haz sobre la muestra, se crea una imagen que contiene diferentes tipos de información sobre la muestra, dependiendo de los electrones detectados, como topografía y densidad. La principal limitación es la falta de especificidad; no se puede saber la identidad molecular de una estructura sin un método de marcaje específico para EM, lo cual es más complejo que en FM.
La Necesidad de Correlación: ¿Por Qué CLEM?
Las limitaciones inherentes de la FM y la EM por separado crean un vacío en nuestra capacidad para comprender completamente los sistemas biológicos. La FM nos dice dónde está algo específico (información funcional/molecular) pero con una resolución limitada que no permite ver el detalle ultraestructural de su entorno. La EM nos muestra el detalle ultraestructural de todo (información estructural/contextual) pero no nos dice qué es molecularmente algo a menos que tenga una morfología muy distintiva o se apliquen técnicas de marcaje de EM, que no siempre son posibles o tan versátiles como en FM.
Consideremos un ejemplo en neurociencia. Podríamos querer saber la ubicación exacta de una proteína específica en una sinapsis (uniones entre neuronas). Con FM, podemos marcar fluorescentemente la proteína y ver puntos brillantes que indican su presencia. Pero la resolución de FM no es suficiente para ver la estructura detallada de la sinapsis: la membrana presináptica, el espacio sináptico, la membrana postsináptica, las vesículas, etc. Con EM, podemos ver todas esas estructuras sinápticas con gran detalle. Pero si no sabemos cómo se ve la sinapsis de interés morfológicamente (y a menudo no son tan distintivas), no podemos estar seguros de que la sinapsis que vemos en EM sea la que contiene la proteína marcada que vimos en FM.
Aquí es donde la Microscopía Correlativa de Luz y Electrones (CLEM) se vuelve indispensable. Permite obtener una imagen de fluorescencia de la muestra, identificando la ubicación de los marcadores específicos, y luego obtener una imagen electrónica de la misma región, revelando su ultraestructura detallada. Al superponer o correlacionar estas dos imágenes, los investigadores pueden ver la ubicación exacta de las moléculas marcadas dentro de su contexto ultraestructural de alta resolución.
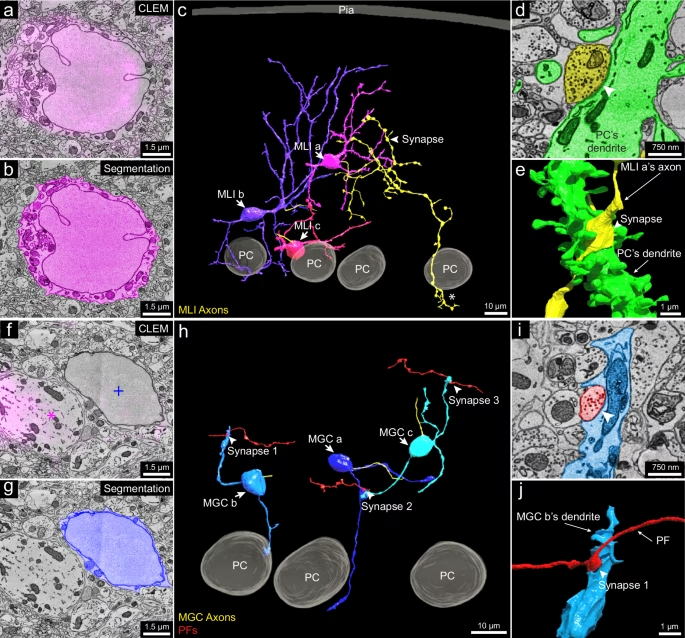
Ventajas Clave del CLEM
Realizar CLEM permite obtener lo mejor de ambas técnicas de microscopía. Se logra la especificidad y la información funcional proporcionada por la FM, junto con la alta resolución y el rico contexto ultraestructural de la EM. Esto es particularmente valioso en campos donde la relación entre la función molecular y la estructura detallada es crucial, como la biología celular, la patología y especialmente la neurociencia.
Las principales ventajas incluyen:
- Combinación de Información: Obtener simultáneamente información funcional (quién está ahí y dónde) y estructural (cómo es el entorno).
- Superación de Limitaciones: La resolución limitada de FM se complementa con la alta resolución de EM, y la falta de especificidad de EM se complementa con el marcaje selectivo de FM.
- Localización Precisa: Identificar con precisión la ubicación de moléculas o estructuras específicas dentro del contexto celular y tisular detallado.
- Comprensión Integral: Permite una comprensión más profunda de los procesos biológicos al vincular la función con la ultraestructura.
Esta capacidad de correlacionar la información molecular con el detalle ultraestructural abre nuevas vías para la investigación, permitiendo a los científicos abordar preguntas que antes eran inaccesibles con las técnicas individuales.
Comparativa: FM vs EM vs CLEM
| Característica | Microscopía de Fluorescencia (FM) | Microscopía Electrónica (EM) | Microscopía Correlativa (CLEM) |
|---|---|---|---|
| Resolución Típica | Micrométrica (baja) | Nanométrica (alta) | Contexto de alta resolución con localización específica |
| Tipo de Información | Funcional, molecular, específica | Estructural, ultraestructural, contextual | Combinada: Localización molecular/funcional dentro de contexto ultraestructural |
| Preparación de Muestra | Relativamente sencilla (compatible con muestras vivas) | Compleja (requiere fijación y preparación especial) | Muy compleja (compatible con ambas, requiere marcaje y preparación robusta) |
| Costo/Complejidad | Moderado | Alto | Muy alto (equipo y experiencia especializada) |
| Aplicaciones Clave | Visualización de proteínas, organelos, procesos dinámicos en células vivas | Detalle ultraestructural de células, tejidos, materiales | Localización precisa de moléculas/estructuras dentro de su entorno ultraestructural |
Preguntas Frecuentes sobre CLEM
Dado su potencial y complejidad, es común tener preguntas sobre la aplicación de CLEM.
¿Qué tipo de muestras se pueden estudiar con CLEM?
Se pueden estudiar una amplia variedad de muestras biológicas, desde células cultivadas hasta tejidos complejos como el cerebro. La clave es que la preparación de la muestra debe ser compatible con ambas técnicas. Esto a menudo implica fijación, marcaje fluorescente, y luego procesamiento adicional (como inclusión en resina y cortes finos) para la microscopía electrónica, asegurando que la fluorescencia se preserve lo suficiente para la adquisición de la imagen de luz inicial.
¿Es CLEM una técnica difícil de realizar?
Generalmente, sí. CLEM es una técnica avanzada que requiere experiencia significativa tanto en microscopía de fluorescencia como electrónica. Además, la preparación de muestras es un desafío clave, ya que deben ser adecuadas para ambos métodos. El paso de correlacionar con precisión las imágenes obtenidas de los dos microscopios, a menudo con diferentes magnificaciones y distorsiones, requiere software especializado y habilidades técnicas considerables.
¿Qué nivel de detalle puedo esperar con CLEM?
La información estructural de detalle proviene del microscopio electrónico, por lo que se puede alcanzar resolución nanométrica para el contexto ultraestructural. La microscopía de fluorescencia proporciona la ubicación de los marcadores específicos, pero la resolución de esta localización está limitada por la difracción de la luz (aunque técnicas avanzadas de superresolución en FM pueden mejorar esto, la correlación con EM sigue siendo valiosa por el contexto ultraestructural).
¿CLEM permite ver procesos dinámicos en tiempo real?
La microscopía electrónica típicamente requiere muestras fijadas (no vivas) y a menudo operan en condiciones de vacío, lo que impide la visualización de procesos dinámicos en tiempo real durante la adquisición de la imagen de EM. Sin embargo, es posible realizar experimentos donde se observan procesos dinámicos en células vivas utilizando FM, luego se fija rápidamente la muestra en un momento clave del proceso, y finalmente se procesa para EM y se correlaciona con las imágenes de FM previas. Esto permite correlacionar un estado funcional dinámico con la ultraestructura en ese momento específico.
Conclusión
En resumen, la Microscopía Correlativa de Luz y Electrones (CLEM) representa un avance significativo en la visualización biológica. Al superar las limitaciones inherentes de la microscopía de fluorescencia y la microscopía electrónica cuando se usan de forma aislada, CLEM permite a los investigadores obtener una comprensión sin precedentes de la relación entre la función molecular y la estructura ultraestructural. Esta capacidad es fundamental para abordar preguntas complejas en neurociencia y muchas otras áreas de la biología, proporcionando una visión más completa y detallada del mundo celular. Aunque es una técnica compleja y exigente, el poder de obtener información específica y contextual de la misma muestra la convierte en una herramienta invaluable para la investigación de vanguardia.
Si quieres conocer otros artículos parecidos a CLEM: Uniendo Luz y Electrones puedes visitar la categoría Neurociencia.
