En el vasto y complejo universo de la neurociencia, visualizar las intrincadas redes neuronales y las estructuras celulares en su contexto tridimensional es un desafío fundamental. Durante décadas, los científicos han dependido de cortar el tejido cerebral en finas secciones para poder examinarlo bajo el microscopio. Si bien esta técnica ha sido invaluable, inherentemente fragmenta la información tridimensional y puede dificultar la comprensión de circuitos neuronales a gran escala o la morfología completa de neuronas individuales. Aquí es donde entra en juego una técnica transformadora que ha abierto una nueva ventana a la visualidad biológica: CLARITY.

CLARITY, acrónimo de Clear Lipid-exchanged Acrylamide-hybridized Rigid Imaging/immunostaining compatible Tissue Hydrogel, es un método innovador desarrollado en 2013 que permite hacer que el tejido biológico, particularmente el cerebro, sea ópticamente transparente manteniendo su estructura intacta. Su objetivo principal es permitir la visualización profunda y la adquisición de imágenes en 3D de muestras biológicas completas sin necesidad de seccionarlas, facilitando así el estudio detallado de la anatomía, la conectividad y la composición molecular del tejido.

- ¿Qué es CLARITY? La Transformación del Tejido
- El Proceso Detallado de CLARITY
- Importancia y Aplicaciones de CLARITY en Neurociencia y Más Allá
- Optimización y Desafíos
- Preguntas Frecuentes sobre CLARITY
- ¿Qué hace que el tejido sea transparente en CLARITY?
- ¿Se destruye la estructura del tejido durante CLARITY?
- ¿Puedo usar CLARITY en cualquier tipo de tejido?
- ¿Qué tipo de marcaje molecular es compatible con CLARITY?
- ¿Necesito un microscopio especial para ver tejidos clarificados con CLARITY?
- ¿Cuánto tiempo tarda el proceso de CLARITY?
- Conclusión
¿Qué es CLARITY? La Transformación del Tejido
En esencia, CLARITY transforma el tejido biológico en una forma híbrida. Reemplaza los componentes que dispersan la luz, principalmente los lípidos de las membranas celulares, con un hidrogel transparente. Este hidrogel no solo proporciona transparencia sino que también sirve como un andamiaje estructural que ancla las moléculas intrínsecas del tejido, como proteínas y ácidos nucleicos, en su lugar original. Al preservar la estructura molecular y anatómica mientras se elimina la opacidad causada por los lípidos, CLARITY permite que la luz penetre mucho más profundamente en el tejido, posibilitando la obtención de imágenes de alta resolución a través de volúmenes significativos.
La técnica fue ideada por Kwanghun Chung y Karl Deisseroth en la Universidad de Stanford y ha sido aplicada a una amplia variedad de tejidos y órganos, incluyendo cerebros, médulas espinales, riñones, pulmones e intestinos, así como en el estudio de diversas enfermedades como el Alzheimer, la esclerosis múltiple y el cáncer.
El Proceso Detallado de CLARITY
La aplicación de CLARITY implica una serie de pasos químicos y físicos cuidadosamente controlados para lograr la transparencia del tejido y permitir su posterior análisis. Los pasos principales incluyen la fijación, la polimerización del hidrogel, la extracción de lípidos, el marcaje molecular y el ajuste del índice de refracción.
1. Fijación del Tejido y Polimerización del Hidrogel
El primer paso es la fijación del tejido, a menudo mediante perfusión transcardial o inmersión en una solución que contiene formaldehído (PFA) y monómeros de hidrogel como acrilamida y bis-acrilamida. Los agentes fijadores como el PFA crean enlaces químicos entre las proteínas y los ácidos nucleicos, mientras que los monómeros de acrilamida se infiltran en el tejido. La polimerización del hidrogel se inicia típicamente calentando la muestra en presencia de un iniciador térmico (como VA-044) y en ausencia de oxígeno (que inhibe la polimerización). Durante este proceso, los monómeros de acrilamida se unen químicamente tanto entre sí (formando la malla de hidrogel) como a las proteínas y ácidos nucleicos fijados. Esto crea una red de hidrogel que encapsula y soporta la estructura molecular del tejido.
La composición de la solución de hidrogel es crucial, ya que afecta la densidad de la malla. Una malla densa (mayor concentración de acrilamida y PFA) proporciona mayor estabilidad y reduce la pérdida de proteínas, pero ralentiza la extracción de lípidos y la penetración de las moléculas de marcaje. Por el contrario, una malla más porosa (menor concentración) acelera estos procesos pero puede comprometer la estabilidad estructural. Los investigadores han ajustado estas concentraciones para optimizar el equilibrio según el tipo de tejido y los objetivos del estudio.
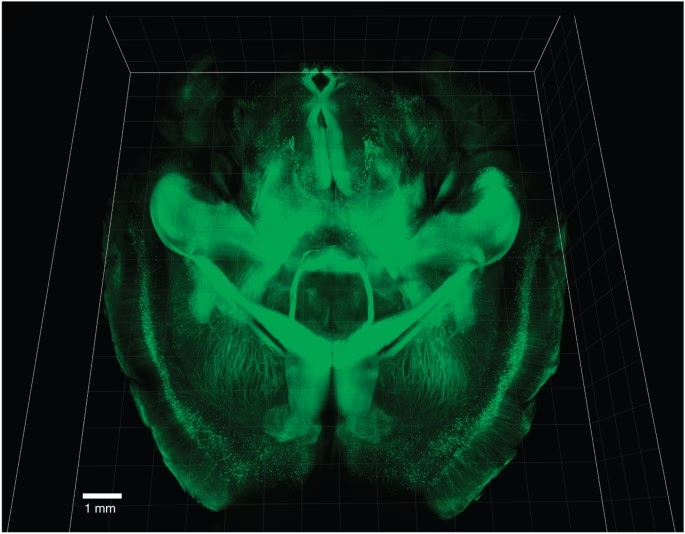
2. Extracción de Lípidos
Este es el paso clave para lograr la transparencia. Las membranas lipídicas son la principal causa de dispersión de la luz en el tejido. Su eliminación se realiza utilizando detergentes, típicamente dodecilsulfato de sodio (SDS). Existen dos métodos principales para facilitar la extracción de lípidos:
- Difusión térmica pasiva: La muestra se incuba en una solución de SDS a una temperatura elevada (por ejemplo, 37-60°C) con agitación suave. El calor acelera la difusión de las micelas de SDS en el tejido, donde solubilizan los lípidos. Este método es más simple de implementar pero puede ser muy lento, tardando semanas o incluso meses para tejidos grandes, y las temperaturas elevadas pueden dañar las moléculas endógenas.
- Electroforesis: Se aplica un campo eléctrico a través del tejido sumergido en la solución de SDS. El campo eléctrico acelera el transporte de las micelas de SDS hacia el interior del tejido y la migración de los lípidos solubilizados hacia el exterior. Este método es significativamente más rápido que la difusión pasiva, reduciendo el tiempo de extracción a días u horas para tejidos más pequeños. Sin embargo, la electroforesis presenta desafíos, como el riesgo de daño tisular (deformación o pérdida de epitopes/fluorescencia) debido al calor generado y a campos eléctricos no homogéneos. Se han desarrollado variantes (como ETC, stochastic electrotransport, ACT) para mitigar estos problemas mediante el control preciso de la temperatura, el voltaje y el diseño de las cámaras de clearing.
La concentración de SDS y el pH de la solución también influyen en la eficiencia de la extracción. Una mayor concentración de SDS (como 8% en PACT) puede acelerar el proceso, aunque 4% es también común. El pH ligeramente alcalino (pH 8.0-8.5) suele ser óptimo.
| Método de Extracción de Lípidos | Principio | Tiempo de Elución | Complejidad | Frecuencia de Cambio de Buffer SDS | Volumen de Buffer SDS | Circulación |
|---|---|---|---|---|---|---|
| Difusión Térmica Pasiva | Transporte de micelas de detergente por difusión inducida por calor | Semanas a meses | Fácil | Ocasionalmente | Pequeño (decenas de ml) | No |
| Electroforesis | Transporte de micelas de detergente por campos eléctricos | Varios días a horas | Difícil | Frecuentemente | Grande (varios litros por circulación) | Sí (para control de temperatura) |
Es importante señalar que, si bien la electroforesis es más rápida, la elección entre un método pasivo o activo a menudo depende del tipo de tejido, su tamaño y los recursos disponibles. Métodos pasivos mejorados, como PACT (Perfusión de Acrilamida-CLARITY de Tejido) o PARS (Perfusión y Anclaje mediante el Sistema Vascular), buscan acelerar la difusión pasiva modificando la fijación o utilizando el sistema vascular intrínseco para la entrega del buffer de clearing.
3. Marcaje Molecular
Una vez que el tejido es transparente, se pueden visualizar moléculas de interés. Esto se logra de varias maneras:
- Marcadores fluorescentes endógenos: Si el tejido contiene proteínas fluorescentes (como GFP o tdTomato) expresadas genéticamente, su fluorescencia se preserva en gran medida gracias al hidrogel.
- Marcaje con anticuerpos: Los anticuerpos específicos para ciertas proteínas pueden difundirse en el tejido transparente y unirse a sus objetivos. Estos anticuerpos suelen estar etiquetados con fluoróforos o se detectan con anticuerpos secundarios fluorescentes. La penetración de anticuerpos en tejidos gruesos puede ser lenta (días a semanas por difusión pasiva), similar a la extracción de lípidos. Se han adaptado métodos electroforéticos o basados en presión (como PRESTO) para acelerar la penetración de anticuerpos.
- Marcaje de ácidos nucleicos: Se pueden usar sondas de hibridación (como sm-FISH o HCR) para detectar ARN específicos en el tejido. Técnicas como EDC-CLARITY han sido desarrolladas para retener y visualizar ARN de manera eficiente en tejidos clarificados.
La capacidad de realizar múltiples rondas de marcaje y eliminación de anticuerpos en la misma muestra es una ventaja significativa de CLARITY, ya que el andamiaje de hidrogel mantiene la estructura intacta.
4. Ajuste del Índice de Refracción (RI Matching)
Para obtener imágenes óptimas, el tejido clarificado debe sumergirse en una solución con un índice de refracción similar al del tejido (aproximadamente 1.46). Esto minimiza la dispersión residual de la luz en la interfaz entre el tejido y el medio circundante, mejorando la transparencia óptica y permitiendo la adquisición de imágenes más nítidas a mayor profundidad. Se han utilizado diversas soluciones para este propósito, como FocusClear, RIMS (solución de ajuste del índice de refracción), sRIMS, cRIMS, nRIMS, TDE (2,2′-thiodiethanol) y soluciones basadas en CUBIC. La elección de la solución puede depender del tipo de tejido, los marcadores fluorescentes utilizados y la necesidad de controlar la expansión del tejido.
| Solución de Ajuste de RI | Ingredientes Principales |
|---|---|
| FocusClear | Desconocidos (comercial) |
| RIMS | 88% Histodenz en buffer fosfato 0.02 M |
| sRIMS | 70% Sorbitol en buffer fosfato 0.02 M |
| cRIMS | 88% Histodenz en buffer fosfato 0.005 M |
| nRIMS | 80% Nycodenz |
| TDE en PBS | 63% 2,2′-thiodiethanol en PBS |
| Solución CUBIC-mount | 50% Sacarosa, 25% Urea, 25% N, N, N', N'-tetrakis (2-hidroxipropil) etilendiamina |
Encontrar la solución de ajuste de RI óptima a veces requiere probar diferentes concentraciones y solventes, ya que la composición interna del tejido puede variar.
Importancia y Aplicaciones de CLARITY en Neurociencia y Más Allá
CLARITY ha revolucionado la forma en que los neurocientíficos pueden estudiar la arquitectura cerebral. Al permitir la visualización en 3D de cerebros intactos o grandes volúmenes de tejido, supera las limitaciones del seccionamiento tradicional. Esto es particularmente valioso para:
- Mapeo de circuitos a gran escala: Permite seguir las proyecciones neuronales a través de largas distancias y comprender la conectividad global.
- Análisis morfológico detallado: Facilita la visualización y reconstrucción completa de neuronas individuales, incluyendo sus dendritas y axones complejos, que podrían extenderse a lo largo de múltiples secciones en la histología convencional.
- Estudios cuantitativos: Permite contar células o analizar densidades de sinapsis en volúmenes definidos sin la necesidad de tediosas reconstrucciones a partir de secciones.
- Análisis molecular y celular: La compatibilidad con el marcaje de proteínas y ácidos nucleicos posibilita el estudio de la distribución de biomoléculas y la identificación de tipos celulares en su contexto anatómico nativo.
Aunque CLARITY se originó en la neurociencia, su aplicación se ha extendido a otros órganos y sistemas, permitiendo el estudio de la vasculatura, la estructura de órganos internos y tejidos con alto contenido lipídico como el hueso (con adaptaciones como PACT-deCAL).
La técnica es compatible con varios tipos de microscopía, incluyendo microscopía confocal, microscopía de dos fotones y, de manera óptima para grandes volúmenes, microscopía de hoja de luz (light sheet microscopy). La transparencia lograda permite una penetración de la luz y una relación señal-ruido significativamente mejoradas.
Optimización y Desafíos
Aunque el protocolo original fue un avance importante, la implementación de CLARITY puede ser compleja y requiere optimización. Varios laboratorios han desarrollado variantes (PACT, PARS, mPACT, ETC, ACT, etc.) para mejorar la velocidad, reducir el daño tisular, aumentar la reproducibilidad o adaptar la técnica a tejidos específicos. Factores como la composición del hidrogel, la temperatura y el voltaje durante la electroforesis, la duración de los pasos de clearing y marcaje, y la elección de las soluciones de ajuste de RI son críticos y a menudo deben ajustarse empíricamente.
Desafíos comunes incluyen lograr una transparencia uniforme en tejidos muy grandes, prevenir la deformación o el daño durante la electroforesis, optimizar la penetración de anticuerpos en muestras densas y evitar artefactos como la formación de burbujas o la acumulación de residuos. A pesar de estos desafíos, la continua mejora de los protocolos y la aparición de nuevas variantes hacen que CLARITY sea cada vez más accesible y robusta.
Preguntas Frecuentes sobre CLARITY
Aquí respondemos algunas preguntas comunes sobre esta técnica:
¿Qué hace que el tejido sea transparente en CLARITY?
La transparencia se logra eliminando los lípidos de las membranas celulares, que son los principales causantes de la dispersión de la luz. Los lípidos se reemplazan por un hidrogel transparente que soporta la estructura restante del tejido.
¿Se destruye la estructura del tejido durante CLARITY?
No, el hidrogel de acrilamida forma un andamiaje dentro del tejido que ancla las proteínas y ácidos nucleicos en su posición original, preservando así la estructura anatómica y molecular.

¿Puedo usar CLARITY en cualquier tipo de tejido?
Aunque se desarrolló inicialmente para el cerebro, CLARITY y sus variantes se han aplicado con éxito a una amplia gama de órganos como médula espinal, riñón, hígado (con más dificultad), pulmón, intestino, etc. La optimización del protocolo puede ser necesaria para diferentes tejidos.
¿Qué tipo de marcaje molecular es compatible con CLARITY?
CLARITY es compatible con marcadores fluorescentes endógenos, marcaje con anticuerpos (inmunohistoquímica) y marcaje de ácidos nucleicos (hibridación in situ). Las rondas múltiples de marcaje son posibles.
¿Necesito un microscopio especial para ver tejidos clarificados con CLARITY?
Si bien la microscopía de hoja de luz es ideal para imágenes rápidas de grandes volúmenes, los tejidos suficientemente transparentes pueden ser imaged con microscopios confocales o incluso epifluorescentes, dependiendo de la profundidad y resolución requeridas.
¿Cuánto tiempo tarda el proceso de CLARITY?
El tiempo varía significativamente dependiendo del tamaño del tejido y el método de extracción de lípidos utilizado. La difusión pasiva puede tardar semanas o meses, mientras que la electroforesis puede reducirlo a días u horas para muestras más pequeñas. El marcaje también puede llevar varios días.
Conclusión
CLARITY representa un avance significativo en las técnicas de visualización biológica, ofreciendo una capacidad sin precedentes para explorar la arquitectura tridimensional intacta de tejidos complejos. Al permitir la transparencia óptica mientras se preservan las estructuras moleculares, ha abierto nuevas vías para la investigación en neurociencia y más allá. Las continuas mejoras y variaciones del protocolo expanden su aplicabilidad y accesibilidad, consolidando a CLARITY como una herramienta poderosa en el estudio detallado de la biología a nivel celular y de sistemas.
Si quieres conocer otros artículos parecidos a CLARITY: Transparencia Neural en 3D puedes visitar la categoría Neurociencia.

