El cannabis, también conocido como marihuana, ha experimentado un cambio significativo en su estatus legal en muchas partes del mundo, lo que ha llevado a un aumento considerable en su uso. Se estima que millones de personas lo consumen globalmente, y en países como Estados Unidos, el uso ha crecido constantemente en las últimas décadas, especialmente entre adolescentes y adultos jóvenes. Paralelamente, la potencia de los productos de cannabis, medida por la concentración de su principal constituyente psicoactivo, el Δ9-tetrahidrocannabinol (THC), ha aumentado notablemente. Esta creciente exposición y potencia plantean importantes interrogantes sobre los efectos del cannabis en la salud cerebral a lo largo de la vida, un área de creciente investigación científica.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
Este artículo profundiza en los hallazgos sobre cómo los cannabinoides afectan el cerebro desde una perspectiva neurocientífica, basándose en estudios preclínicos y observaciones clínicas. Exploraremos los mecanismos a nivel molecular y celular, los efectos en la cognición, la estructura y función cerebral, y su posible relación con el riesgo cerebrovascular, prestando especial atención a los periodos de desarrollo cerebral particularmente sensibles.
El Sistema Endocannabinoide y los Cannabinoides
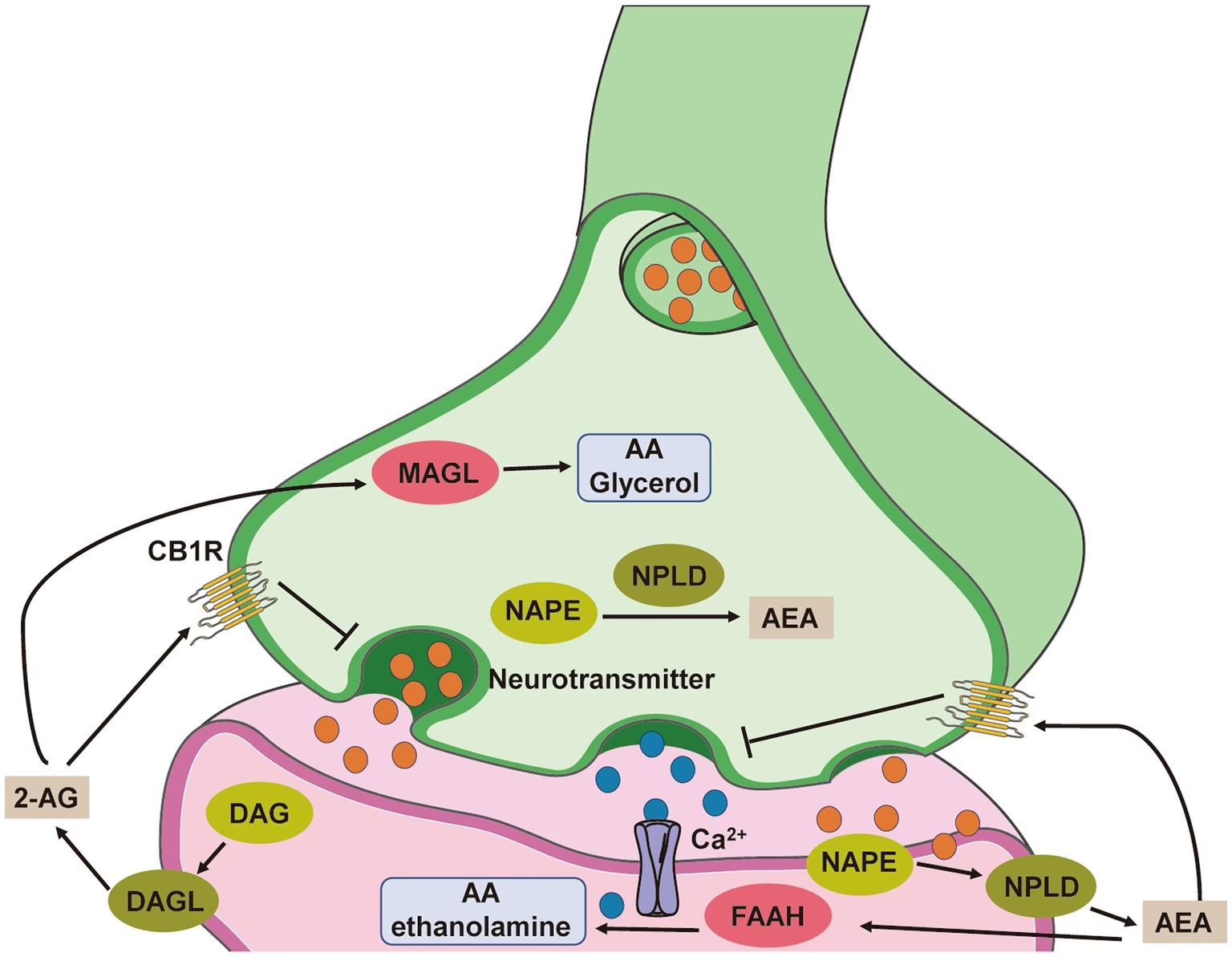
El cerebro humano posee un sistema de señalización intrínseco llamado Sistema Endocannabinoide (SEC). Este sistema está compuesto por receptores (principalmente el receptor cannabinoide tipo 1, CB1, y el tipo 2, CB2), ligandos endógenos (endocannabinoides como la anandamida y el 2-araquidonilglicerol) y enzimas involucradas en su síntesis y degradación. Los endocannabinoides no se almacenan, sino que se sintetizan bajo demanda y desempeñan un papel crucial en la regulación de la neurotransmisión y procesos cerebrales clave como la plasticidad sináptica, la neuroinflamación, la neurogénesis, la migración neuronal y el desarrollo de la materia blanca.
Los cannabinoides exógenos provienen principalmente de la planta de cannabis (Cannabis sativa, indica, ruderalis), de la cual se han extraído más de 100 fitocannabinoides. Los más abundantes son el THC y el cannabidiol (CBD). El THC es el componente psicoactivo principal y actúa principalmente activando los receptores CB1 y CB2. El receptor CB1 se expresa densamente en el sistema nervioso central, especialmente en áreas como el hipocampo, la amígdala y la corteza prefrontal, modulando la liberación de neurotransmisores como dopamina, GABA y glutamato. El receptor CB2 se encuentra predominantemente en células inmunes, incluyendo la microglía.
El CBD, a diferencia del THC, no activa directamente los receptores CB1 y CB2. En cambio, interactúa con una variedad de otras vías de señalización, incluyendo el receptor huérfano GPR55, el transportador de nucleósidos equilibrativo 1, el canal TRPM8, el receptor de serotonina 5-HT1A, el canal TRPA1 y los receptores de glicina α1/α3 a bajas concentraciones. A altas concentraciones, activa el receptor nuclear PPARγ y los canales TRPV1/TRPV2. El CBD es un cannabinoide no psicoactivo con propiedades antioxidantes y antiinflamatorias, y su potencial terapéutico está siendo investigado para diversas condiciones neurológicas.
Cannabinoides de Interés Médico e Ilícito
Existen varios cannabinoides aprobados para uso médico en diferentes países, así como cannabinoides sintéticos de alta potencia disponibles en el mercado ilegal.
| Tipo de Cannabinoide | Principio Activo | Indicación Médica (Ejemplos) |
|---|---|---|
| Médico (Aprobado) | Nabilona (análogo sintético de THC) | Náuseas y vómitos asociados a quimioterapia* |
| Médico (Aprobado) | Dronabinol (THC sintético) | Anorexia en pacientes con SIDA o cáncer, náuseas y vómitos asociados a quimioterapia* |
| Médico (Aprobado) | CBD Purificado (Epidiolex) | Convulsiones asociadas al síndrome de Lennox-Gastaut y Dravet en pacientes >1 año, convulsiones asociadas al complejo de esclerosis tuberosa en pacientes >1 año* |
| Médico (Aprobado) | Nabiximols (extracto de THC y CBD) | Espasticidad en esclerosis múltiple†, dolor neuropático en esclerosis múltiple†, dolor severo en cáncer avanzado† |
| Ilícito | K2, Spice, Kronic, Kaos (Canabimiméticos sintéticos) | Diseñados originalmente para investigación, se unen a receptores cannabinoides con alta afinidad. Pueden causar alucinaciones, agitación, psicosis, pérdida de memoria a corto plazo, convulsiones, coagulopatía e infarto de miocardio. |
* Aprobado por la FDA de EE. UU. † Aprobado por Health Canada.
Mecanismos Neurobiológicos en Modelos Preclínicos
Gran parte de nuestra comprensión de los efectos de los cannabinoides a nivel molecular y celular proviene de estudios en modelos animales, que permiten controlar variables y estudiar periodos de desarrollo específicos. El SEC modula la plasticidad sináptica, fundamental para la adaptación y el aprendizaje del cerebro. El THC, al activar inespecíficamente los receptores CB1, interfiere con la acción fisiológica de los endocannabinoides, alterando la conectividad y función de las redes neuronales.
El THC activa receptores CB1 en interneuronas GABAérgicas y astrocitos, influyendo en la liberación de glutamato en el hipocampo. También afecta la transmisión de otros neurotransmisores clave para la memoria como acetilcolina, adenosina y serotonina. Además, la activación de receptores CB1 mitocondriales por el THC puede disminuir la respiración celular y el suministro de ATP, fundamental para la neurotransmisión, lo que podría contribuir a los déficits cognitivos.
La exposición a largo plazo al THC puede inducir una desregulación y desensibilización de los receptores CB1, efectos que parecen ser más intensos y generalizados tras la exposición durante la adolescencia en comparación con la edad adulta. La exposición crónica durante la adolescencia puede alterar el equilibrio excitatorio/inhibitorio, provocar poda sináptica excesiva y desincronización de redes neuronales, afectando la corteza prefrontal (PFC) y el sistema dopaminérgico mesolímbico. Estos cambios podrían ser la base molecular de los déficits cognitivos y alteraciones emocionales observadas a largo plazo.
Además de sus efectos neuronales, el THC puede inducir neuroinflamación. La exposición a largo plazo durante la adolescencia activa la microglía y los astrocitos, aumentando la producción de mediadores proinflamatorios como TNF-α, iNOS y COX-2, y reduciendo citoquinas antiinflamatorias como IL-10. Esta respuesta neuroinflamatoria se ha asociado con deterioro de la memoria en la edad adulta. La dosis de THC también es crucial, con dosis más bajas pudiendo producir efectos similares si se administran en etapas más tempranas de la adolescencia.
Efectos de la Exposición Prenatal
La exposición a cannabinoides durante el embarazo (Exposición Prenatal a Cannabinoides - EPC) se ha asociado con resultados adversos en niños, incluyendo peor rendimiento neurocognitivo y volúmenes intracraneales reducidos. Estudios preclínicos sugieren que la EPC altera propiedades intrínsecas y sinápticas en regiones como la PFC, amígdala e hipocampo, afectando el procesamiento cognitivo y la regulación emocional. Se observan cambios en el equilibrio excitatorio/inhibitorio y disfunciones en el sistema glutamatérgico.
Las alteraciones en las vías de señalización del SEC causadas por la EPC durante el desarrollo pueden afectar procesos como la proliferación neuronal, supervivencia y crecimiento axonal. Esto podría explicar la interneuronopatía observada en crías expuestas, a menudo más pronunciada en hembras. También se ha asociado con un retraso en el cambio del papel del GABA, que inicialmente es excitatorio en el desarrollo temprano y luego se vuelve inhibitorio. Cualquier alteración en esta secuencia temporal crítica puede perturbar el comportamiento cognitivo y emocional de la descendencia.
La EPC también puede afectar la maduración de monoaminas y estar implicada en una señalización de recompensa aberrante. Además, se asocia con una desregulación prolongada de la respuesta al estrés, lo que podría aumentar la susceptibilidad a trastornos psiquiátricos. Comprender cómo la EPC interfiere con el SEC durante el neurodesarrollo es clave para buscar posibles intervenciones.
Efectos en la Cognición Humana
La intoxicación aguda con cannabis puede causar deterioro de la memoria de trabajo y episódica, desinhibición conductual e impulsividad, afectando el rendimiento en actividades cotidianas como la conducción. Un estudio reciente mostró que el THC dominante o una mezcla de THC y CBD afectaron negativamente el rendimiento en pruebas de conducción, mientras que el CBD dominante tuvo un efecto similar al placebo. Estos efectos agudos suelen ser transitorios y pueden estar influenciados por la tolerancia y el uso de otras sustancias.
Los efectos a largo plazo del cannabis en la cognición son menos consistentes. Metaanálisis en adultos que consumen cannabis casi a diario durante más de dos años han encontrado un rendimiento neurocognitivo global ligeramente peor en comparación con no usuarios, con efectos significativos en dominios como toma de decisiones, aprendizaje verbal, retención y función ejecutiva. Metaanálisis en usuarios jóvenes (<26 años) también mostraron diferencias globales similares, aunque con efectos menores y dominios específicos afectados.
Sin embargo, estudios longitudinales con gemelos, que controlan mejor los factores genéticos y ambientales compartidos, han arrojado resultados mixtos. Algunos sugieren que el menor rendimiento cognitivo (como el CI) podría preceder al uso de cannabis, o que las diferencias observadas se deben a factores de riesgo compartidos, en lugar de un declive directo causado por el cannabis. No obstante, un estudio longitudinal a 25 años (CARDIA) encontró que los años acumulados de exposición al cannabis se asociaron con un peor rendimiento en memoria verbal.
Efectos Estructurales y Funcionales del Cerebro
Las técnicas de neuroimagen, como la resonancia magnética (RM), han investigado los efectos del cannabis en la estructura y función cerebral, con resultados variados.
Cambios Estructurales
Los hallazgos sobre alteraciones en la estructura cerebral relacionadas con el uso de cannabis son inconsistentes. Algunos metaanálisis han sugerido que el consumo regular se asocia con volúmenes más pequeños en el hipocampo y la corteza orbitofrontal medial y lateral. Sin embargo, otros estudios grandes no han encontrado relación entre el uso de cannabis y los volúmenes de varias estructuras subcorticales o medidas de superficie cortical (grosor, área, índice de girificación), incluso considerando la dependencia o la edad de inicio del uso. Un estudio longitudinal sí observó una asociación dosis-dependiente entre el uso de cannabis y el adelgazamiento de la corteza prefrontal en adolescentes.
Cambios Funcionales
Los estudios de RM funcional (fMRI) han reportado efectos más consistentes, especialmente después del uso prolongado. Metaanálisis de estudios de fMRI basados en tareas en usuarios adultos y adolescentes han encontrado patrones de activación cerebral alterados. Los usuarios de cannabis mostraron mayor activación en ciertas áreas (giros temporales transversos superior y posterior, giro frontal inferior, giro parietal inferior, putamen) y menor activación en otras (estriado, ínsula, giro frontal medio) durante diversas tareas cognitivas. Estas anomalías funcionales pueden persistir a pesar de la abstinencia, sugiriendo mecanismos neuroadaptativos compensatorios.
En contraste, algunos estudios clínicos en poblaciones específicas, como pacientes con dolor crónico o esclerosis múltiple usando cannabis médico con THC (dronabinol) o extractos de THC/ CBD, no encontraron efectos adversos significativos en síntomas neurocognitivos o medidas de volumen cerebral.
Riesgo Cerebrovascular
La evidencia que vincula el consumo de marihuana con un aumento en el riesgo de factores de riesgo cerebrovascular específicos o la enfermedad cerebrovascular es limitada y proviene principalmente de estudios observacionales, transversales y series de casos, que son propensos a sesgos. Los efectos adversos postulados podrían incluir activación del sistema nervioso simpático, cambios en la presión arterial, activación plaquetaria y efectos electrofisiológicos. El uso concomitante de tabaco y otras sustancias puede contribuir a estos efectos, que a menudo son de corta duración.
Aunque la reacción aguda más común al cannabis es una disminución de la presión arterial, algunos estudios sugieren una asociación modesta entre el uso reciente de cannabis y una mayor presión arterial sistólica o prevalencia de hipertensión en usuarios de 30 a 59 años, especialmente en usuarios intensivos, aunque esta asociación a menudo pierde significancia al ajustar por el uso de tabaco y alcohol. La relación entre el uso de marihuana y la hipertensión podría contribuir a asociaciones a largo plazo con resultados cerebrovasculares, pero este mecanismo requiere más estudio.
Se han reportado casos de infarto de miocardio (IM) tras el uso de marihuana, principalmente en adultos jóvenes sin factores de riesgo vascular preexistentes, con el IM ocurriendo poco después del consumo. El riesgo de IM se elevó significativamente en la hora posterior a fumar marihuana, sugiriendo un papel como desencadenante agudo de enfermedad cardiovascular. Sin embargo, estudios longitudinales a largo plazo han mostrado resultados contradictorios respecto a la asociación entre el uso acumulado de marihuana y eventos cardiovasculares como IM o accidente cerebrovascular.
La relación entre el cannabis y el riesgo de accidente cerebrovascular (ACV) o ataque isquémico transitorio (AIT) también es mixta. Mientras que algunos informes y series de casos sugieren una relación con el uso reciente e intensivo, estudios de casos y controles, poblacionales y basados en bases de datos nacionales han sido equívocos, dependiendo del diseño del estudio, los factores de confusión considerados (como el tabaquismo y el consumo de alcohol) y la población estudiada. Datos de estudios que han examinado la dosis o frecuencia sugieren que el uso regular y frecuente podría aumentar el riesgo de ACV. Un estudio basado en datos hospitalarios encontró que el uso de cannabis se asoció con un riesgo relativo un 17% mayor de ACV isquémico agudo, riesgo que aumentó al 31% con el uso concomitante de tabaco.
Debido a sus efectos vasoactivos, el uso de cannabis se ha implicado en algunos casos de síndrome de vasoconstricción cerebral reversible (SVCR) y estenosis arterial intracraneal, especialmente en usuarios jóvenes. Estudios preclínicos muestran que los cannabinoides pueden tener efectos complejos sobre el tono vascular y la aterogénesis; la activación del receptor CB1 promueve la inflamación y disfunción endotelial, procesos vinculados a la aterosclerosis, mientras que el CB2 podría tener un papel ateroprotector.
En poblaciones específicas, como mujeres embarazadas, un estudio longitudinal encontró que el trastorno por consumo de cannabis se asoció con el doble de riesgo de accidente cerebrovascular hemorrágico. Los cannabinoides sintéticos como Spice también se han asociado con eventos cerebrovasculares agudos, incluyendo hemorragias, a menudo vinculadas a adulterantes.
Preguntas Frecuentes
- ¿El uso de cannabis causa daño cerebral irreversible? La investigación muestra efectos complejos y dependientes de la edad de exposición. Durante la adolescencia, un periodo crítico de desarrollo, el uso prolongado puede inducir cambios estructurales y funcionales que persisten. En adultos, los efectos a largo plazo sobre la cognición y estructura cerebral son menos consistentes, y algunos estudios sugieren que los factores de riesgo preexistentes pueden influir más que el cannabis directamente.
- ¿Cómo afecta el cannabis la memoria? Agudamente, el cannabis, particularmente el THC, puede deteriorar la memoria de trabajo y episódica. Los efectos a largo plazo en la memoria son un área de investigación activa con resultados mixtos, aunque algunos estudios sugieren asociaciones con peor memoria verbal en usuarios crónicos.
- ¿Hay diferencia entre los efectos del THC y el CBD? Sí, el THC es el principal componente psicoactivo que interactúa con los receptores CB1 y CB2, responsable de los efectos eufóricos y muchos de los efectos cognitivos adversos. El CBD no es psicoactivo y actúa a través de diferentes vías, mostrando propiedades antiinflamatorias y antioxidantes, con potencial terapéutico en ciertas condiciones neurológicas y sin los mismos efectos cognitivos agudos que el THC.
En conclusión, la evidencia científica sugiere que los cannabinoides, especialmente el THC, pueden tener efectos significativos en el cerebro, particularmente durante periodos vulnerables del desarrollo como la exposición prenatal y la adolescencia. Estos efectos incluyen alteraciones en la plasticidad sináptica, neurotransmisión, neuroinflamación y posibles cambios estructurales y funcionales a largo plazo. Si bien los efectos agudos en la cognición son claros, los efectos a largo plazo en adultos son más complejos y a menudo influenciados por factores de confusión. La relación con el riesgo cerebrovascular también presenta resultados mixtos y requiere más investigación rigurosa. La distinción entre los efectos del THC y el CBD es crucial, así como la consideración de la potencia y la frecuencia del uso. Dada la creciente disponibilidad del cannabis, es fundamental continuar investigando sus efectos en la salud cerebral para informar a la población y guiar las políticas de salud pública.
Si quieres conocer otros artículos parecidos a Efectos Neurológicos de los Cannabinoides puedes visitar la categoría Neurociencia.
