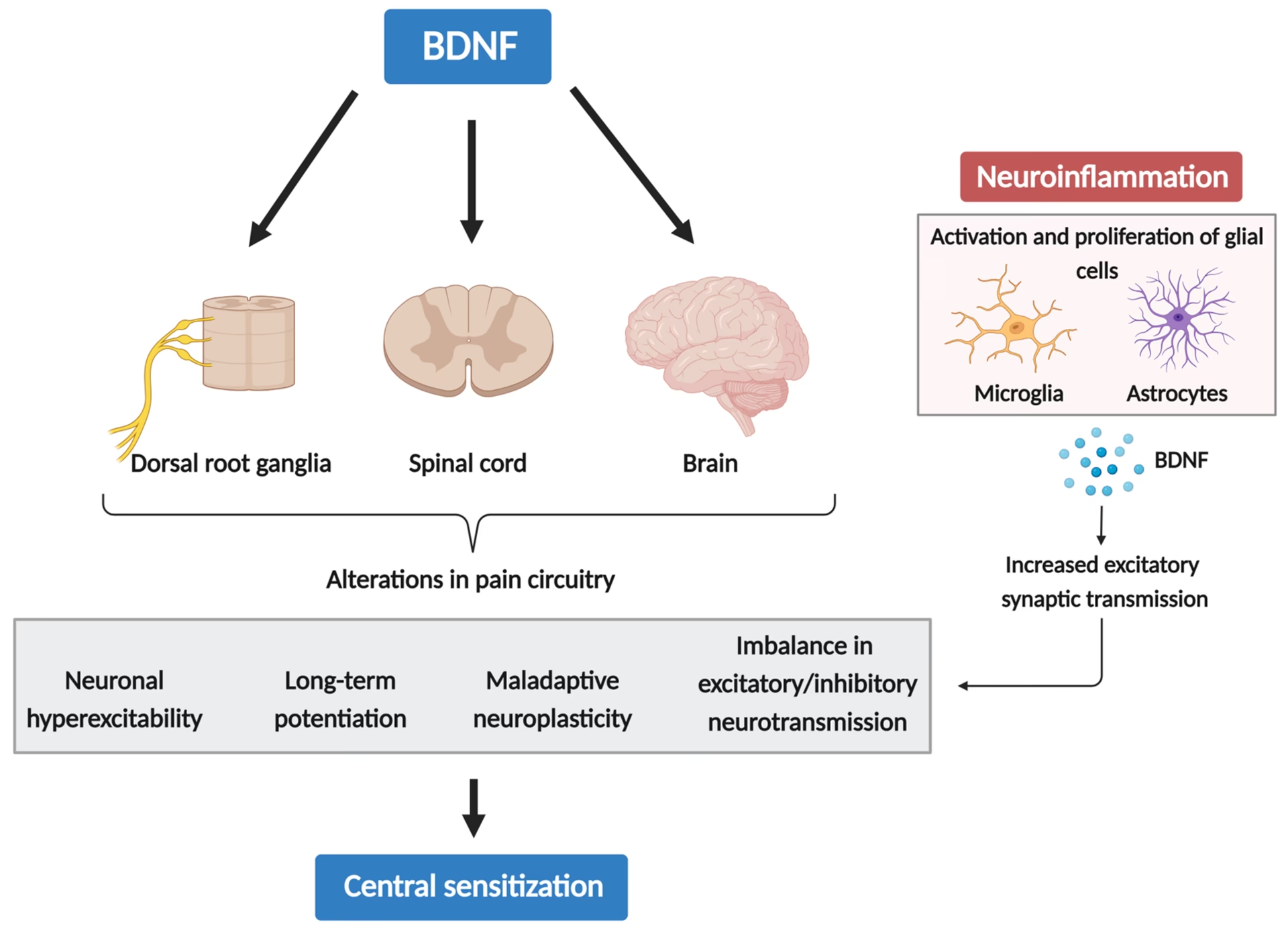
La capacidad del cerebro para reorganizarse, formar nuevas conexiones neuronales y adaptarse a lo largo de la vida, conocida como neuroplasticidad, es fundamental para el aprendizaje, la memoria y la resiliencia ante el daño. Esta asombrosa habilidad depende de una compleja red de señales moleculares, entre las que destaca una proteína con un nombre que sugiere su origen principal: el Factor Neurotrófico Derivado del Cerebro, o BDNF (por sus siglas en inglés, Brain-Derived Neurotrophic Factor).

Tradicionalmente asociado con la salud cerebral, investigaciones recientes están revelando que el BDNF no es exclusivo del sistema nervioso central. De hecho, su presencia en otros tejidos, notablemente en el músculo esquelético, está redefiniendo nuestra comprensión de cómo el cuerpo interactúa con el cerebro y cómo actividades como el ejercicio pueden influir en la neuroplasticidad. Este artículo profundiza en la naturaleza del BDNF, sus diferentes formas y, crucialmente, su papel subestimado en el músculo humano y cómo la actividad física lo moviliza, conectando la fuerza de tus músculos con la agilidad de tu mente.
- ¿Qué es el BDNF y por qué es importante?
- El BDNF Más Allá del Cerebro: Un Protagonista Muscular
- Las Fibras Musculares Tipo I: Centros de Producción de Pro-BDNF
- Ejercicio: Un Impulsor del BDNF Circulante
- Lactato, Ayuno y la Regulación del BDNF
- BDNF y su Relevancia en Trastornos Neurológicos y el Estrés
- Comparación: Pro-BDNF vs mBDNF
- Preguntas Frecuentes
- Conclusión
¿Qué es el BDNF y por qué es importante?
El BDNF pertenece a la familia de las neurotrofinas, proteínas que desempeñan un papel vital en el desarrollo, la supervivencia y la función de las neuronas. Es un promotor clave del crecimiento neuronal, la diferenciación celular, la formación de sinapsis (sinaptogénesis) y, en general, de la plasticidad neural. Sin estas funciones, procesos como el aprendizaje y la consolidación de la memoria serían imposibles.
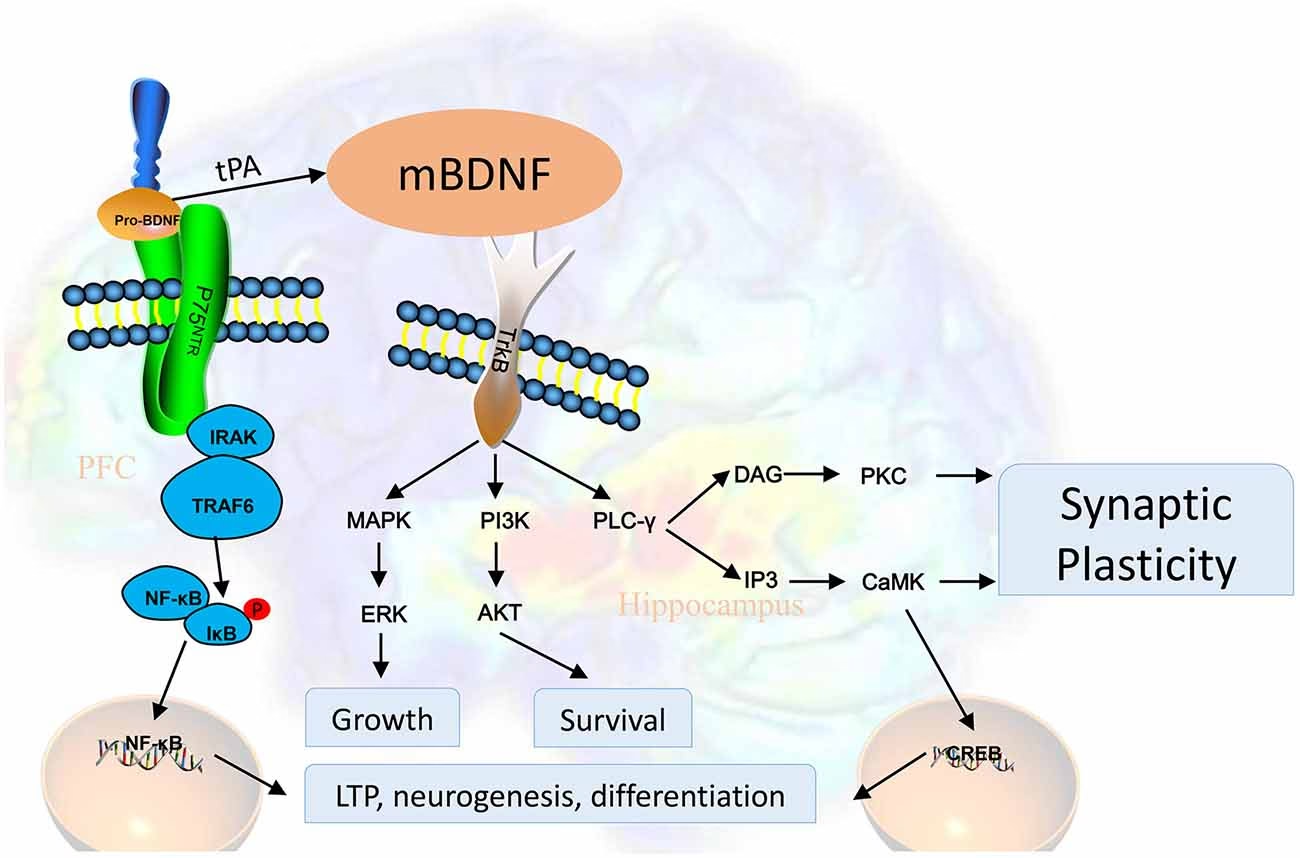
Sin embargo, el BDNF no nace en su forma final. Se sintetiza inicialmente como una isoforma precursora más grande, conocida como pro-BDNF. Esta molécula, con una masa molecular de aproximadamente 28-32 kDa, puede ser escindida (cortada), tanto dentro como fuera de la célula, para generar la forma madura del BDNF (mBDNF), que pesa alrededor de 14 kDa, y un propéptido de 17 kDa. La forma madura es la que convencionalmente se asocia con los efectos promotores de la plasticidad.
La distinción entre pro-BDNF y mBDNF es crucial, ya que no son simplemente precursor y producto. Ambas isoformas son biológicamente activas, pero interactúan con diferentes receptores y pueden tener efectos opuestos. Mientras que la forma madura (mBDNF) se une específicamente al receptor de tirosina quinasa B (TrkB), promoviendo el crecimiento y la supervivencia neuronal, el pro-BDNF se une al receptor p75NTR, el cual, sorprendentemente, se ha relacionado con la apoptosis (muerte celular programada) o un efecto de "poda" neuronal. Esta dualidad sugiere una función de "yin-yang" para las dos isoformas, donde el equilibrio entre pro-BDNF y mBDNF (el ratio BDNF/pro-BDNF) podría ser tan importante como sus niveles absolutos. De hecho, se ha sugerido que este ratio se altera en diversas condiciones neurológicas, como la enfermedad de Alzheimer.
El BDNF Más Allá del Cerebro: Un Protagonista Muscular
Aunque el BDNF está altamente expresado en el sistema nervioso central, su presencia no se limita a él. Se sabe que circula en la sangre, en parte unido a las plaquetas, y que sus niveles séricos son significativamente más altos que los plasmáticos debido a esta unión plaquetaria. Pero, ¿y el músculo esquelético?
Las primeras evidencias de BDNF en músculo surgieron en ratas, donde se detectó ARNm de BDNF. Sin embargo, cuantificar la proteína BDNF en músculo humano ha sido un desafío y un tema de debate. Estudios anteriores han arrojado resultados inconsistentes, a menudo sin distinguir claramente entre las isoformas pro-BDNF y mBDNF.
Una investigación detallada, utilizando diversas técnicas como inmunoblotting, ELISA (ensayo inmunoabsorbente ligado a enzimas), inmunohistoquímica y qPCR (reacción en cadena de la polimerasa cuantitativa), ha arrojado luz sobre este misterio. Los hallazgos son contundentes: el pro-BDNF se expresa de manera consistente y clara en el músculo esquelético humano. Las cantidades medidas por ELISA varían aproximadamente entre 40 y 250 pg por miligramo de músculo seco, lo que indica una presencia significativa.
En contraste, la forma madura (mBDNF) fue difícil o imposible de detectar en las células musculares con las técnicas utilizadas. Incluso con alta carga proteica, los niveles de mBDNF en músculo eran extremadamente bajos, sugiriendo que, bajo condiciones fisiológicas, el músculo esquelético humano contiene principalmente la isoforma precursora, pro-BDNF, y no la forma madura.
Las Fibras Musculares Tipo I: Centros de Producción de Pro-BDNF
El músculo esquelético no es uniforme; está compuesto por diferentes tipos de fibras musculares con distintas características metabólicas y funcionales. Las fibras Tipo I, también conocidas como fibras de contracción lenta u oxidativas, son más resistentes a la fatiga y se utilizan predominantemente en actividades de resistencia y de baja a moderada intensidad. Las fibras Tipo II, o fibras de contracción rápida, son más potentes pero se fatigan más rápido, siendo clave en actividades de alta intensidad.
La investigación revela una sorprendente dependencia del tipo de fibra en la expresión de pro-BDNF. Se encontró que las fibras musculares Tipo I tienen una expresión de pro-BDNF aproximadamente 4 veces mayor que las fibras Tipo II. Esta diferencia se observó consistentemente tanto a nivel de proteína (mediante inmunoblotting e inmunohistoquímica) como a nivel de ARNm (mediante análisis de RNA-seq). Esto sugiere que la mayor tasa de transcripción del gen del BDNF en las fibras Tipo I contribuye a sus niveles proteicos más elevados.
Esta dependencia del tipo de fibra tiene implicaciones significativas. Si el pro-BDNF muscular es relevante para la comunicación músculo-cerebro, entonces la composición de fibras musculares de un individuo, y qué tipo de fibras se activan durante el ejercicio, podrían influir en los niveles de BDNF circulante. Las personas con un mayor porcentaje de fibras Tipo I en sus músculos (comunes en atletas de resistencia) tienden a tener una mayor expresión total de pro-BDNF en el músculo.
Ejercicio: Un Impulsor del BDNF Circulante
Es bien sabido que el ejercicio físico tiene efectos beneficiosos en la salud cerebral y la neuroplasticidad, y se ha sugerido que el BDNF media parte de estos efectos. Estudios previos han demostrado que el ejercicio aumenta los niveles circulantes de BDNF en humanos, y que el cerebro libera BDNF durante la actividad física.
La nueva evidencia sobre la alta expresión de pro-BDNF en el músculo esquelético añade una nueva capa de complejidad a esta relación. La investigación muestra que el ejercicio agudo de resistencia resulta en un aumento tanto en los niveles plasmáticos de mBDNF (aproximadamente un 55%) como de pro-BDNF (aproximadamente un 20%).
Dado que el músculo contiene principalmente pro-BDNF y el ejercicio aumenta los niveles circulantes de ambas isoformas, una hipótesis plausible es que el músculo esquelético libera pro-BDNF a la circulación durante o después del ejercicio. Una vez en el torrente sanguíneo, este pro-BDNF podría ser escindido por proteasas extracelulares para convertirse en mBDNF. La observación de que el aumento de pro-BDNF en plasma a menudo precede o acompaña al aumento de mBDNF es coherente con este mecanismo.
Esto sugiere que el músculo esquelético actúa como una fuente importante de BDNF circulante, particularmente de la isoforma precursora, estableciendo un vínculo directo entre la contracción muscular (especialmente de las fibras Tipo I) y los niveles sistémicos de una molécula clave para la salud cerebral. El ejercicio, al activar estas fibras, moviliza pro-BDNF, que luego podría influir en la plasticidad cerebral.
Lactato, Ayuno y la Regulación del BDNF
Más allá del ejercicio en sí, otros factores metabólicos generados durante la actividad física o estados nutricionales alterados, como el lactato y los cuerpos cetónicos (ej. β-hidroxibutirato o β-HB), han sido propuestos como posibles estimuladores de la producción o liberación de BDNF, especialmente en el cerebro. La investigación exploró si estos factores también influyen en el BDNF muscular o plasmático en humanos.

La infusión de lactato durante el ejercicio de resistencia elevó significativamente los niveles plasmáticos de lactato. Interesantemente, esta elevación adicional de lactato resultó en un aumento aún mayor en los niveles plasmáticos de mBDNF (un 115% de aumento respecto al reposo, significativamente más que el 55% observado solo con ejercicio y solución salina), sin afectar los niveles de pro-BDNF en plasma o músculo. Esto sugiere que, si bien el lactato puede potenciar el aumento de mBDNF circulante, es probable que lo haga a través de un mecanismo que no implique un aumento en la liberación de pro-BDNF desde el músculo. Podría, por ejemplo, estimular la liberación de mBDNF directamente desde el cerebro u otros tejidos, o facilitar la escisión de pro-BDNF ya presente en la circulación.
Por otro lado, un período de ayuno de 3 días, que provoca un aumento considerable en los niveles plasmáticos de β-HB (aproximadamente 10 veces), tuvo un efecto limitado en los niveles de BDNF. Se observó un pequeño aumento (10-13%) en el pro-BDNF plasmático, pero no hubo cambios significativos en el mBDNF plasmático. La respuesta al ayuno fue similar independientemente de la composición de fibras musculares del individuo. Estos hallazgos sugieren que, aunque el β-HB puede influir en el BDNF en otros contextos (como se ha visto en modelos animales para el BDNF cerebral), no parece ser un regulador importante del metabolismo del BDNF muscular o de sus niveles plasmáticos en respuesta al ayuno en humanos, al menos en comparación con el impacto del ejercicio.
BDNF y su Relevancia en Trastornos Neurológicos y el Estrés
La importancia del BDNF va más allá de la plasticidad general; está implicado en la respuesta al estrés, la formación de recuerdos (particularmente los asociados al miedo) y en la capacidad de extinguir respuestas de miedo inapropiadas. Interacciona con las hormonas del estrés y se cree que juega un papel clave en la vulnerabilidad o resiliencia a trastornos inducidos por el estrés y el trauma, como el Trastorno de Estrés Postraumático (PTSD).
Se ha observado que el BDNF influye tanto en la consolidación de las experiencias de miedo como en el aprendizaje de extinción exitoso (la capacidad de aprender que un estímulo previamente temido ya no es peligroso). Un desequilibrio en el sistema BDNF podría contribuir a la persistencia de recuerdos traumáticos y a la dificultad para superarlos. La implicación del BDNF en diversas enfermedades neuropsiquiátricas y neurológicas, como la depresión clínica, la enfermedad de Alzheimer y la esclerosis lateral amiotrófica, subraya su papel central en la salud del sistema nervioso.
Con la evidencia de que el músculo esquelético es una fuente significativa de pro-BDNF y que el ejercicio modula sus niveles circulantes, se refuerza la idea de que la actividad física no solo beneficia al cuerpo, sino que también impacta directamente en el cerebro a través de mediadores moleculares como el BDNF. Esto abre nuevas vías para entender cómo el ejercicio puede ser una herramienta terapéutica o preventiva en el manejo de trastornos neurológicos y psiquiátricos.
Comparación: Pro-BDNF vs mBDNF
| Característica | Pro-BDNF | mBDNF (BDNF Madura) |
|---|---|---|
| Masa Molecular | ~28-32 kDa | ~14 kDa |
| Forma | Precursora | Madura |
| Receptor Principal | p75NTR | TrkB |
| Efecto Principal (en neuronas) | Poda/Apoptosis (generalmente) | Crecimiento/Plasticidad (generalmente) |
| Expresión en Músculo Humano | Alta y detectable | Muy baja o indetectable |
| Aumento en Plasma por Ejercicio | Moderado (~20%) | Significativo (~55%, potenciado por lactato) |
Preguntas Frecuentes
Q: ¿Qué es el BDNF?
A: El BDNF es una proteína (neurotrofina) esencial para el crecimiento, la supervivencia y la función de las neuronas, y es clave para la neuroplasticidad, el aprendizaje y la memoria.
Q: ¿Cuál es la diferencia entre pro-BDNF y mBDNF?
A: El pro-BDNF es la forma precursora inactiva (o con efectos diferentes) que se sintetiza primero. El mBDNF es la forma madura y activa resultante de la escisión del pro-BDNF. Tienen diferentes pesos moleculares y se unen a distintos receptores con efectos a veces opuestos.
Q: ¿Por qué es importante que el BDNF esté en el músculo?
A: La presencia significativa de pro-BDNF en el músculo esquelético, especialmente en las fibras Tipo I, sugiere que el músculo actúa como una fuente de esta molécula. La actividad muscular, como el ejercicio, puede liberar pro-BDNF a la circulación, influyendo así en los niveles sistémicos y, potencialmente, en la salud cerebral.
Q: ¿Cómo influye el ejercicio en los niveles de BDNF?
A: El ejercicio agudo aumenta los niveles circulantes tanto de pro-BDNF como de mBDNF. Se cree que el músculo libera pro-BDNF, que luego puede convertirse en mBDNF en la sangre. Este aumento de BDNF circulante puede contribuir a los beneficios del ejercicio en la función cerebral y la plasticidad.
Q: ¿El tipo de ejercicio importa para el BDNF muscular?
A: Dado que el pro-BDNF es mucho más abundante en las fibras musculares Tipo I (activadas en ejercicio de resistencia), las actividades que reclutan predominantemente estas fibras podrían ser particularmente efectivas para aumentar la liberación de pro-BDNF muscular.
Q: ¿El lactato o el ayuno afectan el BDNF?
A: La infusión de lactato durante el ejercicio potencia el aumento de mBDNF plasmático, aunque no parece afectar el pro-BDNF muscular. Un ayuno de 3 días que aumenta el β-HB causa un pequeño aumento en el pro-BDNF plasmático, pero no en el mBDNF, sugiriendo efectos limitados en este contexto.
Conclusión
La investigación reciente está redefiniendo nuestra comprensión del BDNF, demostrando que su influencia se extiende significativamente más allá del cerebro. El músculo esquelético humano emerge como un actor crucial en este panorama, albergando cantidades sustanciales de la isoforma precursora, pro-BDNF, predominantemente en las fibras Tipo I. El ejercicio físico actúa como un potente estímulo, aumentando los niveles circulantes de pro-BDNF y mBDNF, sugiriendo un mecanismo por el cual la contracción muscular puede comunicarse con el cerebro y promover la neuroplasticidad.
Estos hallazgos no solo profundizan nuestro conocimiento de la fisiología del BDNF, sino que también refuerzan la importancia crítica del músculo esquelético como un órgano endocrino activo en la señalización neuroplástica. La conexión entre el músculo que se mueve y el cerebro que se adapta a través de moléculas como el BDNF subraya aún más el valor del ejercicio para mantener y mejorar la salud cerebral a lo largo de la vida. Comprender mejor estos mecanismos podría abrir nuevas vías terapéuticas para abordar una amplia gama de trastornos neurológicos y psiquiátricos.
Si quieres conocer otros artículos parecidos a BDNF: El Músculo, Clave de Neuroplasticidad puedes visitar la categoría Neurociencia.