En el complejo universo de nuestras células cerebrales, las neuronas dependen de una intrincada red de estructuras internas para funcionar correctamente. Entre ellas, los microtúbulos actúan como vías férreas cruciales para el transporte de materiales a lo largo de los axones, las largas extensiones que las neuronas utilizan para comunicarse. Una proteína fundamental asociada a estos microtúbulos es la proteína Tau.
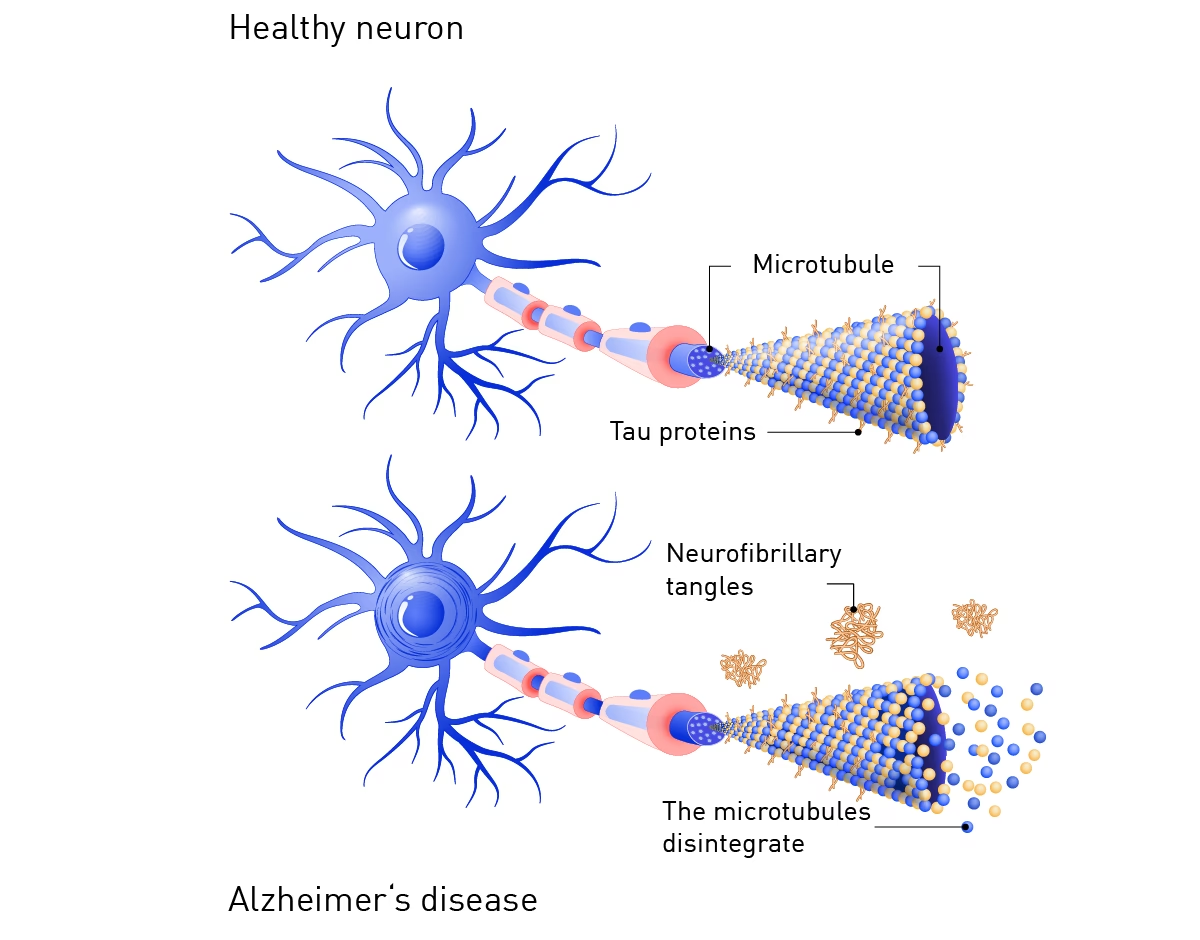
Durante mucho tiempo, se ha sabido que la Tau se localiza principalmente en el axón, desempeñando un papel vital en la estabilización de los microtúbulos. Sin embargo, los mecanismos exactos de cómo logra esta localización específica, especialmente durante el desarrollo neuronal, han sido un enigma. Investigaciones recientes arrojan luz sobre este proceso, revelando hallazgos sorprendentes que desafían algunas ideas preconcebidas y abren nuevas vías para comprender enfermedades neurodegenerativas como el Alzheimer.
La Localización de Tau en el Axón: Un Proceso Dinámico
La localización preferencial de la proteína Tau en el axón es un rasgo distintivo de las neuronas maduras. Esta distribución asimétrica es crucial para la función axonal normal, incluyendo el transporte axonal, la plasticidad sináptica y la polaridad neuronal. Tradicionalmente, se pensaba que esta localización dependía en gran medida del transporte activo a lo largo de los microtúbulos y de un mecanismo de 'filtro' en el segmento inicial del axón (AIS) que impedía que Tau entrara en el soma y las dendritas.
Estudios más detallados utilizando neuronas de hipocampo de rata cultivadas han observado que la localización axonal de Tau ocurre predominantemente durante las primeras etapas del desarrollo neuronal. Utilizando anticuerpos capaces de detectar Tau total, independientemente de su estado de fosforilación, se ha confirmado que la Tau endógena se acumula en los axones distales ya en las neuronas en estadio 3 (2-3 días in vitro, DIV), volviéndose más marcada en estadio 4 (4-5 DIV) y restringiéndose casi por completo al axón en neuronas maduras (16 DIV). Este proceso comienza pronto, incluso antes de la madurez completa.
Un desafío significativo para los investigadores ha sido replicar esta localización axonal en modelos experimentales, particularmente al expresar Tau exógena. Cuando Tau se expresa de forma constitutiva en neuronas cultivadas, a menudo se distribuye de manera uniforme por toda la célula, incluyendo el soma y las dendritas, lo que se conoce como 'mislocalización'. Esto dificultaba el estudio preciso de los mecanismos de localización axonal.
Sin embargo, un hallazgo clave en investigaciones recientes es que la expresión transitoria de Tau exógena en neuronas muy inmaduras, imitando el patrón de expresión de la Tau endógena durante el desarrollo, sí logra su correcta localización en el axón. Esto sugiere que existe una ventana temporal crítica durante el desarrollo neuronal para la correcta localización de Tau.
Mecanismos Inesperados de Localización
Utilizando este nuevo modelo experimental, se han descubierto aspectos sorprendentes sobre cómo Tau llega al axón. Contrario a lo esperado, la localización axonal de Tau no requirió una unión estable a los microtúbulos. De hecho, una forma de Tau a la que se le eliminó el dominio de unión a microtúbulos (MTBD) mostró una alta difusividad pero aún así se localizó correctamente en el axón. Esto es un hallazgo notable, ya que el MTBD es la región tradicionalmente asociada con la interacción de Tau con los microtúbulos.
Por otro lado, una mutación en la región rica en prolina 2 de Tau, que imita la desfosforilación en ciertos sitios, resultó en una unión reforzada a los microtúbulos y, paradójicamente, en una mislocalización en el soma y las dendritas. Estos resultados sugieren que una unión demasiado fuerte o estable a los microtúbulos podría en realidad impedir que Tau entre o se mantenga en el axón, contribuyendo a su mislocalización en otras partes de la neurona, especialmente cuando se expresa en neuronas maduras.
Esta investigación propone un nuevo mecanismo para la localización axonal de Tau que es independiente de su dominio de unión a microtúbulos en el sentido tradicional, y que parece estar influenciado por el estado de fosforilación y posiblemente por la interacción con otras proteínas o estructuras dentro de la neurona en desarrollo. Comprender estos mecanismos es vital, no solo para entender la neurobiología básica, sino también porque la mislocalización de Tau y su agregación patológica son características centrales de la enfermedad de Alzheimer y otras tauopatías.
Tau y la Enfermedad de Alzheimer: Un Objetivo Terapéutico Clave
La enfermedad de Alzheimer (EA) es el tipo de demencia más común, caracterizada por la pérdida progresiva de memoria y el deterioro cognitivo. Neuropatológicamente, la EA se define por la acumulación de placas de proteína amiloide-beta en el espacio extracelular y la formación de ovillos neurofibrilares intracelulares, compuestos principalmente por la proteína Tau hiperfosforilada y agregada. Si bien la hipótesis amiloide ha dominado la investigación durante décadas, los ensayos clínicos dirigidos únicamente a eliminar el amiloide han tenido resultados decepcionantes.
Cada vez hay más evidencia que sugiere que la disfunción de la proteína Tau está más estrechamente correlacionada con la gravedad de la demencia que la carga de amiloide. Los ovillos neurofibrilares se acumulan de manera que sigue la progresión de los síntomas cognitivos, comenzando en las regiones relacionadas con la memoria y extendiéndose a otras áreas del cerebro a medida que la enfermedad avanza. Esto ha llevado a un cambio de enfoque, haciendo de la proteína Tau un objetivo terapéutico muy prometedor.
Estrategias Terapéuticas Dirigidas a Tau
El desarrollo de terapias dirigidas a Tau es complejo, ya que Tau es una proteína intracelular y tiene múltiples modificaciones post-traduccionales (como fosforilación, acetilación, truncamiento) que pueden influir en su función y patología. A pesar de los desafíos, varias estrategias están siendo investigadas y probadas en ensayos clínicos:
Prevención de Modificaciones Post-Traduccionales Patológicas: La hiperfosforilación es un paso clave en la formación de ovillos. Inhibir las enzimas (quinasas) que fosforilan Tau o activar las que la desfosforilan podría ser beneficioso. La GSK-3 (glucógeno sintasa quinasa-3) y la Fyn quinasa son ejemplos de quinasas objetivo. Sustancias como Tideglusib (inhibidor de GSK-3) o Saracatinib (inhibidor de Fyn) han estado en ensayos, aunque con resultados mixtos o en etapas tempranas. La acetilación patológica de Tau también es un objetivo, con inhibidores de acetiltransferasa como Salsalate en estudio.
Prevención de la Desestabilización de Microtúbulos: Los oligómeros de amiloide y la Tau patológica pueden desestabilizar los microtúbulos. Estabilizar estas estructuras neuronales podría preservar la función axonal. Epothilone D y Abeotaxane son ejemplos de estabilizadores de microtúbulos que se han probado en ensayos clínicos, aunque su desarrollo para la EA ha enfrentado dificultades.
Inhibición de la Agregación de Tau: Evitar que las moléculas de Tau se agreguen en ovillos patológicos es otra estrategia. Sustancias como el cloruro de metiltioninio y sus derivados (como el leuco-metiltioninio bis) han mostrado capacidad para inhibir la agregación de Tau in vitro y en modelos animales, pero los ensayos clínicos en EA no han demostrado beneficios significativos hasta ahora, aunque se sigue investigando.
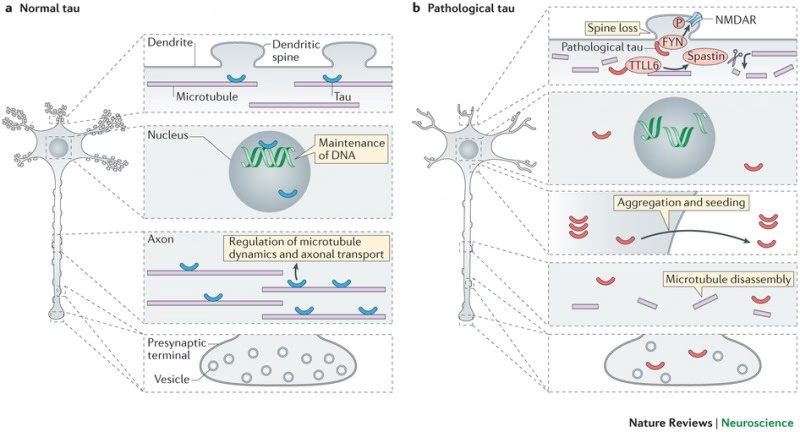
Tau is a microtubule (MT)-associated protein (MAP) that is thought to be localized in the axon of a neuron in normal physiological conditions (Binder et al., 1985; Peng et al., 1986; Brion et al., 1988; Migheli et al., 1988; Trojanowski et al., 1989). Inmunoterapia Dirigida a Tau: Esta estrategia busca utilizar el sistema inmunológico del paciente para eliminar la Tau patológica. Hay dos enfoques principales:
Inmunización Activa (Vacunas): Se administra un fragmento de Tau (o un péptido que lo imita) para estimular al sistema inmune del paciente a producir anticuerpos contra la Tau patológica. AADvac-1 y ACI-35 son vacunas en desarrollo. Los primeros resultados de AADvac-1 han sido prometedores en cuanto a seguridad e inmunogenicidad, sugiriendo una correlación entre niveles de anticuerpos y menor progresión.
Inmunización Pasiva (Anticuerpos Monoclonales): Se administran directamente anticuerpos pre-fabricados que se unen a Tau patológica para marcarla y facilitar su eliminación. Varios anticuerpos dirigidos a diferentes partes de Tau (como el extremo N-terminal o regiones específicas) están en ensayos clínicos (ej. BIIB092, ABBV-8E12, RO7105705). La inmunoglobulina intravenosa (IVIg), que contiene anticuerpos policlonales, también ha sido probada, aunque sin éxito claro en ensayos a gran escala.
Desafíos y Perspectivas Futuras
A pesar del optimismo, el desarrollo de terapias dirigidas a Tau enfrenta múltiples desafíos. Uno de los principales es que Tau patológica se acumula principalmente dentro de las neuronas, lo que dificulta el acceso de muchos fármacos, particularmente los anticuerpos de gran tamaño, que pueden tener problemas para cruzar la barrera hematoencefálica y entrar en las células. Apuntar a formas extracelulares de Tau (que se cree que se propagan entre neuronas de manera similar a los priones) o desarrollar anticuerpos más pequeños o fragmentos de anticuerpos podría mejorar la entrega.
Otro desafío crucial es la complejidad de la propia proteína Tau y su patología. Tau sufre diversas modificaciones, puede existir en diferentes conformaciones patológicas ('cepas'), y su toxicidad puede no estar ligada únicamente a la agregación visible en ovillos. Comprender mejor qué formas de Tau son más tóxicas y en qué momento de la enfermedad son más relevantes es fundamental para diseñar terapias efectivas.
Además, los ensayos clínicos deben mejorar. Es necesario seleccionar a los pacientes en las etapas más tempranas de la enfermedad (incluso antes de los síntomas evidentes), ya que el daño neuronal masivo ya ha ocurrido cuando aparecen los síntomas clínicos. También se requieren diseños de estudio más robustos, con grupos de control adecuados y medidas de resultado sensibles que evalúen tanto la patología como la función cognitiva.
Preguntas Frecuentes sobre la Proteína Tau
¿Qué es la proteína Tau? Es una proteína asociada a los microtúbulos, estructuras que forman el citoesqueleto de las neuronas, especialmente importante en el axón.
¿Cuál es la función normal de Tau? Su función principal es estabilizar los microtúbulos neuronales y facilitar el transporte de sustancias a lo largo del axón.
¿Cómo se relaciona Tau con la enfermedad de Alzheimer? En el Alzheimer, Tau se modifica anormalmente (hiperfosforilación, etc.), se pliega de forma incorrecta y se agrega para formar ovillos neurofibrilares dentro de las neuronas. Esta patología de Tau está fuertemente vinculada al daño neuronal y al deterioro cognitivo.
¿Por qué se investigan terapias dirigidas a Tau para el Alzheimer? Dado que la patología de Tau se correlaciona bien con la gravedad de la demencia y que las terapias dirigidas a la proteína amiloide no han tenido éxito claro, Tau se considera un objetivo terapéutico prometedor para ralentizar o detener la progresión de la enfermedad.
¿Qué tipos de terapias dirigidas a Tau existen? Se están desarrollando y probando terapias que buscan prevenir las modificaciones patológicas de Tau, evitar su agregación, estabilizar los microtúbulos o utilizar la inmunoterapia (vacunas o anticuerpos) para eliminar la Tau patológica.
¿Ya hay medicamentos dirigidos a Tau aprobados para el Alzheimer? No, actualmente no hay medicamentos específicamente dirigidos a la patología de Tau que estén aprobados para el tratamiento del Alzheimer. Las terapias existentes solo ofrecen un alivio sintomático temporal. La investigación en este campo está en etapas tempranas, pero es muy activa.
La investigación sobre la proteína Tau, tanto en su función normal de localización axonal como en su papel patológico en el Alzheimer, está en constante evolución. Los nuevos conocimientos sobre los mecanismos de localización de Tau y el desarrollo de diversas estrategias terapéuticas dirigidas a esta proteína son pasos cruciales hacia la comprensión y el eventual tratamiento de enfermedades neurodegenerativas que afectan a millones de personas en todo el mundo.
Si quieres conocer otros artículos parecidos a La Proteína Tau: Guardián del Axón y Objetivo en el Alzheimer puedes visitar la categoría Neurociencia.
