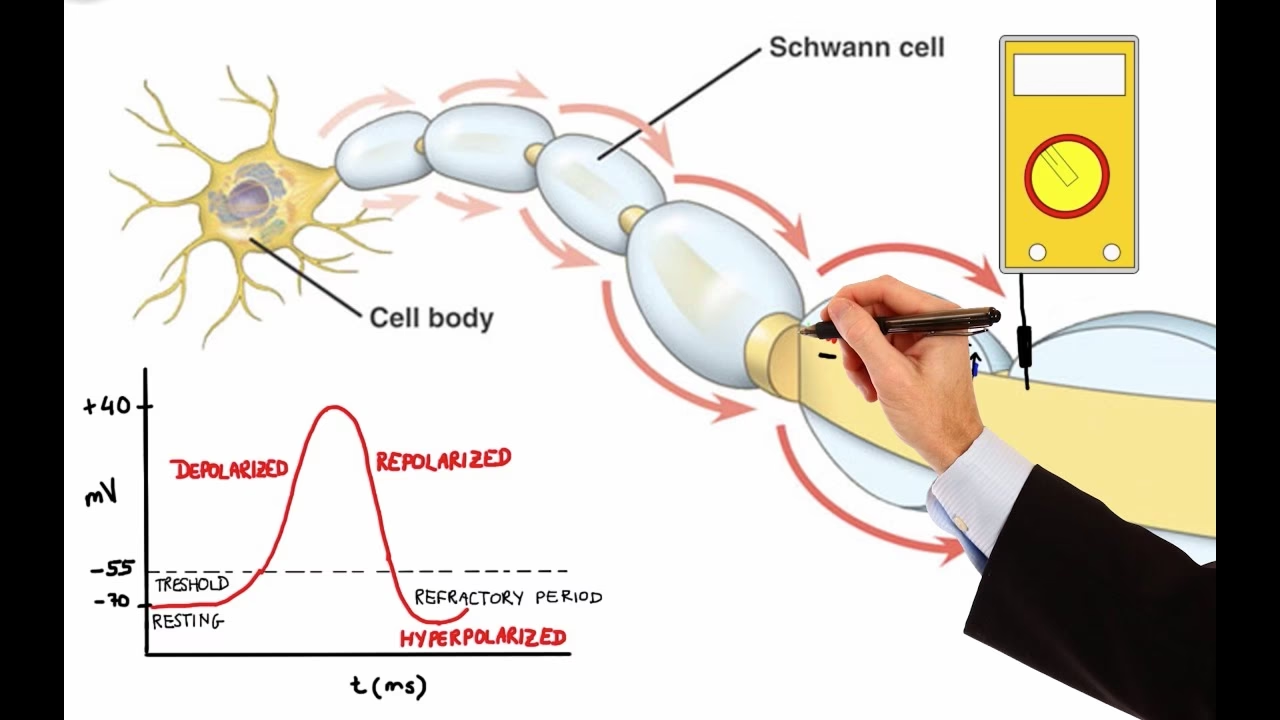
Nuestro cuerpo funciona gracias a una compleja red de comunicación eléctrica. En el corazón de esta red se encuentran los potenciales de acción, breves y rápidos cambios en el voltaje a través de la membrana de células excitables como las neuronas, las células musculares y las células cardíacas especializadas. Estos impulsos eléctricos son fundamentales para todo, desde pensar y mover un dedo hasta el latido constante de nuestro corazón. Sin embargo, la pregunta sobre si un potencial de acción alcanza los 30 o los 40 milivoltios (mV) revela una fascinante verdad: no todos los potenciales de acción son iguales. Sus características, incluyendo el umbral para activarse y el pico que alcanzan, varían significativamente dependiendo del tipo de célula y los mecanismos iónicos involucrados.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
Para entender esta variación, debemos sumergirnos en el funcionamiento de la membrana celular y los canales iónicos que actúan como compuertas controladas por voltaje.
- ¿Qué es un Potencial de Acción?
- El Potencial de Acción Neuronal: La Chispa del Cerebro
- El Potencial de Acción Cardíaco: El Ritmo del Corazón
- Comparando los Potenciales: Neuronas vs. Marcapasos Cardíaco
- El Principio de Todo o Nada
- Codificación por Frecuencia (Neuronal)
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es un Potencial de Acción?
En su esencia, un Potencial de Acción es una inversión transitoria y rápida del potencial de membrana. Normalmente, las células excitables mantienen un potencial de reposo negativo (el interior de la célula es más negativo que el exterior). Cuando un estímulo suficiente alcanza un nivel crítico, conocido como Umbral, se desencadena un potencial de acción. Este evento es de naturaleza 'todo o nada': si el estímulo no alcanza el umbral, no hay potencial de acción; si lo alcanza o lo supera, se genera un potencial de acción completo de amplitud constante para ese tipo celular, independientemente de cuán fuerte sea el estímulo por encima del umbral.
La generación y propagación de los potenciales de acción permiten transmitir información a largas distancias a lo largo de las células nerviosas (neuronas) o coordinar la contracción en el músculo cardíaco.
El Potencial de Acción Neuronal: La Chispa del Cerebro
Las neuronas son el ejemplo clásico de células que utilizan potenciales de acción para comunicarse. Su potencial de reposo se sitúa típicamente entre -40 mV y -80 mV, a menudo alrededor de -60 mV en muchas neuronas del cerebro. Este potencial de reposo negativo se debe principalmente a la distribución desigual de iones a través de la membrana celular y a la mayor permeabilidad de la membrana al potasio (K+) en comparación con otros iones como el sodio (Na+).
El interior de la célula tiene una alta concentración de K+ y una baja concentración de Na+, mientras que el exterior es lo opuesto. Los canales de potasio que están abiertos en reposo permiten que el K+ salga de la célula (a favor de su gradiente de concentración), dejando cargas negativas en el interior. La ligera permeabilidad al Na+ en reposo permite una pequeña entrada de Na+, lo que hace que el potencial de reposo sea ligeramente menos negativo de lo que sería si solo dependiera del K+. La ecuación de Goldman-Hodgkin-Katz describe cómo las permeabilidades y concentraciones de múltiples iones (principalmente K+ y Na+ en reposo) determinan el potencial de membrana.
Cuando una neurona recibe un estímulo (por ejemplo, de otra neurona), su potencial de membrana comienza a despolarizarse (volverse menos negativo). Si esta despolarización alcanza el Umbral (típicamente alrededor de -55 mV, aunque varía), se desencadena un potencial de acción.
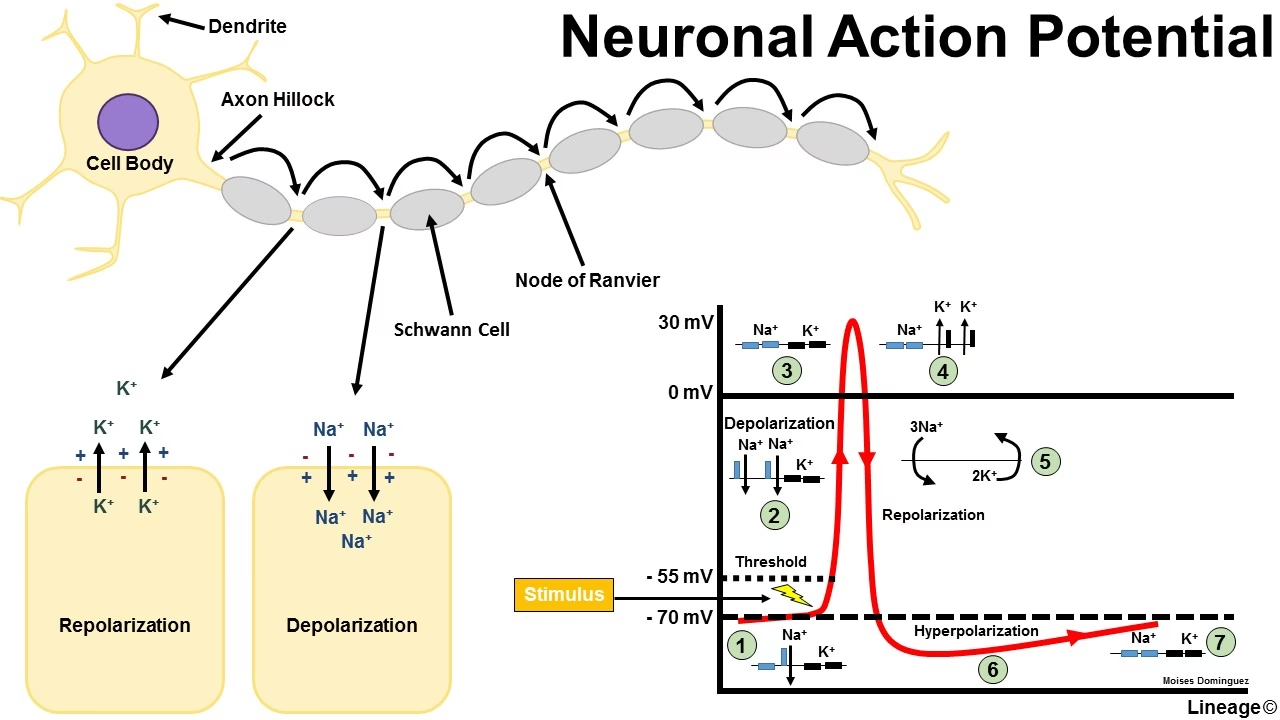
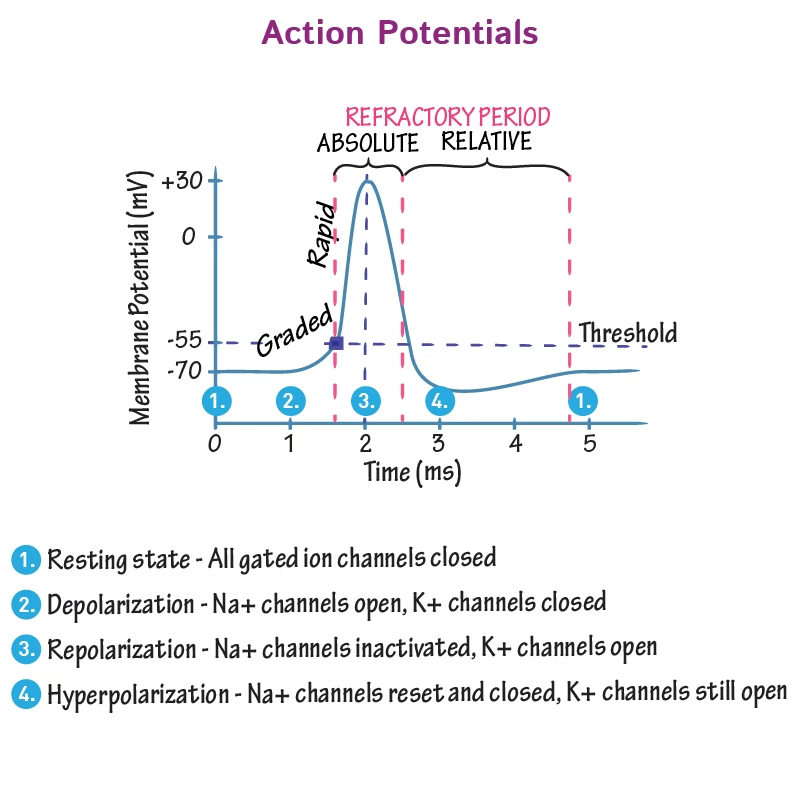
Las fases del potencial de acción Neuronal son:
- Fase Ascendente (Despolarización): Al alcanzar el umbral, se abren de forma masiva los canales de sodio (Na+) dependientes de voltaje. El Na+ entra rápidamente en la célula (influjo), impulsado tanto por su gradiente de concentración como por la carga negativa interna. Este rápido influjo de cargas positivas causa una despolarización veloz, llevando el potencial de membrana desde el umbral hasta un pico positivo.
- Pico: El potencial de membrana alcanza su valor máximo, que en muchas neuronas es de aproximadamente +30 mV. En este punto, los canales de Na+ dependientes de voltaje comienzan a inactivarse y cerrarse.
- Fase Descendente (Repolarización): Casi al mismo tiempo que los canales de Na+ se inactivan, se abren los canales de potasio (K+) dependientes de voltaje. El K+ sale de la célula (eflujo), llevando cargas positivas hacia el exterior. Esto hace que el potencial de membrana regrese rápidamente hacia valores negativos.
- Hiperpolarización (o Periodo Refractario): Los canales de K+ dependientes de voltaje son relativamente lentos para cerrarse. Por lo tanto, la salida de K+ continúa por un breve tiempo después de que el potencial de membrana ha alcanzado el potencial de reposo. Esto causa que el potencial de membrana se vuelva temporalmente más negativo que el potencial de reposo, un estado conocido como hiperpolarización o post-potencial hiperpolarizante. Finalmente, los canales de K+ se cierran, y la actividad de la bomba sodio-potasio ayuda a restablecer las concentraciones iónicas a largo plazo.
La velocidad de la fase de despolarización neuronal, y por lo tanto la duración total del potencial de acción (alrededor de 1 milisegundo), se debe a la apertura *rápida* de los canales de Na+ dependientes de voltaje.

Las neuronas codifican la intensidad de un estímulo mediante la *frecuencia* de los potenciales de acción, no por su amplitud. Un estímulo más fuerte provoca una mayor frecuencia de disparo de potenciales de acción.
El Potencial de Acción Cardíaco: El Ritmo del Corazón
Las células marcapasos del corazón, ubicadas principalmente en el Nódulo SA (sinoauricular) y el nódulo AV (auriculoventricular), tienen una propiedad única: generan potenciales de acción de forma espontánea y rítmica, sin necesidad de un estímulo externo. A diferencia de las neuronas, estas células no tienen un verdadero potencial de reposo estable.
El potencial de acción en las células marcapasos cardíacas es diferente al neuronal, a menudo llamado respuesta lenta. Sus fases son:
- Fase 4 (Potencial de Marcapasos o Despolarización Espontánea): Después de la repolarización completa (alrededor de -60 mV), la membrana comienza a despolarizarse lentamente por sí sola. Esta despolarización espontánea se debe a varios factores: la apertura de canales iónicos especiales que conducen una lenta corriente de entrada de Na+ (conocida como la "corriente divertida" o Corriente If), la apertura de canales de calcio (Ca++) de tipo T (transitorio) a medida que la membrana se despolariza ligeramente (alrededor de -50 mV), y una disminución gradual en la salida de K+ debido al cierre de los canales de K+ responsables de la repolarización anterior.
- Umbral: La despolarización espontánea de la Fase 4 continúa hasta que el potencial de membrana alcanza el Umbral, que en las células del nódulo SA está entre -40 y -30 mV. Este umbral es menos negativo que el de las neuronas.
- Fase 0 (Despolarización): Al alcanzar el umbral, se abren Canales de Calcio tipo L (de larga duración) dependientes de voltaje. El influjo de Ca++ a través de estos canales es la principal corriente despolarizante. A diferencia de las neuronas que usan Na+ rápido, el influjo de Ca++ es más lento, lo que resulta en una fase de despolarización menos pronunciada (pendiente más lenta) en comparación con los potenciales de acción neuronales.
- Fase 3 (Repolarización): Los canales de Ca++ tipo L comienzan a inactivarse y cerrarse. Simultáneamente, se abren los canales de potasio (K+) dependientes de voltaje, permitiendo la salida de K+ (eflujo). Este eflujo de K+ repolariza la membrana, devolviéndola a su potencial más negativo (alrededor de -60 mV), momento en el cual comienza una nueva Fase 4, reiniciando el ciclo.
La velocidad de conducción de estos potenciales de acción es más lenta que en las neuronas, lo cual es importante para la función del nódulo AV en retrasar la señal eléctrica entre las aurículas y los ventrículos.
Comparando los Potenciales: Neuronas vs. Marcapasos Cardíaco
La confusión sobre si el potencial de acción es 30 o 40 mV surge de la comparación de dos tipos celulares muy diferentes. El +30 mV se refiere al pico positivo alcanzado por un potencial de acción neuronal, impulsado por el rápido influjo de Na+. El rango de -40 a -30 mV se refiere al umbral más positivo requerido para desencadenar el potencial de acción en las células marcapasos cardíacas, cuya despolarización inicial es más lenta y depende del Ca++.
| Característica | Neuronal | Marcapasos Cardíaco (Nódulo SA) |
|---|---|---|
| Propiedad Fundamental | Potencial de reposo estable, activado por estímulo | No tiene potencial de reposo estable, despolarización espontánea |
| Potencial de Reposo / Potencial Máximo Diastólico | -40 a -80 mV (Ej: -60 mV) | Alrededor de -60 mV (punto más negativo) |
| Umbral | Alrededor de -55 mV | Entre -40 y -30 mV |
| Ion Principal de la Fase Despolarizante (Fase 0) | Na+ rápido | Ca++ lento (Canales tipo L) |
| Velocidad de la Fase Despolarizante | Muy rápida | Lenta |
| Pico del Potencial de Acción | Alrededor de +30 mV | Varía, pero generalmente más bajo que en neuronas (no alcanza +30 mV) |
| Repolarización | Eflujo de K+ | Eflujo de K+, inactivación de canales de Ca++ tipo L |
| Post-potencial | Hiperpolarización (undershoot) | Comienza la despolarización espontánea (Fase 4) |
| Propósito Primario | Transmisión rápida de información | Generación de ritmo cardíaco autónomo |
El Principio de Todo o Nada
A pesar de sus diferencias, tanto los potenciales de acción neuronales como los del nódulo SA comparten el principio de Todo o Nada. Una vez que el potencial de membrana alcanza el umbral, se activan suficientes canales iónicos dependientes de voltaje de manera coordinada para generar la respuesta completa. Un estímulo más fuerte no produce un potencial de acción más grande, solo afecta la *probabilidad* de alcanzar el umbral (en neuronas) o la *velocidad* de despolarización de la fase 4 (en células marcapasos, influenciada por factores externos como el sistema nervioso autónomo), lo que a su vez afecta la frecuencia de disparo.
Codificación por Frecuencia (Neuronal)
Una característica clave de la comunicación Neuronal es la codificación de la intensidad del estímulo mediante la frecuencia de los potenciales de acción. Un estímulo débil por encima del umbral puede generar una baja frecuencia de potenciales de acción, mientras que un estímulo fuerte generará una alta frecuencia de potenciales de acción. Esta frecuencia es lo que transmite la información sobre la intensidad al sistema nervioso central.
Preguntas Frecuentes (FAQ)
¿Por qué el potencial de reposo es negativo?
Se debe a la distribución desigual de iones a través de la membrana celular (más K+ dentro, más Na+ fuera) y a la mayor permeabilidad de la membrana al K+ en reposo. La salida de K+ deja un exceso de cargas negativas en el interior.
¿Qué causa el umbral?
El umbral es el voltaje crítico en el que una despolarización abre una cantidad suficiente de canales iónicos (Na+ en neuronas, Ca++ en nódulo SA) dependientes de voltaje para que el influjo de iones positivos se vuelva autogenerativo y supere la salida de iones positivos, impulsando una despolarización rápida.
¿Por qué el potencial de acción es "todo o nada"?
Porque una vez que se alcanza el umbral, la apertura de los canales iónicos dependientes de voltaje es un proceso regenerativo. La entrada de iones positivos despolariza aún más la membrana, lo que abre *más* canales dependientes de voltaje, creando un ciclo de retroalimentación positiva que impulsa el potencial de acción hasta su pico máximo para ese tipo celular.
¿Son todos los potenciales de acción iguales?
No. Varían en forma, duración, umbral y los iones principales involucrados en la despolarización, dependiendo del tipo de célula excitable (neuronas, diferentes tipos de células musculares, células marcapasos cardíacas, etc.).
¿Cuál es la principal diferencia iónica en la despolarización entre una neurona y una célula marcapasos del nódulo SA?
La despolarización rápida (Fase 0) en las neuronas es causada principalmente por el influjo rápido de Na+ a través de canales de Na+ dependientes de voltaje. En las células marcapasos del nódulo SA, la despolarización (Fase 0) es causada principalmente por el influjo más lento de Ca++ a través de canales de Ca++ tipo L dependientes de voltaje.
Conclusión
Los potenciales de acción son los pulsos eléctricos fundamentales que permiten la comunicación y la función en las células excitables. La aparente discrepancia entre 30 y 40 mV se resuelve al comprender que estos valores se refieren a diferentes aspectos (pico vs. umbral) de potenciales de acción distintos en tipos celulares diferentes: el pico de +30 mV en neuronas impulsado por sodio, y el umbral de -40 a -30 mV en células marcapasos cardíacas impulsado por calcio. Estudiar estos impulsos no solo revela los mecanismos biofísicos de la vida a nivel celular, sino que también subraya la elegante diversidad de las señales eléctricas que orquestan las funciones de nuestro complejo organismo, desde el pensamiento hasta el latido constante del corazón.
Si quieres conocer otros artículos parecidos a El Potencial de Acción: Mucho Más Que Un Número puedes visitar la categoría Neurociencia.