Las enfermedades que afectan el cerebro y alteran funciones cognitivas, intelectuales, el comportamiento, el estado de ánimo, la memoria, la percepción de la realidad y la función social son extraordinariamente complejas. Lamentablemente, para muchas de ellas, no existen estrategias preventivas ni terapéuticas uniformemente efectivas. Esta amplia y diversa gama de dolencias humanas, que incluye trastornos del neurodesarrollo (como el trastorno del espectro autista), enfermedades neurodegenerativas (como el Alzheimer, Parkinson, ELA) y trastornos neuropsiquiátricos (como la esquizofrenia, el trastorno bipolar, la depresión mayor), representa una carga sustancial para la salud a nivel mundial.
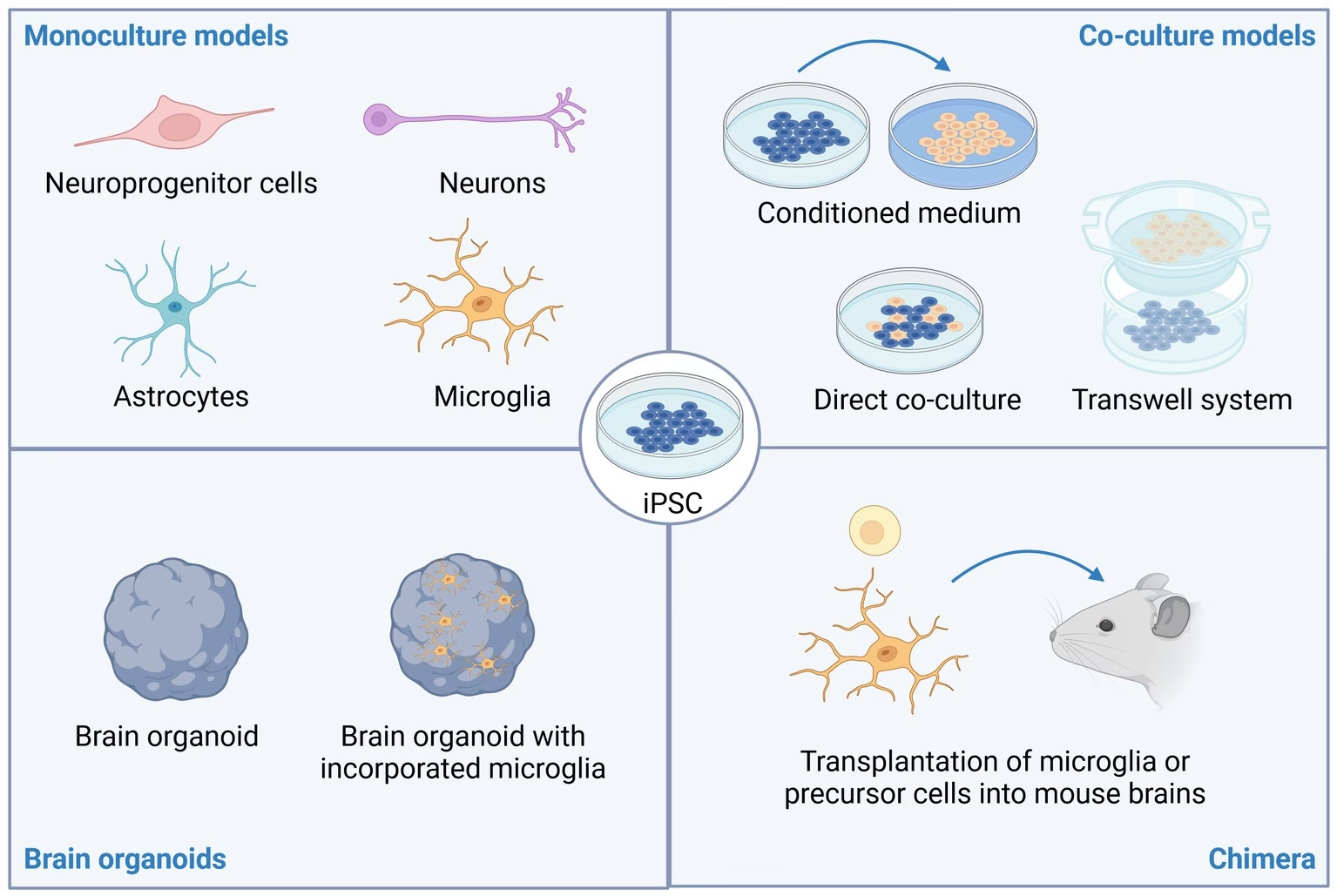
Los avances en genómica han mejorado nuestra comprensión de la base genética de estas enfermedades, pero los mecanismos neurobiológicos críticos involucrados en su origen y progresión aún no están completamente definidos. Dado que el acceso a células cerebrales humanas vivas para su estudio directo no es viable en la mayoría de los casos, los investigadores han recurrido a sistemas modelo que pueden recrear algunos aspectos de la enfermedad. Uno de estos modelos innovadores está representado por las Células Madre Pluripotentes Inducidas (iPSC) y sus derivados.
- ¿Qué son las Células Madre Pluripotentes Inducidas (iPSC)?
- La Crucial Importancia de las iPSC en la Investigación del Cerebro
- Aplicaciones de las iPSC en Modelado de Enfermedades Neurológicas
- Formatos de Cultivo: 2D, Organoides y Assembloides
- Modelado de Enfermedades Neurodegenerativas y el Desafío del Envejecimiento
- Modelado de la Iniciación del Cáncer con iPSC
- Modelado de Enfermedades Infecciosas: El Ejemplo del COVID-19
- Preguntas Frecuentes (FAQ)
- Comparación de Modelos para el Estudio de Enfermedades Neurológicas
¿Qué son las Células Madre Pluripotentes Inducidas (iPSC)?
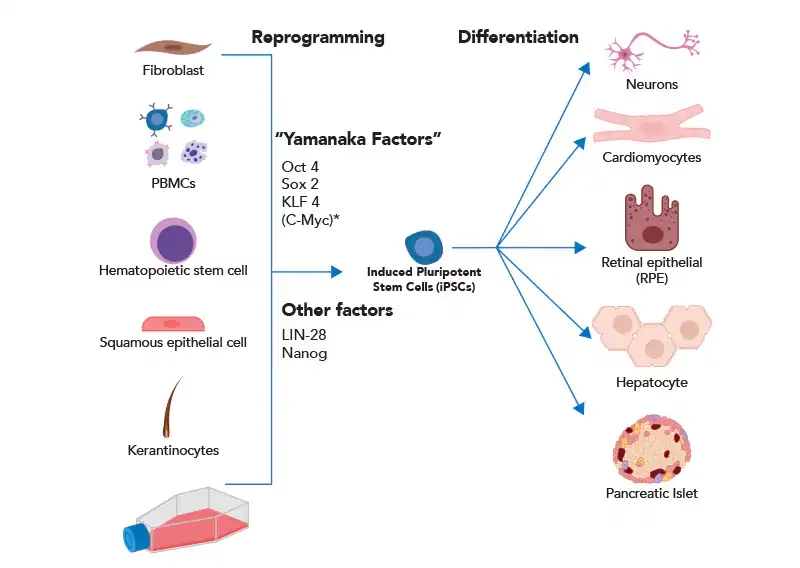
Las iPSC son células derivadas de células somáticas, como las células de la piel o de la sangre, que han sido reprogramadas de vuelta a un estado similar al embrionario, conocido como estado pluripotente. Este estado pluripotente les confiere la capacidad de diferenciarse en virtualmente cualquier tipo de célula del cuerpo humano, incluyendo neuronas, astrocitos, oligodendrocitos y otras células cerebrales.
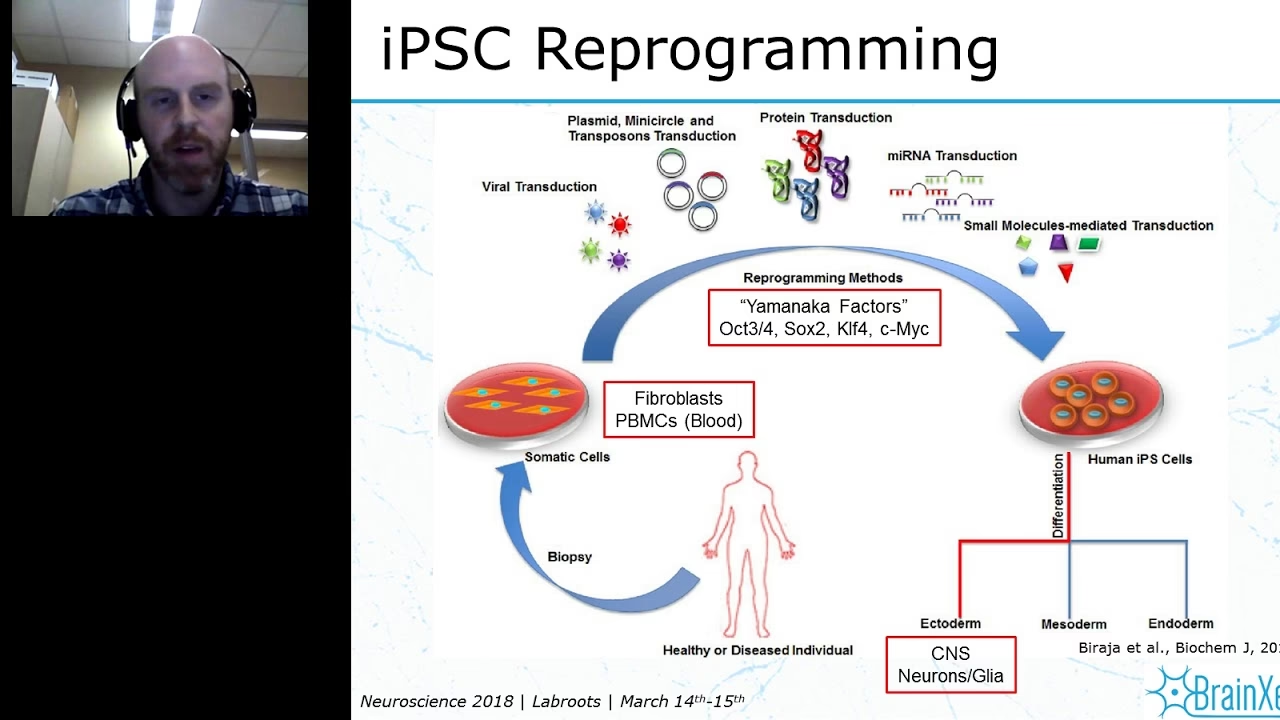
El proceso de reprogramación celular es una técnica innovadora que permite a los científicos tomar una célula especializada de un adulto (que ya ha cumplido su función, como una célula de la piel) y, mediante la introducción de ciertos factores de transcripción, hacer que 'olvide' su identidad especializada y regrese a un estado más primitivo y flexible. Lo crucial es que estas células pluripotentes inducidas conservan el complemento genético completo del donante, ya sea un paciente con una enfermedad o un individuo sano.
Esta capacidad de generar una fuente ilimitada de cualquier tipo de célula humana a partir de una simple muestra de tejido abre un vasto potencial para la investigación, el descubrimiento de fármacos y las terapias celulares. En el campo de la neurociencia, esto significa que podemos generar en el laboratorio los tipos específicos de células cerebrales afectadas por una enfermedad, a partir de la propia genética de los pacientes.
La Crucial Importancia de las iPSC en la Investigación del Cerebro
La complejidad del cerebro humano y las diferencias significativas entre especies hacen que los modelos animales tradicionales no siempre recapitulen fielmente la patología de las enfermedades neurológicas y psiquiátricas humanas, especialmente aquellas sin una etiología genética clara. Además, estudiar las células cerebrales humanas en su contexto de enfermedad es extremadamente difícil debido a la inaccesibilidad del tejido vivo. Las iPSC superan estas limitaciones al permitir a los investigadores:
- Generar tipos celulares específicos del cerebro humano (neuronas, glía) que son relevantes para una enfermedad particular.
- Estudiar estas células con el fondo genético exacto de un paciente, incluyendo mutaciones causales o factores de riesgo genético.
- Modelar la interacción entre diferentes tipos celulares en un contexto humano.
- Realizar experimentos controlados in vitro que no son posibles en el cerebro vivo.
Desde hace más de una década, la investigación basada en iPSC se ha convertido en un pilar fundamental en el estudio de las enfermedades cerebrales, con un crecimiento constante de laboratorios dedicados a esta área.
Aplicaciones de las iPSC en Modelado de Enfermedades Neurológicas
La aplicación más común de las células derivadas de iPSC en neurociencia es el modelado de enfermedades. Esta tecnología permite a los investigadores crear 'enfermedades en una placa', proporcionando una ventana sin precedentes a los mecanismos subyacentes a nivel celular y molecular.
Modelado de Enfermedades Usando la Genética del Paciente
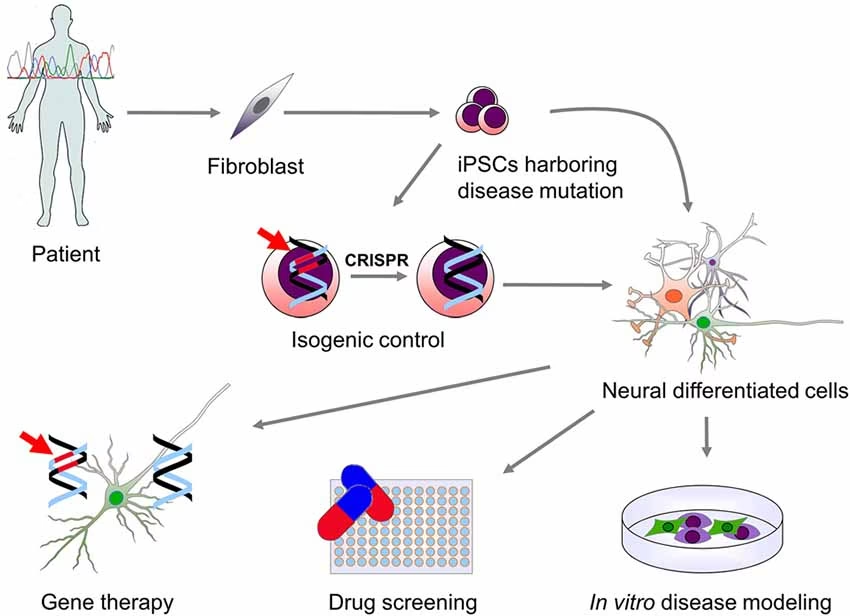
Una ventaja clave es que las iPSC pueden derivarse de células somáticas de pacientes afectados por una enfermedad particular y que portan mutaciones o factores de riesgo genético asociados. Estas iPSC, con un fondo genético relevante para la enfermedad, pueden ser diferenciadas en los tipos celulares afectados para revelar fenotipos específicos de la patología.
Por ejemplo, neuronas diferenciadas a partir de iPSC de pacientes con enfermedad de Alzheimer familiar han mostrado recapitular la patología de amiloide β, la fosforilación de tau y otros fenotipos observados en los pacientes. De manera similar, los astrocitos derivados de iPSC de pacientes con enfermedad de Alexander (causada por mutaciones en GFAP) revelan fenotipos específicos de la enfermedad, como una función celular alterada.
Modelos Isogénicos Mediante Edición Genética
Alternativamente, las mutaciones relevantes para la enfermedad pueden introducirse o corregirse mediante técnicas de edición genética como CRISPR/Cas9. Esto permite derivar modelos isogénicos, donde un par de líneas celulares de iPSC (una con la mutación y otra corregida) comparten el mismo fondo genético excepto por la mutación estudiada. Esto es increíblemente útil para limitar la variación individual y aumentar el poder estadístico de los experimentos.
Por ejemplo, corrigiendo la mutación causante de la enfermedad de Alexander en iPSC de pacientes, se obtienen líneas de control isogénicas. Al diferenciar ambas líneas a astrocitos, se pueden comparar directamente sus fenotipos y atribuir las diferencias a la mutación de GFAP. De igual forma, se han creado modelos isogénicos para estudiar el impacto de factores de riesgo genético sutiles, como variantes SNP en el gen CLU asociadas al Alzheimer, que afectan la función de otras células cerebrales como los oligodendrocitos.
Modelado con Cohortes de Pacientes y Cribado de Fármacos
La derivación de iPSC a partir de grandes cohortes de pacientes permite combinar estudios de asociación de genoma completo (GWAS) con análisis fenotípicos a nivel celular. Esto puede revelar la asociación de SNP específicos con fenotipos de enfermedad, como la producción de amiloide β en neuronas corticales de pacientes con Alzheimer. Estas cohortes de iPSC también son valiosas para el cribado de alto rendimiento (high-content screening) de posibles candidatos terapéuticos.
Formatos de Cultivo: 2D, Organoides y Assembloides
Las células derivadas de iPSC pueden cultivarse en diferentes formatos, cada uno con sus propias ventajas para modelar distintos aspectos de las enfermedades:
- Cultivos 2D: Las células se cultivan en una monocapa plana sobre una superficie. Son útiles para estudiar fenotipos celulares básicos, como la morfología, la viabilidad, la captación de neurotransmisores o la agregación de proteínas. Permiten estudios de alto rendimiento.
- Organoides Cerebrales 3D: Son estructuras tridimensionales autoorganizadas que imitan la arquitectura y composición celular de regiones cerebrales en desarrollo. Permiten estudiar interacciones célula-célula más complejas, migración celular, diferenciación y el desarrollo de redes neuronales. Han sido utilizados para modelar trastornos del desarrollo como el Síndrome de Down o el Trastorno del Espectro Autista, revelando alteraciones en la proliferación de progenitores neuronales y la producción de interneuronas.
- Assembloides: Son estructuras más avanzadas que combinan organoides de diferentes regiones cerebrales para estudiar la interacción entre ellas. Por ejemplo, assembloides cortico-ganglionares derivados de iPSC de pacientes con Síndrome de Rett han mostrado hiperexcitabilidad neuronal y actividad epileptiforme característica de la enfermedad.
Sin embargo, una limitación de los organoides cerebrales es la falta de vascularización, lo que puede llevar a necrosis en el núcleo y maduración incompleta. La trasplantación de organoides o células derivadas de iPSC en cerebros de roedores (modelos quiméricos) permite estudiar su comportamiento en un entorno complejo in vivo y evaluar déficits conductuales asociados a la disfunción de las células humanas trasplantadas.
Modelado de Enfermedades Neurodegenerativas y el Desafío del Envejecimiento
Las enfermedades neurodegenerativas, como el Alzheimer, Parkinson o ELA, son predominantemente enfermedades relacionadas con la edad. El envejecimiento es un fuerte factor de riesgo y está intrínsecamente ligado a sus mecanismos de progresión.
El proceso de reprogramación a iPSC, sin embargo, rejuvenece las células, borrando las marcas epigenéticas asociadas al envejecimiento. Las células derivadas de iPSC son típicamente 'fetales' y carecen de fenotipos de envejecimiento, lo cual representa una limitación para el modelado de estas enfermedades.
A pesar de esto, se han desarrollado varias estrategias para abordar este desafío y estudiar eventos relacionados con la edad o inducir fenotipos de envejecimiento en células derivadas de iPSC:
- Inducción de Estrés Celular: Exponer las células a compuestos que alteran la homeostasis celular, como la rotenona (que causa estrés mitocondrial), puede inducir fenotipos asociados al envejecimiento, como la senescencia celular.
- Expresión Ectópica de Progerina: La sobreexpresión de progerina, una variante truncada de la lamina A (proteína implicada en el síndrome de progeria de Hutchinson-Gilford, una enfermedad de envejecimiento acelerado), puede inducir fenotipos de envejecimiento, como degeneración de neuritas y acumulación de neuromelanina, en neuronas derivadas de iPSC.
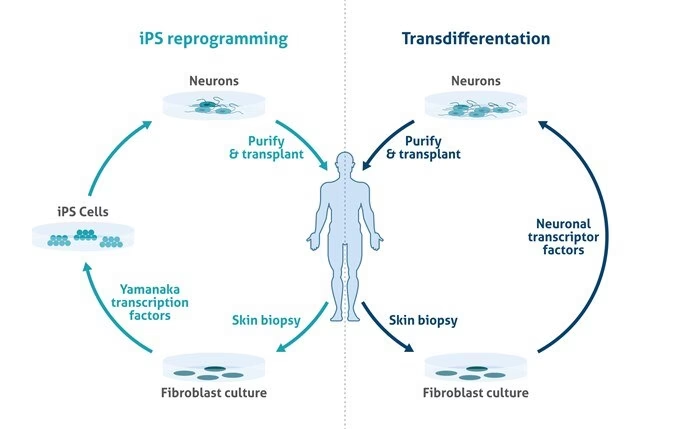
- Transdiferenciación Directa: Una estrategia prometedora es la transdiferenciación directa de fibroblastos de pacientes (células de la piel) a neuronas, sin pasar por el estado iPSC. Estas neuronas transdiferenciadas retienen la edad epigenética y los fenotipos asociados al envejecimiento del donante, permitiendo estudiar el impacto del envejecimiento en la patogénesis de enfermedades neurodegenerativas.
- Mimetización de Condiciones del Entorno del Envejecimiento: Modelar eventos relacionados con la edad, como la disrupción de la barrera hematoencefálica (BHE) que ocurre con el envejecimiento, exponiendo organoides cerebrales derivados de iPSC a suero humano, puede inducir patología similar al Alzheimer (acumulación de amiloide β y tau fosforilada).
Estas estrategias están proporcionando nuevas perspectivas sobre cómo el envejecimiento interactúa con otros factores de riesgo para impulsar la neurodegeneración.
Modelado de la Iniciación del Cáncer con iPSC
Dada su capacidad proliferativa, las iPSC también son modelos valiosos para estudiar la iniciación del cáncer. A diferencia de las líneas celulares cancerosas primarias (que ya han sufrido la transformación), las iPSC, al ser reprogramadas de células normales, permiten estudiar cómo mutaciones somáticas u otros eventos alteran los programas moleculares y celulares normales para transformarlos en células cancerosas.
Por ejemplo, células madre neurales derivadas de iPSC que portan una mutación específica asociada a un tipo de tumor cerebral pediátrico (glioma pontino intrínseco difuso) muestran programas de expresión génica aberrantes que promueven su proliferación y 'stemness'. De manera similar, organoides colónicos derivados de iPSC de pacientes con cáncer colorrectal familiar (con mutaciones en el gen APC) exhiben una actividad elevada de la vía de señalización WNT y mayor proliferación celular.
Modelado de Enfermedades Infecciosas: El Ejemplo del COVID-19
Los modelos celulares derivados de iPSC también han demostrado ser cruciales para el estudio de interacciones entre virus y células humanas. La pandemia de COVID-19 impulsó a la comunidad científica a adaptar rápidamente plataformas experimentales para investigar el tropismo, los mecanismos de entrada y el ciclo de vida del SARS-CoV-2, así como para evaluar posibles terapias.
Aunque existen modelos animales y líneas celulares permisivas al SARS-CoV-2, los modelos derivados de iPSC tienen la ventaja de revelar el tropismo y las vulnerabilidades específicas humanas. Se han utilizado modelos de células derivadas de iPSC para estudiar la infección por SARS-CoV-2 en diversos tipos celulares y organoides relevantes para las manifestaciones extrapulmonares del COVID-19, incluyendo:
- Células epiteliales alveolares del pulmón: muestran citotoxicidad e inflamación tras la infección.
- Macrófagos y células epiteliales pulmonares en cocultivo: revelan el papel protector de los macrófagos.
- Organoides de glándula salival y capilares: indican posibles reservorios y vías de diseminación del virus.
- Cardiomiocitos: muestran disrupción miofibrilar, alteración del latido y muerte celular.
- Progenitores neurales, neuronas, astrocitos y organoides cerebrales: el SARS-CoV-2 puede infectarlos, llevando a fenotipos como hiperfosforilación de tau, sugiriendo posibles efectos neurológicos a largo plazo.
Curiosamente, la susceptibilidad de las neuronas y astrocitos derivados de iPSC a la infección por SARS-CoV-2 puede depender de la variante del gen APOE, un conocido factor de riesgo para el Alzheimer.
Preguntas Frecuentes (FAQ)
- ¿Qué significa iPSC?
- iPSC significa Células Madre Pluripotentes Inducidas. Son células adultas (como de piel o sangre) que han sido reprogramadas para volver a un estado similar al de las células madre embrionarias, con la capacidad de diferenciarse en cualquier tipo celular.
- ¿Para qué se utilizan las iPSC en neurociencia?
- Se utilizan principalmente para crear modelos celulares humanos de enfermedades neurológicas, psiquiátricas y neurodegenerativas en el laboratorio. Permiten estudiar los mecanismos de la enfermedad, buscar nuevos objetivos terapéuticos y probar fármacos.
- ¿Qué son los cultivos neuronales derivados de iPSC?
- Son poblaciones de neuronas generadas en el laboratorio a partir de iPSC. Estas neuronas pueden provenir de iPSC de pacientes con enfermedades neurológicas, lo que permite estudiar cómo la genética del paciente afecta la función neuronal.
- ¿Son las iPSC una cura para las enfermedades cerebrales?
- Actualmente, las iPSC son una herramienta de investigación fundamental. Permiten comprender mejor las enfermedades y desarrollar posibles terapias (farmacológicas o celulares), pero no son una cura directa en sí mismas. La terapia celular basada en iPSC para el cerebro está aún en etapas de investigación.
Comparación de Modelos para el Estudio de Enfermedades Neurológicas
| Tipo de Modelo | Ventajas | Limitaciones | Aplicación en Neurociencia |
|---|---|---|---|
| Modelos Animales | Permiten estudiar el organismo completo y el comportamiento. | Diferencias significativas entre especies, no siempre recapitulan la patología humana compleja. | Estudio de circuitos neuronales y comportamiento. |
| Líneas Celulares Tradicionales | Fáciles de cultivar, alto rendimiento. | No representan la complejidad celular del cerebro, a menudo no son de origen humano relevante. | Estudios celulares básicos, cribado inicial. |
| Tejido Post-mortem Humano | Tejido humano relevante. | Limitado acceso, estado estático (final de la enfermedad), células muertas o moribundas. | Estudio de patología avanzada. |
| iPSC y Derivados (2D) | Origen humano, fondo genético del paciente, acceso a tipos celulares específicos. | Falta de complejidad tridimensional y de tejido, ausencia de vascularización en modelos simples. | Modelado de fenotipos celulares básicos, estudios genéticos, cribado de fármacos. |
| iPSC y Derivados (Organoides/Assembloides) | Origen humano, complejidad celular 3D, desarrollo de redes neuronales. | Falta de vascularización (en cultivo), maduración incompleta, no recapitulan el cerebro completo. | Modelado del desarrollo cerebral, interacciones célula-célula, fenotipos complejos. |
| Modelos Quiméricos (iPSC en Roedores) | Combina células humanas con entorno in vivo, vascularización de organoides trasplantados. | Complejidad técnica, no es un cerebro completamente humano. | Estudio del comportamiento celular in vivo, evaluación de déficits conductuales. |
En resumen, las iPSC han transformado radicalmente la investigación en neurociencia al proporcionar modelos celulares humanos sin precedentes de enfermedades cerebrales complejas. Permiten diseccionar los mecanismos patológicos a nivel genético y celular, identificar posibles objetivos terapéuticos y avanzar hacia enfoques de medicina personalizada y terapia celular. Aunque existen desafíos, como el modelado del envejecimiento y la complejidad de los cultivos 3D, las estrategias emergentes continúan expandiendo el potencial de esta poderosa tecnología para desentrañar los misterios del cerebro y sus afecciones.
Si quieres conocer otros artículos parecidos a iPSC en Neurociencia: Modelando el Cerebro Humano puedes visitar la categoría Neurociencia.