El desarrollo del sistema nervioso es uno de los procesos más complejos y fascinantes en la biología. A partir de una simple capa de células, se forma una red intrincada de miles de millones de neuronas y células gliales, conectadas de manera precisa para dar lugar a la conciencia, el movimiento, la percepción y todas las funciones que definen a un organismo. Este viaje constructivo no ocurre de la noche a la mañana, sino a través de una serie de etapas orquestadas con precisión.
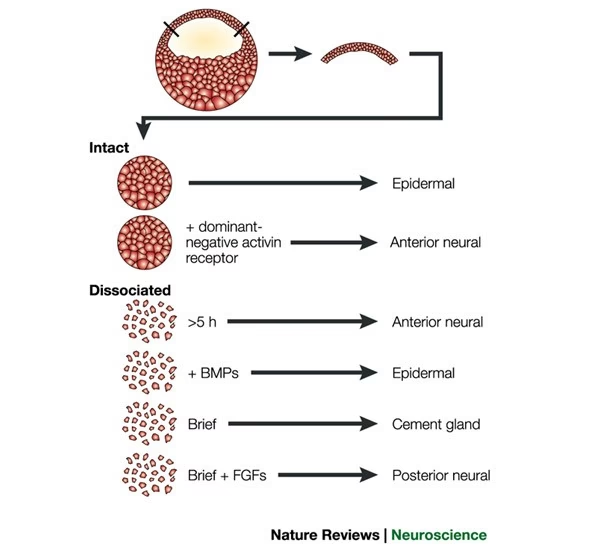
Este asombroso proceso comienza con la inducción neural, donde señales moleculares instruyen a una porción del ectodermo embrionario a convertirse en tejido neural. Si bien la inducción es el punto de partida crucial, las etapas posteriores son igualmente vitales para el cableado final del cerebro y la médula espinal. El material proporcionado se centra en algunas de estas fases subsiguientes, ofreciendo una ventana a cómo el sistema nervioso primitivo se organiza, cómo las neuronas sobreviven y establecen conexiones, y cómo estas conexiones se refinan.
Regionalización Cerebral: Los Primeros Pliegues
Una vez que el tejido neural se ha especificado, el tubo neural, la estructura precursora del sistema nervioso central, comienza a sufrir cambios morfológicos significativos. En las primeras etapas del desarrollo de vertebrados, la parte superior del tubo neural se flexiona de manera prominente. Esta flexión, conocida como la flexura mesencefálica o flexura cefálica, ocurre a nivel del futuro mesencéfalo (cerebro medio).
Por encima de esta flexura, encontramos el prosencéfalo, que dará origen al futuro cerebro anterior. Por debajo, se sitúa el rombencéfalo, la base para el futuro cerebro posterior. El mesencéfalo se encuentra entre ellos, justo en el punto de la flexura. Estas divisiones principales son el primer paso en la segmentación del cerebro, estableciendo las bases para las diferentes funciones que cada región asumirá en el organismo maduro.
Posteriormente, el prosencéfalo se subdivide aún más. La placa alar del prosencéfalo experimenta una expansión considerable para formar el telencéfalo, la estructura que eventualmente dará lugar a los hemisferios cerebrales, responsables de funciones cognitivas superiores como el pensamiento y la memoria. Mientras tanto, la placa basal del prosencéfalo se convierte en el diencéfalo, del cual se desarrollarán estructuras como el tálamo y el hipotálamo, cruciales para el procesamiento sensorial y la regulación homeostática. También es en la placa basal del prosencéfalo donde se forma la vesícula óptica, que con el tiempo dará lugar a componentes visuales esenciales como el nervio óptico, la retina y el iris.
Estas etapas de regionalización son fundamentales para establecer la arquitectura básica del cerebro, definiendo las áreas que se diferenciarán en estructuras con roles especializados. Después de la regionalización, siguen otras etapas como el patrón, la neurogénesis (nacimiento de nuevas neuronas) y la migración neuronal, donde las neuronas recién formadas viajan a sus posiciones finales en el sistema nervioso.
El Papel Vital de los Factores Neurotróficos
La supervivencia de las neuronas en desarrollo no es algo garantizado. Existe un proceso selectivo donde muchas neuronas mueren por apoptosis (muerte celular programada) si no establecen las conexiones correctas o no reciben las señales de supervivencia adecuadas. Aquí es donde entran en juego los factores neurotróficos.
Los factores neurotróficos son proteínas que actúan como factores de supervivencia para las neuronas. La hipótesis neurotrófica, formulada por Victor Hamburger y Rita Levi Montalcini a partir de sus estudios en el sistema nervioso en desarrollo de pollos, postula que los axones en crecimiento compiten por cantidades limitadas de factores tróficos producidos por las células objetivo a las que se dirigen. Los axones que no logran obtener suficiente soporte trófico mueren por apoptosis.
Hamburger descubrió que al implantar una extremidad adicional en un embrión de pollo, aumentaba el número de motoneuronas espinales. Inicialmente pensó que la extremidad extra inducía la proliferación de neuronas, pero él y sus colegas demostraron más tarde que en realidad lo que ocurría era una gran cantidad de muerte de motoneuronas durante el desarrollo normal, y la extremidad extra prevenía esta muerte celular. Esto sustentó la idea de que las células objetivo liberan algo que es esencial para la supervivencia neuronal.
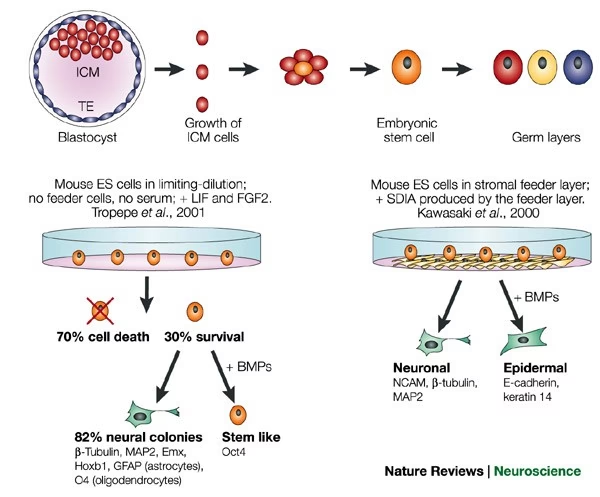
Rita Levi Montalcini y Stanley Cohen lograron purificar el primer factor trófico, el Factor de Crecimiento Nervioso (NGF), un descubrimiento por el que fueron galardonados con el Premio Nobel. El NGF es el miembro prototípico de una familia de neurotrofinas que incluye también al Factor Neurotrófico Derivado del Cerebro (BDNF), la Neurotrofina-3 (NT3) y la Neurotrofina-4 (NT4). Estos factores regulan la supervivencia de diversas poblaciones neuronales a lo largo del sistema nervioso.
Los receptores principales para el NGF y factores relacionados son las proteínas Trk. Las proteínas Trk son receptores tirosina quinasa. Cuando una neurotrofina se une a su receptor Trk específico, induce la dimerización y fosforilación del receptor, lo que a su vez activa diversas vías de señalización intracelular esenciales para la supervivencia y el crecimiento neuronal, incluyendo las vías de la MAP quinasa, Akt y PKC.
Pero las neurotrofinas no son los únicos factores tróficos. El Factor Neurotrófico Ciliar (CNTF) es otra proteína que actúa como factor de supervivencia para las motoneuronas, entre otras poblaciones neuronales. El CNTF actúa a través de un complejo receptor que incluye las proteínas CNTFRα, GP130 y LIFRβ. La activación de este complejo receptor conduce a la fosforilación y el reclutamiento de la quinasa JAK. La JAK quinasa, a su vez, fosforila la proteína LIFRβ, que actúa como un sitio de anclaje para los factores de transcripción STAT. La JAK quinasa fosforila las proteínas STAT, las cuales se disocian del receptor y se translocan al núcleo para regular la expresión génica, promoviendo así la supervivencia celular.
Otro factor importante es el Factor Neurotrófico Derivado de la Glía (GDNF). Este factor pertenece a la familia de proteínas TGFb y es un potente factor trófico para neuronas en el estriado, una región del cerebro involucrada en el movimiento y la recompensa. El receptor funcional para GDNF es un heterodímero compuesto por receptores de tipo 1 y tipo 2. La activación del receptor de tipo 1 conduce a la fosforilación de proteínas Smad, las cuales también se translocan al núcleo para activar la expresión génica, promoviendo la supervivencia y el mantenimiento de las neuronas a las que se dirigen.
La existencia y acción coordinada de estos factores neurotróficos son cruciales para asegurar que solo las neuronas que han establecido conexiones apropiadas y funcionales sobrevivan, mientras que aquellas que son redundantes o están mal conectadas son eliminadas, optimizando así la eficiencia y precisión del cableado neuronal.
Dinámica Sináptica: Formación y Eliminación
Una vez que las neuronas han migrado a sus posiciones finales y han sobrevivido gracias al soporte trófico, deben establecer conexiones funcionales entre sí y con sus células objetivo, un proceso conocido como formación sináptica. Sin embargo, el desarrollo no se detiene aquí. Las conexiones iniciales a menudo son excesivas o imprecisas, y el sistema nervioso pasa por una fase de refinamiento crucial: la eliminación sináptica, también llamada poda sináptica.
Un ejemplo clásico de eliminación sináptica ocurre en la unión neuromuscular, donde una única fibra muscular es inervada inicialmente por axones de varias motoneuronas diferentes. A medida que el desarrollo avanza hacia la edad adulta, la mayoría de estas conexiones se eliminan, dejando a cada fibra muscular inervada por el axón de una única motoneurona. Este proceso competitivo asegura un control motor preciso.
Los mecanismos exactos de esta competencia y eliminación aún se investigan, pero se han propuesto varias hipótesis. Estudios *in vitro* sugieren que la competencia podría involucrar una sustancia neurotrófica limitada que es liberada, o que la actividad neuronal confiere una ventaja a las conexiones postsinápticas fuertes al dar resistencia a una toxina que también se libera con la estimulación nerviosa. Es decir, las sinapsis más activas o eficientes tendrían una ventaja competitiva.
En condiciones *in vivo*, se sugiere que las fibras musculares podrían seleccionar a la neurona más fuerte a través de una señal retrógrada (una señal que viaja desde la célula muscular de vuelta a la neurona), o que mecanismos de eliminación sináptica dependientes de la actividad neuronal determinan la identidad del axón "ganador" en cada placa motora terminal. Este proceso de poda es esencial para esculpir los circuitos neuronales y optimizar su funcionamiento.

Mapeo Cerebral y Neurogénesis Adulta
Comprender completamente el desarrollo del sistema nervioso implica no solo conocer las etapas celulares y moleculares, sino también cómo la conectividad global (el "cableado") cambia con el tiempo. Las técnicas de mapeo cerebral buscan visualizar y comparar estas conexiones a lo largo de la vida de un organismo. En 2021, los científicos mapearon y compararon los cerebros completos de ocho gusanos C. elegans en diferentes etapas de su desarrollo a nivel neuronal, y también el cableado completo de un único músculo de mamífero desde el nacimiento hasta la edad adulta. Estos estudios de mapeo proporcionan vistas detalladas de la dinámica de las conexiones a lo largo del desarrollo.
Finalmente, aunque la mayor parte de la neurogénesis ocurre durante el desarrollo embrionario y postnatal temprano, se sabe que también ocurre neurogénesis en partes específicas del cerebro adulto. Este proceso, conocido como neurogénesis adulta, permite la generación de nuevas neuronas a lo largo de la vida en regiones como el hipocampo, y se cree que juega un papel en el aprendizaje y la memoria.
Preguntas Frecuentes
¿Qué es la inducción neural?
La inducción neural es la etapa inicial del desarrollo del sistema nervioso, donde las células ectodérmicas reciben señales para convertirse en tejido neural. Sin embargo, la información detallada proporcionada aquí se centra en las etapas posteriores a este proceso inicial.
¿Qué sucede después de la inducción neural?
Después de la inducción, el sistema nervioso en desarrollo pasa por etapas como la regionalización del cerebro, el patrón, la formación y migración de neuronas, la acción de factores neurotróficos para la supervivencia y la formación y eliminación de sinapsis.
¿Por qué mueren algunas neuronas durante el desarrollo?
Según la hipótesis neurotrófica, la muerte neuronal (apoptosis) ocurre debido a la competencia por cantidades limitadas de factores neurotróficos producidos por las células objetivo. Las neuronas que no reciben suficiente soporte trófico mueren.
¿Cómo funcionan los factores neurotróficos como el NGF?
Factores como el NGF se unen a receptores específicos en la superficie neuronal (como los receptores Trk). Esta unión activa cascadas de señalización intracelular (como las vías MAP quinasa, Akt o PKC) que promueven la supervivencia de la neurona.
¿Qué es la eliminación sináptica?
La eliminación sináptica es un proceso de poda donde se eliminan conexiones sinápticas redundantes o menos activas. Por ejemplo, en la unión neuromuscular, múltiples motoneuronas compiten por inervar una fibra muscular, pero al final solo una conexión prevalece.
Tabla Comparativa: Mecanismos de Señalización de Factores Neurotróficos
| Factor Neurotrófico | Familia / Tipo | Receptor Principal | Vías de Señalización Clave |
|---|---|---|---|
| NGF, BDNF, NT3, NT4 | Neurotrofinas | Receptores Trk (Tirosina Quinasa) | MAP quinasa, Akt, PKC |
| CNTF | Citocina | Complejo (CNTFRα, GP130, LIFRβ) | JAK/STAT |
| GDNF | Familia TGFb | Heterodímero (Receptores tipo 1 y 2) | Smad |
En resumen, el desarrollo del sistema nervioso es un proceso dinámico que va mucho más allá de la especificación inicial. Las etapas de regionalización cerebral, la supervivencia neuronal mediada por factores neurotróficos como el NGF, y el refinamiento de conexiones a través de la eliminación sináptica son solo algunos ejemplos de los complejos mecanismos que aseguran que el cerebro se forme y se cablee correctamente, sentando las bases para la función neuronal a lo largo de la vida.
Si quieres conocer otros artículos parecidos a Desarrollo Neuronal Vertebrado puedes visitar la categoría Neurociencia.
