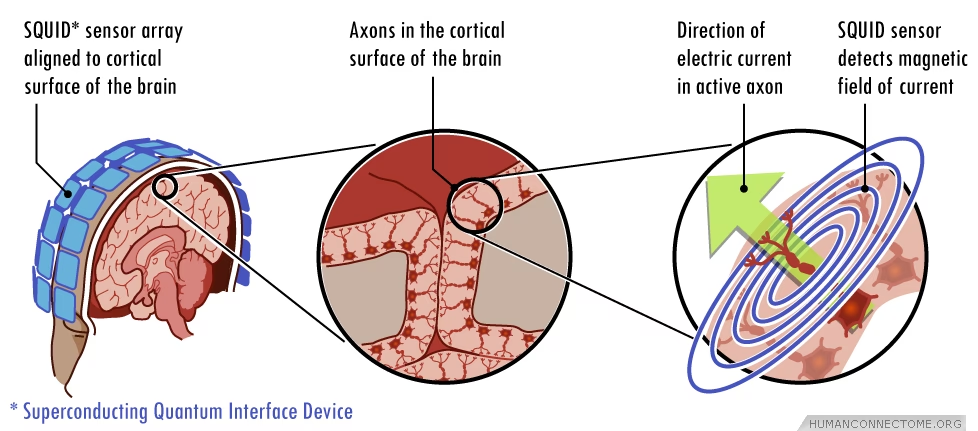
La actividad eléctrica y magnética del cerebro es la base de su funcionamiento, desde los pensamientos más complejos hasta las funciones más básicas del organismo. Para comprender y diagnosticar trastornos neurológicos, especialmente aquellos relacionados con la actividad eléctrica anormal como la epilepsia, los investigadores y clínicos emplean diversas técnicas de neuroimagen funcional. Entre las más destacadas se encuentran la Electroencefalografía (EEG) y la Magnetoencefalografía (MEG), ambas capaces de registrar la actividad cerebral en tiempo real, aunque con diferencias fundamentales que las hacen complementarias y, en ciertos contextos, una más adecuada que la otra.
Aunque el EEG es una técnica ampliamente conocida y utilizada por su accesibilidad y capacidad para detectar actividad eléctrica cortical, existen escenarios clínicos y de investigación donde la MEG ofrece ventajas significativas. La principal diferencia radica en lo que miden y cómo los campos generados por la actividad neuronal atraviesan los tejidos. El EEG mide los campos eléctricos generados por las corrientes iónicas dentro de las neuronas. Estos campos eléctricos, al propagarse a través del cerebro, el cráneo y el cuero cabelludo, se distorsionan considerablemente, lo que dificulta la localización precisa de la fuente de la actividad. Por otro lado, la MEG mide los campos magnéticos asociados a estas mismas corrientes neuronales. A diferencia de los campos eléctricos, los campos magnéticos atraviesan los tejidos biológicos (incluido el cráneo) con mucha menos distorsión. Esta propiedad confiere a la MEG una capacidad superior para localizar con precisión el origen de la actividad neuronal dentro del cerebro, una característica crucial en aplicaciones como el mapeo cerebral prequirúrgico y el manejo de la epilepsia.
Indicaciones Clínicas Aprobadas de la MEG
Actualmente, en los Estados Unidos, la Magnetoencefalografía tiene dos indicaciones clínicas aprobadas por la Administración de Alimentos y Medicamentos (FDA). La primera es para el mapeo cerebral pre-operatorio. Esta aplicación permite identificar la ubicación de áreas cerebrales funcionalmente importantes, como las relacionadas con el lenguaje o el movimiento (conocida como corteza elocuente), antes de una cirugía, reduciendo el riesgo de dañar estas áreas críticas durante el procedimiento. La segunda indicación aprobada es para su uso en la cirugía de epilepsia. Es en este contexto donde la capacidad de localización superior de la MEG se vuelve particularmente valiosa.
La MEG en el Tratamiento Quirúrgico de la Epilepsia
El éxito de la cirugía de epilepsia depende, en gran medida, de la capacidad para identificar y extirpar el área exacta del cerebro donde se originan las crisis, conocida como el foco epiléptico. Esta es la información más crítica que se necesita antes de la cirugía. La MEG puede contribuir sustancialmente a esta localización. Al ser una técnica no invasiva, la MEG detecta las descargas epilépticas interictales (IIEDs), que son actividades eléctricas anormales que ocurren entre las crisis convulsivas, como las puntas (spikes) o las ondas agudas (sharp waves). Utilizando técnicas apropiadas de localización de fuente, la MEG permite determinar la ubicación precisa de los generadores corticales de estas descargas.
Además de localizar el foco epiléptico, la MEG también ayuda a identificar la corteza elocuente, es decir, las áreas cerebrales responsables de funciones vitales como el lenguaje, la memoria o las funciones motoras y sensoriales. Al conocer la ubicación de estas áreas funcionales en relación con el foco epiléptico, los cirujanos pueden planificar la resección (extirpación) del tejido epiléptico de manera segura, minimizando el riesgo de déficits neurológicos postoperatorios. La contribución de la MEG a la localización precisa del foco y a la identificación de la corteza elocuente la convierte en una herramienta indispensable en la evaluación prequirúrgica de pacientes con epilepsia refractaria.
Registro y Análisis de MEG para Epilepsia: Estándares Clínicos
La American Clinical Magnetoencephalography Society (ACMEGS) ha establecido directrices para el registro y análisis clínico rutinario de MEG y EEG espontáneos en todas las edades, considerando ciertos puntos como estándares mínimos.
Equipamiento y Registro
Un requisito fundamental es el uso de una sala blindada magnéticamente. Esta sala especial es necesaria para minimizar la interferencia de campos magnéticos externos (provenientes del entorno, equipos eléctricos, etc.) que podrían enmascarar las débiles señales magnéticas generadas por el cerebro. La sala debe cumplir con los estándares operativos y de seguridad actuales y ser inspeccionada regularmente. Dentro de la sala, el mobiliario, como la cama o la silla del paciente, debe ser no magnético y compatible con el sistema MEG.
Es esencial utilizar un sistema de cabeza completa (whole-head system) aprobado por la FDA para registrar simultáneamente la actividad de todo el cerebro. Todos los componentes del sistema MEG, tanto hardware como software, deben contar con la aprobación de la FDA. La grabación simultánea de MEG y EEG es considerada la más beneficiosa para un estudio clínico de epilepsia. Por lo tanto, en todas las grabaciones espontáneas de MEG para epilepsia, se dispone de datos de EEG y MEG para el análisis.
La precisión de la localización de la fuente depende críticamente de conocer la posición exacta de la cabeza del paciente en relación con el conjunto de sensores del MEG. Para ello, se utiliza un sistema de digitalización fiable. Esto se logra con mayor frecuencia determinando la posición de varias bobinas indicadoras de posición de la cabeza colocadas sobre el paciente. Estas bobinas emiten señales eléctricas transitorias que crean fuentes magnéticas localizables por el MEG, permitiendo determinar la posición de la cabeza en el espacio de los sensores.
Antes de la grabación, se digitalizan las posiciones de al menos tres puntos fiduciales externos (generalmente el nasión, el punto preauricular izquierdo y el derecho), las bobinas indicadoras de posición de la cabeza u otros puntos de referencia anatómicos. Esto crea un sistema de coordenadas cartesiano que permite la co-registro de los datos de MEG con una resonancia magnética (MRI) del paciente, lo cual es indispensable para la localización de la fuente. Se recomienda medir la posición de la cabeza antes y después de cada segmento de grabación, o de forma continua si la opción está disponible, para cuantificar cualquier movimiento de la cabeza y evaluar la calidad de los datos.
La frecuencia de muestreo del sistema MEG debe configurarse apropiadamente para garantizar la adquisición adecuada de las señales de interés. Para evitar el aliasing (un artefacto que ocurre cuando la señal no se muestrea lo suficientemente rápido), se debe aplicar un filtro de paso bajo con una frecuencia de corte igual o menor a la mitad de la frecuencia de muestreo antes de la conversión digital. También se suele requerir un filtro de paso alto para minimizar los efectos de grandes señales de baja frecuencia. Sin embargo, a diferencia del EEG, las grabaciones espontáneas de MEG pueden realizarse sin un filtro de paso alto (acoplado a corriente continua).
Es fundamental visualizar en tiempo real las formas de onda de una muestra de canales de MEG y EEG para monitorizar la calidad de la grabación. También puede ser útil mostrar registros de electrooculograma (EOG, para movimientos oculares), electrocardiografía (ECG, para actividad cardíaca) y electromiograma (EMG, para actividad muscular), ya que estas actividades fisiológicas pueden generar artefactos en las señales cerebrales. Todos los datos registrados deben incluir la misma señal de tiempo sincronizada, independientemente del método de sincronización utilizado.
Se deben realizar regularmente procedimientos de ajuste de sensores y control de calidad general según las instrucciones operativas de los sistemas MEG y EEG específicos. Confirmar el rendimiento preciso del sistema utilizando un fantasma (un modelo que simula la actividad cerebral) debe realizarse tan a menudo como sea posible, preferiblemente semanalmente.
La duración mínima de las sesiones de registro espontáneo de MEG-EEG debe ser de 30 minutos. Preferiblemente, esto debe incluir períodos tanto de vigilia como de sueño, ya que el sueño tiene un efecto activador sobre las IIEDs, aumentando la probabilidad de detectarlas. Se recomienda una grabación más larga si las IIEDs no son lo suficientemente frecuentes para permitir una interpretación clínica razonable. En algunos casos, puede ser necesario repetir el estudio con tiempos de grabación más largos, privación adicional de sueño, manipulación de medicamentos antiepilépticos (coordinada con el epileptólogo del paciente), sedación u otros medios clínicamente aceptables para aumentar el rendimiento diagnóstico.
La hiperventilación es un procedimiento de activación estándar en los estudios de EEG clínico para epilepsia y puede implementarse durante un estudio MEG-EEG. Sin embargo, la MEG puede contaminarse con grandes artefactos causados por los movimientos de cabeza asociados a la hiperventilación. Por lo tanto, si se utiliza, los datos de MEG inmediatamente después de la hiperventilación pueden ser los más útiles.
Análisis de Datos
El análisis de los datos de MEG y EEG comienza con la inspección visual de las formas de onda (los 'datos brutos' u originales tal como se recolectaron) para toda la grabación. Esto sigue los principios establecidos para el EEG clínico y es un paso inicial obligatorio. La inspección visual tiene varios objetivos: (1) identificar artefactos, (2) evaluar la calidad e integridad general de los datos y (3) identificar ritmos de fondo, asimetrías y otras características del fondo, así como las IIEDs. Para las IIEDs, se deben evaluar y reportar sistemáticamente sus características morfológicas y temporales, tanto en los datos de MEG como en los de EEG.
El uso de filtros es generalmente necesario para eliminar señales biológicas irrelevantes (como el ECG o el EOG) y el ruido inherente del sistema MEG y el entorno. La selección particular de filtros (paso alto, paso bajo, paso banda o notch) depende del análisis a realizar y de las características del sistema MEG utilizado. Esta selección requiere una comprensión conceptual adecuada del método de filtrado y experiencia práctica en su uso. La mayoría de las rutinas analíticas actuales para la localización de focos epilépticos utilizando datos espontáneos de MEG-EEG se benefician del uso de un filtro de paso alto de 1-4 Hz y un filtro de paso bajo de 40-70 Hz.
El análisis de fuente se utiliza para estimar la ubicación de los generadores corticales de la actividad neuromagnética de interés. Para los estudios de epilepsia, las IIEDs identificadas (puntas y ondas agudas) son las más utilizadas para este propósito. El análisis de fuente de actividad de onda lenta o actividad rápida está actualmente bajo investigación y podría convertirse en práctica estándar en el futuro si demuestra ser útil. Si se registra una crisis durante el estudio, el inicio de la crisis puede localizarse utilizando métodos similares al análisis de puntas, considerando las posibles diferencias entre la generación de descargas interictales e ictales durante la localización.
La localización de fuente mediante el modelado de dipolo equivalente único (Single ECD model) debe realizarse en todas las IIEDs bien definidas, lo que incluye puntas (20-70 ms) y ondas agudas (70-200 ms). La significancia clínica de ambos tipos de IIEDs en la localización del foco epiléptico es equivalente. La morfología, localización y características temporales de las IIEDs identificadas visualmente deben reportarse de manera estándar. Aunque no son utilizadas rutinariamente por la mayoría de los magnetoencefalógrafos clínicos, el análisis de componentes principales (PCA) y el análisis de componentes independientes (ICA) pueden ser útiles para estimar el número razonable de fuentes en la señal por encima del ruido de fondo. Si también se ha estimado el nivel de ruido de fondo, el ICA puede ser útil para identificar y eliminar ciertos artefactos, como el artefacto del ECG o del movimiento ocular.
Se pueden seleccionar varios puntos de tiempo en la forma de onda de la IIED para el análisis de fuente. Esto incluye el pico de la punta o un punto en la fase ascendente de la punta. Seleccionar el pico de una punta de gran amplitud garantiza una alta relación señal-ruido (SNR), lo que minimiza los errores de cálculo. Sin embargo, el campo en esta latencia puede no representar el origen de la punta. Si una evaluación de los mapas de campo secuenciales sobre una sola fase de la punta no muestra rotación, se puede asumir una fuente estable y modelar solo en el pico de la punta para obtener la mayor SNR. Si es evidente la rotación del campo, es útil modelar puntos de tiempo antes del pico para buscar una fuente más temprana y a lo largo del curso temporal de la punta para identificar una posible propagación. Es importante notar que modelar puntos de tiempo fuera del pico significará una menor SNR y un volumen de confianza mayor, lo que requiere una interpretación más cuidadosa de los resultados. Los generadores corticales después del pico de la punta, como la onda posterior, suelen ser complejos y no se modelan bien con un ECD.
Co-registro con MRI Cerebral
Para poder relacionar la actividad cerebral registrada por el MEG con la anatomía específica del paciente, es indispensable realizar un co-registro con una resonancia magnética (MRI) cerebral. Se requiere una exploración volumétrica con reconocida alta fidelidad neuroanatómica, como un eco de gradiente ponderado en T1 o un flash multi-eco con dos ángulos de flip diferentes. Las dimensiones del voxel deben ser isotrópicas (1 mm es óptimo) con una matriz de exploración y reconstrucción de al menos 256 × 256 (una resolución más alta no es necesaria) para permitir buenas superposiciones.
El campo de visión de la MRI debe ser 'piel a piel', es decir, incluir la cara, las orejas y todo el cuero cabelludo (la orientación sagital de la adquisición de cortes es la mejor) para permitir una identificación precisa de los puntos fiduciales superficiales (como el nasión y los puntos preauriculares) que se utilizan para el co-registro de MEG a MRI. Los métodos de co-registro dependen del sistema MEG y del software adicional utilizado para la localización de la fuente. Se puede implementar cualquier método de co-registro aprobado, fiable, preciso y establecido.
Informe de Resultados
Los médicos remitentes deben recibir los resultados de la MEG en forma de trazados de EEG y MEG de puntas o ondas agudas representativas utilizadas para el análisis de fuente, además de un Mapa de Imagen de Fuente (MSI). El MSI debe contener una localización de fuente de dipolo y su momento por punta, co-registrado con la MRI cerebral del paciente. Esto proporciona una representación visual clara de dónde se estima que se origina la actividad epiléptica en el cerebro del paciente.
MEG vs EEG en Epilepsia: Una Comparativa
Basándonos en la información proporcionada, podemos esbozar una comparación clave entre MEG y EEG en el contexto de la epilepsia:
| Característica | Magnetoencefalografía (MEG) | Electroencefalografía (EEG) |
|---|---|---|
| Principio de Medición | Campos magnéticos generados por corrientes neuronales. | Campos eléctricos generados por corrientes neuronales. |
| Distorsión por Tejidos (Craneo) | Mínima, los campos magnéticos lo atraviesan bien. | Considerable, los campos eléctricos se distorsionan. |
| Precisión de Localización de Fuente (en epilepsia) | Superior, permite una localización más precisa del foco epiléptico. | Menor debido a la distorsión de la señal. |
| Rol en Cirugía de Epilepsia | Contribuye sustancialmente a la localización del foco epiléptico y la corteza elocuente. | Proporciona información general y sobre IIEDs, pero menos precisión de localización. |
| Registro Simultáneo | Casi siempre se registra simultáneamente con EEG en estudios de epilepsia. | Casi siempre se registra simultáneamente con MEG en estudios de epilepsia. |
| Sensibilidad a Artefactos por Movimiento | Sensible a movimientos de cabeza (ej. durante hiperventilación). | Menos sensible a movimientos de cabeza. |
| Requisitos de Entorno | Requiere una sala blindada magnéticamente para reducir interferencias. | No requiere blindaje magnético especial. |
| Técnicas de Análisis de Fuente | Modelado de Dipolo Equivalente Único (ECD) es común para IIEDs; PCA, ICA para análisis más complejos. | Datos disponibles para análisis de fuente, aunque la precisión está limitada por la distorsión. |
Esta tabla subraya por qué, en el contexto específico de la evaluación prequirúrgica de la epilepsia, donde la localización precisa es paramount, la MEG a menudo se elige o se complementa con el EEG debido a su inherente ventaja en la localización de fuentes.
Preguntas Frecuentes sobre MEG y Epilepsia
- ¿Qué son las descargas epilépticas interictales (IIEDs)?
- Son actividades eléctricas anormales en el cerebro, como puntas o ondas agudas, que ocurren entre las crisis convulsivas. Su detección y localización son clave para identificar el foco epiléptico.
- ¿Por qué se registra el EEG al mismo tiempo que el MEG en los estudios de epilepsia?
- La grabación simultánea de EEG y MEG es beneficiosa porque proporciona datos complementarios. El EEG es sensible a diferentes configuraciones de corriente neuronal (radiales) que el MEG (tangenciales) y puede detectar actividad más superficial. Tener ambos conjuntos de datos mejora la capacidad de análisis y diagnóstico.
- ¿Cómo ayuda la MEG a localizar el foco epiléptico?
- La MEG detecta los campos magnéticos generados por las IIEDs. Como estos campos atraviesan el cráneo con mínima distorsión, se pueden aplicar técnicas de localización de fuente (como el modelado de dipolo equivalente) para estimar con precisión la ubicación tridimensional en el cerebro donde se originaron estas descargas.
- ¿Qué es el co-registro con MRI y por qué es necesario?
- El co-registro es el proceso de alinear los datos funcionales del MEG (que muestran dónde ocurre la actividad) con una imagen anatómica detallada del cerebro del paciente obtenida por MRI (que muestra la estructura). Es necesario para visualizar la ubicación estimada de la fuente de la actividad (el foco epiléptico) en el contexto de la anatomía individual del paciente, lo cual es crucial para la planificación quirúrgica.
- ¿Cuánto tiempo dura una grabación típica de MEG-EEG para epilepsia?
- La duración mínima recomendada es de 30 minutos, pero se prefiere que sea más larga. Se recomienda incluir períodos de vigilia y sueño, ya que el sueño a menudo activa las IIEDs, aumentando las posibilidades de detectarlas.
- ¿Qué se entiende por 'corteza elocuente' y por qué es importante identificarla con MEG?
- La corteza elocuente se refiere a las áreas cerebrales responsables de funciones críticas como el lenguaje, el movimiento, la sensación o la memoria. Identificar su ubicación con MEG (mediante mapeo funcional) es vital antes de la cirugía de epilepsia para evitar extirpar tejido cerebral que controla estas funciones esenciales, minimizando así el riesgo de déficits neurológicos permanentes.
- ¿Qué artefactos pueden afectar una grabación de MEG?
- Los artefactos comunes incluyen actividad cardíaca (ECG), movimientos oculares (EOG), actividad muscular (EMG) y, en el contexto de la hiperventilación, movimientos de cabeza significativos. El blindaje magnético de la sala ayuda a reducir el ruido ambiental.
- ¿Cómo se analizan visualmente los datos brutos de MEG y EEG?
- Se examinan las formas de onda a lo largo del tiempo para identificar artefactos, evaluar la calidad general de la grabación, observar los ritmos de fondo y, lo más importante para la epilepsia, detectar y caracterizar las IIEDs (puntas y ondas agudas), prestando atención a su morfología y ocurrencia temporal.
Conclusión
La Magnetoencefalografía (MEG) representa un avance significativo en las técnicas de neuroimagen funcional, particularmente en el campo de la epileptología. Su capacidad única para medir los campos magnéticos cerebrales con mínima distorsión a través del cráneo le confiere una ventaja crucial sobre el EEG para la localización precisa de los generadores de las descargas epilépticas. Esta precisión, combinada con la identificación de la corteza elocuente, hace que la MEG sea una herramienta invaluable en la evaluación prequirúrgica de pacientes con epilepsia, permitiendo una planificación quirúrgica más segura y efectiva. Aunque el EEG sigue siendo una herramienta esencial y se registra simultáneamente, la MEG proporciona la información de localización detallada que a menudo es determinante para el éxito de la cirugía de epilepsia.
Si quieres conocer otros artículos parecidos a MEG vs EEG: Mapeo Cerebral y Epilepsia puedes visitar la categoría Neurociencia.