La perfusión cerebral es un parámetro fisiológico fundamental, estrechamente ligado a la función del tejido. Los trastornos de la perfusión son causas importantes de morbilidad y mortalidad médica. La Resonancia Magnética (RM) ofrece diversas metodologías para medir parámetros relacionados con el flujo, pero la medición directa de la perfusión tisular en unidades clásicas (ml/g/min) requiere un trazador nominalmente difusible. Aquí es donde entra en juego la técnica de etiquetado de spin arterial (ASL), un enfoque innovador que utiliza el agua de la sangre arterial, etiquetada magnéticamente, como trazador endógeno para estimar el flujo sanguíneo cerebral (FSC) de forma no invasiva. Desde su introducción a principios de la década de 1990, el ASL ha evolucionado significativamente, beneficiándose de la mejora en la relación señal-ruido (SNR) de los sistemas de RM de alto campo y el desarrollo de secuencias de pulsos mejoradas, lo que ha allanado el camino para su aplicación cada vez más extendida en trastornos neurológicos y psiquiátricos.
El principio básico detrás del ASL es el etiquetado magnético de los protones del agua de la sangre arterial antes de que entren en el tejido de interés. Esto se logra aplicando pulsos de radiofrecuencia para invertir la magnetización del agua sanguínea. Se adquieren imágenes después de un período de etiquetado y flujo utilizando técnicas de adquisición rápida. Siempre se adquiere un par de imágenes: una imagen etiquetada (donde la magnetización del agua sanguínea está invertida) y una imagen de control (donde la magnetización no está invertida). La diferencia de señal entre las imágenes etiquetadas y de control es proporcional a la cantidad de magnetización invertida y entregada al tejido. Si toda la sangre etiquetada ha llegado al vóxel de imagen en el momento de la adquisición, la diferencia de señal será proporcional al FSC. Las implementaciones principales actuales de ASL son el etiquetado pulsado y el pseudocontinuo.
Principios Técnicos Clave del ASL
Etiquetado Arterial Pulsado (PASL)
En el ASL pulsado (PASL), el agua de la sangre arterial se etiqueta utilizando un pulso adiabático corto de inversión, típicamente de aproximadamente 10 ms. Estos pulsos están diseñados para invertir instantáneamente el agua sanguínea en una región particular, generalmente ubicada inferiormente al cerebro. Después del etiquetado, se requiere un período de retardo post-etiquetado (también conocido como tiempo de entrada para PASL), durante el cual la sangre invertida se mueve desde la región de etiquetado hacia el cerebro, perdiendo gradualmente su etiqueta a través de la relajación longitudinal T1. Por esta razón, PASL es intrínsecamente una técnica con menor SNR que el ASL pseudocontinuo (PCASL). La adquisición de control para PASL consiste en aplicar un pulso de radiofrecuencia con potencia equivalente al pulso de etiquetado, pero que tiene un efecto neto cero sobre la magnetización del agua sanguínea en la región de etiquetado.
Técnica de Etiquetado Arterial Pseudocontinuo (PCASL)
En PCASL, se utiliza un período de etiquetado largo (1-2 segundos) compuesto por una serie de pulsos muy cortos (≈1 ms). Esta serie de pulsos cortos está diseñada para invertir la magnetización de la sangre entrante de manera adiabática o pseudo-estado estacionario. Es útil pensar en la sangre siendo continuamente invertida a medida que fluye a través de un "plano de etiquetado" en dirección inferior-superior. Si la fase de cada segundo pulso en la serie de pulsos de PCASL se desplaza 180°, el agua sanguínea que fluye se perturba mínimamente, lo que permite la adquisición de imágenes de control no etiquetadas. PCASL ha sido adoptado recientemente como el método de etiquetado de elección para la imagenología clínica, debido a su facilidad de implementación y alta SNR.
Ventajas y Desventajas: PASL vs. PCASL
La principal ventaja de PCASL sobre PASL es su mayor SNR, un beneficio sustancial en una técnica que está intrínsecamente limitada por la SNR. Esto se debe a que en PCASL, la sangre arterial es continuamente invertida a medida que pasa por el plano de etiquetado, lo que significa que toda la sangre tiene la misma cantidad de decaimiento T1 cuando llega al tejido, independientemente de cuándo fue etiquetada. Sin embargo, los beneficios de PCASL no son tan grandes en la práctica como se predeciría teóricamente debido a (a) la eficiencia de inversión de los pulsos de RF utilizados en PASL, que es mayor que la lograda con la serie de pulsos de inversión adiabática inducida por flujo de PCASL; (b) la sensibilidad de la serie de etiquetado de PCASL a los efectos fuera de resonancia; y (c) los tiempos de llegada arterial más largos para PCASL, para los cuales se requiere que el plano de etiquetado intercepte las principales arterias alimentadoras con flujo en una dirección conocida, generalmente colocadas distalmente a la losa de etiquetado de PASL. En consecuencia, para cualquier estudio dado, siempre vale la pena considerar los pros y contras específicos de PCASL y PASL para elegir la opción más apropiada.
La Importancia Crítica del Tiempo de Retardo Post-Etiquetado
Un aspecto importante de todas las técnicas ASL es la introducción del retardo post-etiquetado (o tiempo de entrada) entre el final del pulso de etiquetado y el tiempo de adquisición de la imagen. Si el retardo post-etiquetado es más largo que el tiempo de tránsito más largo entre el plano de etiquetado y el volumen de imagen, la señal de ASL se vuelve insensible a las variaciones en el tiempo de llegada arterial, siempre y cuando los valores T1 de la sangre y el tejido sean similares (cierto para la sustancia gris, pero no para la sustancia blanca). Esto permite la cuantificación del FSC y minimiza la aparición de señal intravascular en las imágenes ASL, aunque a expensas de la SNR, debido a la relajación T1 del bolo. Además, la elección del retardo post-etiquetado depende de la edad del sujeto, mostrando los sujetos mayores tiempos de llegada arterial más largos. El retardo post-etiquetado recomendado para poblaciones clínicas pediátricas y adultas es de 1500 ms y 2000 ms, respectivamente.
Alteraciones del Tiempo de Tránsito: ASL con Múltiples Tiempos de Entrada
La mayoría de las secuencias ASL clínicamente disponibles utilizan solo un único retardo entre el etiquetado y la adquisición de imágenes, basado en valores originales calculados a partir de adultos jóvenes sanos. En caso de oclusión de vasos proximales, hay una llegada retardada de sangre al parénquima, lo que puede sugerir falsamente una reducción del FSC relativo estimado con ASL y un aumento de la señal ASL en los vasos arteriales alimentadores, conocido como artefacto de tránsito arterial. La reducción del gasto cardíaco, como se ve frecuentemente en poblaciones de edad avanzada, conduce a efectos similares, por ejemplo, en las regiones de la zona fronteriza vascular. El uso de secuencias ASL con múltiples tiempos de entrada tiene como objetivo superar esta deficiencia metodológica, pero debido a los tiempos de imagenización más largos requeridos, actualmente no se recomiendan en la práctica clínica diaria.
Tabla Comparativa de Técnicas de Perfusión Cerebral
| Característica | ASL (Etiquetado Spin Arterial) | FDG PET (Tomografía por Emisión de Positrones con FDG) | DSC MRI (RM de Contraste de Susceptibilidad Dinámica) |
|---|---|---|---|
| Invasividad/Contraste | No invasivo, utiliza agua como trazador endógeno. | Invasivo, utiliza trazador radiactivo (FDG). | Invasivo, utiliza agente de contraste (Gadolinio). |
| Trazador | Agua de la sangre etiquetada magnéticamente. | Glucosa radiactiva (Fluorodesoxiglucosa). | Agente de contraste paramagnético intravascular. |
| Parámetro Principal Medido | Flujo Sanguíneo Cerebral (FSC) | Metabolismo de la glucosa (indicador indirecto del metabolismo sináptico). | Variación de la susceptibilidad magnética inducida por el contraste (permite calcular FSC, Volumen Sanguíneo Cerebral - VSC, Tiempo de Tránsito Medio - TTM, etc.). |
| Aplicaciones Clínicas Típicas | Demencia, Ictus (crónico/agudo), Malformaciones AV, Epilepsia, Tumores, Trastornos Psiquiátricos. | Demencia (patrones de hipometabolismo), Epilepsia (foco interictal), Tumores. | Ictus agudo (mismatch), Tumores (VSC, diferenciación de necrosis). |
| Ventajas | No invasivo, sin radiación, cuantificación directa del FSC, se puede combinar con RM estructural, útil cuando el contraste está contraindicado. | Estándar para metabolismo, patrones bien establecidos en demencia, permite trazadores específicos (amiloide/tau). | Rápido, ampliamente disponible, estándar en ictus agudo, buena resolución espacial. |
| Desventajas | SNR limitado, sensible al tiempo de tránsito (puede subestimar con flujo lento), cuantificación puede ser desafiante, menos fiable en sustancia blanca. | Radiación, costo, resolución espacial limitada, no siempre disponible, metabolismo no es específico de la enfermedad. | Requiere contraste (riesgos en alergia/insuficiencia renal), artefactos por contraste, cuantificación de FSC más compleja, afectado por vasos grandes/cavidades de resección. |
Aplicaciones Clínicas Emergentes del ASL
Enfermedades Neurodegenerativas
La demencia, especialmente la enfermedad de Alzheimer (EA), es una de las aplicaciones prometedoras de ASL. Existe un acoplamiento estrecho entre la perfusión y el metabolismo cerebral, lo que implica que los patrones de hipometabolismo conocidos en FDG PET en la demencia pueden trasladarse a patrones de hipoperfusión en imágenes ASL. Estudios en EA establecida han demostrado consistentemente una reducción en el FSC en una distribución parietal posterior, incluyendo el precúneo, el cíngulo posterior y el giro angular, un patrón notablemente similar al visto con FDG PET. Esta similitud se mantiene incluso después de corregir por atrofia, ilustrando el valor diagnóstico independiente de ASL. Patrones similares se observan en el deterioro cognitivo leve (DCL), y hay evidencia preliminar de que la perfusión anormal en el precúneo puede predecir la conversión a EA. En la demencia frontotemporal (DFT), ASL muestra hipoperfusión predominantemente frontal, diferenciándola de la EA. ASL también puede ser útil en la demencia con cuerpos de Lewy y la demencia vascular, aunque con patrones que a veces se solapan con la EA. La capacidad de ASL para medir la perfusión en sustancia blanca es limitada, lo que representa un desafío en algunas de estas patologías.
Enfermedad Cerebrovascular
El ASL ha demostrado ser valioso en la imagenología de la isquemia cerebral. Permite obtener imágenes de perfusión sin material de contraste, lo cual es crucial para pacientes con contraindicaciones (como insuficiencia renal). Si bien el DSC sigue siendo el método predominante en el ictus agudo, estudios recientes han mostrado una concordancia razonable entre ASL y DSC para identificar el déficit de perfusión. El ASL puede ser particularmente útil cuando muestra perfusión normal o hiperperfusión (a veces vista después de la recanalización del vaso), ya que elimina la posibilidad de un mismatch difusión-perfusión que reflejaría tejido en riesgo. Para pacientes con enfermedad cerebrovascular conocida, especialmente con flujo lento o tiempos de llegada arterial prolongados, las técnicas de ASL de larga duración de etiquetado y largo retardo post-etiquetado, o el ASL multiretraso, son fundamentales para una medición adecuada de la perfusión. Estas últimas permiten medir tanto la perfusión como el tiempo de llegada arterial.
Malformaciones y Fístulas Arteriovenosas
Una aplicación clínica útil e inesperada del ASL es su capacidad para identificar lesiones con cortocircuito arteriovenoso. Dado que la mayor parte del agua etiquetada se extrae en los capilares y no llega a las venas en el tejido normal, la señal ASL en estructuras venosas es indicativa de la ausencia de un lecho capilar funcional, como ocurre en las malformaciones arteriovenosas (MAV) y las fístulas arteriovenosas durales (FAVD). La señal ASL aparece en las estructuras venosas, a menudo de manera muy llamativa. Esto puede ser más sensible que la angiografía convencional para identificar lesiones pequeñas o residuales después del tratamiento.
Epilepsia
El principal interés del ASL en el contexto de la epilepsia es localizar un posible foco epileptogénico. Durante el período peri-ictal agudo, el FSC típicamente aumenta debido a la actividad neuronal patológica, mientras que en el período interictal crónico, el FSC típicamente se reduce, ya que la región epileptogénica suele ser menos funcional y activa en comparación con el tejido cerebral normal. La hipoperfusión en las imágenes ASL se correlaciona con la hipoperfusión en las imágenes PET interictales y los datos electrofisiológicos, indicando el uso potencial de ASL para la localización del foco epiléptico.
Neoplasias
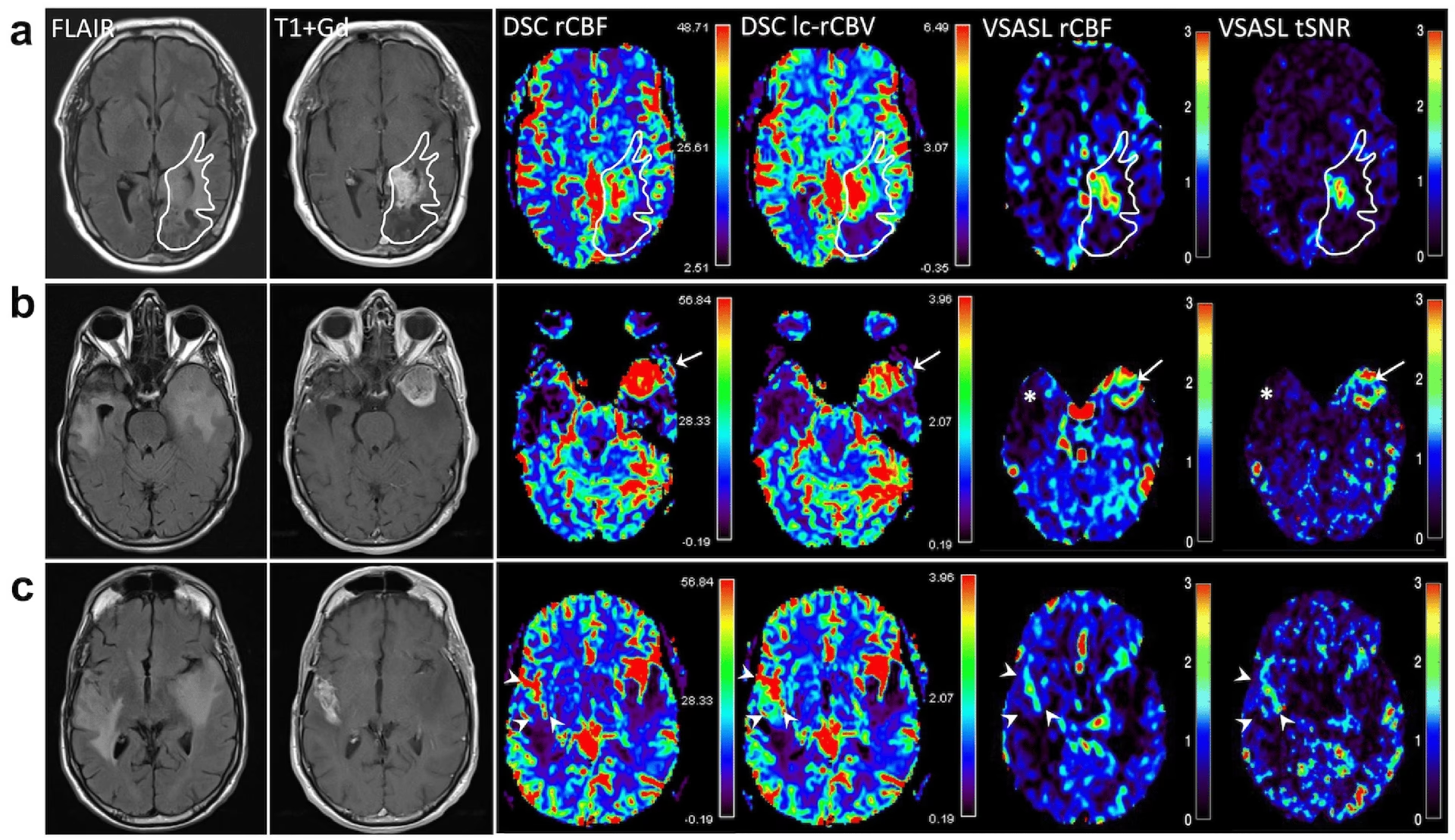
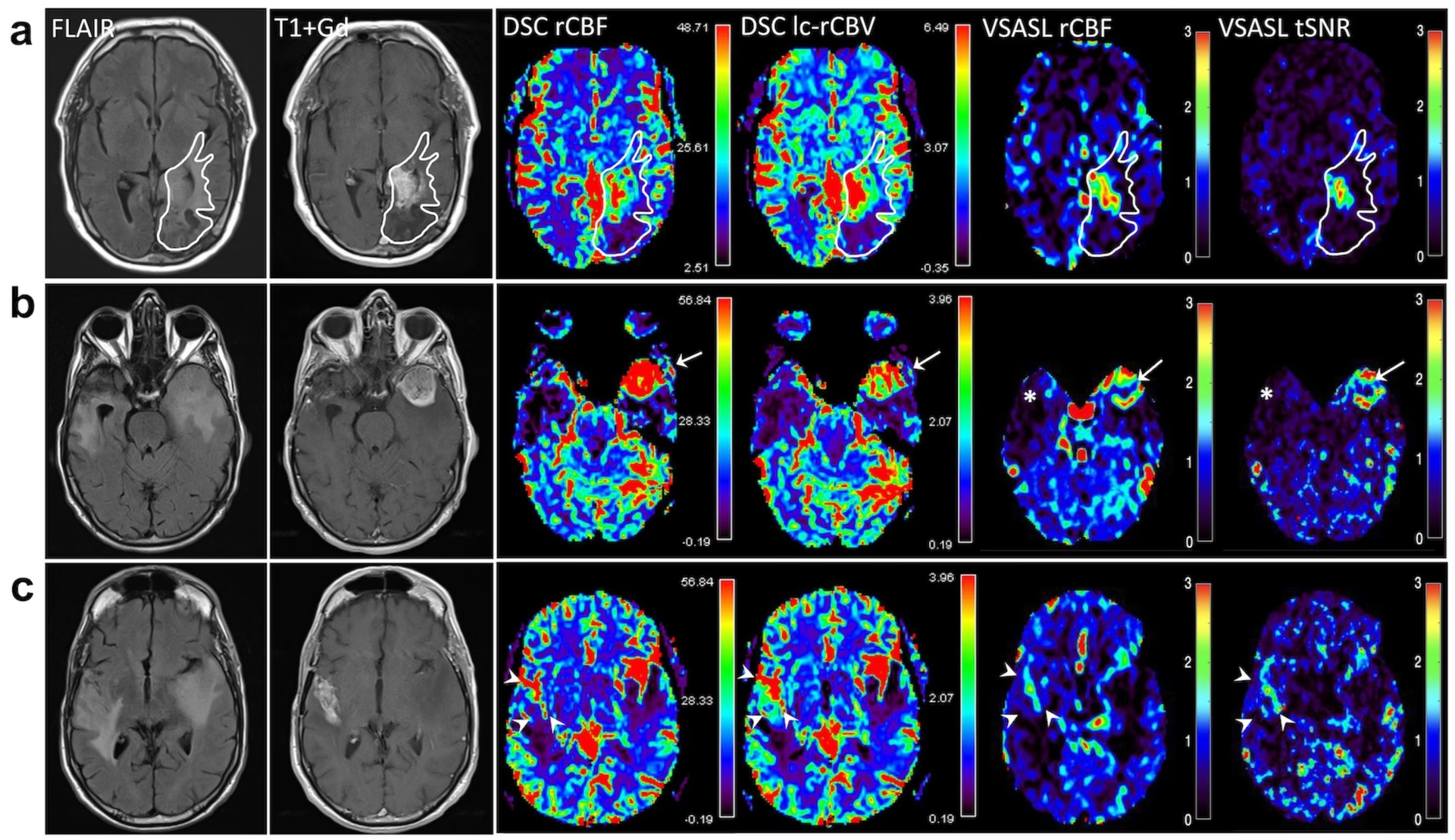
Los cambios hemodinámicos están presentes en muchas neoplasias del sistema nervioso central. En general, el FSC y el volumen sanguíneo cerebral (VSC) aumentan con el grado del tumor. ASL es de particular interés en casos donde la perfusión basada en Gadolinio está contraindicada (por ejemplo, alergia, insuficiencia renal). ASL es prometedor para diferenciar la progresión del tumor de causas benignas de realce, como la necrosis por radiación. La necrosis por radiación se asocia típicamente con FSC reducido, mientras que la mayoría de los tumores recurrentes muestran FSC aumentado. ASL puede ser superior a DSC en esta distinción, especialmente alrededor de las cavidades de resección. La naturaleza cuantitativa de ASL permite evaluar los cambios en el FSC a lo largo del tiempo o con el tratamiento para evaluar su impacto en el pronóstico.
Aplicaciones en Investigación y Otras Áreas
Enfermedades Psiquiátricas y Neurológicas
Un número creciente de investigaciones ha evaluado el ASL en diversas enfermedades psiquiátricas y neurológicas. El ASL puede detectar alteraciones sutiles donde las imágenes de RM estructural convencionales no muestran cambios visibles. Esto incluye estudios en depresión (con patrones complejos de hipo e hiperperfusión), psicosis (patrones variables de FSC), trastorno de estrés postraumático (TEPT) (alteraciones en el FSC cortical y subcortical) y lesión cerebral traumática leve (LCTM) (reducción o aumento del FSC regional, que puede persistir). ASL también se ha utilizado para investigar el dolor (cambios en el FSC en respuesta a estímulos dolorosos) y la migraña (posibles alteraciones en el FSC durante o entre ataques). Los resultados iniciales son interesantes, pero la variabilidad entre estudios subraya la necesidad de una estandarización estricta.
Extensiones del ASL
El ASL superselectivo permite mapear territorios vasculares específicos (por ejemplo, territorios de la carótida o vertebrobasilar), lo cual puede ser útil científicamente (evaluar el impacto de variantes vasculares) o clínicamente (planificación quirúrgica, evaluación de lesiones vasculares múltiples). La imagen de reserva cerebrovascular mide la capacidad del cerebro para aumentar el FSC en respuesta a un desafío (como la inhalación de CO2 o la administración de acetazolamida). Esta técnica puede desenmascarar déficits no aparentes en imágenes de rutina y es un factor de riesgo importante para eventos cerebrovasculares subsiguientes. El ASL, al ser no invasivo, es un método ideal para este tipo de pruebas de estrés.
RM Funcional (fMRI) y ASL
Los estudios de RM funcional (fMRI) generalmente se basan en el efecto dependiente del nivel de oxígeno en la sangre (BOLD) y el acoplamiento neurovascular. Dado que el efecto BOLD no mide directamente la activación neuronal sino la respuesta vascular indirecta, las alteraciones del acoplamiento neurovascular pueden influir en la señal BOLD resultante. La combinación de ASL y fMRI puede ayudar a separar las contribuciones vasculares y neuronales de la respuesta BOLD. Además, es posible utilizar las series temporales de los datos crudos de ASL para calcular mapas de activación fMRI o redes de conectividad funcional en estado de reposo, conocidos de fMRI. Aunque la calidad de estos resultados basados en ASL suele ser inferior a la de la fMRI BOLD clásica, su naturaleza cuantitativa y la posibilidad de obtenerlos junto con mapas de perfusión hacen que ASL sea una herramienta valiosa en la investigación de la función cerebral.
Limitaciones Actuales y Perspectivas Futuras
Aunque ASL ha avanzado considerablemente, aún enfrenta limitaciones. La señal ASL es intrínsecamente débil, lo que la hace susceptible al ruido (baja SNR). La precisión de la cuantificación del FSC puede verse afectada por variaciones en el tiempo de llegada arterial, aunque el ASL multiretraso mitiga este problema. La medición fiable en sustancia blanca sigue siendo un desafío. A pesar de estas limitaciones, el desarrollo metodológico continuo busca aumentar la robustez, mejorar la reproducibilidad y refinar la cuantificación del FSC. La creciente disponibilidad de implementaciones robustas de ASL en plataformas de RM comerciales y la acumulación de evidencia sobre su utilidad clínica y de investigación sugieren que ASL continuará expandiendo su papel en la neuroimagen.
Preguntas Frecuentes sobre la Perfusión Cerebral por ASL
¿Qué es la Perfusión Cerebral por ASL?
Es una técnica de Resonancia Magnética no invasiva que mide el flujo sanguíneo cerebral utilizando el agua de la sangre arterial como trazador magnético natural, sin necesidad de inyectar un agente de contraste externo.
¿Cómo funciona el ASL?
Funciona etiquetando magnéticamente el agua de la sangre que fluye hacia el cerebro. Luego se adquieren imágenes y se compara la señal de las imágenes con sangre etiquetada con las de control (sin etiquetar). La diferencia de señal está relacionada con la cantidad de sangre que ha llegado al tejido, permitiendo estimar el flujo sanguíneo.
¿Es seguro el ASL?
Sí, el ASL se considera seguro ya que no requiere la inyección de agentes de contraste intravenosos ni implica exposición a radiación ionizante, a diferencia de otras técnicas como el PET o el DSC MRI con Gadolinio.
¿Qué enfermedades puede ayudar a diagnosticar o evaluar el ASL?
El ASL es útil en diversas condiciones neurológicas y psiquiátricas, incluyendo la demencia (para identificar patrones de hipoperfusión), el ictus (tanto agudo como crónico), malformaciones arteriovenosas, epilepsia (para localizar focos), tumores cerebrales (especialmente cuando el contraste está contraindicado, o para diferenciar recurrencia de necrosis por radiación) y trastornos como el TEPT o la LCTM.
¿Cuál es la diferencia entre ASL y un MRI con contraste?
Un MRI con contraste típicamente utiliza un agente (como el Gadolinio) inyectado para realzar ciertas estructuras o patologías. El ASL es un tipo de técnica de RM que *no* requiere la inyección de un contraste externo; utiliza el agua de la sangre como "contraste" endógeno al etiquetarla magnéticamente.
¿El ASL puede reemplazar otras técnicas de perfusión o funcionales como PET o DSC?
En muchos casos, ASL proporciona información comparable y complementaria. Puede ser una alternativa viable, especialmente cuando el contraste o la radiación son una preocupación (p. ej., en insuficiencia renal, alergias, o estudios repetidos/pediátricos). Sin embargo, cada técnica tiene sus fortalezas y debilidades, y la elección depende de la aplicación clínica específica y la disponibilidad.
¿Qué significa el Tiempo de Retardo Post-Etiquetado (PLD)?
Es el tiempo entre el momento en que se etiqueta la sangre arterial y el momento en que se adquiere la imagen. Es crucial para asegurar que la sangre etiquetada haya tenido tiempo de llegar al tejido cerebral antes de ser medida. Un PLD incorrecto puede llevar a subestimaciones del flujo, especialmente en casos de flujo sanguíneo lento.
Si quieres conocer otros artículos parecidos a Perfusión Cerebral por ASL: Una Mirada Profunda puedes visitar la categoría Neurociencia.