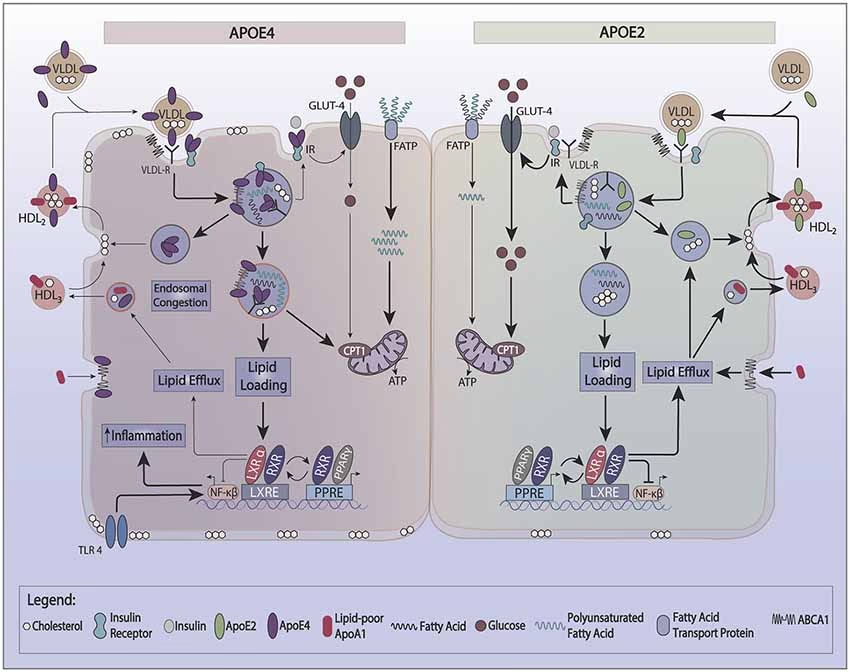
La Apolipoproteína E (ApoE) es una proteína bien conocida por su papel fundamental en el metabolismo de los lípidos en el cuerpo. Sin embargo, la investigación reciente ha revelado que sus funciones se extienden mucho más allá del simple transporte de grasas, jugando roles complejos tanto en el sistema inmunológico como, de manera crucial, en el funcionamiento y la salud del sistema nervioso central (SNC).
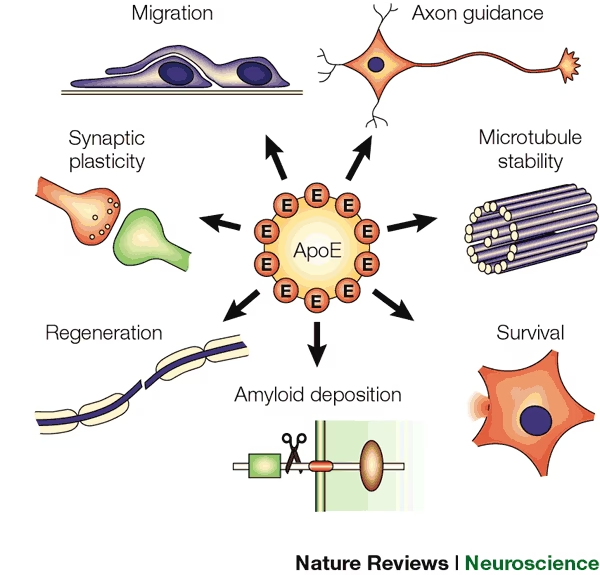
En el contexto del sistema inmune, particularmente en enfermedades neuroinflamatorias, la ApoE ha surgido como un actor potencial. Paralelamente, en el cerebro, la ApoE y sus receptores desempeñan roles intrincados que son vitales para la función sináptica, la plasticidad y el mantenimiento neuronal. Comprender estas funciones multifacéticas es clave para desentrañar los mecanismos subyacentes de diversas enfermedades, desde trastornos neurodegenerativos como el Alzheimer hasta condiciones inflamatorias crónicas como la Esclerosis Múltiple (EM).
- ApoE y su Misterioso Vínculo con la Esclerosis Múltiple
- Los Receptores de ApoE: Centinelas de la Función Celular
- Más Allá del Lípido: Receptores de ApoE en el Sistema Nervioso Central
- Reelin, Receptores de ApoE y la Señalización Sináptica
- Regulación del Calcio y Receptores de ApoE
- Polimerización de Actina Postsináptica
- ApoE e Isoformas: Impacto en el Tráfico Endocítico
- Roles Presinápticos de los Receptores de ApoE
- El Rol Crucial de los Astrocitos y los Receptores de ApoE
- Tabla de Frecuencias de Genotipo ApoE
- Preguntas Frecuentes sobre ApoE y sus Receptores
- ¿Qué es la Apolipoproteína E (ApoE)?
- ¿Cuál es la función principal de los receptores de ApoE?
- ¿Cómo se relaciona ApoE con la Esclerosis Múltiple?
- ¿Por qué el alelo *APOE ε4* se asocia con mayor riesgo de Enfermedad de Alzheimer?
- ¿Los receptores de ApoE solo se encuentran en las neuronas?
- ¿Qué es Reelin y cómo interactúa con los receptores de ApoE?
- Conclusiones
ApoE y su Misterioso Vínculo con la Esclerosis Múltiple
La Esclerosis Múltiple es una enfermedad crónica, inflamatoria y desmielinizante que afecta principalmente al sistema nervioso central. Se caracteriza por la infiltración de células inmunes, como linfocitos y macrófagos, que causan daño a la mielina y los axones. Aunque su etiología es multifactorial y su patogénesis aún no está completamente clara, diversos estudios han explorado el papel de la ApoE en esta enfermedad.
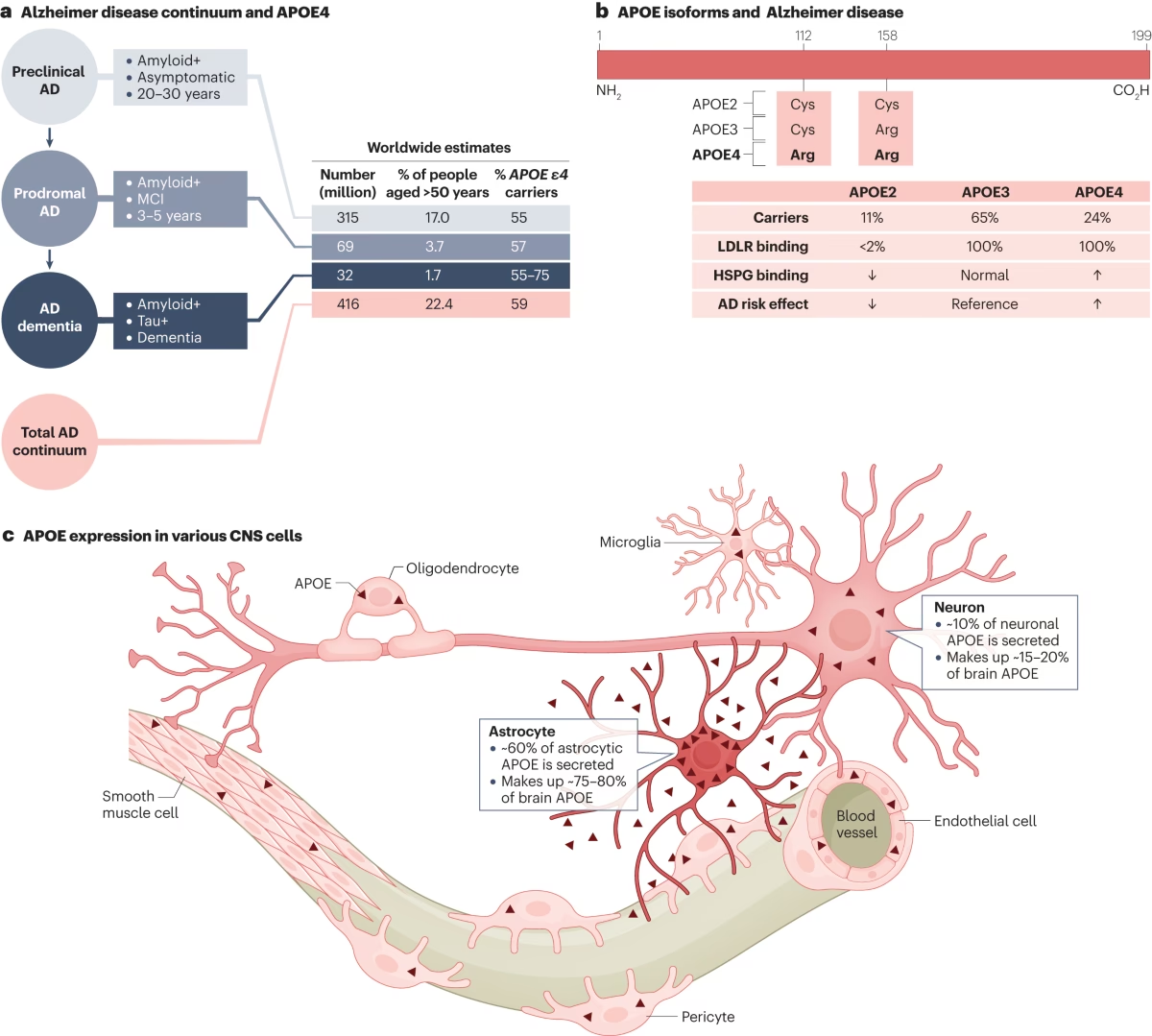
El interés en la ApoE en el contexto de la EM a menudo se centra en sus diferentes isoformas, codificadas por los alelos *APOE ε2*, *APOE ε3* y *APOE ε4*. La isoforma ε4, en particular, ha sido extensamente estudiada debido a su conocida asociación con un mayor riesgo de Enfermedad de Alzheimer. Se ha planteado la hipótesis de que los genotipos de ApoE podrían influir en los mecanismos de mantenimiento y reparación del sistema nervioso, lo que podría llevar a cursos clínicos distintos en la EM dependiendo de la presencia de un alelo específico.
Un estudio utilizando imágenes por resonancia magnética (IRM) en pacientes con EM encontró volúmenes cerebrales totales más bajos en portadores del alelo ε4 en comparación con aquellos que no lo portaban. Este hallazgo sugiere que la restauración neuronal comprometida asociada al *APOE ε4* podría estar relacionada con una mayor destrucción tisular en la EM. Sin embargo, la frecuencia relativamente baja del alelo *APOE ε4*, especialmente el genotipo *APOE 4/4*, en la población general hace que sea difícil sacar conclusiones definitivas sin estudios a gran escala.
Niveles de ApoE en Fluidos Biológicos de Pacientes con EM
La búsqueda de biomarcadores útiles para evaluar el curso y el pronóstico de la EM es un área de investigación activa. Varios estudios han analizado los niveles de ApoE en el líquido cefalorraquídeo (LCR) y el suero de pacientes con EM, aunque los resultados han sido contradictorios.
En algunos estudios, se observó una disminución de los niveles de ApoE en el LCR de pacientes con EM, de forma similar a lo reportado en el Síndrome de Guillain-Barré (SGB), una neuropatía periférica análoga a la EM. Otros estudios también mostraron concentraciones más bajas de ApoE en el suero de pacientes con EM en comparación con sujetos sanos. Dada la limitada permeabilidad de la barrera hematoencefálica a la ApoE, una disminución en el LCR podría deberse a una reducción de la síntesis local de ApoE en el cerebro. Sin embargo, la disminución en suero es más difícil de explicar y podría ser parte de una respuesta de fase aguda suprimida.
Por otro lado, otros estudios no encontraron esta disminución de ApoE en el LCR, o incluso reportaron resultados completamente opuestos, mostrando niveles más altos. La falta de correlación clara entre los niveles de ApoE en suero o LCR con la edad, el curso clínico o el pronóstico de la EM en algunos estudios, junto con la heterogeneidad del estado inflamatorio y la integridad de la barrera hematoencefálica en diferentes etapas de la enfermedad, podrían explicar estas discrepancias. Se necesitan investigaciones más amplias y con estratificación detallada para aclarar estos hallazgos.
Alelos de APOE y Características Clínicas de la EM
La posible implicación de la ApoE en la EM se ha visto reforzada por estudios de ligamiento genético que identificaron el cromosoma 19q13, donde se encuentra el gen *APOE*, como candidato para enfermedades autoinmunes. La distribución geográfica de la frecuencia del alelo *APOE ε4* en Europa, con un gradiente creciente de sur a norte, muestra una similitud con la incidencia de la EM, lo que llevó a la hipótesis de que una mayor frecuencia de *APOE ε4* podría estar asociada con la enfermedad.
Sin embargo, la mayoría de los estudios no han confirmado una alteración significativa en la distribución de los alelos de *APOE* en pacientes con EM en comparación con poblaciones sanas. La rareza de los homocigotos *APOE 4/4* tanto en sujetos sanos como en pacientes con EM ha dificultado el estudio de esta asociación específica. Solo unos pocos estudios han abordado esta cuestión, sin llegar a una conclusión positiva, con una notable excepción que sugirió que la homocigosidad para *APOE ε4* podría ser más común en pacientes con EM. Se requieren más estudios a gran escala para dilucidar completamente la distribución de los alelos de *APOE* en la EM.
A pesar de las presunciones, los estudios de asociación alélica previos no han confirmado una relación clara entre el alelo *APOE ε4* y la susceptibilidad a la EM. Algunos estudios han explorado si los alelos de *APOE* influyen en la edad de inicio de la enfermedad, con resultados contradictorios. Mientras que un estudio sugirió un inicio más temprano en portadores de *APOE ε4* (especialmente en mujeres afroamericanas en comparación con caucásicas), la mayoría de los otros no encontraron tal asociación positiva.
La clasificación de la EM se basa en subtipos clínicos como la EM Remitente-Recurrente (EMRR), la EM Primaria Progresiva (EMPP), la EM Secundaria Progresiva (EMSP) y la EM Progresiva Recurrente (EMPR). Hasta la fecha, no hay evidencia clara de una asociación entre el polimorfismo de ApoE y un subtipo clínico específico de EM. La mayoría de los estudios han negado esta asociación, aunque el tamaño muestral relativamente pequeño en muchas investigaciones puede haber limitado su poder estadístico.
La Escala Expandida del Estado de Discapacidad (EDSS) es el método más común para cuantificar la gravedad y la tasa de progresión de la EM. Varios estudios han examinado la relación entre los alelos de *APOE* y la gravedad de la enfermedad, nuevamente con resultados inconsistentes. Algunos estudios, utilizando biomarcadores de daño axonal o análisis en cohortes de pacientes, sugirieron que los portadores de *APOE ε4* podrían tener enfermedades más graves. Sin embargo, otros estudios no encontraron esta asociación, o la limitaron solo a mujeres. Además, algunas investigaciones revelaron que *APOE ε4* no se asociaba con un curso clínico más grave ni parecía influir en la recuperación de las exacerbaciones. La heterogeneidad de las manifestaciones clínicas y el tamaño de la muestra en estos estudios podrían explicar los resultados contradictorios, sugiriendo que la relación entre *APOE ε4* y la gravedad clínica, si existe, podría no ser muy fuerte.
APOE y la Progresión de la EM
Si los alelos de *APOE* influyen en las recaídas o la progresión de la EM es otra área de investigación con resultados mixtos. Si bien la mayoría de los estudios iniciales apoyaron la hipótesis de una asociación entre el alelo *APOE ε4* y una progresión más rápida de la enfermedad, otros no lo hicieron. Datos de neuroimagen han mostrado una pérdida acelerada de tejido cerebral y una mayor proporción de lesiones que evolucionan a "agujeros negros" en pacientes con EM portadores de *APOE ε4*, con una reducción anual del volumen cerebral significativamente mayor en estos individuos. Estos hallazgos de imagen sugieren que *APOE ε4* podría estar relacionado con una progresión más severa.
Algunos estudios reportaron que la presencia del alelo *APOE ε4* se asociaba con un peor pronóstico evaluado por EDSS y otros índices, mientras que un metaanálisis no respaldó consistentemente este hallazgo. Es importante destacar que la mayoría de estos estudios son retrospectivos, lo que puede introducir limitaciones en la evaluación precisa de la progresión. A pesar de no estar completamente claro, se postula que la isoforma ApoE ε4, debido a su mayor afinidad por los lípidos, podría asociarse con un peor pronóstico en la EM, relacionado con una capacidad comprometida de remielinización o regeneración.
ApoE y Deterioro Cognitivo en la EM
El deterioro cognitivo es una manifestación común en la EM, afectando hasta el 65% de los pacientes y a menudo presentándose en las etapas tempranas. La asociación entre el alelo *APOE ε4* y los déficits cognitivos en la EM ha sido respaldada por numerosos estudios. Sin embargo, la interpretación debe ser cautelosa, ya que el deterioro cognitivo en la EM puede ser tanto un síntoma directo del daño a la mielina y axonal, reflejando la gravedad de la enfermedad, como una manifestación temprana de una neurodegeneración subyacente (como la Enfermedad de Alzheimer) que coexiste pero es independiente de la EM per se.
Curiosamente, se ha observado que la presencia del alelo *APOE ε2* podría ser protectora contra los síntomas depresivos en la EM, una condición común que interactúa con las funciones cognitivas y no cognitivas. Se necesitan más estudios para comprender los mecanismos detrás de este posible efecto protector.
Los Receptores de ApoE: Centinelas de la Función Celular
Los receptores de ApoE son miembros de la familia de receptores de lipoproteínas de baja densidad (LDL), una familia antigua y altamente conservada. Inicialmente identificados por su papel en el transporte de partículas lipoproteicas, esta familia incluye siete miembros principales: receptor de LDL (LDLR), receptor relacionado con LDLR 1 (LRP1), receptor de lipoproteínas de muy baja densidad (VLDLR), Megalina (LRP2), receptor de Apolipoproteína E 2 (Apoer2 o LRP8), LRP4 y LRP1b.
Todos comparten una estructura conservada que les permite interactuar con la ApoE, razón por la cual los términos "familia de receptores de LDL" y "receptores de ApoE" a menudo se usan como sinónimos. Su estructura incluye un dominio intracelular corto que media la transducción de señales y el tráfico, un dominio transmembrana y un gran dominio extracelular responsable de la unión al ligando.
El papel clásico de estos receptores es mediar la captación celular de partículas lipídicas. Por ejemplo, LDLR y LRP1 se unen a partículas de ApoE en remanentes de quilomicrones y VLDL. Este proceso es crucial para la homeostasis del colesterol, y las deficiencias en ApoE o LDLR pueden llevar a hipercolesterolemia severa.
Más Allá del Lípido: Receptores de ApoE en el Sistema Nervioso Central
En el SNC, el colesterol y los fosfolípidos producidos por las células gliales son vitales para la formación y el mantenimiento de sinapsis saludables. La mayor parte del colesterol es liberado por los astrocitos en forma de partículas que contienen ApoE. La deficiencia de ApoE en el cerebro, incluso si se limita al SNC, resulta en una reducción del número de sinapsis. Esto subraya un papel de la ApoE y sus receptores que va más allá del simple transporte de lípidos.
En el cerebro, la ApoE se une a varios receptores, incluyendo Ldlr, Lrp1, Apoer2 y Vldlr. Estos receptores desempeñan una variedad de funciones adicionales a las del tráfico de lípidos, como la transmisión sináptica, la modulación de la estructura de las espinas dendríticas y la función de los astrocitos.
Reelin, Receptores de ApoE y la Señalización Sináptica
Varios receptores de ApoE, especialmente Lrp1, Apoer2 y Vldlr, se han identificado en la densidad postsináptica, donde interactúan con componentes sinápticos clave. Por ejemplo, Lrp1 interactúa con el receptor NMDA (NMDAR), promoviendo su endocitosis. Apoer2/Lrp8 y Vldlr forman complejos con proteínas de andamiaje como PSD-95 y los receptores de glutamato.
El ligando principal para Apoer2 y Vldlr en el SNC no es la ApoE, sino la glicoproteína Reelin. Reelin es una proteína extracelular secretada con numerosas funciones, crucial para la migración neuronal y la estratificación cortical durante el desarrollo cerebral. En el cerebro adulto, Reelin es secretada por interneuronas GABAérgicas y neuronas glutamatérgicas, y sus niveles disminuyen con la edad y en la Enfermedad de Alzheimer.
Cuando Apoer2/Lrp8 y Vldlr se unen a Reelin, se agrupan e inducen la fosforilación de la proteína adaptadora Disabled-1 (Dab1). Esto tiene varias consecuencias importantes. Primero, la activación de Src y Fyn mediada por Dab1 conduce a la fosforilación de las subunidades NR2 de los NMDARs, lo que aumenta la entrada de Ca2+ cuando los receptores se activan y reduce la endocitosis de NMDARs. Esto resulta en una mayor entrada neta de Ca2+ en la dendrita y promueve la potenciación a largo plazo (LTP).
Segundo, Dab1 activa PI3 quinasa y posteriormente Akt, que fosforila GSK3β, reduciendo la fosforilación de sus dianas, incluida la proteína tau, relevante en el contexto del Alzheimer. Estos efectos de Reelin son protectores de la función sináptica.
En contraste, los oligómeros de beta-amiloide (Aβ), una característica patológica del Alzheimer, tienen efectos antagónicos. Aβ se une a receptores nicotínicos de acetilcolina α7 y receptores metabotrópicos de glutamato (mGluR5), activando la calcineurina (PP2B). PP2B regula STEP, que desfosforila y desactiva Fyn, y desfosforila los mismos residuos de tirosina en NMDARs que son fosforilados por Reelin-Apoer2. Esto lleva a una endocitosis excesiva de NMDARs. Además, Aβ activa GSK3β, lo que reduce la LTP y puede inducir la hiperfosforilación de tau. Como resultado, los oligómeros de Aβ reducen la LTP. Es importante destacar que la aplicación de Reelin puede prevenir la reducción de LTP inducida por Aβ.
Las alteraciones en la señalización de Reelin en el cerebro adulto se han implicado en trastornos neuropsiquiátricos. Aunque Reelin es vital para el desarrollo, la deficiencia de ApoE no lo es, lo que sugiere roles distintos. La pérdida de Reelin en ratones adultos no causa un deterioro cognitivo significativo en ausencia de patología amiloide, pero la sobreexpresión de Aβ en ratones deficientes en Reelin resulta en un deterioro cognitivo severo. Esto subraya el papel protector de Reelin y la señalización de sus receptores contra los efectos deletéreos de Aβ.
Regulación del Calcio y Receptores de ApoE
La desregulación de la homeostasis del Ca2+ es un mecanismo intensamente estudiado sobre cómo Aβ causa disfunción sináptica temprana. El flujo de Ca2+ es fundamental para la regulación de la fuerza sináptica, desencadenando LTP o depresión a largo plazo (LTD). En el Alzheimer, la homeostasis del Ca2+ tiende a niveles de reposo más altos, lo que se ha demostrado en modelos de ratón y en respuesta a Aβ. Varios mecanismos propuestos para el efecto de Aβ incluyen la mejora directa de la entrada de Ca2+ a través de receptores (posiblemente NMDARs extrasinápticos) o la acción de los oligómeros de Aβ como canales de fuga de calcio.
Los almacenes intracelulares de calcio, como el retículo endoplasmático, también se ven afectados en el Alzheimer, con la presenilina 1 jugando un papel en la regulación de la liberación de Ca2+. La disfunción de los sistemas de amortiguación y detección de Ca2+ (como calbindina D-28k y calmodulina), cuyos niveles se reducen con la edad y en el Alzheimer, junto con el aumento de las fugas de Ca2+, exacerba la desregulación del Ca2+ y la transmisión sináptica.
El efecto principal de los niveles más altos de Ca2+ en reposo parece inclinar la balanza de la plasticidad sináptica hacia la LTD, lo que podría resultar en la pérdida de huellas de memoria y sinapsis. Los receptores de ApoE activados por Reelin son esenciales para mantener la fuerza de la señal frente al "ruido" de los niveles crecientes de Ca2+ inducidos por los mecanismos del Alzheimer. Este mecanismo proporciona protección a la sinapsis, manteniendo su fuerza en las etapas tempranas de la enfermedad hasta que Aβ y tau se acumulan a niveles insuperables.
Polimerización de Actina Postsináptica
El mantenimiento de la homeostasis del Ca2+ es crucial para la regulación de la señalización postsináptica, que a su vez es importante para el crecimiento, mantenimiento y retracción de las espinas dendríticas, los principales sitios de transmisión postsináptica. Este proceso dinámico continúa a lo largo de la vida y depende de múltiples señales.
Aquí, Reelin y los receptores de ApoE juegan un papel en la complejidad dendrítica a través del control de la polimerización de la actina. La señalización de Reelin activa PI3 quinasa, que inicia una cascada que induce la fosforilación de LIM quinasa-1 (LIMK-1), la cual a su vez fosforila cofilina en un sitio inhibidor. Esto bloquea la actividad despolimerizadora de la actina de cofilina. Como resultado, la polimerización de actina y el crecimiento de las espinas dendríticas muestran un aumento neto en presencia de Reelin. En contraste, Aβ tiene el efecto opuesto, reduciendo la actividad de LIMK, lo que lleva a cofilina activa desfosforilada, despolimerización de filamentos de actina y la formación de agregados de actina.
Aunque no se ha demostrado definitivamente una oposición directa entre Reelin y Aβ a nivel de la polimerización de actina, se ha observado que los ratones con reemplazo dirigido de *APOE ε4* tienen una reducción en la complejidad de las espinas dendríticas, un hallazgo que se refleja en portadores humanos de *APOE ε4*. Esto sugiere que los receptores de ApoE desempeñan un papel importante en la neurona postsináptica, separado de la modulación de la plasticidad sináptica, al regular los cambios estructurales en la propia espina dendrítica.
ApoE e Isoformas: Impacto en el Tráfico Endocítico
Las diferentes isoformas de ApoE (ε2, ε3, ε4) difieren en solo dos residuos de aminoácido (112 y 158). ApoE2 tiene cisteína en ambos, ApoE3 cisteína en 112 y arginina en 158, y ApoE4 arginina en ambos. La presencia de arginina en la posición 112 en ApoE4 favorece una interacción entre sus dominios N-terminal y C-terminal, dándole una mayor tendencia a formar estructuras específicas y a agregarse a 37°C.
Estas diferentes propiedades estructurales de ApoE4 tienen un efecto importante en su papel en el tráfico de receptores. En condiciones normales, las partículas que contienen ApoE son internalizadas por los receptores, los cuales son luego reciclados de vuelta a la superficie celular a través de endosomas de reciclaje. Sin embargo, cuando ApoE4 está presente, el paso final del reciclaje se retrasa y el proceso se estanca en el endosoma, presumiblemente debido a la propensión de ApoE4 a formar estructuras agregadas en el pH más bajo del endosoma. Esto significa que, en presencia de *APOE ε4*, el reciclaje de los receptores de Reelin y los receptores de glutamato atrapados en la misma vesícula de vuelta a la sinapsis se ralentiza, la señalización de Reelin se atenúa y la homeostasis de los receptores de glutamato se ve afectada.
De esta manera, *APOE ε4* induce un estado de "resistencia a Reelin" que probablemente afecta no solo la plasticidad sináptica, sino también la homeostasis del Ca2+, la remodelación de espinas y los roles presinápticos y astrocíticos. Este mecanismo contribuye a la disfunción neuronal temprana observada en portadores de *APOE ε4*.
Roles Presinápticos de los Receptores de ApoE
Aunque la mayoría de la investigación se ha centrado en los roles postsinápticos, datos emergentes indican que los receptores de ApoE también tienen un papel importante en la regulación de la liberación de vesículas presinápticas. Estudios recientes han demostrado que Apoer2 y Vldlr también se expresan en la membrana presináptica.
La señalización de Reelin a través de Apoer2 y Vldlr en la membrana presináptica conduce a elevaciones transitorias de Ca2+ intracelular. Esta elevación de Ca2+ aumenta específicamente la fusión de vesículas que contienen VAMP7, una proteína SNARE alternativa que participa en la liberación espontánea de vesículas. Reelin no parece afectar otras señalizaciones mediadas por proteínas SNARE. Aunque aún no se ha determinado el efecto de las isoformas de ApoE en estos cambios presinápticos, es probable que *APOE ε4* tenga un impacto similar al que ejerce en la postsinapsis.
Otro rol presináptico para los receptores de ApoE podría implicar la producción de glutamato. Estudios en ratones con reemplazo dirigido de *APOE ε4* han mostrado niveles disminuidos de glutamato, niveles aumentados de glutamina (su precursor) y un aumento tardío en el transportador vesicular de glutamato 1 (vglut1). Esto sugiere una capacidad reducida de las neuronas presinápticas con *APOE ε4* para convertir glutamina en glutamato y un aumento compensatorio en la carga vesicular de glutamato. Se necesitan más estudios para determinar el impacto de esta alteración en la producción de glutamato in vivo.
El Rol Crucial de los Astrocitos y los Receptores de ApoE
La mayor parte de la ApoE en el cerebro es expresada por los astrocitos. La ApoE derivada de astrocitos es importante para el transporte de colesterol a través de partículas tipo HDL que contienen ApoE, las cuales juegan un papel vital en el desarrollo y mantenimiento sináptico. Interesantemente, datos recientes sugieren que la ApoE y sus receptores median procesos en los astrocitos más allá del tráfico de lípidos.
Un posible papel de la señalización de los receptores de ApoE en los astrocitos es la modulación de la poda sináptica. Los astrocitos participan activamente en la poda sináptica fagocitando sinaptosomas (estructuras que contienen terminales presinápticos y postsinápticos). Las isoformas de ApoE afectan diferencialmente este proceso, con *APOE ε4* limitando la capacidad de los astrocitos para podar sinapsis. Lrp1, altamente expresado en astrocitos, es responsable de la fagocitosis de mielina degradada y es probable que medie, al menos en parte, el efecto de las isoformas de ApoE en la poda sináptica.
Además de la poda, la importancia de los astrocitos para una transmisión sináptica efectiva es cada vez más reconocida. Los astrocitos pueden detectar la actividad sináptica a través de receptores glutamatérgicos. El flujo iónico a través de estos receptores causa alteraciones en los almacenes intracelulares de Ca2+ que desencadenan la liberación de diversas sustancias desde el astrocito, incluyendo glutamato, D-serina y ATP. Este proceso, llamado "gliotransmisión", puede afectar la transmisión sináptica.
Recientemente se describió un papel para Lrp4 en la gliotransmisión. En los astrocitos, la señalización de Agrina a través de Lrp4 conduce a un aumento en la liberación de ATP, que luego se metaboliza a adenosina en el espacio extracelular. La adenosina actúa sobre los receptores de adenosina A1 (A1A) en la membrana presináptica, reduciendo la probabilidad de liberación de vesículas que contienen glutamato y, por lo tanto, disminuyendo la transmisión glutamatérgica. El mecanismo exacto por el cual la señalización Agrina-Lrp4 regula la liberación de ATP desde los astrocitos aún no está claro.
Al discutir los efectos de la señalización de los receptores de ApoE en los astrocitos, es importante señalar que la activación glial se ve afectada por la isoforma de ApoE, con *APOE ε4* causando la mayor activación. La activación glial es un indicador de cambios proinflamatorios que se encuentran comúnmente en cerebros con Alzheimer. Aunque va más allá del alcance directo de este artículo, es un aspecto crucial de la interacción entre ApoE, los astrocitos y la neuroinflamación.
En resumen, los astrocitos, a menudo considerados solo células de soporte, son partes activas de la sinapsis tripartita, y los receptores de ApoE están involucrados activamente en la configuración de sus funciones. A medida que el campo avanza, surgirán más estudios que evalúen estos nuevos roles en la neurodegeneración.
Tabla de Frecuencias de Genotipo ApoE
Para ilustrar la distribución de los genotipos de ApoE en poblaciones sanas, presentamos datos de dos estudios a gran escala mencionados en la literatura proporcionada:
| Genotipo | Prevalencia (%) - Utermann et al. [62] | Prevalencia (%) - Menzel et al. [63] |
|---|---|---|
| E4/4 | 2.8 | 2.3 |
| E3/3 | 59.8 | 62.7 |
| E2/2 | 1.0 | 0.8 |
| E4/3 | 22.9 | 20.3 |
| E4/2 | 1.5 | 3.0 |
| E3/2 | 12.0 | 11.0 |
| Sujetos Totales | 1031 | 1000 |
Esta tabla muestra que el genotipo *APOE 3/3* es, con diferencia, el más común, mientras que los genotipos que incluyen el alelo *APOE ε4* (E4/4, E4/3, E4/2) representan una porción significativa de la población, y el genotipo *APOE 4/4* es relativamente raro.
Preguntas Frecuentes sobre ApoE y sus Receptores
¿Qué es la Apolipoproteína E (ApoE)?
La Apolipoproteína E es una proteína que participa en el metabolismo de los lípidos, transportando colesterol y otras grasas en la sangre y el cerebro. Es codificada por el gen *APOE*, que tiene tres alelos principales: ε2, ε3 y ε4, dando lugar a diferentes isoformas proteicas.
¿Cuál es la función principal de los receptores de ApoE?
Los receptores de ApoE, que forman parte de la familia de receptores de LDL, tienen como función principal la internalización de partículas lipoproteicas que contienen ApoE, siendo cruciales para el metabolismo del colesterol. Sin embargo, en el cerebro, también tienen roles importantes en la señalización sináptica, la plasticidad y la función glial, interactuando con otros ligandos como Reelin.
¿Cómo se relaciona ApoE con la Esclerosis Múltiple?
Existe investigación que explora la asociación entre los alelos de *APOE*, especialmente el *APOE ε4*, y la susceptibilidad, gravedad y progresión de la Esclerosis Múltiple. Los resultados son contradictorios, pero sugieren una posible influencia en los mecanismos de reparación neuronal y neuroinflamación, aunque no hay una conclusión definitiva.
¿Por qué el alelo *APOE ε4* se asocia con mayor riesgo de Enfermedad de Alzheimer?
El alelo *APOE ε4* aumenta el riesgo de Enfermedad de Alzheimer de aparición tardía. Se cree que esto se debe a varios mecanismos, incluyendo una menor capacidad para eliminar el péptido beta-amiloide (lo que favorece su acumulación) y un impacto negativo en la función sináptica al alterar el tráfico de los receptores de ApoE, lo que lleva a una especie de "resistencia" a señales protectoras como la de Reelin.
¿Los receptores de ApoE solo se encuentran en las neuronas?
No. Aunque son cruciales para la función sináptica (en las membranas pre y postsinápticas), los receptores de ApoE también se encuentran en otros tipos celulares del cerebro, como los astrocitos, donde desempeñan roles en el transporte de lípidos, la poda sináptica y la gliotransmisión.
¿Qué es Reelin y cómo interactúa con los receptores de ApoE?
Reelin es una glicoproteína secretada que actúa como ligando principal para algunos receptores de ApoE (Apoer2 y Vldlr) en el SNC. La unión de Reelin a estos receptores activa cascadas de señalización que son importantes para la migración neuronal durante el desarrollo y, en el cerebro adulto, para la plasticidad sináptica, la homeostasis del Ca2+ y la estabilidad del citoesqueleto de actina, contrarrestando parcialmente los efectos negativos de Aβ.
Conclusiones
La ApoE y su familia de receptores son mucho más que meros actores en el metabolismo de los lípidos. Desempeñan roles intrincados y vitales en el sistema nervioso central, regulando la función sináptica, la plasticidad, la homeostasis del calcio, la estructura dendrítica y las interacciones con las células gliales como los astrocitos. La influencia de las diferentes isoformas de ApoE, particularmente el APOE ε4, en estos procesos es significativa y se asocia con un mayor riesgo de trastornos neurodegenerativos como el Alzheimer, en parte al comprometer la función de sus receptores y la señalización protectora de Reelin.
En el contexto de la Esclerosis Múltiple, si bien la asociación no es tan clara ni consistente como en el Alzheimer, la investigación sugiere un posible papel del genotipo de ApoE en la susceptibilidad, la gravedad y la progresión de la enfermedad, posiblemente a través de mecanismos relacionados con la neuroinflamación, la reparación neuronal y el daño tisular. Los resultados contradictorios en los estudios de EM resaltan la complejidad de esta enfermedad y la necesidad de investigaciones más amplias y detalladas.
La comprensión completa de las múltiples funciones de la ApoE y sus receptores, y cómo las diferentes isoformas impactan estos roles, es fundamental para desarrollar nuevas estrategias terapéuticas dirigidas a abordar enfermedades neurológicas y neuroinflamatorias. La investigación futura deberá seguir desentrañando los mecanismos moleculares precisos por los cuales ApoE y sus receptores influyen en la comunicación neuronal y glial, y cómo estos procesos se ven alterados en la enfermedad.
Si quieres conocer otros artículos parecidos a ApoE: Rol en Inmunidad y SNC puedes visitar la categoría Neurociencia.