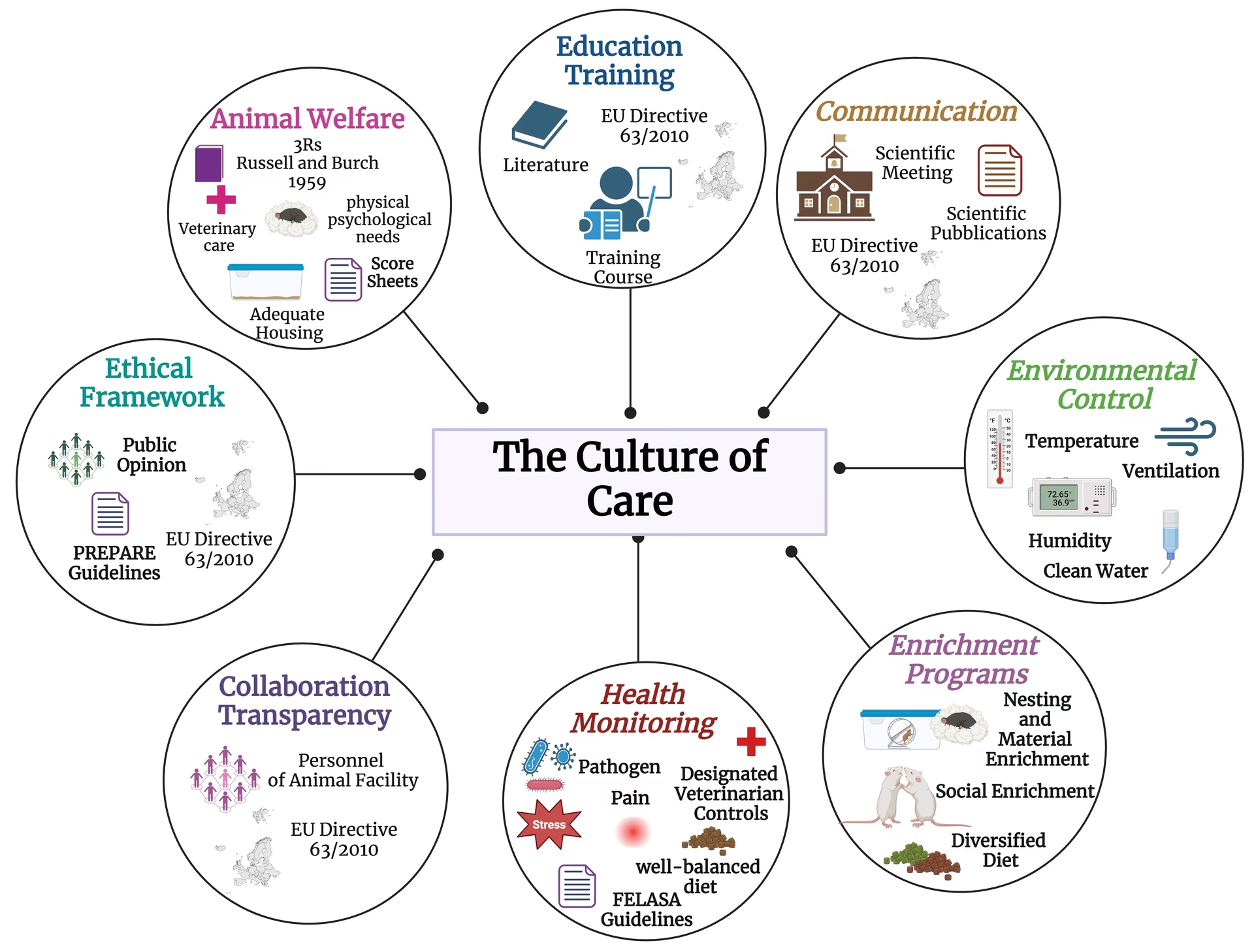
El estudio de las funciones cognitivas complejas, como el aprendizaje, la memoria y la atención, representa uno de los mayores desafíos en neurociencia. Estas capacidades no son el resultado de la acción aislada de componentes neurales, sino que emergen de interacciones intrincadas entre múltiples sistemas cerebrales. Dada esta complejidad inherente, los modelos in vitro, si bien son valiosos para el estudio de procesos celulares o moleculares específicos, resultan insuficientes para comprender plenamente las bases neurales de la cognición en un organismo vivo e intacto. Es aquí donde los modelos animales adquieren una importancia crítica.
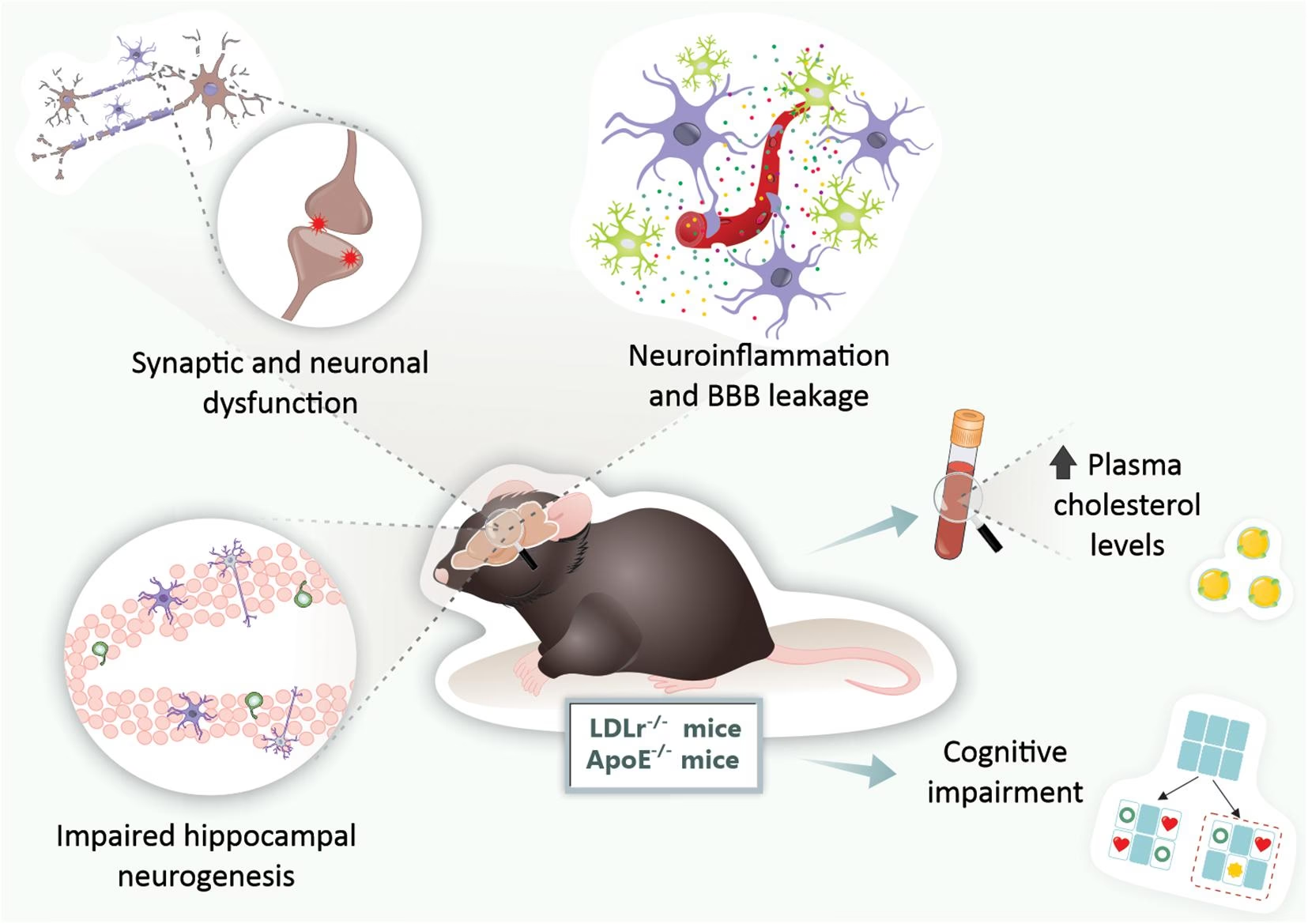
Los modelos animales de deterioro cognitivo son herramientas indispensables no solo para dilucidar las bases neurales de la función cognitiva, sino también para evaluar la eficacia de posibles fármacos terapéuticos y determinar la neurotoxicidad de contaminantes ambientales y sustancias de abuso. Permiten a los investigadores manipular variables de una manera controlada que sería imposible o poco ética en estudios con humanos, proporcionando información detallada sobre los mecanismos subyacentes a la cognición y sus disfunciones.
- La Necesidad de Modelos Animales en el Estudio de la Cognición
- Tipos de Modelos Animales Utilizados
- Modelos Farmacológicos de Disfunción Cognitiva
- Aplicaciones en Neurotoxicología
- Modelos Genéticos y Moleculares
- Modelando Síndromes Específicos: Envejecimiento y Neurotrauma
- Enfoque en el Deterioro Cognitivo Leve (DCL)
- Desafíos y Consideraciones
- Preguntas Frecuentes
- Conclusión
La Necesidad de Modelos Animales en el Estudio de la Cognición
La cognición implica una serie de procesos dinámicos que dependen de la plasticidad neuronal, la comunicación entre vastas redes de neuronas y la integración de información a través de diferentes áreas cerebrales. Comprender cómo funcionan estos procesos a nivel de sistema requiere el estudio en un organismo completo. Los modelos animales, que comparten muchas similitudes neuroanatómicas y fisiológicas con los humanos, especialmente los mamíferos, ofrecen esta posibilidad. Permiten investigar cómo los cambios en la actividad neuronal, la estructura cerebral o la química del cerebro afectan directamente el comportamiento cognitivo.
Además de explorar las bases fundamentales, los modelos animales son esenciales en la investigación traslacional. La identificación y el desarrollo de nuevos tratamientos para trastornos cognitivos, como la enfermedad de Alzheimer, el trastorno por déficit de atención con hiperactividad (TDAH), la enfermedad de Parkinson o la esquizofrenia, dependen en gran medida de la capacidad de probar experimentalmente la seguridad y eficacia de compuestos candidatos antes de pasar a ensayos clínicos en humanos. Los modelos animales que reproducen aspectos de estas condiciones permiten este paso crucial.
Tipos de Modelos Animales Utilizados
Históricamente, los modelos animales más utilizados en el estudio de la cognición han sido mamíferos como monos, ratas y ratones. Cada una de estas especies presenta ventajas y desventajas. Los monos, por ejemplo, tienen una mayor similitud neuroanatómica con los humanos, pero son costosos, requieren más tiempo para los experimentos y plantean mayores desafíos éticos y logísticos.
Las ratas y los ratones son más accesibles, económicos y permiten estudios a mayor escala. Su genoma es bien conocido y existen numerosas herramientas genéticas disponibles para manipularlos, lo que los hace particularmente útiles para investigar las bases moleculares y genéticas de la cognición. Recientemente, se están desarrollando modelos no mamíferos, a menudo denominados modelos complementarios, que incluyen peces (especialmente el pez cebra), moscas (drosophila) y gusanos planos (C. elegans). Estos modelos, aunque con menor complejidad neural que los mamíferos, son excelentes para la detección de alto rendimiento (high-throughput screening) de compuestos potencialmente tóxicos o terapéuticos y para el estudio de mecanismos neuromoleculares básicos. Su uso es complementario a los modelos mamíferos, aprovechando las ventajas únicas de cada uno.
Modelos Farmacológicos de Disfunción Cognitiva
Los modelos farmacológicos son quizás los más comunes para inducir y estudiar la disfunción cognitiva. Consisten en administrar sustancias químicas que alteran la función de sistemas de neurotransmisores específicos, permitiendo investigar su rol en el aprendizaje, la memoria o la atención. Son cruciales para entender cómo ciertos sistemas contribuyen a la cognición y para probar fármacos que buscan mejorarla.
El sistema de neurotransmisores mejor caracterizado en su relación con la función cognitiva es el colinérgico, particularmente la Acetilcolina. Se ha demostrado que tanto los receptores muscarínicos como los nicotínicos están críticamente involucrados. Los fármacos que alteran la transmisión colinérgica, como la escopolamina (un antagonista muscarínico), pueden inducir déficits de memoria en animales, aunque estos modelos a veces se consideran "indiscriminados" para la detección de fármacos con potencial terapéutico amplio.
Otro sistema de neurotransmisores extensamente estudiado es el glutamatérgico, especialmente a través de los receptores NMDA (N-metil-D-aspartato), que son fundamentales para la plasticidad sináptica y, por ende, para el aprendizaje y la memoria. El bloqueo de estos receptores puede modelar ciertos aspectos del deterioro cognitivo.
Además, sustancias de abuso como el etanol pueden producir síndromes de deterioro cognitivo, lo que también se modela farmacológicamente en animales para estudiar los mecanismos de la neurotoxicidad aguda y crónica sobre la cognición.
Aplicaciones en Neurotoxicología
Los modelos animales de deterioro cognitivo han tenido un éxito notable en el campo de la neurotoxicología. Permiten evaluar el impacto de la exposición a toxicantes ambientales o industriales en el desarrollo y la función cognitiva.
Un ejemplo clásico es el plomo. La exposición al plomo durante el desarrollo produce déficits cognitivos persistentes que han sido bien modelados en monos y roedores. Otros metales como el mercurio, así como compuestos orgánicos como los bifenilos policlorados (PCBs), también han sido ampliamente estudiados mediante modelos animales para entender sus efectos neurotóxicos sobre la cognición a largo plazo.
Los neurotoxicantes también pueden usarse como herramientas para investigar la función de sistemas cerebrales específicos. El MPTP (1-metil-4-fenil-1,2,3,6-tetrahidropiridina), un neurotóxico que afecta selectivamente a las neuronas dopaminérgicas de la sustancia negra, ha sido fundamental para descubrir el papel crucial de este sistema en la función cognitiva y motora, y ha servido como base para desarrollar modelos de la enfermedad de Parkinson y probar terapias.
Modelos Genéticos y Moleculares
Los ratones, en particular, se han vuelto invaluables para determinar las bases moleculares de la función cognitiva gracias a las tecnologías de manipulación genética. Los ratones transgénicos (que expresan genes adicionales) y los ratones knockout (en los que se ha inactivado un gen específico) permiten estudiar el papel de proteínas o vías moleculares particulares en la cognición.
Por ejemplo, se han desarrollado ratones transgénicos que sobreexpresan proteínas implicadas en la enfermedad de Alzheimer, como la proteína precursora de amiloide (APP) y la presenilina 1 (PS1). Estos modelos desarrollan depósitos de péptido β-amiloide y déficits cognitivos que imitan aspectos de la enfermedad humana, siendo un foro prometedor para el desarrollo de nuevas terapias.
Asimismo, los ratones knockout para receptores colinérgicos específicos se utilizan para dilucidar el papel preciso de diferentes componentes del sistema colinérgico en diversas facetas de la función cognitiva, complementando los estudios farmacológicos.
Modelando Síndromes Específicos: Envejecimiento y Neurotrauma
Los modelos animales pueden simular síndromes de deterioro cognitivo con una causa bien definida, como el envejecimiento o el neurotrauma.
El envejecimiento es un proceso natural que a menudo se acompaña de un declive cognitivo. El estudio en especies de vida más larga, como los monos, permite observar y caracterizar el deterioro cognitivo asociado a la edad de manera similar a los humanos, proporcionando una base sólida para desarrollar e investigar intervenciones.
El neurotrauma, como las lesiones cerebrales traumáticas, causa déficits cognitivos tanto en humanos como en animales. Los modelos animales de neurotrauma reproducen estos déficits y permiten estudiar los mecanismos subyacentes al daño y la disfunción, así como evaluar la eficacia de tratamientos que promuevan la recuperación o mitiguen el daño a largo plazo.

Enfoque en el Deterioro Cognitivo Leve (DCL)
El Deterioro Cognitivo Leve (DCL) es un estado de transición entre el envejecimiento cognitivo normal y la demencia, siendo la enfermedad de Alzheimer la causa más común de conversión. Comprender sus mecanismos patogénicos y desarrollar tratamientos requiere modelos animales específicos que capturen las características clave de esta condición.
Modelar el DCL en animales presenta desafíos únicos, ya que, a diferencia de la demencia severa, los déficits son sutiles y a menudo solo detectables con tareas conductuales difíciles. Además, un animal no puede verbalizar quejas de memoria, un síntoma principal en humanos. Sin embargo, a pesar de que la correspondencia con la patología humana nunca es perfecta, los modelos animales son muy útiles para dos propósitos principales: entender los mecanismos de la enfermedad y probar la actividad de nuevos fármacos.
Características de un Modelo Animal de DCL
Basándose en la descripción clínica del DCL, un modelo animal ideal debería presentar las siguientes características:
- Edad avanzada.
- Deterioro discreto (sutil) de la memoria.
- Cambios neuropatológicos leves.
- Cambios en el sistema colinérgico.
Además, estas características deberían asociarse con una actividad motora y conducta alimentaria normales, para distinguirlo de modelos de patologías más severas que afectan otras funciones. En algunos modelos, especialmente aquellos relacionados con el DCL vascular, pueden estar presentes alteraciones cerebrovasculares.
Modelos Específicos de DCL
Ratas Envejecidas
Las ratas envejecidas han sido extensamente utilizadas para investigar el deterioro de la memoria asociado a la edad y los cambios neuroquímicos subyacentes. Pueden considerarse un modelo natural de DCL en animales. La edad a la que se detecta el deterioro depende de la cepa de rata, el tipo de tarea conductual y, crucialmente, el intervalo entre la adquisición y el recuerdo (intervalo de retención).
En muchas cepas, un deterioro cognitivo inicial y sutil puede detectarse a partir de los 14-16 meses de edad, especialmente con tareas más demandantes o con intervalos de retención prolongados. Este deterioro se vuelve más pronunciado con la edad. A los 14-19 meses, muchas ratas presentan las características clave del modelo de DCL: edad avanzada relativa, deterioro sutil de la memoria y cambios neuropatológicos leves, como astrogliosis o una disminución en la liberación de Acetilcolina.
La siguiente tabla resume la edad a la que se ha detectado deterioro cognitivo en ratas en diferentes estudios y con diferentes pruebas:
| Cepa | Edad (meses) | Prueba Conductual |
|---|---|---|
| Wistar | 16 | Evitación pasiva |
| Emd:Wi-AF/Han | 19 | Evitación activa unidireccional |
| Wistar | 16-18 | Reconocimiento de objetos |
| Fisher-344 | 15 | Memoria/reconocimiento social |
| Long-Evans | 24 | Laberinto de agua de Morris |
| Long-Evans | 14 | Laberinto radial de ocho brazos |
| Fischer-344 | 16 | Laberinto de agua de Morris |
| Sprague-Dawley | 15 | Tarea de no-coincidencia con la muestra retardada |
| Fischer-344 | 14 | Laberinto de agua (determinación de lugar alocéntrica) |
| Wistar | 17 | Alternancia retardada |
A pesar de su utilidad y conveniencia, los modelos de rata envejecida a veces generan "falsos positivos" en la prueba de fármacos, donde un compuesto muestra eficacia en el modelo pero no en ensayos clínicos humanos.
Ratas con Patología Cerebrovascular
Las ratas espontáneamente hipertensas (SHRs) son consideradas un modelo de hipertensión y enfermedad cardiovascular en humanos. También presentan déficits de aprendizaje a una edad más temprana que las ratas normotensas, a menudo alrededor de los 12 meses. Este deterioro cognitivo, caracterizado por un aprendizaje más lento y más errores, junto con daños cerebrales hipertensivos leves (astrogliosis, atrofia hipocampal) y déficits colinérgicos sutiles, las convierte en un modelo de DCL que ocurre en pacientes con enfermedades cerebrovasculares. La mejora del rendimiento cognitivo con inhibidores de la ECA o agentes potenciadores cognitivos apoya su relevancia para estudiar el DCL vascular.
Ratones Envejecidos y Transgénicos
Los ratones envejecidos, similar a las ratas, también muestran deterioro cognitivo con la edad, detectable a partir de los 9-18 meses dependiendo de la cepa y la prueba. Este deterioro se asocia con cambios neuropatológicos, como la disminución de neuronas colinérgicas septales.
Los ratones transgénicos que sobreexpresan APP y PS1, modelos de enfermedad de Alzheimer, pueden considerarse modelos de DCL en sus etapas tempranas (alrededor de los 8-10 meses). En esta fase inicial, presentan un deterioro cognitivo detectable (especialmente en tareas de memoria espacial), pero con una carga de placas β-amiloide mínima y déficits colinérgicos iniciales, antes de desarrollar la neuropatología severa y el deterioro cognitivo marcado de las etapas tardías que se asemejan más a la demencia plena. Estos modelos son valiosos para probar tratamientos que buscan prevenir o retrasar la progresión del DCL a la demencia.
Monos Envejecidos
Los monos, especialmente los macacos Rhesus, son utilizados para estudiar el envejecimiento cognitivo debido a su similitud con los humanos. Aunque muchos monos viejos mantienen una buena función cognitiva, el DCL puede detectarse en monos de edad media (aproximadamente 15 años) o en monos viejos cuando se les presentan tareas visuoespaciales o de memoria con intervalos de retención difíciles. El deterioro observado en monos envejecidos, que generalmente no es tan catastrófico como la pérdida de memoria en la enfermedad de Alzheimer humana severa, a menudo se considera un modelo de DCL. Responden a tratamientos con fármacos que actúan sobre sistemas como el colinérgico o el dopaminérgico, aunque, al igual que con las ratas, la traducción a la clínica humana no siempre está garantizada.
Desafíos y Consideraciones
Identificar o desarrollar un modelo animal que reproduzca todas las características del DCL humano es difícil debido a las diferencias inherentes entre especies. La incapacidad de los animales para verbalizar sus síntomas es una limitación obvia. Además, la neuropatología y los mecanismos subyacentes pueden no ser idénticos.
No obstante, incluso si solo reproducen parcialmente la condición humana, los modelos animales son inmensamente útiles para dos propósitos clave: profundizar en la comprensión de los mecanismos patogénicos del DCL y evaluar el potencial terapéutico de nuevos fármacos antes de los ensayos en humanos. La elección del modelo animal y la tarea conductual es crucial para detectar los déficits sutiles que caracterizan al DCL.
Preguntas Frecuentes
¿Por qué no estudiar la cognición solo en humanos?
Estudiar la cognición en humanos es fundamental, pero hay limitaciones. Los modelos animales permiten manipulaciones experimentales (genéticas, farmacológicas, lesiones) que no son posibles ni éticas en humanos. Facilitan el estudio detallado de los mecanismos neurales a nivel molecular, celular y de circuito, y permiten probar la seguridad y eficacia de posibles tratamientos de forma controlada antes de la aplicación en personas.
¿Son éticos los modelos animales en investigación?
La investigación con animales está estrictamente regulada por comités de ética y normativas internacionales. Se busca minimizar el número de animales utilizados (Reducción), refinar los procedimientos para reducir al máximo el sufrimiento (Refinamiento) y, siempre que sea posible, reemplazar el uso de animales por métodos alternativos (Reemplazo). Los modelos animales se utilizan solo cuando son esenciales para responder preguntas científicas que no pueden abordarse de otra manera, y siempre bajo supervisión veterinaria.
¿Qué tan bien se traducen los resultados de los modelos animales a los humanos?
La traducción de los resultados de modelos animales a humanos es un desafío constante en la investigación biomédica. Aunque los modelos animales comparten similitudes con los humanos, también existen diferencias significativas. La eficacia de un fármaco en un modelo animal no garantiza su éxito en humanos, y viceversa. Es por eso que se requieren múltiples modelos y una validación rigurosa a través de ensayos clínicos.
¿Qué son los modelos complementarios y para qué sirven?
Los modelos complementarios, como los peces cebra o las moscas, son organismos no mamíferos utilizados en investigación. Aunque su complejidad neural es menor que la de mamíferos, son ventajosos por su ciclo de vida corto, gran número de descendientes, facilidad de manipulación genética y bajo costo. Son ideales para estudios de alto rendimiento (screening) de grandes bibliotecas de compuestos o para investigar mecanismos moleculares básicos de la cognición que están conservados evolutivamente, complementando la investigación en modelos mamíferos más complejos.
Conclusión
Los modelos animales son pilares insustituibles en la neurociencia cognitiva. Han sido y siguen siendo esenciales para desentrañar las complejas bases neurales del aprendizaje, la memoria y la atención. Su aplicación en el estudio de trastornos cognitivos, la evaluación de la neurotoxicidad de toxicantes y el desarrollo de nuevos tratamientos es fundamental. Si bien el modelado de condiciones sutiles como el Deterioro Cognitivo Leve (DCL) presenta desafíos inherentes y la traducción a la clínica humana no es automática, la investigación con modelos animales, incluyendo ratas, ratones, monos y modelos complementarios, continúa proporcionando información crucial y abriendo caminos para futuras intervenciones terapéuticas.
Si quieres conocer otros artículos parecidos a Modelos Animales en Neurociencia Cognitiva puedes visitar la categoría Neurociencia.