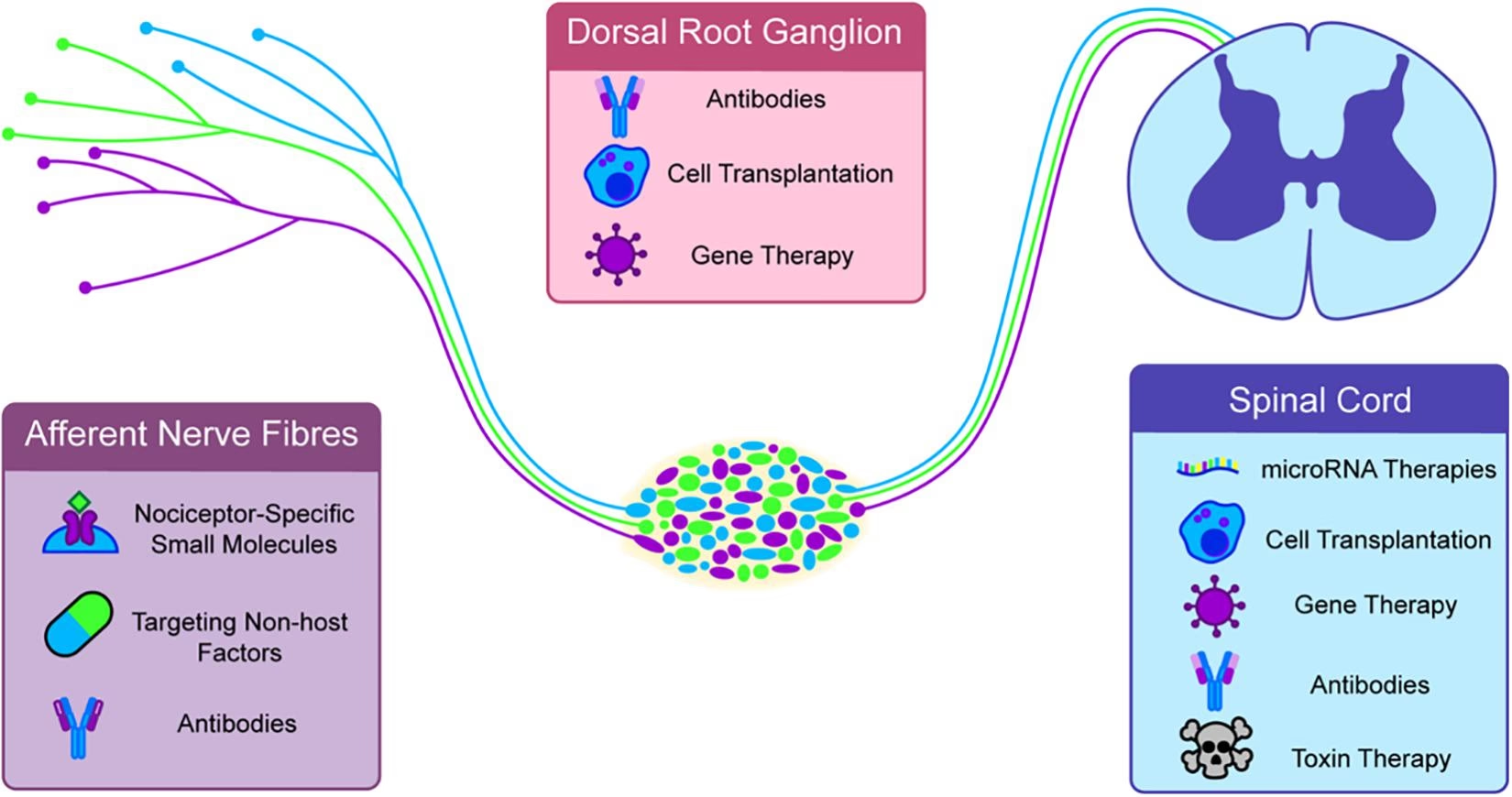
El dolor es una experiencia sensorial y emocional compleja, fundamental para nuestra supervivencia. Actúa como un sistema de advertencia crucial, alertándonos sobre posibles daños tisulares o irritantes ambientales. Sin embargo, en ciertas circunstancias, lo que comienza como una respuesta protectora aguda puede evolucionar hacia un estado de dolor crónico y debilitante. Una de las causas más comunes de dolor es la inflamación, un proceso biológico complejo que implica la liberación de una variedad de sustancias químicas en el sitio de la lesión o infección.
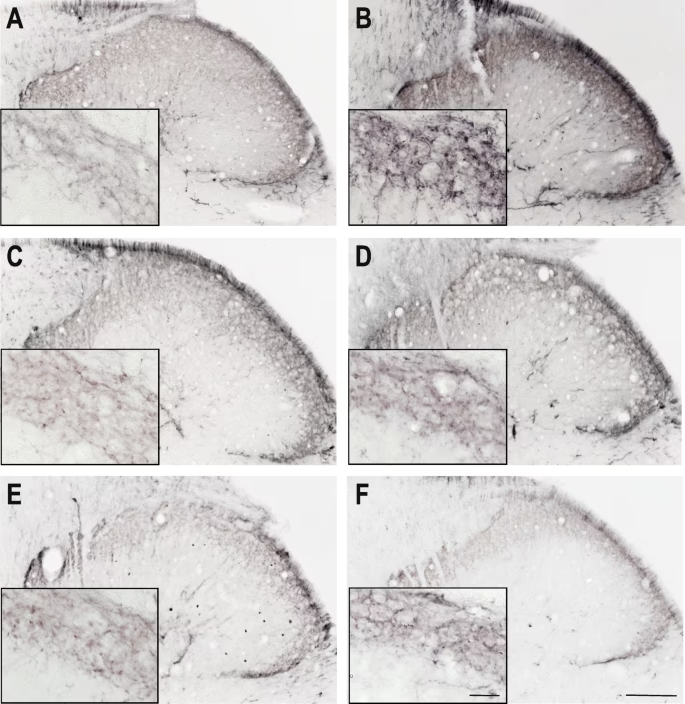
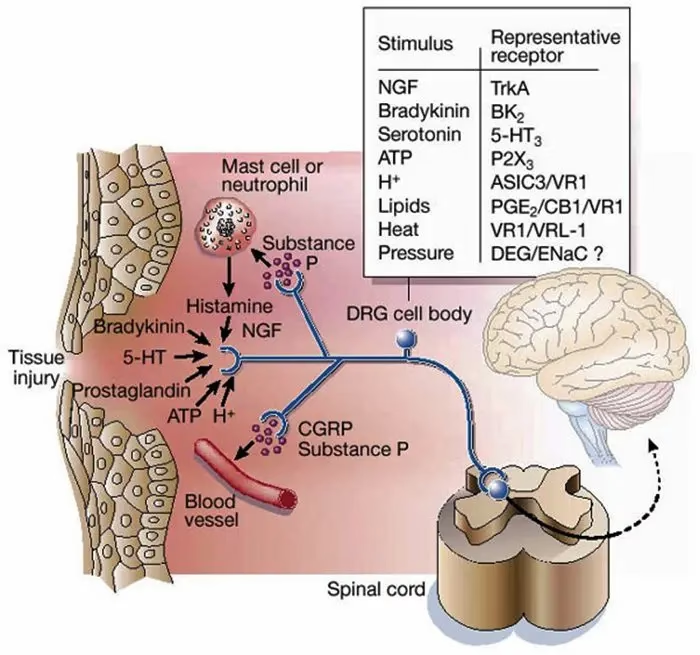
Cuando ocurre una lesión tisular, ya sea por un corte, una quemadura, una infección o una irritación, el cuerpo inicia una respuesta inflamatoria. Este proceso tiene como objetivo eliminar el agente dañino, limpiar los tejidos lesionados y comenzar el proceso de curación. Como parte de esta respuesta, diversas células inmunes y residentes en el tejido liberan una mezcla de mediadores químicos en el entorno local. Esta mezcla de sustancias, a menudo referida en el campo de la neurociencia del dolor como la sopa inflamatoria, es un cóctel potente que interactúa directamente con las terminaciones nerviosas sensoriales, particularmente con un tipo especializado de neuronas conocidas como nociceptores.
- ¿Qué Compone la Sopa Inflamatoria?
- La Vía del Dolor Inflamatorio: Un Diálogo Químico-Neural
- Hipersensibilidad en Acción: Alodinia e Hiperalgesia
- Inflamación Neurogénica: Un Bucle de Retroalimentación
- La Transmisión Central del Dolor Inflamatorio
- Dolor Agudo vs. Dolor Crónico Inflamatorio
- El Estudio Molecular: Desentrañando la Sopa
- Implicaciones Terapéuticas
- Preguntas Frecuentes
¿Qué Compone la Sopa Inflamatoria?
La composición exacta de la sopa inflamatoria puede variar dependiendo del tipo de lesión o irritación, pero generalmente incluye una serie de moléculas bioactivas liberadas por células dañadas, células inmunes infiltradas (como leucocitos) y las propias terminaciones nerviosas. Entre los componentes clave identificados se encuentran:
- Bradicinina
- Serotonina
- Adenosín Trifosfato (ATP)
- Histamina
- Prostaglandinas
- Citocinas
Estos mediadores actúan sobre receptores y canales iónicos específicos presentes en la superficie de los nociceptores. La liberación de estas sustancias es un paso crítico en la traducción de un estímulo tisular (la lesión o inflamación) en una señal neuronal (un impulso eléctrico) que el cerebro interpretará como dolor.
La Vía del Dolor Inflamatorio: Un Diálogo Químico-Neural
La vía del dolor inflamatorio comienza en la periferia, en el sitio de la inflamación. Los nociceptores, que son las terminaciones libres de las fibras nerviosas sensoriales primarias (principalmente fibras C amielínicas y fibras Aδ finamente mielinizadas), son los principales detectores de estos estímulos. Estas fibras están densamente distribuidas en tejidos como la piel, las articulaciones, los músculos y los órganos internos.
Cuando los componentes de la sopa inflamatoria se unen a sus receptores en las terminaciones periféricas de los nociceptores, desencadenan una cascada de eventos intracelulares. Estos eventos pueden resultar en dos efectos principales sobre la actividad del nociceptor:
- Activación Directa: Algunos mediadores, como la bradicinina o el ATP, pueden abrir directamente canales iónicos en la membrana del nociceptor, generando una corriente eléctrica que puede alcanzar el umbral para disparar potenciales de acción. Esto inicia la señal de dolor.
- Sensibilización: Otros mediadores, o la acción sostenida de los activadores, pueden aumentar la sensibilidad del nociceptor a estímulos posteriores. Esto significa que el nociceptor se vuelve más propenso a disparar potenciales de acción en respuesta a estímulos (térmicos, mecánicos o químicos) que normalmente no serían dolorosos, o a responder con mayor intensidad a estímulos que ya son dolorosos. Este fenómeno es central para la hipersensibilidad asociada al dolor inflamatorio.
La sensibilización ocurre a través de la modulación de canales iónicos y receptores existentes en la membrana del nociceptor. Por ejemplo, la activación de ciertas proteínas quinasas, como la proteína quinasa A (PKA), por algunos mediadores inflamatorios puede llevar a la fosforilación directa de canales clave para la señalización del dolor, como los canales TRPV1 (sensibles al calor y la capsaicina) y los canales de sodio Nav1.8. Esta fosforilación puede reducir el umbral de activación de estos canales, haciendo que el nociceptor sea más excitable.
Hipersensibilidad en Acción: Alodinia e Hiperalgesia
La sensibilización de los nociceptores periféricos se manifiesta clínicamente como hipersensibilidad al dolor en el área inflamada. Las dos formas principales de hipersensibilidad son:
- Alodinia: La percepción de dolor ante un estímulo que normalmente no es doloroso. Un ejemplo clásico es el dolor que se siente al tocar suavemente la piel quemada por el sol. La quemadura solar causa inflamación y libera componentes de la sopa inflamatoria que sensibilizan los nociceptores. Estímulos inocuos como un toque ligero, detectados por fibras Aβ de bajo umbral, pueden entonces ser percibidos como dolorosos debido a cambios en el procesamiento de la señal, posiblemente involucrando la interacción con nociceptores sensibilizados o cambios en la médula espinal.
- Hiperalgesia: Una respuesta de dolor exagerada a un estímulo que ya es doloroso. En el mismo ejemplo de la quemadura solar, aplicar una presión moderada sobre la piel inflamada duele significativamente más que aplicar la misma presión sobre piel sana.
Estos fenómenos de hipersensibilidad demuestran la notable plasticidad del sistema de transmisión del dolor. La inflamación no solo inicia el dolor, sino que también altera la forma en que el sistema nervioso procesa los estímulos.
Inflamación Neurogénica: Un Bucle de Retroalimentación
Curiosamente, los nociceptores no son solo receptores pasivos de la sopa inflamatoria; también contribuyen activamente a ella y al proceso inflamatorio. Las fibras C, en particular, son conocidas por participar en la inflamación neurogénica. Cuando se activan intensamente, estas fibras liberan neuropéptidos pro-inflamatorios como la Sustancia P y el Péptido Relacionado con el Gen de la Calcitonina (CGRP) desde sus terminaciones periféricas, en un proceso de liberación retrógrada (en dirección opuesta a la transmisión normal de la señal hacia el sistema nervioso central).
La Sustancia P y el CGRP tienen efectos potentes en el tejido local: el CGRP es un vasodilatador potente (contribuyendo al enrojecimiento de la inflamación), mientras que la Sustancia P promueve la extravasación de proteínas plasmáticas de los vasos sanguíneos (contribuyendo a la hinchazón). Estos efectos aumentan aún más la respuesta inflamatoria y pueden liberar o activar otras células para que liberen más componentes de la sopa inflamatoria, creando un bucle de retroalimentación positiva que amplifica tanto la inflamación como el dolor.
La Transmisión Central del Dolor Inflamatorio
Una vez que los potenciales de acción se generan en las terminaciones periféricas de los nociceptores, viajan a lo largo de la fibra nerviosa primaria hasta la médula espinal. Los cuerpos celulares de estas neuronas se encuentran en los ganglios de la raíz dorsal (DRG) para el cuerpo y en el ganglio trigémino para la cara. Desde los DRG, las fibras axonales centrales entran en la médula espinal, donde establecen sinapsis con neuronas de segundo orden en el asta dorsal.
El asta dorsal de la médula espinal tiene una organización laminar precisa. Las fibras C y Aδ que transmiten señales nociceptivas tienden a terminar en las láminas más superficiales (Láminas I y II), haciendo sinapsis con neuronas de proyección que envían información al cerebro y con interneuronas locales. Las fibras Aβ de bajo umbral (tacto ligero) terminan en láminas más profundas (Láminas III y IV), aunque algunas pueden converger con fibras nociceptivas en la Lámina V.
Las neuronas de proyección en las Láminas I y V son las principales vías de salida del asta dorsal hacia el cerebro. Transmiten mensajes de dolor a través de tractos ascendentes como el espinotalámico y el espinorreticulotalámico, que alcanzan el tálamo y el tronco encefálico. Desde el tálamo, la información se proyecta a diversas áreas corticales, incluyendo la corteza somatosensorial (para la localización e intensidad del dolor), la corteza cingulada anterior y la corteza insular (para los aspectos emocionales y afectivos del dolor), y otras áreas como la corteza prefrontal, ganglios basales y cerebelo, cuya implicación en la percepción del dolor es objeto de estudio.
La inflamación periférica no solo sensibiliza los nociceptores periféricos, sino que también puede inducir cambios plásticos en las neuronas del asta dorsal, un fenómeno conocido como sensibilización central. Esto puede amplificar aún más las señales de dolor y contribuir a la persistencia del dolor incluso después de que la inflamación periférica disminuya.
Dolor Agudo vs. Dolor Crónico Inflamatorio
La distinción entre dolor agudo y crónico es fundamental. El dolor inflamatorio agudo, mediado en parte por fibras Aδ rápidas y luego por fibras C, es generalmente intenso pero de duración limitada, coincidiendo con el proceso de curación. Su función protectora es clara.
Sin embargo, si la inflamación persiste o si los cambios plásticos en el sistema nervioso se vuelven duraderos, el dolor puede volverse crónico. El dolor crónico inflamatorio a menudo está predominantemente asociado con la actividad sostenida de las fibras C y la sensibilización tanto periférica como central. Ejemplos de condiciones con un componente importante de dolor inflamatorio crónico incluyen la artritis, la neuralgia post-herpética y ciertos tipos de dolor de espalda crónico. En estos casos, el dolor deja de ser útil como señal de advertencia y se convierte en una enfermedad en sí mismo, con un impacto significativo en la calidad de vida.
La profunda diferencia entre el dolor agudo y crónico subraya que el dolor no es el resultado de un sistema neural inmutable, sino de la interacción de moléculas y circuitos altamente plásticos. La base molecular, bioquímica y neuroanatómica de esta plasticidad es un área clave de investigación actual.
El Estudio Molecular: Desentrañando la Sopa
La investigación moderna, utilizando enfoques genéticos, electrofisiológicos y farmacológicos, está desentrañando los mecanismos moleculares subyacentes a la detección, codificación y modulación de los estímulos nocivos y la influencia de la sopa inflamatoria en estos procesos. Se están identificando los receptores específicos para cada componente de la sopa inflamatoria en los nociceptores (por ejemplo, receptores B2 para bradicinina, receptores P2X3 para ATP, receptores de citocinas) y cómo su activación modifica la excitabilidad neuronal.
La caracterización de la heterogeneidad de los nociceptores (fibras C peptidergicas vs. no peptidergicas, diferentes tipos de fibras Aδ) revela que no todas responden de la misma manera a los componentes de la sopa inflamatoria. Esta diversidad molecular sugiere que diferentes tipos de dolor inflamatorio pueden ser mediados por subpoblaciones específicas de nociceptores.
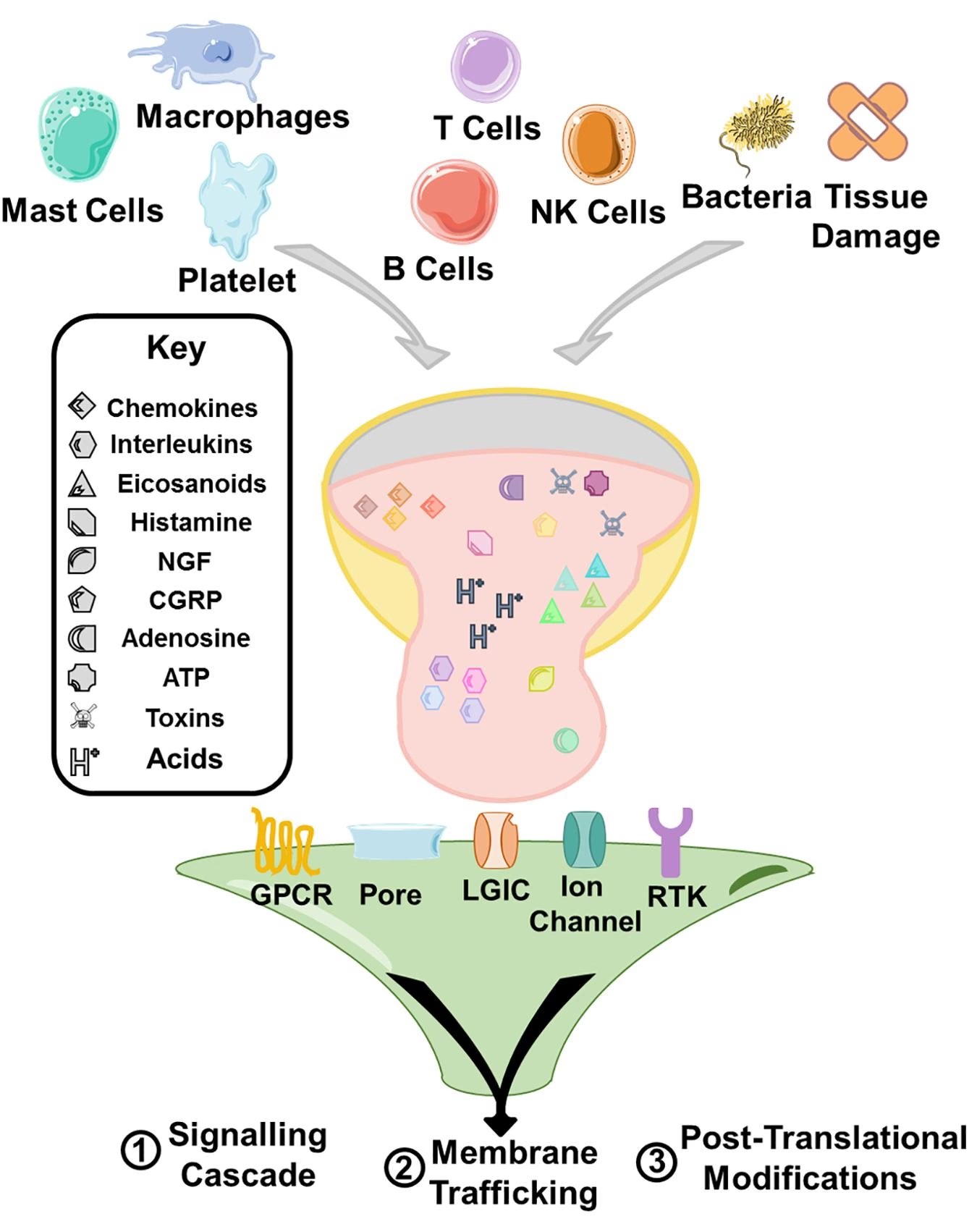
| Mediador Inflamatorio | Origen Principal | Efectos sobre los Nociceptores y el Tejido |
|---|---|---|
| Bradicinina | Tejido dañado, plasma | Activación y sensibilización de nociceptores. Vasodilatación, aumento de la permeabilidad vascular. |
| Serotonina | Plaquetas, mastocitos | Activación y sensibilización de nociceptores. |
| ATP | Células dañadas | Activación de nociceptores (vía receptores P2X). |
| Histamina | Mastocitos | Activación y sensibilización de nociceptores (vía receptores H1). Picazón (en algunos contextos). |
| Prostaglandinas (ej. PGE2) | Células inflamatorias (vía COX) | Sensibilización de nociceptores (vía receptores EP). Vasodilatación, fiebre. |
| Citocinas (ej. IL-1β, TNF-α) | Células inmunes, células residentes | Sensibilización de nociceptores, cambios en la expresión génica. Efectos complejos pro- y anti-inflamatorios. |
| Sustancia P | Terminaciones de fibras C (liberación retrógrada) | Extravasación de plasma, activación de células inmunes. Contribuye a la inflamación neurogénica. |
| CGRP | Terminaciones de fibras C (liberación retrógrada) | Potente vasodilatación. Contribuye a la inflamación neurogénica. |
Implicaciones Terapéuticas
Esta creciente comprensión de la sopa inflamatoria y la vía del dolor inflamatorio ha identificado una serie de posibles dianas terapéuticas para el tratamiento del dolor. Los enfoques farmacológicos actuales y futuros buscan bloquear la producción o acción de los mediadores de la sopa inflamatoria, modular la actividad de los canales iónicos o receptores sensibilizados en los nociceptores, o intervenir en los procesos de sensibilización central en la médula espinal.
Por ejemplo, muchos antiinflamatorios no esteroideos (AINEs) actúan inhibiendo las enzimas ciclooxigenasas (COX), reduciendo así la producción de prostaglandinas, un componente clave de la sopa inflamatoria. Otros fármacos se dirigen a receptores específicos (como los receptores de opioides, que modulan la transmisión del dolor a varios niveles) o a canales iónicos específicos implicados en la excitabilidad de los nociceptores.
Preguntas Frecuentes
¿La sopa inflamatoria causa todo tipo de dolor?
No, la sopa inflamatoria es un factor importante en el dolor asociado con la inflamación y la lesión tisular. Otros tipos de dolor, como el dolor neuropático (causado por daño directo a los nervios) o el dolor nociplástico (dolor amplificado sin evidencia clara de daño tisular o nervioso continuo), implican mecanismos diferentes, aunque puede haber solapamiento.
¿Por qué el dolor inflamatorio a veces se vuelve crónico?
El dolor inflamatorio puede volverse crónico si la inflamación persiste o si los cambios plásticos (sensibilización) en el sistema nervioso periférico y central se vuelven duraderos. Estos cambios pueden hacer que el sistema del dolor funcione de manera anormal, manteniendo la sensación de dolor incluso después de que la causa inicial (la inflamación aguda) se haya resuelto.
¿Se puede medir la sopa inflamatoria?
Sí, los componentes individuales de la sopa inflamatoria (como citocinas, prostaglandinas, neuropéptidos) pueden medirse en fluidos tisulares o en la sangre en el sitio de la inflamación utilizando técnicas bioquímicas y moleculares. Esto ayuda a los investigadores a comprender qué mediadores están involucrados en diferentes tipos de dolor inflamatorio.
¿Cómo se trata el dolor causado por la sopa inflamatoria?
El tratamiento a menudo implica abordar la causa subyacente de la inflamación (por ejemplo, con antibióticos para una infección, o terapias para enfermedades autoinmunes). Farmacológicamente, se pueden usar antiinflamatorios (como AINEs o corticosteroides) para reducir la producción de componentes de la sopa, analgésicos que actúan sobre los nociceptores o en la médula espinal (como opioides o anestésicos locales), y fármacos que modulan la sensibilización central.
En conclusión, la sopa inflamatoria es un elemento crucial en la generación y mantenimiento del dolor asociado a la inflamación. Esta compleja mezcla de mediadores químicos liberados en el sitio de la lesión interactúa potentemente con los nociceptores, no solo activándolos sino también aumentando su sensibilidad. Comprender la composición de esta sopa y cómo actúa sobre la vía del dolor, desde la periferia hasta el cerebro, es fundamental para desarrollar estrategias más efectivas para aliviar el dolor agudo y, especialmente, para prevenir o tratar la transición hacia el dolor crónico.
Si quieres conocer otros artículos parecidos a La Sopa Inflamatoria y el Dolor puedes visitar la categoría Neurociencia.