La Ley de Ohm, una piedra angular de la física que describe la relación entre voltaje, corriente y resistencia en un circuito eléctrico simple (V = I * R), podría parecer alejada del complejo mundo de la biología. Sin embargo, este principio fundamental encuentra aplicaciones sorprendentemente directas y cruciales en el funcionamiento de los sistemas vivos, particularmente en la neurociencia y la fisiología cardiovascular. Comprender cómo la Ley de Ohm se manifiesta en neuronas y vasos sanguíneos nos ofrece una perspectiva poderosa sobre la comunicación celular y la circulación.

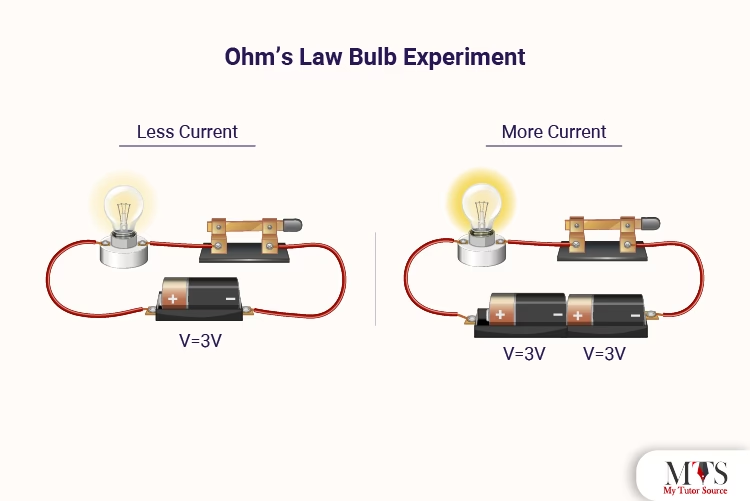
En esencia, la Ley de Ohm establece que la corriente (I) que pasa por un conductor es directamente proporcional a la diferencia de potencial (V) aplicada a través de él e inversamente proporcional a su resistencia (R). Esto se expresa como V = I * R, o I = V / R. En sistemas biológicos, podemos adaptar esta ley. Por ejemplo, en el flujo de fluidos como la sangre, una analogía útil es considerar que el flujo (Q) es proporcional a la diferencia de presión (ΔP) e inversamente proporcional a la resistencia (R) al flujo: Q = ΔP / R. Esta simple relación es clave para entender procesos tan diversos como la transmisión de señales nerviosas y la regulación de la presión arterial.
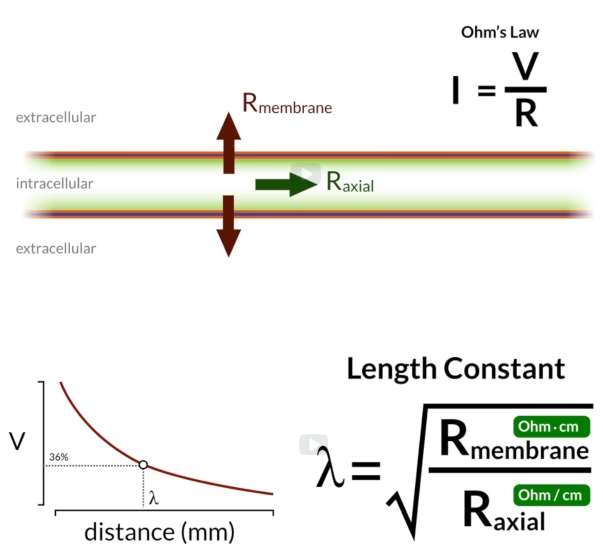
La Ley de Ohm en las Neuronas: Circuitos Bioeléctricos
Las neuronas son células notablemente complejas, pero su membrana celular puede modelarse, en términos eléctricos, como un circuito que combina propiedades de resistencia y capacitancia. La bicapa lipídica de la membrana actúa como un capacitor, una estructura capaz de almacenar carga eléctrica, porque es una barrera aislante que separa dos medios conductores (el interior y el exterior de la célula, ricos en iones). Los canales iónicos incrustados en la membrana actúan como resistencia, ya que permiten que los iones (partículas cargadas, que constituyen la corriente eléctrica en los sistemas biológicos) fluyan a través de la membrana, pero con cierta dificultad o 'resistencia'.
Cuando se inyecta una corriente en una neurona, el cambio en el voltaje de la membrana no es instantáneo. Esto se debe a la propiedad capacitiva de la membrana. Al igual que al encender una luz puede haber un ligero retraso mientras el circuito se carga, la membrana neuronal debe 'cargarse' (acumular iones a ambos lados de la bicapa lipídica) antes de que el voltaje pueda cambiar completamente. La corriente inyectada inicialmente se dedica principalmente a cargar esta capacitancia de la membrana. Una vez que la capacitancia está cargada, la corriente fluye a través de las resistencias (los canales iónicos), y el voltaje de la membrana alcanza un estado estacionario.
Capacitancia de Entrada Neuronal
La capacitancia total de una neurona se conoce como capacitancia de entrada (Cin). Depende de dos factores principales: la capacitancia específica de la membrana (Cm, que es una propiedad del material de la membrana lipídica, típicamente constante entre células) y el tamaño de la célula, es decir, el área de su membrana. La relación es directa: Cin = Cm * Área (membrana). Esto significa que, a diferencia de la resistencia de entrada (que veremos a continuación), la capacitancia de entrada es proporcional al tamaño de la célula. Una célula más grande tiene más área de membrana y, por lo tanto, una mayor capacidad para almacenar carga.
Los factores que influyen en la capacitancia son el área de las 'placas' del capacitor (la superficie de la membrana), la distancia entre ellas (el grosor de la bicapa, que es relativamente constante) y el medio aislante entre ellas (la propia bicapa lipídica, también bastante constante). Por lo tanto, la variación célula a célula en la capacitancia de entrada se debe principalmente a las diferencias en el área de la superficie celular.
Resistencia de Entrada Neuronal
La resistencia de entrada (Rin) de una neurona refleja qué tan difícil es para la corriente fluir a través de la membrana en estado estacionario. Depende de la resistencia específica de la membrana (Rm, relacionada con la densidad y el estado de apertura de los canales iónicos) y también del área de la membrana. La relación es inversa: Rin = Rm / Área (membrana). Una célula más grande con más canales (mayor área) típicamente tendrá una menor resistencia de entrada porque hay más 'caminos' para que los iones fluyan.
La Constante de Tiempo: Velocidad de Respuesta Neuronal
La interacción entre la resistencia de entrada (Rin) y la capacitancia de entrada (Cin) de una neurona define un parámetro crítico llamado constante de tiempo (τ, tau). La constante de tiempo es simplemente el producto de Rin y Cin: τ = Rin * Cin. Esta constante de tiempo representa el tiempo que tarda el potencial de membrana en alcanzar aproximadamente el 63% de su valor de estado estacionario después de una inyección de corriente o un cambio de voltaje. También es el tiempo que tarda en caer al 37% de su valor de estado estacionario cuando la inyección de corriente cesa.
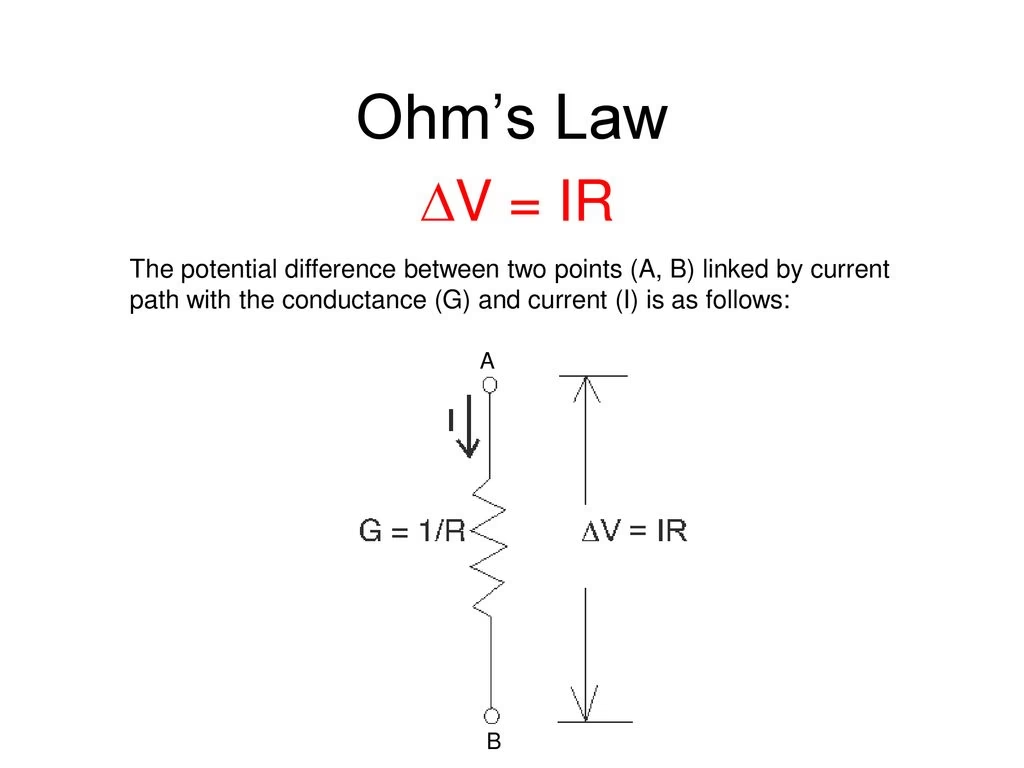
Una constante de tiempo corta significa que el potencial de membrana cambia rápidamente en respuesta a una entrada de corriente, lo que permite a la neurona procesar señales eléctricas a alta velocidad. Por el contrario, una constante de tiempo larga implica una respuesta más lenta. Curiosamente, aunque Rin disminuye con el área y Cin aumenta con el área, cuando se multiplican, la dependencia del área se cancela (τ = (Rm / Área) * (Cm * Área) = Rm * Cm). Esto sugiere que la velocidad intrínseca de respuesta de la membrana (definida por Rm y Cm) es un factor clave en la constante de tiempo, aunque el tamaño celular influye en Rin y Cin individualmente.
Si la membrana neuronal fuera solo resistiva, la respuesta de voltaje sería un pulso cuadrado instantáneo al inyectar corriente. Si fuera solo capacitiva, el voltaje cambiaría linealmente (en teoría, aunque no habría flujo de corriente sin resistencia). Pero como es una combinación de ambos, dispuesta eléctricamente en paralelo, la respuesta de voltaje a un pulso de corriente es una curva exponencial, caracterizada por la constante de tiempo.
| Propiedad | Representación Neuronal | Dependencia del Área Celular | Efecto en la Respuesta |
|---|---|---|---|
| Resistencia (Rin) | Canales iónicos | Inversamente proporcional (Rin = Rm / Área) | Determina el voltaje de estado estacionario (V = I * Rin) |
| Capacitancia (Cin) | Bicapa lipídica | Directamente proporcional (Cin = Cm * Área) | Causa retraso en el cambio de voltaje, almacena carga |
| Constante de Tiempo (τ) | Combinación Rin y Cin (τ = Rin * Cin) | Independiente del Área (τ = Rm * Cm) | Determina la velocidad de la respuesta de voltaje |
La Ley de Ohm en la Circulación: Hemodinámica
La aplicación de la Ley de Ohm al flujo sanguíneo es directa y constituye el fundamento de la hemodinámica. Aquí, la 'corriente' es el flujo sanguíneo (Q), la 'diferencia de potencial' es el gradiente de presión (ΔP) a lo largo de un vaso o sistema de vasos, y la 'resistencia' es la resistencia vascular (R). La ley se expresa como Q = ΔP / R.
El corazón proporciona la fuerza impulsora generando una presión alta en las arterias que disminuye progresivamente a medida que la sangre fluye a través de arteriolas, capilares y venas, regresando al corazón con una presión mucho menor. Esta diferencia de presión entre el inicio y el final del circuito circulatorio es el ΔP que impulsa el flujo sanguíneo.
La resistencia vascular es la oposición al flujo sanguíneo dentro de los vasos. Varios factores influyen en la resistencia: el radio del vaso (el factor más importante, ya que la resistencia es inversamente proporcional a la cuarta potencia del radio), la longitud del vaso y la viscosidad de la sangre. Un vaso más estrecho, más largo o con sangre más viscosa ofrece una mayor resistencia al flujo, lo que, según la Ley de Ohm, disminuirá el flujo si el gradiente de presión se mantiene constante (o aumentará la presión si el flujo se mantiene constante).
La resistencia total en el sistema circulatorio depende de cómo se organizan los vasos. Cuando los vasos están en serie (uno tras otro), la resistencia total es la suma de las resistencias individuales (Rtotal = R1 + R2 + R3 + ...). Cuando están en paralelo (varios caminos posibles para el flujo, como en los lechos capilares), la resistencia total disminuye, calculándose como 1/Rtotal = 1/R1 + 1/R2 + 1/R3 + .... Esto explica por qué, a pesar de que los capilares individuales son muy estrechos (alta resistencia individual), el sistema capilar en su conjunto tiene una resistencia relativamente baja porque hay millones de ellos en paralelo.
Además de la resistencia, la distensibilidad vascular (Compliance, C = ΔV / ΔP) juega un papel crucial. Es la capacidad de un vaso para expandirse en respuesta a un aumento de presión. Las arterias son menos distensibles (más rígidas) que las venas, lo que les permite mantener una presión más alta y amortiguar las pulsaciones generadas por el corazón. La interacción entre la presión generada por el corazón, la resistencia de los vasos y su distensibilidad determina el patrón de flujo sanguíneo y la presión arterial.
Aplicaciones Clínicas y Patología
La comprensión de la Ley de Ohm en biología es fundamental para la medicina. Numerosas patologías cardiovasculares pueden entenderse como alteraciones de los componentes de la ecuación Q = ΔP / R.
La hipertensión arterial, por ejemplo, a menudo implica un aumento de la resistencia vascular sistémica. Esto puede deberse a la vasoconstricción (estrechamiento de los vasos sanguíneos, como ocurre bajo la influencia de la angiotensina II o las catecolaminas como la epinefrina) o a una disminución de la distensibilidad arterial (endurecimiento de las arterias con la edad o aterosclerosis). Un aumento de R, con un flujo sanguíneo (gasto cardíaco) relativamente constante, resulta en un aumento de ΔP (la presión arterial). Fármacos antihipertensivos como los inhibidores de la ECA o los bloqueadores de los canales de calcio actúan reduciendo la resistencia vascular (vasodilatación), mientras que otros pueden afectar el gasto cardíaco.
La medición de la presión arterial misma se basa en estos principios. El método auscultatorio detecta el flujo turbulento que se produce cuando la presión del manguito es mayor que la presión diastólica pero menor que la presión sistólica. La presión sistólica se registra cuando el flujo sanguíneo comienza a pasar (turbulento, audible) a través de la arteria parcialmente ocluida por el manguito. La presión diastólica se registra cuando el flujo sanguíneo vuelve a ser laminar (silencioso) una vez que la presión del manguito cae por debajo de la presión diastólica.
En neurociencia, alteraciones en la resistencia o capacitancia de las neuronas, aunque menos directamente asociadas a enfermedades comunes de forma aislada, pueden afectar la velocidad y la eficiencia de la comunicación neuronal, lo que podría tener implicaciones en trastornos neurológicos.
Preguntas Frecuentes
¿Qué representa la resistencia en una neurona?
Representa la dificultad que tienen los iones para cruzar la membrana celular a través de los canales iónicos abiertos. Cuantos más canales abiertos o más permeables sean, menor será la resistencia.
¿Por qué la membrana neuronal actúa como capacitor?
La bicapa lipídica es una capa aislante que separa dos compartimentos conductores (el interior y exterior celular, ricos en iones). Esta estructura básica (dos conductores separados por un aislante) es la definición de un capacitor, capaz de almacenar carga eléctrica a través de la membrana.

¿Qué es la constante de tiempo neuronal y por qué es importante?
La constante de tiempo (τ) es el producto de la resistencia de entrada (Rin) y la capacitancia de entrada (Cin). Determina la velocidad a la que el potencial de membrana cambia en respuesta a una entrada de corriente. Una τ corta permite respuestas más rápidas, crucial para el procesamiento rápido de información en el sistema nervioso.
¿Cómo se aplica la Ley de Ohm al flujo sanguíneo?
Se aplica como Q = ΔP / R, donde Q es el flujo sanguíneo, ΔP es la diferencia de presión entre dos puntos del sistema circulatorio, y R es la resistencia vascular al flujo. Esta ley describe cómo la presión impulsa el flujo contra la resistencia.
¿Qué es la resistencia vascular y de qué depende principalmente?
Es la oposición al flujo sanguíneo dentro de los vasos. Depende principalmente del radio de los vasos sanguíneos (a menor radio, mayor resistencia), la longitud total del sistema vascular y la viscosidad de la sangre. El radio es el factor más variable y fisiológicamente regulado.
¿Qué es la distensibilidad vascular?
Es la capacidad de un vaso sanguíneo para expandirse en respuesta a un aumento de volumen y presión. Se define como el cambio de volumen (ΔV) dividido por el cambio de presión (ΔP). Vasos más distensibles (como las venas) se expanden más fácilmente ante cambios de presión que vasos menos distensibles (como las arterias).
¿Cómo explica la Ley de Ohm la hipertensión?
La hipertensión a menudo se debe a un aumento crónico de la resistencia vascular sistémica (R) o, en menor medida, a un aumento del gasto cardíaco (Q). Según la Ley de Ohm (ΔP = Q * R), si R aumenta y Q se mantiene, la diferencia de presión (ΔP), que es la presión arterial, debe aumentar.
Conclusión
Desde la dinámica iónica a través de las membranas neuronales hasta el movimiento masivo de sangre por el cuerpo, la sencilla Ley de Ohm proporciona un marco conceptual poderoso para entender procesos biológicos complejos. La resistencia, la capacitancia y las diferencias de presión no son solo conceptos de física; son fuerzas activas que dan forma a la señalización neuronal y regulan la circulación sanguínea, demostrando la unidad de los principios físicos que gobiernan tanto los circuitos electrónicos como los sistemas vivos.
Si quieres conocer otros artículos parecidos a La Ley de Ohm en los Sistemas Vivos puedes visitar la categoría Neurociencia.
