El cerebro no es simplemente un sistema que transmite señales de un punto a otro de forma lineal. Es una máquina dinámica que ajusta, afina y cambia la forma en que la información se procesa y se envía. Este proceso de ajuste se conoce como modulación. La modulación cerebral es fundamental para funciones complejas, permitiendo respuestas flexibles y adaptativas a nuestro entorno. Va más allá de la simple excitación o inhibición sináptica, influyendo en el estado general de las redes neuronales y en la forma en que responden a los estímulos.
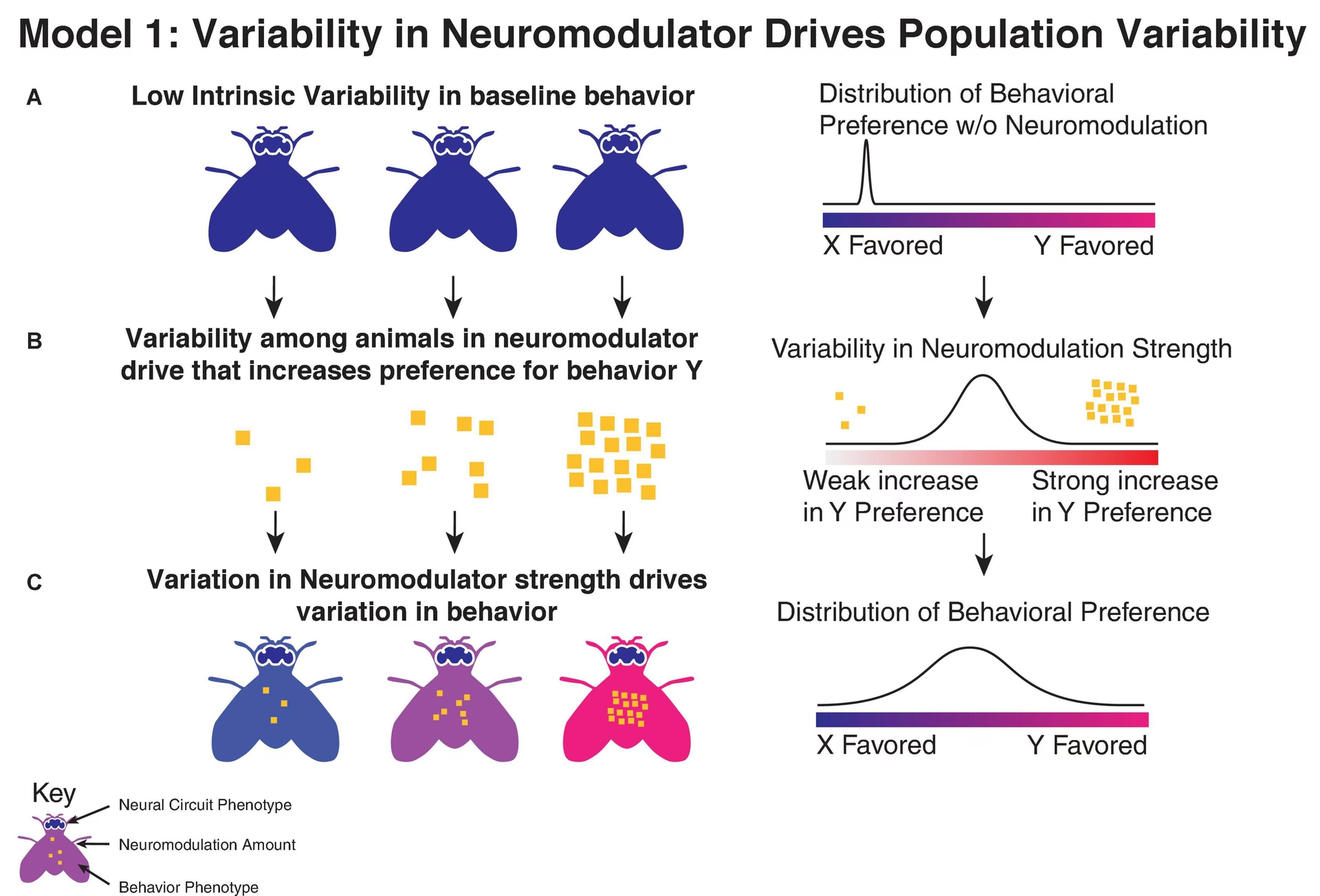
Los sistemas neuromoduladores son redes de neuronas que liberan sustancias químicas, llamadas neuromoduladores, que pueden alterar la actividad de grandes volúmenes del cerebro. A diferencia de los neurotransmisores clásicos que actúan rápidamente en sinapsis específicas, los neuromoduladores a menudo operan a través de un mecanismo conocido como transmisión por volumen.
Transmisión por Volumen: Un Enfoque Amplio
La transmisión por volumen implica la difusión de neurotransmisores o neuromoduladores a través del fluido extracelular del cerebro. Estas sustancias químicas son liberadas en puntos que pueden estar distantes de las células diana, y activan receptores extrasinápticos. Este proceso resulta en una acción transmisora más prolongada en comparación con la rápida transmisión que ocurre en una sola sinapsis.
Dentro de la transmisión por volumen, se distinguen dos modos principales basados en la duración y el patrón de liberación:
Transmisión Tónica vs. Transmisión Fásica
La transmisión por volumen puede manifestarse de maneras distintas, cada una con sus características y funciones particulares. La distinción entre transmisión tónica y fásica es crucial para comprender cómo los neuromoduladores ejercen sus efectos de ajuste a largo plazo o de respuesta rápida.
| Característica | Transmisión Tónica | Transmisión Fásica |
|---|---|---|
| Liberación de Neurotransmisores | Continua, bajo nivel | En ráfagas intensas y agudas |
| Origen de la Liberación | Células gliales, neuronas tópicamente activas | Estimulada por señales (sensoriales, estrés, recompensa) |
| Duración del Efecto | Prolongada, sostenida | Transitorio, momentáneo |
| Función Principal | Estabilidad basal, regulación de línea base, estado de preparación | Ajustes agudos, respuestas a estímulos específicos |
| Neurotransmisores Clave (ejemplos) | Acetilcolina, noradrenalina, dopamina, norepinefrina, serotonina | Dopamina, norepinefrina, serotonina |
| Asociado con | Estado de alerta, atención | Respuestas a estímulos sensoriales, estrés, recompensa |
La transmisión tónica es responsable de liberar neuromoduladores a un nivel bajo y constante, proporcionando una estabilidad a largo plazo y asegurando que las neuronas estén en un estado continuo de preparación para responder a las señales. Neurotransmisores como la acetilcolina, la noradrenalina, la dopamina, la norepinefrina y la serotonina son componentes clave en esta forma de transmisión, mediando estados como el estado de alerta y la atención.
Por otro lado, la transmisión fásica implica la liberación de neuromoduladores en ráfagas intensas y agudas en respuesta a estímulos específicos. Esto crea ajustes momentáneos en la actividad neuronal y está fuertemente asociada con respuestas a entradas sensoriales, factores de estrés externos y estímulos de recompensa, involucrando también a la dopamina, la norepinefrina y la serotonina.
La capacidad de los neuromoduladores para actuar en grandes volúmenes cerebrales y con diferentes patrones temporales les permite influir de manera significativa en el estado general de las redes neuronales, modulando así la forma en que el cerebro procesa la información y genera respuestas.
Modulación en la Vía del Dolor
Uno de los ejemplos más estudiados y clínicamente relevantes de modulación cerebral es la modulación del dolor. El dolor no es simplemente una señal directa que viaja de los receptores a la conciencia; es una experiencia compleja que puede ser alterada significativamente a medida que la señal se transmite a lo largo de las vías neuronales. La modulación del dolor explica por qué las respuestas individuales a un mismo estímulo doloroso pueden variar, por qué la activación de las neuronas del dolor no siempre coincide con la experiencia sensorial del dolor, y fundamenta los mecanismos de acción de la analgesia clínica.
Analgesia e Hiperalgesia: Dos Caras de la Modulación
Contrario a una suposición común, la modulación del dolor no siempre resulta en una disminución de la sensación dolorosa (analgesia). Las vías moduladoras tienen la capacidad de amplificar o facilitar la transmisión del dolor, lo que lleva a un aumento en la experiencia del dolor, conocido como hiperalgesia. Un ejemplo clásico de esto son los opioides: si bien en dosis limitadas alivian el dolor, en dosis altas pueden inducir hiperalgesia. Ciertos marcadores inflamatorios también pueden mediar cambios en la sensación de dolor a través de vías moduladoras que pueden tanto aumentar como disminuir la sensación. La modulación descendente del dolor, que se origina en el cerebro y desciende hacia la médula espinal, puede ser tanto 'facilitadora' (aumentando el dolor) como 'inhibitoria' (disminuyendo el dolor). Sorprendentemente, una única estructura moduladora en el cerebro a menudo puede mediar ambos tipos de modulación.
La Teoría de la Compuerta del Control del Dolor
Un concepto fundamental en la comprensión de la modulación del dolor es la Teoría de la Compuerta (Gate Control Theory - GCT), propuesta por Wall y Melzack. Aunque algunos detalles han sido refinados, sigue siendo una herramienta poderosa para guiar la investigación del dolor. La GCT postula que las señales nociceptivas (dolor) y no nociceptivas (sensación general) convergen y se suman en la sustancia gelatinosa de la médula espinal. Si la intensidad de las señales nociceptivas supera la de las señales no nociceptivas, la 'compuerta' se abre y se propaga una señal de dolor hacia el cerebro.
La teoría sugiere que las fibras nerviosas más grandes tienden a transportar información de sensación general, mientras que las fibras más pequeñas llevan información nociceptiva. La estimulación de las fibras grandes, como ocurre al frotar un área golpeada, puede 'cerrar la compuerta' al aumentar la señal no nociceptiva relativa, reduciendo así la percepción del dolor. Además, la GCT propone que las fibras aferentes descendentes desde el cerebro también pueden modular la actividad en la sustancia gelatinosa, influyendo en la apertura o cierre de la compuerta. Esta teoría ha servido de base para el desarrollo y la explicación de diversas técnicas de alivio del dolor.
Mecanismos Clínicamente Relevantes de Modulación del Dolor
Los sistemas moduladores del dolor son la base de muchos tratamientos analgésicos. La investigación ha identificado una variedad de vías y sustancias que participan activamente en la modulación del dolor, ofreciendo objetivos potenciales para terapias.
Modulación por Opioides Endógenos
El cuerpo produce sus propias sustancias con propiedades analgésicas, conocidas como opioides endógenos. Estos péptidos (como las β-endorfinas, Met-encefalina y dinorfina A) se derivan de precursores proteicos y actúan sobre receptores opioides (μ, κ, δ, NOP/ORL) distribuidos en el sistema nervioso. La disponibilidad de estos receptores puede estar alterada en condiciones de dolor crónico, lo que sugiere su relevancia clínica.
Una diferencia clave entre los opioides endógenos y los exógenos (medicamentos) es su modo de entrega. Los opioides endógenos son transportados a sus sitios de acción específicos por células inmunes, lo que generalmente previene los efectos secundarios centralizados asociados con los opioides exógenos. Se ha observado una relación entre la cantidad de leucocitos en un tejido y el grado de alivio del dolor endógeno, lo que respalda esta idea.
Modulación Autonómica del Dolor
Existe un vínculo establecido entre la función del sistema nervioso autónomo y el dolor. Por ejemplo, pacientes con dolor crónico a menudo muestran respuestas autonómicas atenuadas a estímulos dolorosos agudos en comparación con individuos sanos. Condiciones como la fibromialgia y el síndrome del intestino irritable se asocian con disfunción autonómica, a menudo caracterizada por hiperactividad simpática.
- Modulación Dopaminérgica: La dopamina afecta la sensación de dolor de forma directa e indirecta. Los trastornos del dolor son comunes en enfermedades que afectan la dopamina, como el Parkinson. La dopamina influye en la amígdala, relacionada con el miedo y la ansiedad, actuando como modulador indirecto. En las vías descendentes, puede activar receptores D2 y canales de K+, disminuyendo la liberación de glutamato y reduciendo la transmisión nociceptiva. Dado que muchos antipsicóticos actúan sobre los receptores de dopamina y que la dopamina está implicada en las vías de recompensa, la interacción entre los tratamientos para el dolor (como los opioides) y los sistemas dopaminérgicos es un área importante de investigación.
- Modulación Noradrenérgica: La norepinefrina (noradrenalina) puede tener efectos tanto analgésicos como hiperalgésicos. Fármacos que bloquean su recaptación (como algunos antidepresivos tipo SNRI) tienen eficacia clínica en el tratamiento del dolor, especialmente el neuropático. La modulación noradrenérgica participa en los circuitos moduladores descendentes, como la médula ventromedial rostral (RVM) y la sustancia gris periacueductal (PAG). La RVM integra la modulación descendente a través de células OFF (inhibidoras del dolor) y ON (excitatorias del dolor). La disfunción en esta modulación desde la RVM podría explicar por qué algunas personas progresan de dolor agudo a crónico.
- Modulación Serotoninérgica: La serotonina contribuye a procesos tanto pronociceptivos (aumentando el dolor) como antinociceptivos (disminuyendo el dolor), dependiendo del subtipo de receptor activado (por ejemplo, 5-HT1A, 1B, 1D, 7 tienden a ser antinociceptivos; 5-HT2A, 3 tienden a ser pronociceptivos). La modulación serotoninérgica es un mecanismo central en el dolor crónico. Al igual que la noradrenalina, los antidepresivos que alteran la recaptación de serotonina (SSRI, SNRI, TCA) son eficaces en el tratamiento del dolor neuropático, destacando la importancia de la serotonina en su modulación.
Modulación por Aminoácidos Inhibitorios
El equilibrio entre la excitación y la inhibición neuronal es una forma fundamental de modulación. Ciertos aminoácidos inhibidores desempeñan roles clave en la modulación del dolor.
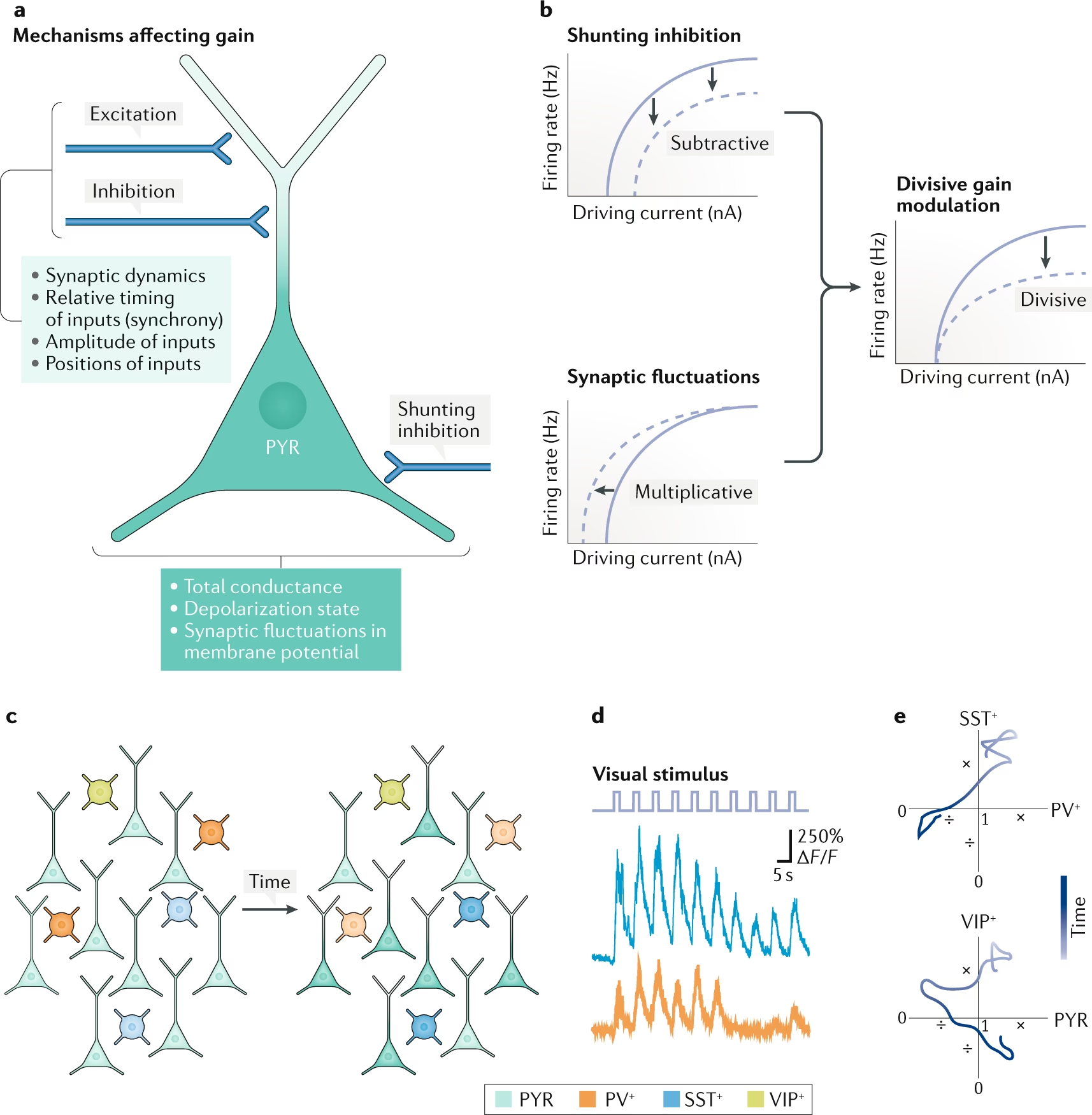
- Colecistoquinina (CCK): Aunque conocida como hormona gastrointestinal, la CCK también actúa en el cerebro y puede influir en el dolor. La CCK central puede inhibir la modulación analgésica descendente desde la RVM. Se ha descrito un efecto 'antiopioide' de la CCK, e incluso se ha sugerido que los agonistas de CCK podrían 'romper' completamente la modulación placebo del dolor. La CCK interactúa con las vías opioides y canabinoides, lo que la convierte en un objetivo potencial de investigación para mejorar la eficacia de otras terapias analgésicas.
- GABA: El principal neurotransmisor inhibitorio en el sistema nervioso central, el GABA (ácido gamma-aminobutírico) es crucial en la modulación descendente del dolor. La pérdida de la inhibición mediada por GABA puede contribuir al desarrollo de dolor inflamatorio y neuropático. Los moduladores alostéricos de los receptores GABAA, particularmente aquellos selectivos para los subtipos α2 y α3, han mostrado potencial analgésico potente en estudios. La activación de los receptores GABA A y GABA B, especialmente a nivel espinal, puede reducir la hiperalgesia postquirúrgica. Ciertas especies reactivas de oxígeno (ROS) pueden atenuar selectivamente la transmisión GABAérgica, lo que podría ser un mecanismo por el cual inducen dolor. Aunque los agonistas de receptores GABA (como las benzodiazepinas) no están optimizados para la analgesia, los receptores GABA representan objetivos terapéuticos potenciales.
- Galanina: Este neuropéptido puede tanto facilitar como inhibir la nocicepción. Se ha asociado con la antinocicepción en modelos de dolor crónico, y sus niveles aumentan en la médula espinal después de daño nervioso periférico. La galanina actúa a través de diferentes subtipos de receptores (GalR1, GalR2, GalR3), que pueden mediar efectos opuestos (por ejemplo, GalR1 y GalR3 son inhibitorios del dolor, mientras que GalR2 es excitatorio). La galanina parece ser importante en la alodinia mecánica y al frío, comunes en neuropatías, y podría estar implicada en las diferencias en los umbrales del dolor en personas obesas.
Modulación Placebo del Dolor
El efecto placebo en el alivio del dolor está bien documentado. Se cree que está mediado, al menos en parte, por la liberación de opioides endógenos, ya que un antagonista de los receptores opioides (naloxona) puede revertir el efecto analgésico del placebo. El placebo puede tanto disminuir las experiencias negativas como aumentar las experiencias agradables. Estudios de neuroimagen sugieren que el placebo disminuye el procesamiento neural en las estructuras del dolor y cambia la forma en que el cerebro 'evalúa' un estímulo potencialmente doloroso, haciéndolo menos doloroso. Aunque existen debates éticos, el uso de tratamientos simulados (sham) en el contexto clínico se ha sugerido como una herramienta valiosa, preferible a intervenciones potencialmente peligrosas o adictivas en ciertos casos.
Modulación No Tradicional del Dolor
Ciertas prácticas consideradas 'no tradicionales' también han demostrado capacidad para modular el dolor. La meditación, por ejemplo, ha mostrado reducir la intensidad y la desagradabilidad del dolor, con cambios observables en la activación cerebral. Se ha notado que los meditadores tienen cortezas frontales más gruesas, mientras que el dolor crónico se asocia con cortezas más delgadas, sugiriendo un posible vínculo estructural. El ejercicio también es importante para la supresión del dolor, especialmente en pacientes con ciertas condiciones crónicas, y una combinación de terapias farmacológicas y ejercicio puede ser beneficiosa. La acupuntura es otra intervención que podría modular el dolor, posiblemente a través de su influencia en el sistema nervioso autónomo y potencialmente a través de las mismas vías opioides endógenas que subyacen al efecto placebo.
Modulación por Opioides Exógenos
Los opioides farmacéuticos son analgésicos muy potentes y ampliamente utilizados. Actúan principalmente inhibiendo los canales de calcio y potasio, lo que impide la liberación de neurotransmisores del dolor. Si bien son muy efectivos, su uso central está limitado por efectos secundarios significativos como la adicción, la depresión respiratoria y el estreñimiento. Los opioides exógenos actúan sobre los mismos tipos de receptores que los opioides endógenos (μ, δ, κ, NOP, ORL), aunque la mayoría de los utilizados clínicamente se dirigen a los receptores μ. La investigación busca activamente formas de mitigar estos efectos secundarios, como la inhibición de receptores σ1 para mejorar la analgesia periférica sin aumentar el estreñimiento.
Modulación por Canabinoides
Los canabinoides, sustancias derivadas del cannabis, han ganado atención por su potencial analgésico. Pueden modular los canales TRP y, en el cerebro, influir en la actividad de las células ON y OFF en la RVM. Se sugiere que funcionan inhibiendo la adenosina y potenciando ciertos receptores de serotonina. Los canabinoides también pueden reducir la transmisión nociceptiva activando el receptor de glicina α3. Se están investigando como una nueva clase de agentes para el tratamiento del dolor crónico, y la investigación sugiere que, junto con los opioides, median la interacción entre la percepción del dolor y los mecanismos de recompensa.
Modulación Eléctrica (Electroanalgesia)
Las técnicas de electroanalgesia, como la Estimulación Nerviosa Eléctrica Transcutánea (TENS), encuentran su base teórica en la Teoría de la Compuerta, al aumentar las señales somatosensoriales competitivas para 'cerrar la compuerta' del dolor. La TENS ha demostrado reducir la intensidad del dolor percibido y disminuir la activación de las estructuras de procesamiento del dolor en estudios de neuroimagen funcional. Otras formas, como la estimulación transcraneal, también han mostrado resultados positivos para ciertas condiciones de dolor crónico. Sin embargo, la investigación sobre electroanalgesia a veces presenta resultados mixtos, en parte debido a la falta de un consenso científico sobre los parámetros óptimos de estimulación, lo que sugiere que, si bien la modulación eléctrica del dolor es posible, su aplicación aún requiere una definición más precisa.
Comentario de Expertos y Direcciones Futuras
La modulación cerebral, particularmente en el contexto del dolor, es un campo de investigación vibrante con un enorme potencial. Comprender cómo el cerebro ajusta las señales sensoriales y emocionales asociadas al dolor es clave para desarrollar terapias más efectivas y personalizadas. La investigación actual apunta a varios objetivos prometedores, como la modulación específica de subtipos de receptores de serotonina para maximizar la analgesia y minimizar los efectos pronociceptivos, o la focalización en el sistema de la colecistoquinina para mejorar la eficacia del placebo y otros analgésicos.
La galanina, especialmente en relación con las neuropatías y el dolor asociado a la obesidad, y los receptores GABA, aún no optimizados para la analgesia, representan vías terapéuticas poco exploradas pero con gran potencial. Los canabinoides, con sus mecanismos de acción novedosos, son un área de investigación activa y prometedora para el dolor crónico.
Un desafío clínico persistente es la falta de medidas objetivas del dolor. Aunque una medida perfecta es poco probable, la investigación explora biomarcadores potenciales como el grosor cortical, la disponibilidad de receptores opioides, el recuento de células inmunes o los polimorfismos alélicos. Estos podrían servir como 'pistas' objetivas para el diagnóstico y la evaluación de la gravedad del dolor, aunque se necesita más investigación para definir su utilidad clínica (sensibilidad, especificidad, costo).
Persisten preguntas significativas que guían la investigación futura. ¿Cuáles son los parámetros óptimos para la electroanalgesia? ¿Podrían los opioides exógenos ser entregados de manera selectiva por células inmunes para reducir los efectos secundarios centrales? ¿Cómo interactúan los tratamientos para el dolor con las enfermedades que afectan los sistemas dopaminérgicos? ¿Puede una mayor comprensión de la función de la RVM explicar la transición del dolor agudo al crónico? ¿Los polimorfismos alélicos identificados explican una mayor proporción de la población con dolor crónico? ¿Podemos desarrollar pruebas para predecir el riesgo individual de desarrollar dolor crónico?
Responder a estas preguntas es fundamental para avanzar en la modulación del dolor, desarrollar nuevas terapias y crear herramientas objetivas para mejorar el manejo del paciente. La complejidad de la modulación cerebral ofrece un vasto paisaje para la exploración científica, prometiendo nuevas formas de aliviar el sufrimiento asociado al dolor crónico.
Preguntas Frecuentes sobre la Modulación Cerebral y el Dolor
¿Qué significa exactamente modulación en el contexto del cerebro?
Significa la capacidad del cerebro para ajustar y afinar la forma en que se procesan y transmiten las señales neuronales, influyendo en el estado general de las redes neuronales y en su respuesta a los estímulos, no solo transmitiendo señales de forma directa.
¿La modulación del dolor siempre reduce el dolor?
No, la modulación del dolor puede causar tanto una disminución de la sensación dolorosa (analgesia) como un aumento de la misma (hiperalgesia), dependiendo de las vías y sustancias involucradas.
¿Qué es la Teoría de la Compuerta del Control del Dolor?
Es una teoría que explica cómo las señales de dolor y no dolor interactúan en la médula espinal y cómo la modulación descendente desde el cerebro puede influir en si la señal de dolor se transmite o se 'bloquea' en la médula.
¿Por qué los opioides que produce mi cuerpo son diferentes de los medicamentos opioides?
Aunque actúan sobre los mismos receptores, los opioides producidos por tu cuerpo (endógenos) son entregados selectivamente a los sitios de acción por células inmunes, lo que ayuda a prevenir los efectos secundarios centralizados y sistémicos comunes de los medicamentos opioides (exógenos).
¿Pueden las terapias no tradicionales como la meditación o el ejercicio ayudar con el dolor?
Sí, la investigación sugiere que estas prácticas pueden modular las vías del dolor a través de diversos mecanismos, potencialmente incluyendo la activación de sistemas analgésicos endógenos y cambios en el procesamiento cerebral del dolor.
¿Existen formas objetivas de medir el dolor, o es siempre subjetivo?
Actualmente, la experiencia del dolor es principalmente subjetiva. Sin embargo, la investigación está explorando biomarcadores potenciales (como cambios en el grosor de ciertas áreas cerebrales o la disponibilidad de receptores) que podrían proporcionar pistas objetivas para comprender y evaluar el dolor, aunque aún no existe una medida perfecta.
Si quieres conocer otros artículos parecidos a El Poder de la Modulación Cerebral puedes visitar la categoría Neurociencia.
