En los últimos años, hemos sido testigos de un aumento significativo en el número de personas que experimentan trastornos mentales, como la ansiedad y la depresión. Esta preocupante tendencia subraya la urgencia de encontrar estrategias de prevención y tratamiento más efectivas. Mientras la farmacoterapia y la psicoterapia continúan siendo pilares del tratamiento, sus limitaciones y posibles efectos secundarios impulsan la búsqueda de enfoques complementarios. Sorprendentemente, gran parte de esta búsqueda nos lleva a un lugar inesperado: nuestro intestino y los miles de millones de microorganismos que lo habitan.
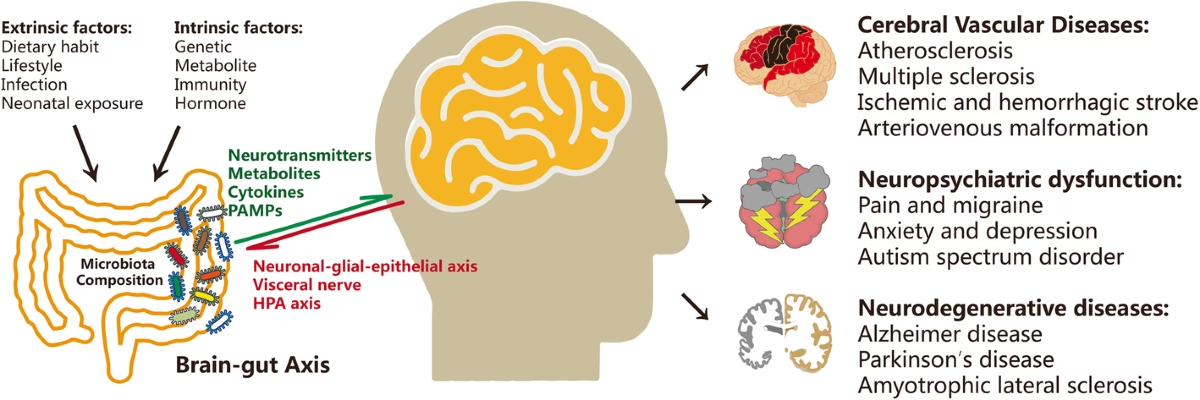
La investigación emergente ha revelado una conexión profunda y bidireccional entre el intestino y el cerebro, mediada por la vasta comunidad de microbios conocida como el microbioma intestinal. Este complejo ecosistema microbiano no solo es vital para la digestión, sino que también ejerce una influencia considerable en nuestra salud general, incluyendo la función cerebral y el bienestar psicológico. De hecho, se ha demostrado que ciertas bacterias intestinales, particularmente las de los filos Firmicutes y Bacteroidetes, afectan la salud mental a través de una intrincada red de comunicación conocida como el eje intestino-cerebro-microbiota. La alteración de este delicado equilibrio microbiano, un estado conocido como disbiosis, se ha relacionado directamente con diversos trastornos mentales, incluyendo ansiedad, depresión, trastorno bipolar, trastorno del espectro autista (TEA) y esquizofrenia, entre otros.
El Eje Intestino-Cerebro-Microbiota: Una Autopista de Comunicación
El concepto del eje intestino-cerebro-microbiota (EI-C-M) representa una perspectiva más holística para entender la salud y la enfermedad, particularmente en el contexto de los trastornos psicológicos. Lejos de ser una relación unidireccional, la comunicación entre el cerebro y el intestino es multidireccional. Esta compleja red involucra el sistema nervioso central (SNC), el sistema nervioso autónomo (SNA), el sistema nervioso entérico (SNE, el "segundo cerebro" del intestino), el eje hipotalámico-pituitario-adrenal (HPA), así como los sistemas neural, endocrino e inmune.
Esencialmente, el EI-C-M permite que las señales del cerebro influyan en las funciones motoras, sensoriales y secretoras del intestino, mientras que simultáneamente permite que las señales y los metabolitos del microbioma intestinal influyan en el desarrollo, la bioquímica, la función y el comportamiento del cerebro. Esta comunicación bidireccional, o incluso multidireccional como algunos sugieren, ofrece un nuevo y emocionante objetivo para la intervención psicológica y proporciona una comprensión más profunda de las bases biológicas de las enfermedades mentales.
Disbiosis y Trastornos Mentales Específicos
La composición del microbioma intestinal es increíblemente compleja y varía entre individuos. Algunas bacterias son protectoras para la salud mental, mientras que otras pueden estar asociadas con el inicio y la progresión de trastornos. La investigación ha identificado patrones de disbiosis específicos relacionados con diferentes condiciones psicológicas.
Ansiedad
La ansiedad es uno de los trastornos mentales más comunes. Estudios han encontrado que las personas con ansiedad a menudo presentan una menor riqueza y diversidad microbiana en comparación con individuos sanos. A nivel de filo, se observa típicamente una disminución de Firmicutes y un aumento de Bacteroidetes y Fusobacteria. A nivel de género, se han asociado con la ansiedad un aumento de Prevotella, Lactobacillales, Sellimonas, Streptococcus y Enterococcus, y una disminución de Faecalibacterium spp. Esto sugiere que modular estas poblaciones bacterianas podría ser un enfoque prometedor para la prevención y el tratamiento de la ansiedad. Sin embargo, se necesita más investigación a nivel de especie, ya que diferentes especies dentro del mismo género pueden tener efectos distintos o incluso opuestos.
Depresión
La depresión es un problema de salud pública global con consecuencias graves. La disbiosis del microbioma intestinal ha sido fuertemente asociada con su aparición y desarrollo. Se han observado diferencias significativas en la composición microbiana fecal entre individuos sanos y pacientes con trastorno depresivo mayor (TDM), incluyendo una reducción en la diversidad alfa en episodios depresivos actuales. Géneros como Dialister y Coprococcus spp. se han encontrado disminuidos en pacientes con depresión. Por el contrario, se han observado niveles más altos de Prevotella, Klebsiella, Streptococcus y Clostridium XI. La infección por Helicobacter pylori también se ha vinculado a un mayor riesgo de síntomas depresivos, especialmente en mujeres. Estudios con trasplantes fecales de pacientes deprimidos a ratones libres de gérmenes han inducido comportamientos similares a la depresión, reforzando el vínculo causal. La modulación del microbioma intestinal emerge como un objetivo potencial para la prevención y el manejo de la depresión.
Trastorno Bipolar
El trastorno bipolar es una enfermedad crónica y recurrente. La evidencia sugiere un vínculo entre el microbioma intestinal y esta condición. Pacientes con trastorno bipolar han mostrado una reducción en la diversidad del microbioma, con un aumento de Clostridiaceae y Collinsella. Otro estudio encontró que Flavonifractor estaba asociado con el trastorno bipolar, mientras que Faecalibacterium y Ruminococcaceae estaban disminuidos. Las discrepancias entre estudios pueden deberse a diferencias en las características de los participantes, lo que subraya la necesidad de investigaciones a gran escala con poblaciones más representativas.
Trastorno del Espectro Autista (TEA)
El TEA es un trastorno del neurodesarrollo heterogéneo. La composición y abundancia del microbioma intestinal difieren entre niños con y sin TEA. Se han encontrado mayores niveles de Clostridium bolteae, Clostridium paraputri y Clostridium perfringens en niños con TEA. Ciertas especies como Clostridium diffiicile y Clostridium clostridiioforme se han encontrado solo en niños con TEA. A nivel de filo, se han observado mayores abundancias de Actinobacteria, Proteobacteria y Bacilli, y menores de Akkermansia muciniphila, Faecalibacterium y Agathobacter. La severidad de los síntomas del TEA también puede estar ligada al microbioma; por ejemplo, niños con TEA y trastornos del sueño mostraron menor abundancia de Faecalibacterium y Agathobacter.
Esquizofrenia
La esquizofrenia, que afecta a cerca del 1% de la población mundial, también se asocia con disbiosis del microbioma intestinal. Se han encontrado bacterias específicas en pacientes con esquizofrenia que están ausentes en individuos sanos, como Lactobacillus fermentum, Enterococcus faecium y Alkaliphilus oremlandii. Algunas bacterias están positivamente correlacionadas con la severidad de los síntomas (Lachnospiraceae, Veillonella, Collinsella, Lactobacillus, Succinivibrio, Corynebacterium), mientras que otras están negativamente correlacionadas (Coprococcus, Ruminococcus, Roseburia, Adlercreutzia, Anaerostipes, Faecalibacterium). El microbioma también puede influir en la neuroquímica a través de la modulación del ciclo glutamato–glutamina–ácido gamma-aminobutírico (GABA).
Mecanismos de Influencia: ¿Cómo se Comunican?
El microbioma intestinal influye en el cerebro y la salud mental a través de múltiples vías:
Producción de Neurotransmisores y Metabolitos
Una de las vías más directas es la capacidad del microbioma para producir y regular neurotransmisores clave y sus precursores. Las bacterias intestinales pueden metabolizar aminoácidos que sirven como bloques de construcción para neurotransmisores como GABA, serotonina, melatonina, dopamina y norepinefrina. Aunque los neurotransmisores producidos en el intestino no siempre cruzan directamente la barrera hematoencefálica (BHE), pueden influir en el SNC a través de la estimulación del nervio vago o mediante vías circulatorias e inmunes indirectas. El triptófano, precursor de la serotonina, sí puede cruzar la BHE, lo que sugiere que los metabolitos microbianos pueden influir directamente en la química cerebral.
| Género/Especie | Neurotransmisor (precursor) | Efecto en el SNC | Efecto Periférico |
|---|---|---|---|
| Candida, Streptococcus, Escherichia, Enterococcus, Lactobacillus bulgaricus | Serotonina (triptófano) | Control motor, regulación cerebelar, sinaptogénesis, emoción, memoria, estrés | Ritmo circadiano, motilidad intestinal, temperatura corporal, dolor visceral, apetito |
| Corynebacterium glutamicum, Lactobacillus plantarum, Lactobacillus paracasei, Lactobacillus lactis, Brevibacterium lactofermentum, Brevibacterium flavum | L-glutamato | Excitatorio, desarrollo cerebral, plasticidad sináptica | |
| Lactobacillus, Bifidobacterium, Escherichia coli, Pseudomonas | GABA (L-glutamato) | Inhibitorio, ansiolítico | Miorrelajante, modera motilidad intestinal, vaciamiento gástrico |
| Bacillus, Serratia, E. coli | Dopamina (L-Dopa) | Comportamiento motivado por recompensa, control motor, cognición, emoción | Estimula secreción exocrina, inhibe motilidad intestinal |
| Bacillus, E. coli, Saccharomyces | Norepinefrina (dopamina) | Hormona del estrés, atención, emoción, sueño, aprendizaje | Media el crecimiento de bacterias patógenas |
| (Dependiente de la producción de triptófano y síntesis de serotonina) | Melatonina (serotonina) | Ritmo circadiano, estado de ánimo | Función gastrointestinal, protege contra permeabilidad intestinal, antioxidante |
Ácidos Grasos de Cadena Corta (AGCC)
Los ácidos grasos de cadena corta (AGCC), como el acético, el butírico y el propiónico, son metabolitos principales producidos por la fermentación de la fibra dietética por las bacterias intestinales. Estos compuestos tienen numerosos efectos beneficiosos para la salud del huésped, incluyendo propiedades neuroprotectoras en el cerebro (particularmente el butirato). A nivel periférico, los AGCC influyen en el tamaño y la función de las células T reguladoras, cruciales para la homeostasis inmune y la regulación de la inflamación. Además, los AGCC fortalecen la función de la barrera intestinal al regular las proteínas de unión estrecha (tight junctions). Una permeabilidad intestinal anormal (intestino permeable) permite que toxinas y microbios crucen la barrera epitelial, desencadenando una respuesta inflamatoria que puede disregular el SNE y la función inmune sistémica, contribuyendo a trastornos psicológicos como la depresión.

Regulación de la Barrera Hematoencefálica (BHE)
Además de la barrera intestinal, los AGCC también parecen regular la permeabilidad de la barrera hematoencefálica (BHE), que controla el acceso de macromoléculas y neurotoxinas potenciales al cerebro. La disfunción de la BHE se ha asociado con condiciones neuropsicológicas como la enfermedad de Alzheimer y el autismo, y se propone un vínculo con la depresión y la esquizofrenia. Estudios con ratones libres de gérmenes (sin microbiota) muestran una mayor permeabilidad de la BHE que puede ser normalizada con la colonización por bacterias productoras de AGCC.
Influencia en el Comportamiento y la Personalidad
Estudios en animales libres de gérmenes han proporcionado información valiosa sobre la influencia del microbioma en el comportamiento del huésped. Estos ratones muestran alteraciones en la expresión del factor neurotrófico derivado del cerebro (BDNF), los AGCC y el eje HPA, así como comportamientos ansiosos y depresivos y alteraciones en la función social. La manipulación del microbioma ha demostrado alterar los niveles de hormonas del estrés como el factor liberador de corticotropina (CRF) y el cortisol. Se ha propuesto una relación entre la composición del microbioma y los rasgos de personalidad, aunque se necesita más investigación.
Intervenciones Dietéticas y Naturales: Un Camino Prometedor
Dado el fuerte vínculo entre la dieta y la composición del microbioma, las intervenciones dietéticas emergen como una estrategia clave para modular el microbioma y, potencialmente, mejorar la salud mental. La dieta occidental moderna, rica en alimentos procesados y baja en fibra, se ha relacionado con cambios microbianos que promueven la inflamación, un factor subyacente en muchos trastornos psicológicos.
Componentes dietéticos específicos han demostrado efectos protectores contra los trastornos mentales al favorecer las bacterias beneficiosas y suprimir las dañinas:
- Probióticos: Microorganismos vivos que, cuando se administran en cantidades adecuadas, confieren un beneficio para la salud del huésped. Géneros como Lactobacillus y Bifidobacterium son bien conocidos y han mostrado efectos prometedores.
- Prebióticos: Sustratos no digeribles que son utilizados selectivamente por microorganismos del huésped confiriendo un beneficio para la salud. La fibra dietética es un ejemplo clásico, alimentando a las bacterias productoras de AGCC.
- Simbióticos: Combinaciones de probióticos y prebióticos.
- Postbióticos: Preparaciones de microorganismos inanimados y/o sus componentes que confieren un beneficio para la salud del huésped. Los AGCC son ejemplos importantes.
- Otros alimentos como productos lácteos, especias (Zanthoxylum bungeanum, curcumina, capsaicina), frutas, verduras y hierbas medicinales también contienen compuestos que pueden modular el microbioma intestinal y ejercer efectos protectores sobre la salud mental.
Adoptar una dieta rica en fibra, frutas, verduras y alimentos fermentados puede promover un microbioma diverso y saludable, lo que a su vez puede tener un impacto positivo en el estado de ánimo y la cognición. Un estudio incluso demostró que la adherencia a una dieta tipo mediterránea resultó en una mejora significativa en los síntomas de depresión.
Tablas Comparativas: Microbioma y Trastornos
| Trastorno Mental | Cambios Observados en la Microbiota (Ejemplos) | Posible Implicación |
|---|---|---|
| Ansiedad | ↓ Diversidad, ↓ Firmicutes/Bacteroidetes, ↓ Faecalibacterium, ↑ Prevotella, Lactobacillales, Streptococcus | Influencia en el comportamiento relacionado con la ansiedad, producción de metabolitos |
| Depresión | ↓ Diversidad, ↓ Dialister, Coprococcus, ↑ Prevotella, Klebsiella, Helicobacter pylori (en mujeres) | Alteración de la bioquímica cerebral, respuesta al estrés |
| Trastorno Bipolar | ↓ Diversidad, ↓ Faecalibacterium, Ruminococcaceae, ↑ Clostridiaceae, Collinsella, Actinobacteria, Coriobacteria, Flavonifractor | Posible influencia en la estabilidad del estado de ánimo |
| Trastorno del Espectro Autista (TEA) | ↑ Clostridium bolteae, Clostridium paraputri, Clostridium perfringens, Actinobacteria, Proteobacteria, Bacilli, ↓ Akkermansia muciniphila, Faecalibacterium, Agathobacter | Alteraciones en el desarrollo neurológico, severidad de síntomas |
| Esquizofrenia | ↓ Coprococcus, Ruminococcus, Roseburia, Faecalibacterium, ↑ Lachnospiraceae, Veillonella, Collinsella, Lactobacillus, Succinivibrio (algunas especies solo en pacientes) | Modulación de la neuroquímica (ej. ciclo GABA), respuesta inmune |
Preguntas Frecuentes
¿Qué es el eje intestino-cerebro?
Es una red de comunicación bidireccional que conecta el sistema nervioso central (cerebro) y el sistema nervioso entérico (intestino), mediada e influenciada por el microbioma intestinal.
¿Cómo afecta el microbioma intestinal a mi cerebro?
Lo hace a través de varias vías, incluyendo la producción de neurotransmisores y otros metabolitos (como los AGCC), la modulación del sistema inmune y la inflamación, y la influencia en la integridad de las barreras intestinal y hematoencefálica.
¿Puede cambiar mi dieta mejorar mi salud mental?
Sí, la dieta es uno de los factores ambientales más importantes que moldea la composición del microbioma. Una dieta rica en fibra, frutas, verduras y alimentos fermentados puede promover un microbioma saludable, lo que está asociado con un mejor bienestar mental.
¿Qué son los probióticos y los prebióticos?
Los probióticos son bacterias beneficiosas vivas que se pueden consumir (en alimentos como el yogur o suplementos). Los prebióticos son tipos de fibra que alimentan a estas bacterias beneficiosas en el intestino.
¿El microbioma es una cura para los trastornos mentales?
No se considera una cura única, sino una pieza importante del rompecabezas. Dirigirse al microbioma, a menudo a través de la dieta o suplementos específicos, es una estrategia prometedora que puede complementar los tratamientos tradicionales como la terapia y la medicación.
Conclusión
La creciente evidencia que vincula el microbioma intestinal con la salud mental representa un cambio de paradigma en nuestra comprensión de los trastornos psicológicos. El eje intestino-cerebro emerge como un actor clave en la predisposición, el inicio y la perpetuación de estas condiciones. La disbiosis del microbioma no es solo un fenómeno acompañante, sino que podría ser un factor causal o contribuyente significativo. La buena noticia es que el microbioma es maleable. Las intervenciones dietéticas, el uso de probióticos, prebióticos y otros productos naturales ofrecen vías emocionantes para modular la composición y función del microbioma intestinal con el objetivo de prevenir y tratar los trastornos mentales. Aunque la investigación está en curso y se necesitan más estudios a nivel de especies bacterianas y sus mecanismos precisos, la integración del conocimiento sobre el microbioma en las estrategias de salud mental, incluyendo un enfoque multidisciplinario que considere la dieta y la salud intestinal, tiene el potencial de mejorar significativamente el bienestar de millones de personas en todo el mundo.
Si quieres conocer otros artículos parecidos a Microbioma Intestinal y Salud Mental puedes visitar la categoría Neurociencia.

