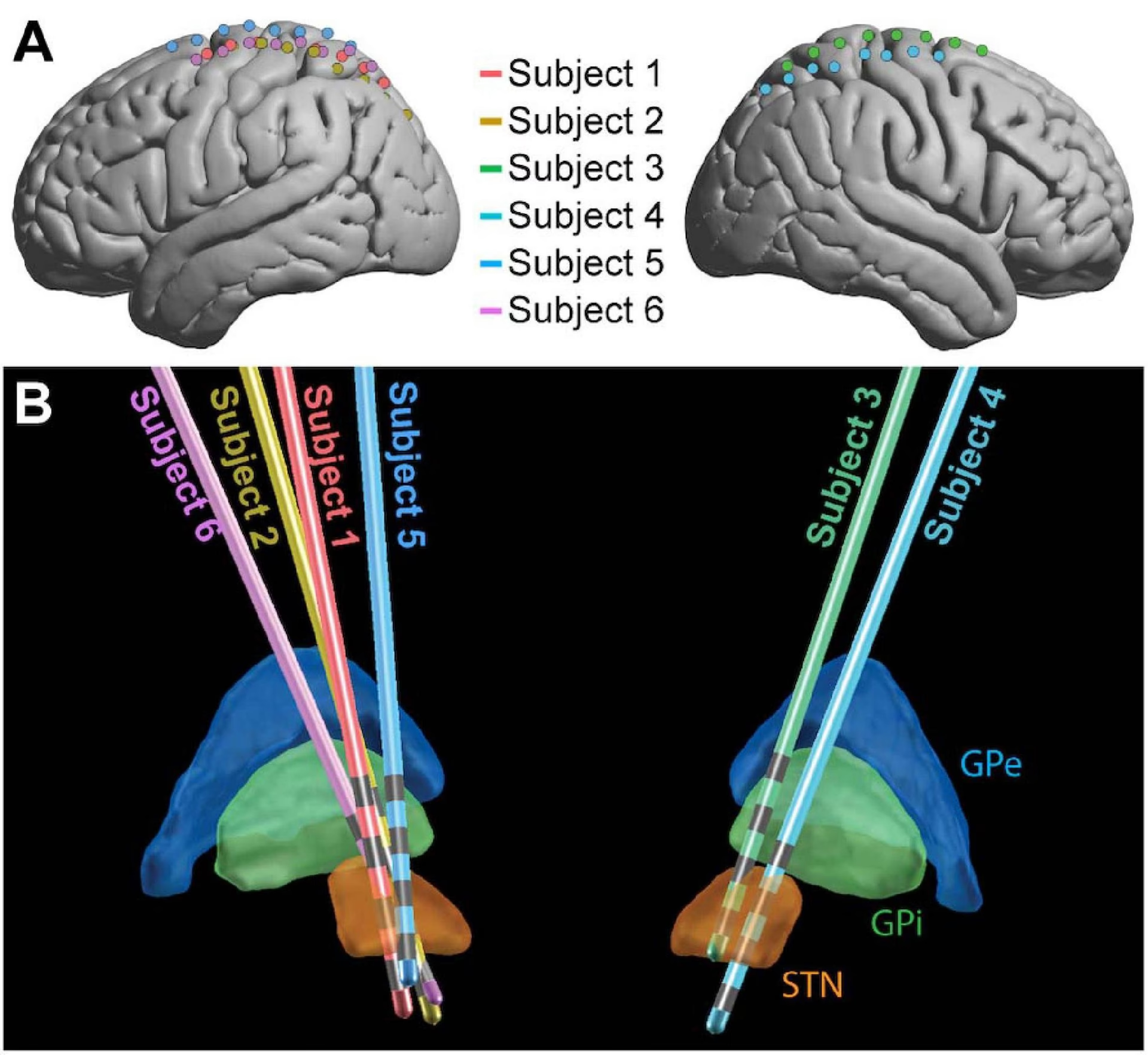
El núcleo subtalámico (NST) es una estructura cerebral fascinante y evolutivamente conservada, identificada en diversas especies, desde lampreas hasta primates. Forma parte integral de la red extendida de los ganglios basales, un conjunto de núcleos subcorticales cruciales para el control del movimiento, el aprendizaje y la motivación. Su descubrimiento en humanos se remonta a 1865 por el neurólogo francés Jules Bernard Luys, quien lo describió inicialmente como el 'cuerpo de Luys'. Sin embargo, su vital importancia en la función motora no se reconoció plenamente hasta 1927, cuando James Martin observó movimientos involuntarios anormales (hemibalismo o hemicorea) en un paciente con daño en esta área. Casos posteriores confirmaron esta conexión, cimentando la comprensión inicial del NST como un actor clave en el control motor.
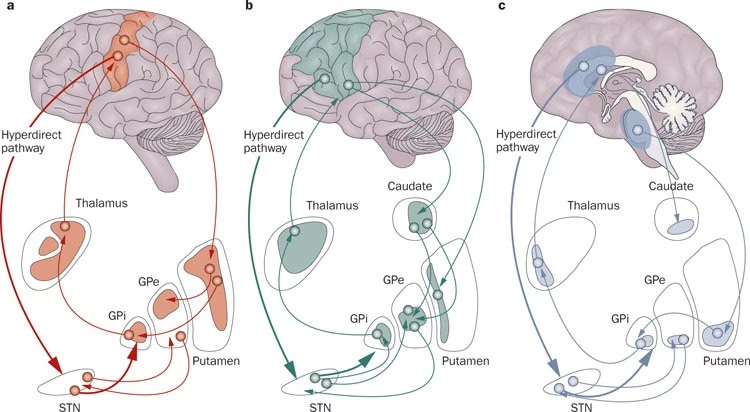
Experimentos en primates no humanos con lesiones ipsilaterales del NST mostraron discinesias contralaterales significativas, reforzando su rol en la regulación del movimiento. De manera crucial, la lesión del NST en modelos animales de la enfermedad de Parkinson (EP) demostró ser capaz de revertir los déficits motores característicos de esta enfermedad. Este hallazgo pionero allanó el camino para una de las terapias más transformadoras en la neurocirugía funcional: la Estimulación Cerebral Profunda (ECP) dirigida al NST.
El NST como Objetivo Terapéutico en la ECP
La Estimulación Cerebral Profunda (ECP) del NST se ha consolidado como un enfoque quirúrgico altamente eficaz para reducir los síntomas motores en pacientes con enfermedad de Parkinson avanzada, a menudo superando incluso la terapia farmacológica en pacientes con complicaciones motoras tempranas. La ECP implica la implantación de electrodos en regiones cerebrales específicas, como el NST, que emiten impulsos eléctricos para modular la actividad neuronal anormal. Este procedimiento ha demostrado ser reversible y ajustable, ofreciendo una alternativa más segura y controlable a las lesiones quirúrgicas que se realizaban en el pasado.
Más allá de la EP, la ECP en el NST se aplica actualmente en el tratamiento de otros trastornos neurológicos y neuropsiquiátricos. Ha mostrado éxito en casos de trastorno obsesivo-compulsivo (TOC) refractario al tratamiento convencional y en ciertas formas de distonía. Además, el NST se perfila como un objetivo prometedor para el síndrome de Tourette severo y resistente, así como para abordar la adicción a las drogas. La capacidad de modular con éxito tanto los trastornos motores como los no motores subraya la compleja y multifacética función del NST.
Sin embargo, a pesar de los notables beneficios, algunos pacientes con ECP en el NST han reportado efectos secundarios adversos. Estos pueden afectar funciones cognitivas, fisiológicas y límbicas. Se han documentado casos de depresión y aumento de peso en ambos sexos, mientras que otros síntomas, como la disfunción sexual y la agresión, se han reportado predominantemente en pacientes masculinos. Es fundamental realizar análisis clínicos detallados para discernir si estos efectos son directamente inducidos por la ECP o si son manifestaciones de la progresión de la propia enfermedad de Parkinson, de comorbilidades o de la medicación concomitante.
El globus pallidus (GP), otra estructura de los ganglios basales, también es un objetivo importante para la ECP en la EP y la distonía. Las comparaciones entre la ECP en el NST y en el globus pallidus interno (GPi) para la distonía han demostrado que ambas son efectivas, aunque la ECP en el NST parece superior para la distonía generalizada, mientras que la ECP en el GPi es más efectiva para la distonía troncal. En la EP, estudios retrospectivos comparando la ECP en el NST y el GPi han mostrado mejoras motoras similares a corto plazo, pero la ECP en el NST se ha asociado con una mayor incidencia de apatía, e incluso con impactos en el estado de ánimo y la calidad de vida, incluyendo casos de suicidio reportados en algunos estudios, aunque la causalidad directa sigue siendo objeto de investigación.
Dada su importancia clínica y el deseo de refinar los tratamientos, comprender a fondo la anatomía del NST, su composición celular y molecular es esencial. Mejorar la especificidad y precisión en los mapas cerebrales estereotácticos utilizados en cirugía, basándose en este conocimiento organizacional, podría optimizar los sitios de implantación de electrodos y potencialmente reducir los efectos secundarios adversos, permitiendo una modulación más selectiva de las funciones específicas del NST.
Anatomía y Organización Interna del NST
Anatómicamente, el núcleo subtalámico se describe como un núcleo compacto situado entre el tálamo y el mesencéfalo, ventral a la zona incerta y adyacente a la sustancia negra. Su característica forma biconvexa, similar a una lente, se mantiene notablemente constante en diferentes especies, incluyendo humanos, ratas, gatos y monos. Tiene una orientación oblicua con ejes rostrocaudal, mediolateral y dorsoventral.
El NST humano contiene, en promedio, alrededor de 225,000 neuronas por hemisferio. Las mediciones de volumen mediante resonancia magnética (RM) varían, reportándose generalmente entre 50 y 80 mm³, aunque otras técnicas sugieren volúmenes mayores (~155 mm³). Esta variación podría deberse a las diferentes técnicas de RM empleadas. A pesar de ser una región pequeña, sus límites están rodeados por densas fibras de estructuras como la cápsula interna y el fascículo lenticular.
Las técnicas de RM han sugerido una compartimentalización anatómica dentro del NST, a menudo referida como el modelo tripartito. Este modelo propone tres regiones: motora, asociativa y límbica, correlacionando anatomía con función. Estos compartimentos, también llamados territorios, dominios o subdivisiones, se extienden a lo largo de los ejes anatómicos del NST. La región dorsolateral se asocia con la función sensoriomotora, la ventromedial (o central) con la función cognitiva/asociativa, y la región más medial con la función límbica. El área límbica, a menudo llamada 'punta límbica', está estrechamente relacionada con el para-NST, sin un límite anatómico claro.

Sin embargo, la organización interna del NST es objeto de intensa investigación y debate. Estudios recientes sugieren que las subdivisiones anatómicas, especialmente las asociativas y límbicas, no tienen límites nítidos, sino que se separan por gradientes funcionales. La evidencia acumulada, incluyendo nuevos marcadores moleculares y estudios de RM, desafía el estricto modelo tripartito. Un análisis de estudios en primates de 1925 a 2010 identificó entre cero y cuatro subdivisiones, con limitada evidencia sólida para tres. Investigaciones más recientes han propuesto incluso seis subpartes arbitrarias basadas en tinciones histológicas. Claramente, la organización interna del NST es más compleja y aún se está dilucidando, probablemente definida por una combinación de anatomía y marcadores moleculares/celulares.
La conectividad del NST es topológicamente organizada y apoya el modelo tripartito, aunque con solapamientos. Recibe aferencias corticales significativas, incluyendo de la corteza motora, orbitofrontal, prefrontal y límbica. Sus eferencias principales se dirigen a otras estructuras de los ganglios basales, como el GP (externo e interno), la sustancia negra (pars reticulata y compacta), el núcleo pedúnculopontino y el pálido ventral. La conectividad de la red motora, en particular, ha demostrado ser predictiva de la eficacia de la estimulación subtalámica en la EP. La convergencia de vías motoras y no motoras en ciertas regiones del NST podría explicar los efectos tanto beneficiosos como adversos de la ECP sobre comportamientos no motores.
Composición Celular y Marcadores Moleculares
El núcleo subtalámico es predominantemente un núcleo cerebral excitatorio. La mayoría de sus neuronas utilizan glutamato como neurotransmisor principal. Marcadores como el ARN mensajero (ARNm) del transportador vesicular de glutamato 2 (VGLUT2) se distribuyen ampliamente en el NST, indicando su identidad glutamatérgica. Una pequeña población de interneuronas GABAérgicas también está presente, siendo más numerosas en la región anteromedial del NST humano. El NST recibe una compleja aferencia de neurotransmisores, incluyendo GABA, serotonina y dopamina, reflejada en la presencia de sus receptores en las neuronas subtalámicas.
En cuanto a las aferencias glutamatérgicas, se ha identificado la proteína VGLUT1 en el NST humano, sugiriendo proyecciones de la corteza y otras áreas excitatorias. Los receptores de glutamato (AMPA, NMDA, metabotrópicos) también están presentes en las neuronas del NST.
Las aferencias GABAérgicas provienen principalmente del globus pallidus externo (GPe) y el pálido ventral (VP). Los receptores GABA A y GABA B se localizan en las neuronas del NST, mostrando una distribución diferencial, por ejemplo, los receptores GABA A subtipo α3 se localizan en la región ventromedial anterior.
La serotonina está presente en fibras que pasan por el NST, con una detección abundante en las partes mediales en monos y humanos. Los receptores de serotonina 5'HT1B y 5'HT2C también se encuentran en el NST.
El NST recibe proyecciones dopaminérgicas escasas de la sustancia negra pars compacta (SNc) y el área tegmental ventral (VTA). Los receptores de dopamina, especialmente D2R, se distribuyen de forma gradiente en el NST humano, con co-localización con receptores de adenosina A2A. En ratas, el D1R muestra alta expresión, y su estimulación parece aumentar la tasa de disparo de las neuronas del NST.
Además de los neurotransmisores, las proteínas de unión a calcio son marcadores moleculares clave en el NST. La Parvalbúmina (PARV) y la Calbindina 2 (CALB2) muestran una distribución segmentada en el NST humano y de mono. Aproximadamente el 50% de las neuronas son PARV-positivas (principalmente en la región dorsal/lateral) y el 50% CALB2-positivas (principalmente en la región ventral/medial), con cierta superposición central. Esta distribución molecular sugiere subdivisiones funcionales y dinámicas de calcio diferenciales. Se ha propuesto que las neuronas PARV+ procesan funciones motoras, mientras que las CALB2+ están más involucradas en funciones límbicas.
Estudios recientes en roedores, utilizando técnicas avanzadas como la secuenciación de ARN de núcleo único (snRNASeq) y la hibridación in situ fluorescente (FISH), han revelado una heterogeneidad molecular sorprendente. Han identificado nuevos marcadores y perfiles de expresión génica combinatorios que permiten definir dominios moleculares dentro del NST. Por ejemplo, el ARNm de Pitx2 y Vglut2 se distribuyen por todo el NST del ratón, mientras que otros como Col24a1 y PV muestran patrones de expresión opuestos, lo que ha llevado a proponer dominios moleculares distintos (STNa, STNb, STNc) que difieren del modelo tripartito tradicional en primates. También se ha identificado una pequeña tira dorsal (STNds) con perfil GABAérgico.
Funciones y Comportamientos Regulados por el NST
La función más conocida del NST es su papel en el control motor. La activación del NST se asocia con la inhibición del movimiento, principalmente a través de las vías indirecta e hiperdirecta de los ganglios basales. La región dorsolateral del NST (dlSTN) es la principal implicada en funciones motoras, siendo el objetivo prioritario para la ECP en la enfermedad de Parkinson. Estudios en primates sugieren una regionalización dentro del dlSTN, donde la región medial regula las extremidades superiores y la lateral las inferiores.
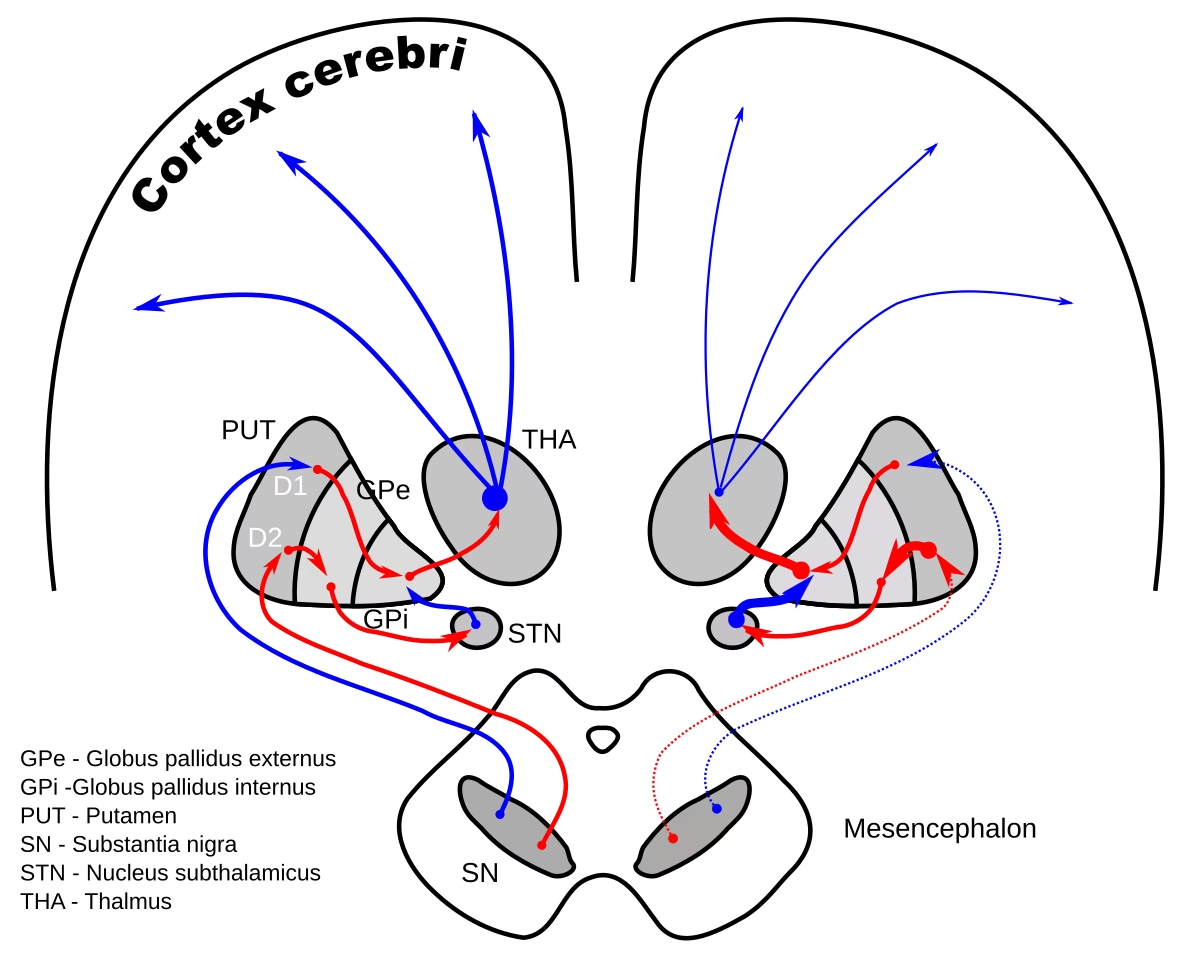
La vía indirecta de los ganglios basales se opone a la vía directa, promoviendo la inhibición del movimiento. El NST recibe aferencias inhibitorias del GPe y proyecta de manera excitatoria al GPi y SNr. Experimentos de optogenética en ratones han demostrado que la inhibición del NST promueve el movimiento, mientras que la excitación lo inhibe, o incluso aumenta comportamientos específicos como el acicalamiento. La reducción condicional de la expresión de Vglut2 en el NST también induce hiperlocomoción, sugiriendo roles opuestos de las neuronas glutamatérgicas del NST en el comportamiento motor versus el motivado.
El NST también es un mediador importante del comportamiento de búsqueda de recompensa y las funciones límbicas. El aumento de peso reportado por algunos pacientes con ECP podría estar relacionado con cambios en el gasto energético, niveles de neuropéptidos o ingesta de alimentos. Lesiones del NST en roedores aumentan la motivación por la comida. La actividad neuronal del NST aumenta durante la alimentación, particularmente para alimentos placenteros, y la manipulación optogenética bidireccional del NST puede aumentar o disminuir la ingesta de alimentos. Las funciones límbicas del NST probablemente están influenciadas por su conexión con el pálido ventral (VP), que proyecta selectivamente a la región ventral del NST, correlacionada con el dominio límbico. Esta vía VP-NST se ha implicado en la recaída en la búsqueda de alcohol en modelos de adicción.
El NST está involucrado en la motivación para el consumo de drogas de abuso. La ECP en el NST ha demostrado disminuir el esfuerzo por la ingesta de cocaína, pero aumentar la ingesta de comida, sugiriendo patrones de actividad distintos para recompensas naturales y artificiales. Las oscilaciones neuronales en bandas theta y beta en el NST se correlacionan con el consumo de cocaína. La ECP a baja frecuencia (30 Hz) ha reducido la búsqueda compulsiva de cocaína en ratas.
En cuanto a la función cognitiva, el NST contribuye al control de la acción, la toma de decisiones, la atención, las funciones ejecutivas y el aprendizaje/memoria verbal. Estudios en monos y humanos lo asocian con la selección entre comportamientos correctos e incorrectos. Las aferencias corticales a la región ventromedial del NST, el área asociativa, son importantes para la cognición. Sin embargo, estudios de ECP en pacientes con EP han identificado un declive en la actividad cognitiva en áreas como la memoria de trabajo y la inhibición de respuesta post-cirugía. En casos de TOC, la ECP en el NST impacta la toma de decisiones y la inhibición de respuesta. Modelos animales con lesiones del NST muestran deterioro en la inhibición de respuesta e aumento de la impulsividad. Las funciones cognitivas del NST dependen de la dinámica oscilatoria y de las aferencias corticales.
El NST en Trastornos Neurológicos
El núcleo subtalámico está implicado en varios trastornos neurológicos. A diferencia de la enfermedad de Parkinson, donde el NST permanece anatómicamente intacto (aunque hiperactivo), en otras patologías como la parálisis supranuclear progresiva (PSP), la enfermedad de granos argirófilos (AGD), la enfermedad de Huntington, y ciertas ataxias espinocerebelosas y la atrofia dentatorrubropalidoluysiana (DRPLA), la patología del NST incluye pérdida neuronal y gliosis astrocítica. En la enfermedad de Huntington, el NST experimenta una reducción significativa en volumen y número de neuronas.
En la enfermedad de Parkinson, el NST se vuelve hiperactivo, mostrando patrones de disparo anormales ('bursting') a una tasa más alta. Esta hiperactividad contribuye a los síntomas motores y se correlaciona con su severidad. Se hipotetiza que la pérdida de neuronas dopaminérgicas en la SNc en la EP causa una disfunción en las vías de los ganglios basales, llevando a una actividad excesiva del NST y una activación anormal de la vía indirecta, lo que resulta en movimientos involuntarios aumentados y dificultad para ejecutar movimientos intencionados.
Aunque la ECP en el NST es un tratamiento clave para la EP avanzada y otros trastornos, no hay vínculos directos a la patología celular o anatómica del NST en todos estos trastornos. La intervención se centra en modular la actividad de disparo alterada. La desregulación del disparo neuronal en el NST en pacientes con EP se correlaciona con la severidad del déficit motor, no con cambios anatómicos en el NST. Se ha propuesto que las alteraciones en la neurotransmisión del NST en la EP son impulsadas por las aferencias GABAérgicas del GP y las dopaminérgicas de la SNc. Sin embargo, la densidad de receptores GABA B parece disminuida en otras áreas de los ganglios basales en pacientes con EP.
En cuanto a los marcadores celulares, la distribución segmentada de PARV y CALB2 en el NST parece inalterada en casos de EP post-mortem. La presencia de cuerpos de Lewy en el NST de pacientes con EP sugiere disfunción celular en lugar de pérdida neuronal. La investigación de marcadores moleculares en el NST en el contexto de enfermedades es un área activa, con el objetivo de entender mejor las bases celulares de la disfunción.
Perspectivas Futuras
La creciente comprensión de la heterogeneidad molecular del NST ofrece nuevas vías para explorar las bases neurobiológicas de su papel en la regulación motora, límbica y cognitiva. Aunque aún estamos lejos de comprender completamente la complejidad de esta área cerebral crucial, asociar esta heterogeneidad con la regulación de comportamientos distintos será significativo en diversos campos. En el futuro, enfoques terapéuticos más refinados, como la estimulación optogenética dirigida a tipos celulares específicos o la aplicación híbrida de estimulación eléctrica y optogenética, podrían mejorar las técnicas actuales de ECP, reduciendo los efectos adversos y la estimulación de áreas no deseadas.
Es crucial caracterizar funcionalmente los marcadores moleculares identificados en el NST y evaluar su regulación en el contexto de las enfermedades relacionadas con el NST. Se necesitan más estudios para expandir nuestro conocimiento de la arquitectura interna del NST y su vasta red en los neurocircuitos y el control del comportamiento. El examen de los perfiles moleculares en el NST, tanto en fisiología normal como en trastornos neurológicos, ayudará a una mejor comprensión de su papel en la salud y la enfermedad, proporcionando información valiosa para mapas cerebrales más precisos que, a su vez, puedan conducir a enfoques de tratamiento más refinados.
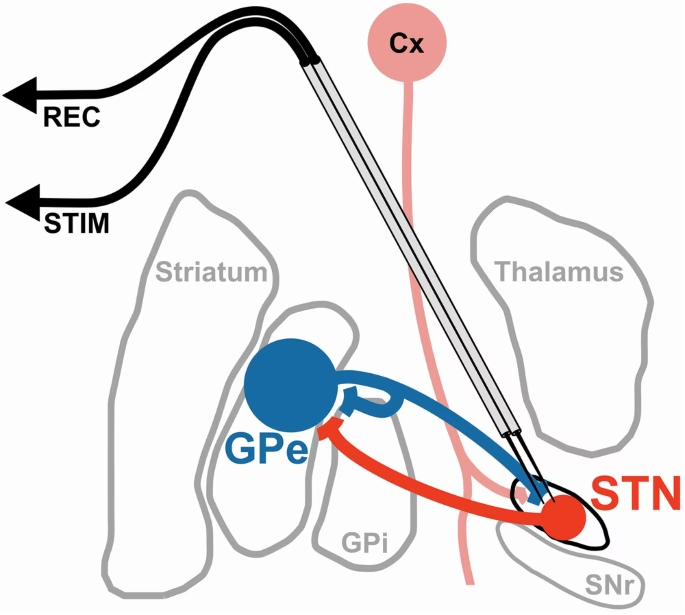
Preguntas Frecuentes sobre el NST
¿Qué significa STN en neurociencia?
STN es la abreviatura en inglés para Subthalamic Nucleus, que se traduce al español como Núcleo Subtalámico (NST).
¿Cuál es la función principal del Núcleo Subtalámico?
Aunque no se comprende completamente, se sabe que el NST es crucial en el control motor, particularmente en la inhibición del movimiento a través de las vías indirecta e hiperdirecta de los ganglios basales. También está involucrado en funciones límbicas (recompensa, motivación) y cognitivas (control de la acción, toma de decisiones).
¿Cómo se relaciona el NST con la enfermedad de Parkinson?
En la enfermedad de Parkinson, el NST se vuelve hiperactivo, contribuyendo significativamente a los síntomas motores como la rigidez, bradicinesia y temblor. Modular esta hiperactividad es el objetivo principal de tratamientos como la ECP.
¿Qué es la ECP en el NST?
La Estimulación Cerebral Profunda (ECP) en el NST es un procedimiento quirúrgico en el que se implantan electrodos en el núcleo subtalámico para administrar impulsos eléctricos que modulan su actividad anormal, aliviando principalmente los síntomas motores de la enfermedad de Parkinson.
¿Tiene efectos secundarios la ECP en el NST?
Sí, aunque es una terapia eficaz, la ECP en el NST puede tener efectos secundarios que varían entre pacientes, incluyendo impactos en funciones cognitivas, estado de ánimo (como apatía o hipomanía), aumento de peso y, en algunos casos, disfunción sexual o agresión. La ubicación exacta de la estimulación influye en los efectos.
¿Es uniforme la estructura del NST?
No, aunque inicialmente se propuso un modelo tripartito (motor, asociativo, límbico), estudios recientes sugieren que el NST tiene una organización interna más compleja, con límites difusos entre regiones y una heterogeneidad celular y molecular significativa que desafía las subdivisiones rígidas.
Comparación de Resultados en ECP del NST: Anestesia Local vs General
Estudios recientes han explorado la eficacia y seguridad de la ECP del NST realizada bajo anestesia general (AG) en comparación con la tradicional anestesia local (AL), buscando minimizar la incomodidad del paciente y los riesgos asociados al estado de vigilia. La experiencia del centro SNUH, por ejemplo, comparó retrospectivamente pacientes operados bajo AL (2005-2006) y AG (2014-2019). Los hallazgos sugieren que la AG no interfiere significativamente con la grabación de microelectrodos (MER) y que la ECP bajo AG, incluso sin estimulación intraoperatoria de prueba, puede ofrecer resultados clínicos similares o superiores, sin un aumento de complicaciones.
| Medición Clínica | Anestesia | Línea Base (Media ± DE) | 6 Meses Post-ECP (Media ± DE) | Valor p (Base vs 6 Meses) | Valor p (Cambio LA vs GA) |
|---|---|---|---|---|---|
| UPDRS Total (On Med) | General | 31.86 ± 16.96 | 24.53 ± 14.95 | 0.004* | 0.205 |
| Local | 32.87 ± 17.76 | 29.29 ± 14.19 | 0.429 | ||
| UPDRS Total (Off Med) | General | 65.93 ± 20.42 | 40.32 ± 21.42 | <0.001* | 0.120 |
| Local | 68.53 ± 20.34 | 47.26 ± 17.85 | <0.001* | ||
| UPDRS Parte III (On Med) | General | 20.83 ± 10.96 | 16.20 ± 9.46 | 0.005* | 0.696 |
| Local | 21.40 ± 12.90 | 16.67 ± 9.35 | 0.063 | ||
| UPDRS Parte III (Off Med) | General | 38.11 ± 13.96 | 21.48 ± 12.33 | <0.001* | 0.136 |
| Local | 40.42 ± 15.30 | 24.68 ± 12.51 | <0.001* | ||
| H&Y (Off Med) | General | 3.05 ± 0.82 | 2.35 ± 0.61 | <0.001* | 0.053 |
| Local | 3.24 ± 0.91 | 2.64 ± 0.72 | 0.002* | ||
| ADL (Off Med) | General | 47.44 ± 23.54 | 61.98 ± 25.58 | <0.001* | 0.500 |
| Local | 50.00 ± 22.18 | 66.92 ± 18.53 | <0.001* | ||
| Dyskinesia Disability | General | 2.72 ± 1.31 | 1.04 ± 1.27 | <0.001* | 0.062 |
| Local | 2.21 ± 1.39 | 0.79 ± 1.21 | <0.001* | ||
| LEDD (mg/día) | General | 1448.00 ± 546.93 | 483.99 ± 330.42 | <0.001* | <0.0001* |
| Local | 1031.63 ± 451.08 | 461.30 ± 284.65 | <0.001* | ||
| SF-36 Physical Health | General | 156.25 ± 72.58 | 203.14 ± 90.03 | <0.001* | 0.600 |
| Local | 132.86 ± 61.09 | 188.34 ± 74.50 | <0.001* |
Nota: * indica significancia estadística (p < 0.05). LEDD: Dosis Diaria Equivalente de Levodopa. UPDRS: Escala Unificada de Calificación de la Enfermedad de Parkinson. H&Y: Estadio de Hoehn & Yahr. ADL: Actividades de la Vida Diaria de Schwab & England. SF-36: Cuestionario de Salud SF-36. La tabla compara los cambios desde la línea base a los 6 meses post-cirugía dentro de cada grupo (Anestesia General vs Local) y si el cambio observado difiere significativamente entre los dos grupos.
Los datos del SNUH también mostraron que la ubicación del electrodo tendió a estar más consistentemente dentro del NST en el grupo de AG (76.7% bilateralmente) comparado con el grupo de AL (53.6% bilateralmente), aunque esto podría reflejar una mayor experiencia quirúrgica en años posteriores. La reducción en la dosis de medicación (LEDD) fue significativamente mayor en el grupo de AG. Estos hallazgos, junto con los de otros centros, sugieren que la ECP del NST bajo AG es una alternativa viable y potencialmente ventajosa para muchos pacientes, minimizando las molestias intraoperatorias y ofreciendo resultados clínicos comparables o mejores.
Conclusión
El núcleo subtalámico es una estructura cerebral pequeña pero de inmensa importancia, fundamental en el control motor y con roles significativos en funciones límbicas y cognitivas. Su disfunción es central en la fisiopatología de la enfermedad de Parkinson y otros trastornos neurológicos. La Estimulación Cerebral Profunda (ECP) del NST ha revolucionado el manejo de la EP avanzada y se está explorando para otras condiciones. A pesar de los éxitos terapéuticos, la compleja organización interna del NST y la heterogeneidad de sus poblaciones neuronales aún no se comprenden completamente. La investigación futura, utilizando técnicas moleculares y funcionales avanzadas, es crucial para refinar nuestra comprensión del NST en la salud y la enfermedad, lo que permitirá desarrollar terapias más precisas y personalizadas, minimizando los efectos secundarios y optimizando los resultados para los pacientes.
Si quieres conocer otros artículos parecidos a Núcleo Subtalámico: Clave en Neurociencia puedes visitar la categoría Neurociencia.