La alta incidencia de personas en situación de discapacidad motora y sensorial ha impulsado de manera significativa la investigación en el campo de las interfaces neuronales y los sistemas de comunicación máquina-cerebro. Estas tecnologías emergentes buscan establecer un puente directo entre el funcionamiento del sistema nervioso y los dispositivos técnicos, con el objetivo de restaurar funciones perdidas, mejorar la calidad de vida e incluso explorar nuevas formas de interacción entre humanos y máquinas.
El desarrollo de estas interfaces es un esfuerzo multidisciplinario que requiere la colaboración de expertos en fisiología, ciencia de los materiales, instrumentación, procesamiento de señales, inteligencia computacional, mecánica, electrónica, robótica e informática. Cada disciplina aporta conocimientos esenciales para lograr una interconexión efectiva, desde la comprensión de cómo funciona el cerebro y los nervios, hasta la creación de electrodos seguros y eficientes, la decodificación de señales neuronales complejas y el diseño de los sistemas que ejecutan las acciones deseadas.
¿Qué son las Interfaces Neuronales y los Sistemas Máquina-Cerebro?
Las interfaces neuronales se definen como sistemas de transducción bidireccionales. Esto significa que son capaces tanto de registrar la actividad bioeléctrica del sistema nervioso (capturar señales) como de aplicar corrientes eléctricas para estimular músculos o nervios (enviar señales). Su propósito fundamental es establecer un contacto directo y funcional entre el tejido neurológico y un dispositivo técnico o computador.
Estos sistemas comprenden varios componentes clave: los electrodos o sensores, que son el punto de contacto directo con el tejido nervioso; las conexiones internas (generalmente cables) que transportan las señales; las conexiones a un procesador externo o implantado; los circuitos encargados de la adquisición y digitalización de los datos; y la unidad controladora del sistema efector, que traduce las señales procesadas en acciones concretas.
Es importante distinguir, aunque a veces se usen indistintamente, que el término "interfaces neuronales" puede ser más amplio, mientras que los "sistemas máquina-cerebro" (o Brain-Computer Interfaces - BCI) a menudo se refieren específicamente a aquellos que interactúan con el cerebro, y pueden ser tanto invasivos (implantados) como no invasivos (externos, como los cascos de electroencefalografía - EEG).
El Rol Crucial de los Electrodos
Dentro de una interfaz neuronal, el electrodo es un elemento fundamental. Es el encargado de capturar las señales bioeléctricas generadas por las neuronas o de aplicar estímulos eléctricos a los tejidos vivos. La calidad y el desempeño de la interfaz dependen en gran medida de las características de estos electrodos.
Biocompatibilidad y Reacciones del Tejido
La interacción entre el electrodo y el tejido neuronal es compleja y exige una alta biocompatibilidad. Esto se refiere tanto a la biocompatibilidad de los materiales en contacto con el tejido (evitando respuestas inflamatorias, alérgicas o de rechazo) como a la biocompatibilidad estructural (diseño, tamaño, forma y superficie total del electrodo para minimizar el daño mecánico durante la inserción y las presiones sobre el tejido circundante).
La implantación de un electrodo en el cerebro inevitablemente causa daño al parénquima, microhemorragias y activa la respuesta inmune del tejido. Esto incluye la activación de la microglia y el aumento de la proliferación de astrocitos, lo que puede llevar al encapsulamiento del electrodo. Este encapsulamiento forma una capa glial alrededor del implante, lo que puede aumentar la impedancia del electrodo y disminuir la relación señal-ruido, afectando su capacidad de registro.
Las investigaciones actuales buscan modificar la superficie de los electrodos utilizando hidrogeles, polímeros o nanotubos que puedan unirse a materiales bioactivos como las neurotrofinas. Estas sustancias pueden potenciar el crecimiento de neuritas hacia el electrodo. También se exploran microtubos que liberen moléculas inhibidoras de factores proinflamatorios para reducir la respuesta del tejido.
Materiales Utilizados
La estabilidad a largo plazo de los implantes requiere que los materiales sean resistentes a la corrosión (especialmente durante la estimulación eléctrica) y al ataque de los fluidos biológicos, enzimas y macrófagos. Los materiales conductores más comunes para los electrodos son el platino, el iridio, el tungsteno y el acero inoxidable. Para el aislamiento de los electrodos, cables y circuitos electrónicos, se utilizan frecuentemente el elastómero de silicona, el politetrafluoroetileno (PTFE) y la poliimida.
Además de la estabilidad, estos materiales deben tener estabilidad electroquímica, bajo consumo de energía, impedancia y frecuencia de respuesta estables, y resistencia al ruido y otros artefactos. También es crucial un comportamiento adecuado durante y después de la polarización eléctrica.
Tipos de Electrodos Neuronales
La evolución de la tecnología ha dado lugar a una variedad de diseños de electrodos, cada uno con características y aplicaciones específicas:
- Microcables: Fueron los primeros utilizados, consisten en cables muy finos (20-50µm) de acero inoxidable o tungsteno con aislamiento. Se organizan en arreglos. Un hecho interesante es que el encapsulamiento glial que ocurre tras la inserción, al reducir el área de contacto expuesta, aumenta la impedancia a un nivel que permite registrar la actividad de neuronas individuales.
- Electrodos Penetrantes (Arrays): Desarrollados para registrar y estimular el sistema nervioso central (SNC), aunque también se usan en el periférico (SNP). Se fabrican en agujas o bloques de vidrio, silicona o poliimida, con puntos de registro dispuestos en arreglos 1D, 2D o 3D.
- Arreglo de Michigan: Caracterizado por tener múltiples puntos de registro a lo largo de cada columna. Esto aumenta la probabilidad de encontrar neuronas a diferentes profundidades corticales. El diseño estándar para implantes crónicos tiene columnas paralelas tipo daga.
- Arreglo de Utah: Con un único punto de registro en la punta de cada electrodo. Permite ubicar una gran cantidad de puntos de registro en un volumen cortical compacto. Se considera que la punta es un punto óptimo para muestrear el campo eléctrico de un potencial de acción.
- Electrodos de Nervio Periférico: Diseñados para interactuar con el SNP.
- Regenerativos: Con orificios que permiten el crecimiento de axones o fibras nerviosas en su interior, facilitando el registro y la estimulación directa sobre axones individuales o pequeños fascículos. El diseño busca un equilibrio entre el número y el diámetro de los orificios para promover la regeneración.
- Tipo Brazalete (Cuff Electrodes): Se colocan alrededor del nervio.
- Intrafasciculares (LIFE): Penetran en los fascículos nerviosos.
- Interfasciculares: Se colocan entre los fascículos.
- Epineurales: Se suturan al epineuro (la capa más externa del nervio). Son tiras longitudinales con puntos de contacto. Tienen bajo riesgo de dañar el tronco nervioso principal.
- Helicoidales: Cintas flexibles que se enrollan alrededor del nervio (circunfacentes). Se adaptan a la forma del nervio, minimizando el trauma mecánico, aunque tienen baja selectividad. Se usan en estimulación funcional del nervio vago.
- Tipo Book (Libro): Bloques de silicona con ranuras donde se colocan las raíces espinales. Contienen electrodos de platino. Se usan principalmente para controlar la función de la vejiga interrumpiendo circuitos reflejos. Son considerados voluminosos.
- Electrodos Ajustables: Buscan superar problemas como la ubicación inadecuada o la pérdida de señal por movimiento del electrodo (respiración, presión sanguínea, encogimiento cerebral). Utilizan sistemas microelectromecánicos (MEMS) para permitir el movimiento y ajuste de la posición del electrodo implantado, por ejemplo, mediante electrólisis controlada.
Interfaces Neuronales Híbridas
Representan una convergencia entre la regeneración neuronal y las prótesis. Combinan elementos sintéticos con componentes biológicos (células, sustancias neurofílicas) para mejorar la integración con el sistema nervioso huésped. Un enfoque es cultivar células sobre el implante sintético para promover conexiones sinápticas. Otro es agregar sustancias que induzcan el crecimiento de prolongaciones neuronales hacia el electrodo. El desafío principal es mantener la conexión entre las células cultivadas y el electrodo una vez implantadas.
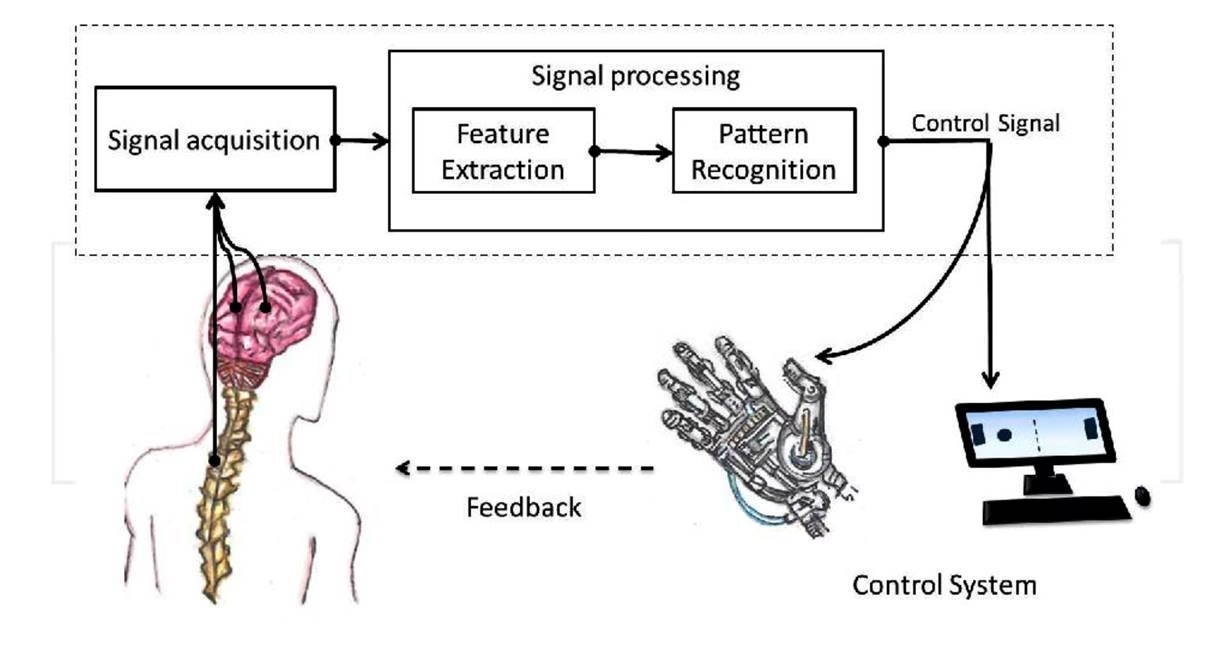
Procesamiento de la Señal Neuronal
Una vez que los electrodos capturan la actividad bioeléctrica, esta señal debe ser procesada e interpretada para ser útil. Los métodos de decodificación se dividen en dos grupos principales:
- Métodos Deductivos: Se basan en modelos que intentan comprender los mecanismos fisiológicos que generan las señales. Por ejemplo, se puede representar la actividad de una población neuronal con un vector y usar algoritmos de ajuste direccional para predecir el movimiento basándose en la tasa de descarga neuronal.
- Algoritmos Clasificadores: No requieren conocimiento previo de la relación entre la actividad neuronal y el resultado deseado. Se basan en el reconocimiento de patrones en las señales registradas, utilizando principios de inteligencia artificial y redes neuronales. Un ejemplo es el algoritmo SOFM (Self-Organizing Feature Map), que clasifica patrones de descarga neuronal y los asocia a direcciones o comandos.
En ambos casos, el procesamiento implica dos pasos principales:
Detección y Clasificación de la Señal
La señal digitalizada pasa por procesos para extraer características relevantes que codifican la intención del paciente. Esto puede incluir filtrado espacial, medición de amplitud de voltaje, análisis espectral o separación de la actividad de neuronas individuales. Las características pueden estar en el dominio del tiempo (como amplitudes de potenciales evocados o tasa de descarga) o en el dominio de la frecuencia (como amplitudes de ritmos µ o β). Es crucial que estas características no estén contaminadas por otras señales bioeléctricas como electromiografía (EMG) o electrooculografía (EOG).

Transducción de la Señal
Esta etapa traduce las características extraídas en comandos para el dispositivo efector. Se pueden usar algoritmos lineales o no lineales (como redes neuronales). Un algoritmo eficaz debe ser adaptable al usuario en varios niveles:
- Adaptación inicial a las características basales del paciente.
- Ajustes periódicos para compensar variaciones espontáneas en la actividad neuronal (hormonas, fatiga, etc.).
- Acomodación a la capacidad adaptativa del propio cerebro, permitiendo que el paciente aprenda a modificar su actividad neuronal para mejorar el control del sistema. Este ciclo cerrado de control es fundamental para la efectividad a largo plazo.
Aplicaciones de las Interfaces Neuronales
Las señales neuronales decodificadas se utilizan como señales de control para una amplia gama de aplicaciones, especialmente enfocadas en superar limitaciones motoras y sensoriales.
Interfaces Neuronales para Funciones Motoras
Estas interfaces permiten a los usuarios controlar dispositivos externos utilizando su actividad cerebral o nerviosa. Las aplicaciones varían en complejidad, desde controles ambientales simples (luz, temperatura) y comunicación a baja velocidad (escribir letras) hasta la operación de mecanismos complejos como sillas de ruedas, prótesis, ortesis, exoesqueletos, robots y cursores de computador.
Aunque para algunos pacientes con control muscular residual puede ser más práctico usar EMG o EOG (más rápidos y precisos actualmente), las interfaces neuronales son vitales para aquellos con pérdida total del control muscular o desórdenes del movimiento. Además, las señales de EEG pueden permitir el control de un mayor número de grados de libertad en comparación con las prótesis mioeléctricas.
Se ha demostrado que las neuronas motoras pueden proporcionar estimaciones fiables de las intenciones de movimiento (fuerza, dirección), lo que abre la puerta a sustituir movimientos de forma casi natural para tareas cotidianas (alcanzar, agarrar, transportar). La capacidad de controlar un cursor en 2D o 3D, incluso en entornos de realidad virtual, muestra el potencial para un control continuo y preciso. El desarrollo de controles de lazo cerrado, con retroalimentación (generalmente visual), mejora significativamente la habilidad del usuario para realizar tareas, ya que aprenden a modular su actividad neuronal.
Futuros desarrollos incluyen la telemetría para mejorar la comunicación inalámbrica, la exploración de otras áreas cerebrales para control de alto nivel y el reconocimiento de movimientos complejos como gestos para convertirlos en comandos o palabras.
Interfaces Neuronales para Funciones Sensitivas
Además de restaurar el control motor, las interfaces neuronales buscan devolver la capacidad de percibir información del entorno, permitiendo una comunicación bidireccional. Esto se logra mediante microestimulación local en las áreas sensoriales del cerebro.
Los avances más notables se han dado en la recuperación de la visión y la audición. Los implantes cocleares, que estimulan eléctricamente el nervio auditivo, han evolucionado a lo largo de varias generaciones. Las prótesis de retina, implantadas intraocularmente, utilizan electrodos para permitir a los pacientes discriminar formas y movimientos. También se investiga la estimulación de la corteza sensorial somática para sustituir el sentido del tacto, por ejemplo, permitiendo reconocer frecuencias de vibración o percibir señales de alerta.
La información sensorial también es crucial como sistema de retroalimentación para los mecanismos efectores motores, imitando la propiocepción natural. Utilizar señales de sensores naturales para regular movimientos controlados por otra interfaz neuronal es un área de investigación activa.
Interfaces Neuronales para Estimulación
Otro tipo de aplicación es la estimulación funcional, que busca modificar el comportamiento o la función cerebral/nerviosa sin la intervención de receptores cognitivos (a diferencia de la estimulación sensorial que reemplaza órganos de los sentidos).
La estimulación eléctrica se ha utilizado terapéuticamente desde los años 50. Una aplicación importante es la Estimulación Cerebral Profunda (DBS) para tratar desórdenes neurológicos como el síndrome de Parkinson, aliviando temblor, rigidez y bradicinesia mediante la estimulación del ganglio basal, específicamente el núcleo subtalámico. Aunque efectiva, la DBS puede tener contraindicaciones como impacto en la fluencia verbal, lo que impulsa el desarrollo de electrodos más precisos, quizás con microactuadores ajustables post-cirugía.
Otras aplicaciones terapéuticas incluyen DBS en pediatría para desórdenes en recién nacidos (sordera) y la posibilidad de implantar múltiples interfaces (DBS y prótesis cocleares). También se investiga la estimulación directa de neuronas en la vía auditiva residual.
La Estimulación Eléctrica Funcional (FES) aplica corrientes en nervios periféricos o porciones neuromusculares. Permite controlar el movimiento de miembros paralizados, activar funciones viscerales (vejiga, respiración), crear percepciones cutáneas, interrumpir dolor o espasmos, y facilitar la recuperación natural. Para lograr movimientos naturales complejos con FES, se necesita comprender mejor la interacción muscular y, a veces, integrar señales vestibulares. Existe una interfaz FES aprobada por la FDA para el control del agarre de la mano mediante estimulación muscular selectiva.

La estimulación directa de la médula espinal también es una opción, con electrodos implantados (a veces usando fotodiodos que convierten luz infrarroja en estímulos eléctricos). La estimulación espinal puede aumentar el tiempo antes de la fatiga muscular en comparación con la periférica, pero presenta desafíos técnicos en el posicionamiento y la estabilidad de los electrodos.
Finalmente, se están desarrollando modelos matemáticos de redes neuronales y microchips que replican la dinámica de regiones cerebrales específicas, lo que podría permitir sustituir funciones neuronales dañadas mediante la implementación de estos modelos predictivos.
Desafíos y Consideraciones Éticas
A pesar de los avances, las interfaces neuronales enfrentan limitaciones significativas. Uno de los mayores retos es la bioestabilidad y biofuncionalidad a largo plazo de los implantes. Los implantes actuales tienen una duración limitada (a veces no superior a un año de registro activo) y conllevan riesgo de reacciones infecciosas.
Esto plantea una importante cuestión ética: la utilización de pacientes en situación de discapacidad para experimentar con implantes crónicos, especialmente cuando existen opciones menos invasivas o con mejor relación costo-beneficio (como el control por EEG o EMG superficial para algunas aplicaciones). Es fundamental desarrollar arreglos de electrodos más estables y duraderos, así como implementar tecnologías telemétricas que reduzcan el riesgo de infección asociado a las conexiones externas.
Más allá de los desafíos técnicos y médicos, las interfaces neuronales plantean profundas cuestiones éticas y sociales. Tienen un potencial extraordinario para transformar la medicina y nuestra interacción con la tecnología, pero también generan preocupaciones críticas sobre la privacidad de los datos neuronales, la autonomía individual (¿quién controla la interfaz?), los derechos humanos (acceso equitativo, evitar el aumento de desigualdades) y la propia definición de lo que significa ser humano.
Existe un debate público sobre si estas tecnologías deberían usarse principalmente para restaurar funciones perdidas debido a una condición médica (lo cual tiene un fuerte apoyo) o si también deberían usarse para aumentar capacidades en personas sanas (lo cual genera más reservas). Abordar estos desafíos técnicos y éticos de manera responsable y con un amplio debate social es crucial para maximizar los beneficios y minimizar los riesgos de esta tecnología transformadora.
Preguntas Frecuentes sobre Interfaces Neuronales
¿Quiénes pueden beneficiarse de las interfaces neuronales?
Principalmente personas con discapacidades motoras o sensoriales severas, como parálisis por lesión medular, esclerosis lateral amiotrófica (ELA), síndrome de enclaustramiento, ceguera, sordera, o aquellas con desórdenes neurológicos como el Parkinson.
¿Son invasivas o no invasivas?
Existen ambos tipos. Las invasivas (implantes) se colocan dentro del cuerpo o cerebro y generalmente ofrecen una señal más fuerte y precisa. Las no invasivas (como cascos de EEG) se colocan en el exterior y son más fáciles de usar pero capturan señales con menos resolución.
¿Pueden las interfaces neuronales leer mis pensamientos?
Actualmente, las interfaces neuronales decodifican patrones de actividad eléctrica asociados a intenciones motoras simples, comandos o estados mentales específicos que el usuario aprende a modular. No leen pensamientos complejos o privados de forma libre.
¿Cuánto duran los implantes neuronales?
La estabilidad a largo plazo es un desafío importante. Los implantes actuales pueden tener una vida útil limitada para el registro activo de señales (a menudo menos de un año), aunque se investigan materiales y diseños para aumentar su durabilidad y reducir las reacciones adversas.
¿Son seguras las interfaces neuronales?
Como cualquier procedimiento médico, especialmente los invasivos, conllevan riesgos (infección, daño tisular, reacciones adversas a materiales). La investigación continua busca mejorar la seguridad y la biocompatibilidad.
Tabla Comparativa de Tipos de Electrodos
| Tipo de Electrodo | Ubicación Típica | Diseño Clave | Ventajas | Desventajas / Desafíos |
|---|---|---|---|---|
| Microcables | SNC (Corteza) | Cables finos, arreglos | Registro de neuronas individuales (con encapsulamiento) | Fragilidad, encapsulamiento que altera impedancia |
| Arreglo de Michigan | SNC (Corteza) | Múltiples puntos a lo largo de columnas | Registra a varias profundidades | Puede requerir implante penetrante |
| Arreglo de Utah | SNC (Corteza) | Punto único en la punta, alta densidad | Alta densidad de puntos de registro en volumen compacto | Posicionamiento de cables, requiere implante penetrante |
| Regenerativos | SNP (Nervios periféricos, médula espinal) | Orificios para crecimiento axonal | Acceso potencial a axones individuales o fascículos | Requiere regeneración nerviosa, equilibrio diámetro/número de orificios |
| Epineurales | SNP (Nervios periféricos) | Tiras suturadas al epineuro | Bajo riesgo de daño al tronco nervioso | Menor selectividad que intrafasciculares |
| Helicoidales (Cuff) | SNP (Nervios periféricos) | Cinta flexible enrollada alrededor del nervio | Se adapta a la forma del nervio, bajo trauma mecánico | Baja selectividad |
| Tipo Book | SNP (Raíces espinales) | Bloque con ranuras para nervios | Usado para control de funciones específicas (vejiga) | Voluminoso, requiere cirugía |
| Ajustables (MEMS) | SNC (Corteza) | Sistemas microelectromecánicos | Permite ajustar posición post-implante, mejora estabilidad | Tecnología compleja en desarrollo |
En conclusión, el campo de las interfaces neuronales es uno de los más prometedores en la neurociencia y la ingeniería biomédica. Los avances en el diseño de electrodos, el procesamiento de señal y las diversas aplicaciones están abriendo caminos para restaurar funciones vitales en personas con discapacidades severas. Sin embargo, persisten desafíos importantes relacionados con la bioestabilidad a largo plazo, la prevención de infecciones y las complejas consideraciones éticas y sociales que acompañan a una tecnología capaz de conectar directamente la mente y la máquina. La investigación continua, impulsada por la necesidad clínica y acompañada de un diálogo ético riguroso, es fundamental para realizar plenamente el potencial transformador de las interfaces neuronales.
Si quieres conocer otros artículos parecidos a Interfaces Neuronales: Conectando Mente y Máquina puedes visitar la categoría Neurociencia.
