El cerebro, una red intrincada de miles de millones de neuronas, opera mediante el delicado equilibrio entre excitación e inhibición. Mientras que las señales excitadoras impulsan a las neuronas a disparar potenciales de acción, las señales inhibidoras actúan como frenos, modulando o silenciando su actividad. Tradicionalmente, pensamos en la inhibición neuronal como un proceso que aleja el potencial de membrana del umbral de disparo, haciendo que la neurona sea menos propensa a activarse. Sin embargo, existe otro mecanismo de inhibición igualmente crucial, aunque a menudo menos conocido, que no depende necesariamente de este cambio en el potencial de membrana: la inhibición por cortocircuito.

Este tipo de inhibición, ligada principalmente a la acción del neurotransmisor GABA (ácido gamma-aminobutírico), juega un papel fundamental en la regulación fina de la actividad neuronal, influyendo en la capacidad de las neuronas para integrar información y responder adecuadamente a los estímulos.
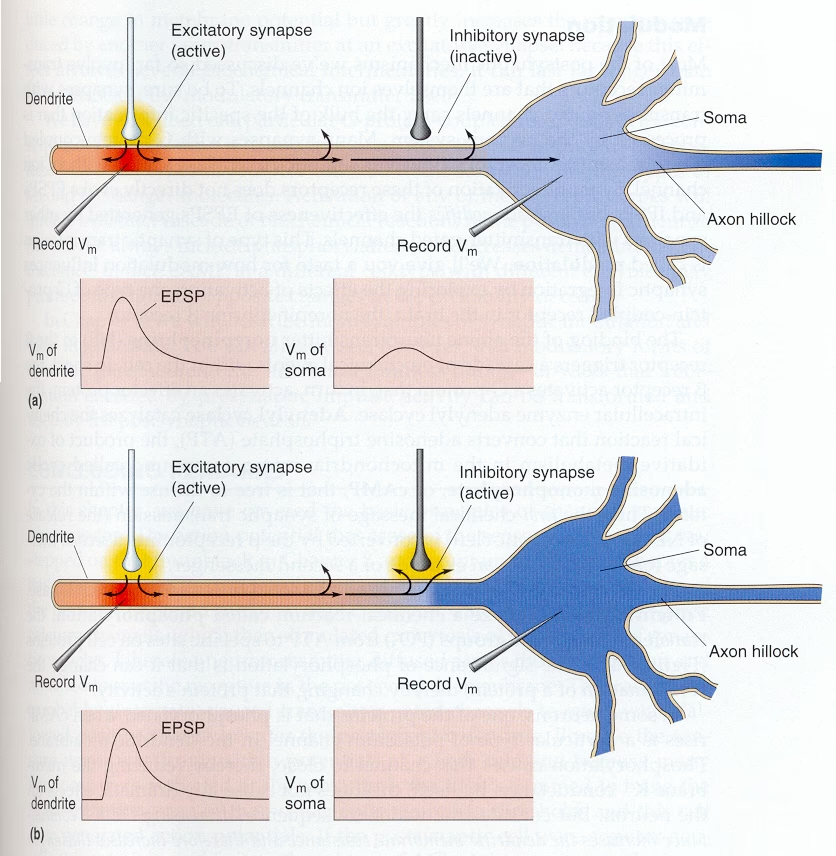
- ¿Qué es la Inhibición por Cortocircuito en Neuronas?
- Inhibición por Cortocircuito vs. Hiperpolarización: ¿Cuál es la Diferencia?
- La Importancia Crucial de los Gradientes de Cloruro y el Transportador KCC2
- Moduladores de los Receptores GABAA
- Preguntas Frecuentes (FAQs)
- Tabla Comparativa: Inhibición Hiperpolarizante vs. Inhibición por Cortocircuito
¿Qué es la Inhibición por Cortocircuito en Neuronas?
La inhibición neuronal mediada por el receptor GABAA (GABAAR) está intrínsecamente ligada al movimiento de iones cloruro (Cl⁻) a través de la membrana plasmática. Cuando el GABA se une a su receptor GABAA, este receptor, que es un canal iónico, se abre, permitiendo que los iones cloruro fluyan a través de la membrana neuronal.
Dependiendo del gradiente electroquímico del cloruro a través de la membrana, la entrada de Cl⁻ puede resultar en una hiperpolarización (el potencial de membrana se vuelve más negativo) o, en ciertas condiciones, en una despolarización (el potencial de membrana se vuelve más positivo). Sin embargo, independientemente de si hay hiperpolarización o despolarización, la apertura de estos canales de cloruro siempre aumenta la conductancia de la membrana para el cloruro. Este aumento de la conductancia se traduce en una disminución local de la resistencia de la membrana.
La inhibición por cortocircuito ocurre precisamente debido a esta caída local en la resistencia de la membrana. Imagina que la membrana neuronal es un circuito eléctrico. Cuando se abre un canal iónico, es como si se abriera un "atajo" o "cortocircuito" a través de la resistencia de la membrana. Esto hace que la corriente iónica generada por las sinapsis excitadoras cercanas se 'desvíe' o 'escape' a través de estos canales abiertos de cloruro, en lugar de propagarse eficazmente para despolarizar la membrana hacia el umbral de disparo.
Aunque no siempre cause una hiperpolarización significativa, este "cortocircuito" reduce drásticamente la capacidad de la neurona para despolarizarse en respuesta a estímulos excitadores. De esta manera, la inhibición por cortocircuito reduce la capacidad de las neuronas para producir potenciales de acción o para regenerar estos potenciales a medida que se propagan hacia los terminales sinápticos. Es un mecanismo de "fuga" de corriente que atenúa la señal excitadora entrante.
Inhibición por Cortocircuito vs. Hiperpolarización: ¿Cuál es la Diferencia?
Ambos, la inhibición por cortocircuito y la hiperpolarización, son formas de inhibición mediada por GABA y el flujo de cloruro. La diferencia principal radica en el mecanismo por el cual ejercen su efecto inhibidor y, potencialmente, en su impacto en la señalización neuronal.
- Hiperpolarización: Ocurre cuando el potencial de equilibrio del cloruro (ECl) es más negativo que el potencial de reposo de la membrana. La apertura de los canales de cloruro permite la entrada de iones Cl⁻, lo que hace que el potencial de membrana se vuelva más negativo (hiperpolarización). Este efecto aleja activamente el potencial de membrana del umbral de disparo, dificultando que la neurona se active. Se considera que tiene un efecto principalmente *sustractivo* sobre la excitación: la despolarización excitadora se "resta" de la hiperpolarización.
En resumen, mientras la hiperpolarización inhibe al alejar el potencial de membrana del umbral, la inhibición por cortocircuito inhibe al reducir la eficacia con la que las corrientes excitadoras pueden despolarizar la membrana, actuando como una fuga de corriente.
La Importancia Crucial de los Gradientes de Cloruro y el Transportador KCC2
La dirección del flujo de iones cloruro a través de los canales GABAA (y, por lo tanto, si el GABA causa hiperpolarización, despolarización o un efecto de cortocircuito puramente resistivo) depende críticamente del gradiente electroquímico del Cl⁻ a través de la membrana. Este gradiente no es estático y está regulado activamente por transportadores de iones de cloruro.
Uno de los transportadores clave es el KCC2 (transportador de K⁺/Cl⁻ tipo 2). KCC2 bombea activamente cloruro fuera de la neurona, utilizando el gradiente de potasio (K⁺) para impulsar la extrusión de Cl⁻. La actividad de KCC2 es fundamental para mantener una baja concentración intracelular de cloruro en las neuronas maduras.
El Cambio en la Acción del GABA Durante el Desarrollo
La actividad de KCC2 no es constante a lo largo de la vida de una neurona. Durante las etapas tempranas del desarrollo neural, la actividad de KCC2 es relativamente baja en las neuronas jóvenes. Esto resulta en concentraciones intracelulares de Cl⁻ más altas en comparación con las neuronas maduras. En este contexto, el potencial de equilibrio del cloruro (ECl) es menos negativo y puede estar cerca o incluso por encima del potencial de reposo.
Cuando el GABA se une a los GABAARs en estas neuronas en desarrollo, la apertura de los canales de cloruro provoca una salida de Cl⁻ (ya que la concentración intracelular es relativamente alta), lo que lleva a una despolarización de la membrana. Aunque la despolarización generalmente se considera excitadora (acerca el potencial al umbral), el GABA despolarizante en estas circunstancias aún puede ejercer acciones inhibidoras, particularmente a través de la inhibición por cortocircuito (la caída en la resistencia de la membrana atenúa las señales excitadoras).
A medida que la neurona madura, la expresión y actividad de KCC2 aumentan significativamente. Este incremento en la extrusión de cloruro reduce la concentración intracelular de Cl⁻ a niveles bajos. Como resultado, el potencial de equilibrio del cloruro (ECl) se vuelve mucho más negativo que el potencial de reposo. En las neuronas maduras, la activación de los GABAARs provoca una entrada de Cl⁻, resultando en una hiperpolarización de la membrana, el modo de inhibición más comúnmente asociado con el GABA en el cerebro adulto.
Este cambio en la polaridad de la respuesta al GABA, de despolarizante a hiperpolarizante, mediado por la maduración de la actividad de KCC2, es un evento crítico durante el desarrollo cerebral. El GABA despolarizante temprano tiene funciones importantes en la morfogénesis y maduración del cerebro, regulando aspectos como la proliferación de células madre neurales, la migración neuronal y la diferenciación. Estos efectos de desarrollo del GABA despolarizante se cree que están mediados por la activación de canales de calcio dependientes de voltaje, lo que lleva a la activación de vías de segundos mensajeros dependientes de calcio.
La regulación de la actividad de KCC2 a nivel postraduccional (por ejemplo, mediante fosforilación y desfosforilación) permite que las células neuronales en desarrollo ejecuten programas celulares apropiados en el momento justo en respuesta a las señales de desarrollo, influyendo en la polaridad del GABA y las cascadas de señalización asociadas.
Implicaciones Patológicas de los Gradientes de Cloruro
La plasticidad de los gradientes de cloruro no solo es importante durante el desarrollo, sino también en condiciones fisiológicas y patológicas. La destrucción o disfunción de estos gradientes, a menudo asociada con una actividad reducida de KCC2 (hipofunción de KCC2), puede contribuir a estados de hiperexcitabilidad neuronal. En estas condiciones, el aumento de Cl⁻ intracelular puede hacer que el GABA se vuelva despolarizante o incluso francamente excitador en neuronas maduras, perdiendo su capacidad inhibidora efectiva.
Esta inversión o debilitamiento de la inhibición mediada por GABA parece contribuir a varias neuropatologías hiperexcitables, como la epilepsia o el dolor neuropático. Comprender los mecanismos que regulan los gradientes de cloruro y la actividad de KCC2 es crucial para desarrollar posibles estrategias terapéuticas dirigidas a restaurar la inhibición adecuada en estos trastornos.
Moduladores de los Receptores GABAA
Los receptores GABAA son sitios importantes para la modulación por diversas sustancias. La unión de estos compuestos a los GABAARs puede alterar la función del canal iónico, influyendo en la magnitud de la inhibición (tanto hiperpolarizante como por cortocircuito).
- Moduladores Endógenos: Incluyen sustancias producidas naturalmente por el cuerpo, como las endozepinas y los neuroesteroides (por ejemplo, la alopregnanolona).
La acción de estos moduladores resalta la importancia terapéutica de la vía GABAérgica en la regulación de la excitabilidad neuronal.
Preguntas Frecuentes (FAQs)
¿La inhibición por cortocircuito es lo mismo que la hiperpolarización?
No exactamente. Ambas son formas de inhibición mediada por canales de cloruro activados por GABA, pero difieren en su mecanismo principal. La hiperpolarización implica un cambio en el potencial de membrana hacia un valor más negativo. La inhibición por cortocircuito implica una reducción de la resistencia de la membrana que atenúa las corrientes excitadoras, independientemente de un cambio significativo en el potencial de membrana, aunque a menudo coexisten o uno puede predominar dependiendo del gradiente de cloruro.
¿Puede el GABA ser excitador?
Sí, bajo ciertas condiciones. Si la concentración intracelular de cloruro es lo suficientemente alta (por ejemplo, en neuronas inmaduras o en ciertas patologías), la activación de los GABAARs puede provocar una salida de cloruro, resultando en una despolarización. Aunque esta despolarización puede ser excitadora en sí misma, incluso el GABA despolarizante puede ejercer efectos inhibidores a través de la inhibición por cortocircuito.
¿Qué papel juega el transportador KCC2?
KCC2 es crucial para establecer y mantener el gradiente de cloruro en las neuronas. Bombea activamente cloruro fuera de la célula. Su actividad determina la concentración intracelular de cloruro y, por lo tanto, si la activación de los GABAARs resultará en una entrada de cloruro (hiperpolarización en neuronas maduras) o una salida de cloruro (despolarización en neuronas inmaduras o patológicas).
¿Cómo contribuye la inhibición por cortocircuito a la función neuronal?
Al reducir la resistencia de la membrana, la inhibición por cortocircuito limita la capacidad de las corrientes excitadoras para despolarizar la neurona. Esto ayuda a regular la integración de las señales sinápticas, a controlar la temporalidad de los disparos neuronales y a prevenir la sobreexcitación, aunque su papel exacto en mecanismos como el control de ganancia sigue siendo objeto de investigación.
¿Por qué es importante estudiar los gradientes de cloruro?
Los gradientes de cloruro son dinámicos y su correcta regulación es vital para la función neuronal normal, tanto durante el desarrollo como en la edad adulta. La disfunción en la regulación del cloruro puede llevar a una alteración de la inhibición mediada por GABA, contribuyendo a trastornos neurológicos caracterizados por hiperexcitabilidad, como la epilepsia o el dolor neuropático.
Tabla Comparativa: Inhibición Hiperpolarizante vs. Inhibición por Cortocircuito
| Característica | Inhibición Hiperpolarizante | Inhibición por Cortocircuito |
|---|---|---|
| Mecanismo Principal | Cambio en el potencial de membrana (se vuelve más negativo) | Disminución de la resistencia de la membrana |
| Flujo de Cloruro (en neuronas maduras) | Entrada de Cl⁻ (si ECl < Potencial de Reposo) | Entrada de Cl⁻ (si ECl < Potencial de Reposo), pero el efecto clave es la fuga de corriente |
| Efecto sobre el Potencial de Membrana | Aleja el potencial del umbral de disparo | Puede o no cambiar significativamente el potencial de membrana; suprime la despolarización excitadora |
| Impacto en la Excitación | Efecto principalmente sustractivo sobre la despolarización excitadora | Atenúa la despolarización excitadora permitiendo fuga de corriente; debatido si tiene efecto divisor o sustractivo en la tasa de disparo |
| Dependencia del Gradiente de Cl⁻ | Alta (determina la dirección del flujo y la magnitud de la hiperpolarización) | Alta (la apertura del canal depende del gradiente, aunque el efecto resistivo ocurre independientemente de la dirección del flujo neto si el canal se abre) |
| Prevalencia (GABA en neuronas maduras) | Predominante (debido a baja [Cl⁻]ᵢ por KCC2) | Presente y coexiste con hiperpolarización; importante para la atenuación de señales |
La inhibición por cortocircuito es un componente esencial del repertorio de mecanismos inhibidores de las neuronas, actuando de manera complementaria a la hiperpolarización para modular la excitabilidad. Su comprensión es vital no solo para desentrañar el funcionamiento básico de los circuitos neuronales, sino también para identificar posibles dianas terapéuticas en trastornos donde el equilibrio entre excitación e inhibición se ha perdido.
Si quieres conocer otros artículos parecidos a La Inhibición por Cortocircuito Neuronal puedes visitar la categoría Neurociencia.

