La neurociencia busca incansablemente comprender cómo los circuitos neuronales y las células individuales dan forma a nuestros pensamientos, emociones y comportamientos. Para desentrañar estos misterios, los investigadores necesitan herramientas que les permitan observar la actividad cerebral en tiempo real y en animales que se comportan de forma natural. Una de estas herramientas, que ha ganado una popularidad significativa en los últimos años, es la fotometría de fibra.
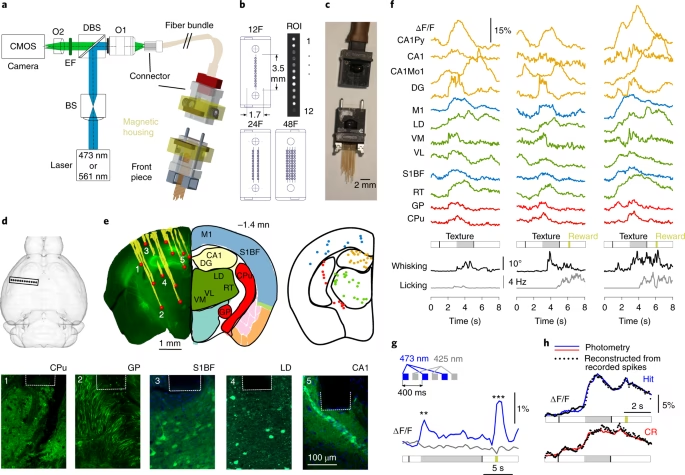
Esta técnica se ha convertido en un pilar fundamental para caracterizar las relaciones entre el cerebro y el comportamiento in vivo. Inicialmente, su uso principal se centró en registrar la dinámica del calcio, que sirve como indicador indirecto de la actividad neuronal, utilizando indicadores codificados genéticamente. Esto abrió nuevas vías de investigación y generó conocimientos profundos sobre funciones cerebrales como el movimiento, la memoria y la motivación, permitiendo estudiar estos procesos a nivel de circuitos definidos y tipos celulares específicos.
Recientemente, el potencial de descubrimiento con la fotometría de fibra se ha expandido enormemente. El desarrollo de una amplia gama de sensores fluorescentes para biomoléculas, incluyendo neuromoduladores y péptidos que antes eran difíciles de estudiar in vivo, ha sido un avance crítico. Esta innovación, combinada con la disponibilidad de sistemas de registro más asequibles y fáciles de usar ('plug-and-play'), ha hecho que el monitoreo de moléculas con alta precisión espacio-temporal durante el comportamiento sea mucho más accesible para laboratorios de todo el mundo. Sin embargo, esta rápida expansión en las aplicaciones de la fotometría de fibra también ha planteado desafíos, ya que ha ocurrido sin una coordinación o consenso sobre las mejores prácticas. Este artículo busca servir como una guía completa para entender qué es la fotometría de fibra y cómo funciona.
- ¿Qué es y Cómo Funciona la Fotometría de Fibra?
- Más Allá del Calcio: Sensores de Neuromoduladores
- Ventajas y Limitaciones de la Fotometría de Fibra
- Integración con Otras Herramientas Neurocientíficas
- Fotometría de Fibra vs. Otras Técnicas de Imagen de Calcio
- Preguntas Frecuentes (FAQ)
- ¿Es la fotometría de fibra lo mismo que la optogenética?
- ¿Qué tipo de señal registra la fotometría de fibra?
- ¿Cuál es la principal limitación de la fotometría de fibra?
- ¿Se puede usar fotometría de fibra para estudiar neurotransmisores?
- ¿Cómo se corrigen los artefactos de movimiento en la fotometría de fibra?
- ¿Qué diferencia hay entre fotometría y espectroscopia en neurociencia?
- Conclusión
¿Qué es y Cómo Funciona la Fotometría de Fibra?
En esencia, la fotometría de fibra es una técnica óptica utilizada en neurociencia para medir la actividad promedio de una población de neuronas o células gliales dentro de una región cerebral específica en animales vivos. A diferencia de otras técnicas que pueden resolver la actividad de neuronas individuales, la fotometría de fibra registra una señal agregada, o 'bulk', de la fluorescencia emitida por un grupo de células modificadas genéticamente.
La técnica se basa en el uso de indicadores fluorescentes codificados genéticamente. Estos indicadores son proteínas que se expresan en las células de interés y cambian su intensidad de fluorescencia en respuesta a cambios en la concentración de iones específicos (como el calcio) o la presencia de ciertas moléculas (como neurotransmisores). El indicador más comúnmente utilizado históricamente ha sido GCaMP, un indicador de calcio codificado genéticamente (GECI).
Para implementar la fotometría de fibra, primero se debe introducir el gen que codifica el indicador fluorescente en las células objetivo. Esto generalmente se logra de dos maneras:
1. Vectores Virales Adenoasociados (AAV): Se inyecta un virus modificado que contiene el gen del indicador en la región cerebral de interés. Estos virus pueden diseñarse para infectar tipos celulares específicos utilizando promotores selectivos, como CaMKII para neuronas excitadoras o GFAP para astrocitos. Esto permite registrar la actividad de una subpoblación genéticamente definida de células.
2. Líneas de Roedores Transgénicos: Se utilizan animales que han sido modificados genéticamente para expresar el indicador fluorescente en todo el cerebro o en tipos celulares específicos desde el desarrollo. La expresión puede variar entre regiones cerebrales dependiendo de la cepa.
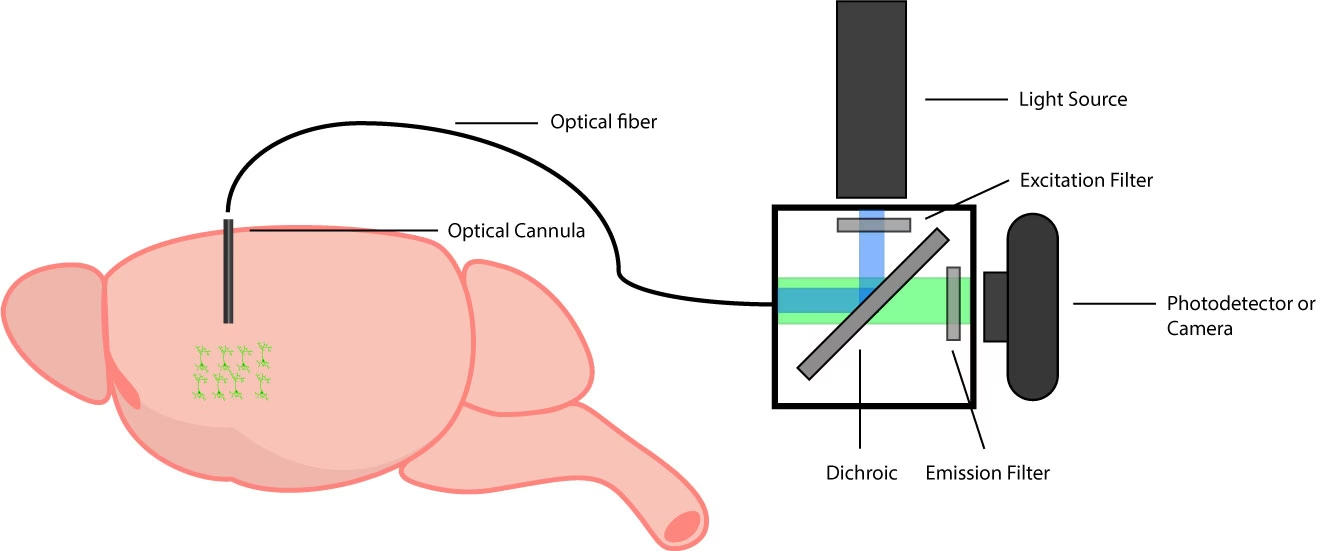
Una vez que las células expresan el indicador, se implanta quirúrgicamente una fibra óptica delgada (cannula óptica) en la región cerebral donde se encuentra el indicador. Esta fibra sirve como guía de luz. Desde una fuente de luz externa (generalmente LEDs), se envía luz de excitación a través de la fibra hacia el tejido cerebral. El indicador fluorescente en las células absorbe esta luz y, si está unido a la molécula de interés (por ejemplo, calcio), emite luz fluorescente de una longitud de onda diferente.
Esta luz de emisión viaja de regreso a través de la misma fibra óptica o una fibra cercana. Un sistema óptico externo, que incluye espejos dicróicos y filtros de emisión, separa la luz de excitación de la luz de emisión. La luz de emisión detectada por un dispositivo de registro, como un fotodetector o un tubo fotomultiplicador (PMT), que convierte la señal luminosa en una señal eléctrica que puede ser registrada y analizada a lo largo del tiempo.
Un aspecto técnico crucial, especialmente con los indicadores de calcio como GCaMP, es el uso de una señal isobéstica. GCaMP tiene dos estados funcionales (unido y no unido a calcio) con espectros de excitación y emisión ligeramente diferentes. La longitud de onda isobéstica (aproximadamente 405-415 nm para GCaMP) es aquella donde la absorción es la misma independientemente de si el calcio está unido o no. Al excitar el indicador con dos longitudes de onda (una sensible al calcio, ~470 nm, y la isobéstica), se obtiene una señal dependiente del calcio y una señal independiente del calcio. La señal independiente del calcio (isobéstica) refleja cambios en la fluorescencia debidos a artefactos de movimiento del animal o autofluorescencia del tejido, no a la actividad celular real. Restando o regresando esta señal de la señal dependiente del calcio, se puede obtener un cambio de fluorescencia más preciso que refleje la actividad celular ('bulk').
La luz de emisión de GCaMP es típicamente de ~525 nm (verde), la cual es detectada y correlacionada con el comportamiento del animal.
Más Allá del Calcio: Sensores de Neuromoduladores
Si bien los GECIs fueron la aplicación inicial y más común, el campo ha experimentado una explosión de nuevos sensores fluorescentes. Ahora existen indicadores genéticamente codificados para una amplia gama de biomoléculas, incluyendo neurotransmisores (como dopamina, serotonina, glutamato), péptidos, iones (como zinc, cloruro) e incluso cambios de pH. Esto ha abierto la puerta a estudiar la liberación y dinámica de estas moléculas en tiempo real durante el comportamiento, algo que antes era extremadamente desafiante.
La capacidad de usar múltiples sensores fluorescentes con diferentes colores (por ejemplo, un indicador verde y uno rojo) permite a los investigadores registrar simultáneamente la actividad de dos poblaciones celulares diferentes en la misma región cerebral, o incluso la dinámica de calcio en un tipo celular y la liberación de un neurotransmisor en otro. Esto se conoce como fotometría de fibra de doble color o múltiples colores, y requiere el uso de indicadores con espectros de excitación y emisión distintos, junto con el equipo óptico adecuado para separar y detectar las diferentes señales.

Ventajas y Limitaciones de la Fotometría de Fibra
Como cualquier técnica científica, la fotometría de fibra tiene sus pros y sus contras que deben considerarse al planificar experimentos.
Beneficios Clave:
- Bajo Costo y Accesibilidad: Comparada con técnicas de imagen de alta resolución como la microscopía de dos fotones, la fotometría de fibra es generalmente menos costosa de implementar y mantener, lo que reduce la barrera de entrada para muchos laboratorios.
- Simplicidad Quirúrgica y Menos Invasiva: La implantación de la fibra óptica es relativamente sencilla y menos invasiva que la implantación de lentes GRIN o ventanas craneales necesarias para otras técnicas de imagen.
- Ideal para Estudios Longitudinales: La implantación de la fibra es bien tolerada por los animales, lo que permite registrar la actividad cerebral durante períodos prolongados a lo largo de días o semanas, facilitando estudios longitudinales y de aprendizaje.
- Permite Comportamientos Naturales: El peso de la fibra conectada es significativamente menor que el de un miniscopio, lo que permite que el animal se mueva de manera más libre y natural durante las tareas conductuales, especialmente en roedores más grandes.
- Versatilidad: Se puede utilizar para registrar actividad tanto en estructuras cerebrales superficiales como profundas.
- Compatibilidad con Otras Técnicas: Es relativamente fácil combinar la fotometría de fibra con otras herramientas neurocientíficas, como la optogenética, la electrofisiología y la administración de fármacos.
Limitaciones Importantes:
- Baja Resolución Espacial y Celular: La principal limitación es que la fotometría de fibra registra una señal promedio de una población de células dentro del campo de visión de la fibra. No permite resolver la actividad de neuronas individuales ni identificar la ubicación precisa de la actividad dentro de la población.
- Animal Tethered: Aunque permite más movimiento que las técnicas con cabeza fija, el animal debe estar conectado a un cable de fibra óptica, lo que puede limitar ligeramente la gama completa de comportamientos naturales, especialmente en animales pequeños como ratones.
- Artefactos de Movimiento: Aunque el uso de la señal isobéstica ayuda, los movimientos del animal pueden generar artefactos en la señal fluorescente que deben ser cuidadosamente manejados durante el análisis.
- Problemas con la Integración Optogenética: La combinación simultánea de fotometría de fibra y optogenética puede ser compleja debido a la posible superposición de los espectros de excitación de los indicadores fluorescentes y las proteínas optogenéticas (ej. GCaMP y Channelrhodopsin-2, ambos excitados por luz azul). Esto requiere una cuidadosa selección de los indicadores y herramientas optogenéticas o el uso de estrategias experimentales específicas para evitar la contaminación de la señal.
Integración con Otras Herramientas Neurocientíficas
Una de las grandes fortalezas de la fotometría de fibra es su capacidad para combinarse con otras técnicas, permitiendo a los investigadores abordar preguntas más complejas.
La integración con la optogenética o los DREADDs (Designer Receptors Exclusively Activated by Designer Drugs) es particularmente poderosa. Mientras que la fotometría de fibra mide la actividad neuronal, la optogenética y los DREADDs permiten manipularla con alta precisión temporal (optogenética) o farmacológica (DREADDs). Al combinar ambas, se puede registrar la actividad neuronal mientras se estimula o inhibe una población celular específica, estableciendo así vínculos causales entre la actividad de un circuito y un comportamiento observado. Sin embargo, como se mencionó, la superposición de espectros de luz entre algunos indicadores de calcio y proteínas optogenéticas requiere el uso de combinaciones con espectros no solapados (por ejemplo, un indicador de calcio verde como GCaMP con una proteína optogenética excitada por luz roja como Crimson, o un indicador de calcio rojo como RCaMP con una proteína optogenética azul como Channelrhodopsin-2).
La combinación con la electrofisiología in vivo también es valiosa. La electrofisiología registra los potenciales de acción (picos eléctricos) de las neuronas con una resolución temporal muy alta. Al registrar simultáneamente la señal de calcio (fotometría) y la actividad eléctrica (electrofisiología) de una población celular o incluso de células individuales (si es posible), se puede obtener una imagen más completa de la dinámica neuronal, correlacionando los cambios lentos en la concentración de calcio con los eventos eléctricos rápidos.
Fotometría de Fibra vs. Otras Técnicas de Imagen de Calcio
Es útil comparar la fotometría de fibra con otras técnicas populares para la imagen de calcio in vivo:
| Característica | Fotometría de Fibra | Miniscopios (Imagen de un fotón) | Microscopía de Dos Fotones |
|---|---|---|---|
| Resolución Espacial/Celular | Baja (Señal 'bulk'/poblacional) | Alta (Neuronas individuales) | Muy Alta (Neuronas, dendritas, axones) |
| Invasividad Quirúrgica | Moderada (Fibra implantada) | Mayor (Lente GRIN/Ventana craneal + Microscopio montado en cabeza) | Variable (Puede requerir ventana, animal fijo o lente GRIN) |
| Comportamiento Animal | Relativamente Libre (Tethered) | Relativamente Libre (Microscopio ligero) | Generalmente Fijo la Cabeza (Limita comportamiento natural) |
| Profundidad de Imagen | Profunda y Superficial (Depende de la fibra) | Profunda y Superficial (Depende de lente/ventana) | Profunda (Hasta ~700 micras sin óptica adicional) |
| Peso/Estrés para el Animal | Bajo | Moderado (Peso del miniscopio) | Ninguno (Cabeza fija, si aplica) |
| Costo Inicial | Moderado | Moderado a Alto | Muy Alto |
| Aplicaciones Típicas | Dinámica de población, neurotransmisores, estudios longitudinales sencillos, integración con optogenética/electrofisiología. | Registro de cientos de neuronas individuales en áreas superficiales/profundas, estudios longitudinales detallados. | Imagen de alta resolución de estructuras subcelulares, estudios detallados en áreas superficiales o con ópticas especiales. |
Como se ve en la tabla, la fotometría de fibra se destaca en su equilibrio entre la capacidad de registrar la actividad in vivo, la accesibilidad y la flexibilidad para integrarse con otras manipulaciones, aunque sacrifica la resolución a nivel de neurona individual que ofrecen los miniscopios o la microscopía de dos fotones.
Preguntas Frecuentes (FAQ)
¿Es la fotometría de fibra lo mismo que la optogenética?
No, no son lo mismo, aunque a menudo se usan juntas. La fotometría de fibra es una técnica para medir la actividad neuronal (generalmente a través de indicadores de calcio o neurotransmisores). La optogenética es una técnica para manipular la actividad neuronal (activando o inhibiendo células con luz). Ambas utilizan fibras ópticas implantadas en el cerebro, lo que facilita su combinación en un mismo experimento, permitiendo a los investigadores medir lo que sucede en el cerebro mientras lo están controlando.

¿Qué tipo de señal registra la fotometría de fibra?
La fotometría de fibra registra una señal de fluorescencia que representa el cambio promedio ('bulk') en la concentración del indicador dentro del volumen de tejido iluminado por la fibra óptica. Para los indicadores de calcio, esto refleja la actividad agregada de la población neuronal o glial. Para los sensores de neurotransmisores, refleja la dinámica de liberación y reabsorción de esa molécula en el espacio extracelular.
¿Cuál es la principal limitación de la fotometría de fibra?
La principal limitación es su baja resolución espacial y celular. No permite distinguir la actividad de neuronas individuales dentro de la población registrada, solo proporciona un promedio de la actividad de todas las células que expresan el indicador y están dentro del campo de visión de la fibra.
¿Se puede usar fotometría de fibra para estudiar neurotransmisores?
Sí, absolutamente. Gracias al desarrollo reciente de sensores fluorescentes genéticamente codificados para neurotransmisores (como dopamina, serotonina, etc.), la fotometría de fibra se utiliza cada vez más para registrar la dinámica de estos neuromoduladores en tiempo real durante el comportamiento.
¿Cómo se corrigen los artefactos de movimiento en la fotometría de fibra?
Una técnica común es utilizar una señal de referencia independiente de la actividad celular, como la señal isobéstica del indicador (ej. excitando GCaMP con luz de 405/415 nm además de 470 nm). La señal isobéstica refleja principalmente cambios debidos al movimiento o autofluorescencia. Restando o regresando esta señal de la señal dependiente de la actividad (ej. GCaMP excitado con 470 nm), se pueden reducir significativamente los artefactos de movimiento.
¿Qué diferencia hay entre fotometría y espectroscopia en neurociencia?
Son técnicas fundamentalmente distintas. La fotometría (en este contexto, fotometría de fibra) mide la intensidad de la luz emitida por indicadores fluorescentes para inferir la actividad celular o la concentración de moléculas específicas. La espectroscopia (como la Espectroscopia por Resonancia Magnética, MRS) es una técnica no invasiva que mide la composición química de un tejido (niveles de metabolitos) analizando los espectros de resonancia de los núcleos atómicos en un campo magnético fuerte. Mientras que la fotometría de fibra mide la dinámica rápida asociada con la actividad neuronal o la liberación de neurotransmisores, la espectroscopia por resonancia magnética proporciona información sobre el metabolismo y la química del tejido, generalmente con una resolución temporal mucho menor.
Conclusión
La fotometría de fibra ha revolucionado la capacidad de los neurocientíficos para estudiar la actividad cerebral en animales que se comportan libremente. Su combinación de accesibilidad, relativa simplicidad y versatilidad, especialmente con la aparición de nuevos sensores para una amplia gama de biomoléculas, la ha convertido en una herramienta indispensable en muchos laboratorios. Aunque tiene limitaciones, particularmente en cuanto a resolución espacial y celular, su capacidad para integrarse con técnicas de manipulación como la optogenética y para registrar dinámicas de población y neuromoduladores la posiciona como una técnica poderosa para desentrañar los complejos circuitos que subyacen al comportamiento.
Si quieres conocer otros artículos parecidos a Fotometría de Fibra: Ventana a la Actividad Neuronal puedes visitar la categoría Neurociencia.
