El campo de la optogenética representa una convergencia fascinante entre la óptica y la ingeniería genética, ofreciendo la capacidad sin precedentes de medir y manipular células, particularmente neuronas, y los procesos biomoleculares que rigen su funcionamiento. Las herramientas y tecnologías desarrolladas bajo este paraguas científico utilizan la luz para detectar, medir y controlar señales moleculares y células individuales o poblaciones, con el objetivo fundamental de comprender sus funciones en circuitos complejos como el cerebro.
Imagina poder activar o silenciar tipos específicos de neuronas simplemente encendiendo una luz. Esto ya no es ciencia ficción, sino la realidad que permite la optogenética. Esta técnica ha transformado radicalmente la forma en que estudiamos el sistema nervioso, permitiendo a los investigadores investigar las bases neuronales del comportamiento y las enfermedades con una resolución espacial y temporal nunca antes vista.
- ¿Qué son las Herramientas Optogenéticas?
- Actuadores Optogenéticos: Osinas Microbianas
- Interruptores Ópticos
- Planificando un Experimento de Optogenética
- Tabla Comparativa de Osinas Microbianas Comunes
- Preguntas Frecuentes sobre Herramientas Optogenéticas
- ¿Qué es la optogenética en términos sencillos?
- ¿Cómo funcionan las opsinas microbianas?
- ¿Cuál es la diferencia entre una herramienta optogenética excitatoria e inhibitoria?
- ¿Qué colores de luz se utilizan en optogenética?
- ¿Se pueden usar varias herramientas optogenéticas al mismo tiempo?
- ¿Cómo se introducen estas herramientas en las neuronas?
- ¿Para qué se utiliza la optogenética en la investigación?
- Conclusión
¿Qué son las Herramientas Optogenéticas?
En esencia, las herramientas optogenéticas son moléculas de origen genético que, al ser expresadas en células objetivo, confieren a estas la capacidad de responder a la luz. Esta respuesta puede ser de diversa naturaleza, como cambios en el potencial de membrana, la liberación de neurotransmisores o la activación de cascadas de señalización intracelular. La clave reside en la capacidad de dirigir la expresión de estas herramientas a poblaciones celulares específicas, a menudo utilizando técnicas de ingeniería genética o sistemas de entrega viral dirigidos.
Las herramientas optogenéticas se pueden clasificar ampliamente en dos grupos principales en función de su función:
- Actuadores: Son herramientas codificadas genéticamente que permiten el control de proteínas o la actividad celular activada por la luz. Ejemplos prominentes incluyen las opsinas microbianas y los interruptores ópticos. Su función principal es modificar el estado eléctrico o bioquímico de la célula.
- Sensores: Son reporteros codificados genéticamente que informan sobre señales moleculares dentro de la célula, activándose también por la luz o emitiendo luz en respuesta a la señal. Un ejemplo común son los indicadores de calcio genéticamente codificados. Aunque cruciales, en este artículo nos centraremos en los actuadores, que son las herramientas que permiten la manipulación directa de la actividad neuronal.
Actuadores Optogenéticos: Osinas Microbianas
Las opsinas son quizás las herramientas optogenéticas más conocidas y utilizadas. Se trata de canales iónicos o bombas activadas por la luz que absorben fotones en longitudes de onda específicas. Tras la activación luminosa, estas proteínas cambian su conformación, abriéndose o cerrándose para permitir o bloquear el flujo de iones a través de la membrana celular.
Existen diversas opsinas microbianas que se encuentran naturalmente en organismos como algas o bacterias. Estas opsinas responden a diferentes colores de luz (por ejemplo, azul, amarillo, verde) e inician respuestas electroquímicas variadas, como la entrada inespecífica de cationes (que despolariza y excita la neurona) o la salida de protones o entrada de cloruro (que hiperpolariza e inhibe la neurona).
La ingeniería genética ha jugado un papel fundamental en la mejora de estas opsinas naturales. Mediante mutaciones puntuales, optimización de codones o la adición de señales de tráfico celular, los investigadores han logrado modificar su espectro de absorción, aumentar su conductancia, acelerar su cinética o mejorar su localización en la membrana plasmática. Esto ha dado lugar a una vasta biblioteca de variantes de opsinas, cada una con propiedades únicas adaptadas a distintos experimentos.
La posibilidad de expresar estas opsinas en subconjuntos específicos de neuronas permite un control espacio-temporal extraordinariamente preciso de su actividad. Al encender y apagar una fuente de luz, se puede activar o silenciar la población neuronal deseada con una resolución de milisegundos.
La aplicación de las opsinas microbianas ha sido fundamental en el estudio de la fisiología del cerebro y el sistema nervioso. Han permitido mapear circuitos neuronales, comprender las bases de comportamientos complejos en organismos modelo como ratones, peces cebra o Drosophila, e investigar las causas y posibles tratamientos de trastornos neurológicos como la enfermedad de Parkinson, la depresión o la adicción a drogas.
Channelrhodopsinas (ChR)
Las Channelrhodopsinas son herramientas optogenéticas fundacionales, descubiertas originalmente en el alga verde Chlamydomonas reinhardtii. Típicamente, permiten una rápida despolarización de las neuronas al exponerlas a la luz, actuando como canales iónicos directos. La Channelrhodopsina-1 (ChR1) se activa con luz azul y permite la entrada inespecífica de cationes. La Channelrhodopsina-2 (ChR2) fue la primera herramienta optogenética ampliamente adoptada. También se activa con luz azul y permite la entrada de cationes. ChR2 es preferida sobre ChR1 por su mayor conductancia a pH fisiológico y su mejor tráfico a la membrana.
Variantes Excitatorias (Despolarizantes) de ChR
El arsenal optogenético se ha expandido significativamente mediante la identificación de nuevas ChRs en otras especies de algas y el desarrollo de variantes sintéticas para mejorar la funcionalidad de ChR. Ejemplos de ChRs de otras especies incluyen CsChR (de Chloromonas subdivisa), CoChR (de Chloromonas oogama) y SdChR (de Scherffelia dubia).
Se han creado variantes sintéticas mediante mutaciones puntuales, optimización de codones y fusiones quiméricas de dominios de dos ChRs diferentes. Estas variantes siguen funcionando como canales catiónicos activados por la luz, resultando en la excitación (despolarización) de la neurona. Las mejoras incluyen:
- Mayor amplitud de fotocorriente: Ejemplos: ChR2(H134R), C1V1(t/t), ChIEF.
- Cinética de canal (encendido/apagado) más rápida: Ejemplos: ChETA, C1V1(t/t), ChrimsonR.
- Espectros de acción de pico desplazados al rojo: Ejemplos: VChR1, C1V1(t/t), Chrimson, ChrimsonR, Chronos.
Variantes Inhibitorias (Hiperpolarizantes) de ChR
Alternativamente, se han creado e identificado en otras especies variantes de ChR que inhiben las neuronas. Estas actúan como canales de cloruro activados por la luz, resultando en la hiperpolarización de las neuronas. Ejemplos de variantes de canales aniónicos de otras especies incluyen GtACR1 y GtACR2 (de la criptófita Guillardia theta).
Otras mejoras en estas variantes inhibitorias incluyen:
- Mayor amplitud de fotocorriente: Ejemplos: iChloC, SwiChRca, Phobos, Aurora.
Halorhodopsinas (NpHR)
Las Halorhodopsinas son bombas de cloruro hacia adentro activadas por la luz, aisladas de halobacterias. La halorhodopsina de tipo salvaje, conocida como NpHR (de Natronomonas pharaoni), causa hiperpolarización (inhibición) de la célula cuando se activa con luz amarilla, inhibiendo así la función de la neurona.
Variantes de NpHR
Se han diseñado variantes con mejoras como:
- Optimización de codones humanos: Ejemplo: Halo.
- Mayor amplitud de fotocorriente: Ejemplos: eNpHR, eNpHR2.0, eNpHR3.0.
- Espectros de acción de pico desplazados al rojo: Ejemplo: Jaws.
Archaerhodopsinas (Arch)
La Archaerhodopsina-3 (Arch) de Halorubrum sodomense también se utiliza comúnmente para inhibir neuronas en experimentos optogenéticos. Arch es una bomba de protones hacia afuera activada por la luz que hiperpolariza (inhibe) la célula cuando se activa con luz verde-amarilla.
Variantes de Arch
Se han desarrollado variantes de Arch con las siguientes mejoras:
- Mayor sensibilidad a la luz: Ejemplo: ArchT.
- Mayor amplitud de fotocorriente: Ejemplos: eArch3.0, eArchT3.0.
Rhodopsina de Leptosphaeria (Mac)
La rhodopsina de Leptosphaeria maculans (Mac) es una bomba de protones hacia afuera activada por luz azul-verde, derivada del hongo Leptosphaeria maculans. Mac y sus variantes permiten la inhibición de neuronas utilizando luz azul-verde.
Variantes de Mac
Se han diseñado variantes de Mac para incluir mejoras como:
- Amplitud de fotocorriente mejorada: Ejemplo: eMac3.0.
Interruptores Ópticos
Además de las opsinas, los investigadores han aprovechado fotorreceptores de plantas y bacterias para crear sistemas proteicos controlados por la luz, conocidos como "interruptores fotosensibles" o interruptores ópticos. Estas proteínas ofrecen un control espacial y temporal exquisito sobre la actividad proteica.
Sistemas basados en fitocromos, criptocromos y dominios LOV (Light Oxygen Voltage) se han utilizado en diversos contextos experimentales, incluyendo la activación de proteínas, la localización subcelular y la activación transcripcional.
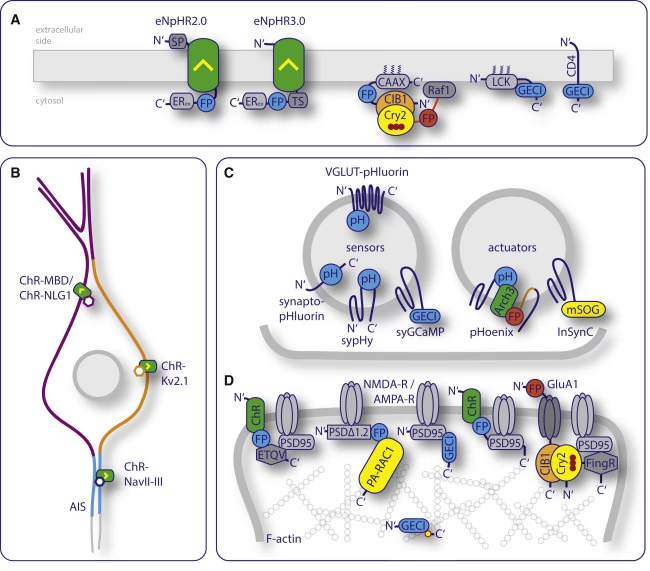
En el sistema Cry2-CIB1, ampliamente utilizado, la luz induce un cambio conformacional en el criptocromo Cry2 que permite la unión a CIB1. Esta unión inducida por la luz puede utilizarse para controlar la localización de una proteína de interés. Por ejemplo, una fusión de Cry2 codificada genéticamente dirigida al núcleo puede reclutar una fusión de CIB1-proteína al núcleo tras la activación luminosa.
Alternativamente, cuando una mitad de una proteína dada, como la recombinasa Cre, se fusiona a Cry2 y la otra mitad a CIB1, la heterodimerización estimulada por la luz puede reconstituir la proteína funcional. Este principio también ha permitido el diseño de factores de transcripción sintéticos de dos partes: Cry2 y CIB1 se fusionan a un dominio de activación transcripcional y a un dominio de unión al ADN, permitiendo que la luz active la transcripción.
Los fitocromos y los dominios LOV funcionan de manera similar a los criptocromos, con cambios inducidos por la luz en la conformación o dimerización de proteínas. Además de las aplicaciones descritas, tanto LOV como Dronpa pueden controlar la actividad de una proteína fusionada a través de interacciones alostéricas.
Planificando un Experimento de Optogenética
Diseñar un experimento optogenético exitoso requiere considerar varios factores clave al seleccionar tanto la opsina como el sistema de entrega.
Excitación o Inhibición Optogenética: Lo primero y más importante: ¿desea activar (despolarizar) o silenciar (hiperpolarizar) las neuronas en su experimento? La respuesta determinará si debe elegir una opsina excitatoria o inhibitoria, respectivamente.
Color de la Luz de Activación: Existe una variedad de longitudes de onda de activación, que van desde el azul hasta el amarillo y el rojo. La luz roja exhibe una mejor penetración en los tejidos, lo que puede permitir colocar la fibra óptica fuera del cerebro, haciendo el procedimiento experimental menos invasivo. Diferentes longitudes de onda de activación también posibilitan la combinación de múltiples opsinas en el mismo experimento. Por ejemplo, podría usar diferentes colores de luz para activar/silenciar la misma población neuronal, o activar diferentes poblaciones neuronales en momentos distintos.
Consideraciones Temporales: La precisión temporal es clave en los experimentos optogenéticos. Su diseño experimental determinará si necesitará períodos cortos o largos de activación/inactivación neuronal. Estos pueden variar desde milisegundos (con ChR2) hasta ser "de larga duración", por ejemplo, segundos a minutos con opsinas de función escalón estables (SSFOs).
Sistemas de Entrega de la Opsin: Dos factores determinan qué población neuronal se manipula en un experimento dado: la expresión de la opsina y el área que se está iluminando. Hay varias formas diferentes de controlar la expresión de la opsina. Generalmente, la expresión más robusta y estable se logra en una línea de ratones transgénicos. Por ejemplo, en el ratón VGAT-ChR2, donde ChR2 se expresa bajo el control del transportador vesicular de gamma-aminobutírico (GABA) (VGAT), ChR2 se expresa en todas las neuronas GABAérgicas. En este caso, la subpoblación de neuronas GABAérgicas activadas por la luz se controla mediante la colocación de la fibra óptica.
El uso de vectores virales para la entrega de la opsina resulta en una expresión más localizada de la opsina. Dependiendo del virus y el sistema promotor utilizados, hay un tiempo de incubación (días a semanas) hasta que se alcanza la expresión máxima de la opsina. Este enfoque es especialmente potente cuando se combina con tecnología de recombinasa sitio-específica como Cre-lox. Esta tecnología permite expresar una opsina solo en una subpoblación de células genéticamente definida dentro del sitio de inyección del vector viral, en lugar de en todas las células. Por ejemplo, usar un vector viral con una opsina 'floxed' en un animal VGAT-cre resultará en la expresión de la opsina solo en neuronas inhibitorias cerca del sitio de inyección.
Tabla Comparativa de Osinas Microbianas Comunes
| Tipo de Opsin | Variante | Descripción | Pico de Respuesta (nm) | Función Principal |
|---|---|---|---|---|
| Channelrhodopsinas (canales catiónicos) | ChR2 | Canal catiónico activado por luz, ampliamente utilizado (CrChR2) | 470 | Excitación rápida |
| Channelrhodopsinas (canales catiónicos) | ChR2/H134R | Variante con mayor fotocorriente que CrChR2 | 450 | Excitación (mayor corriente) |
| Channelrhodopsinas (canales catiónicos) | ChETA | Mutación E123T; cinética más rápida, menor fotocorriente | 490 | Excitación (rápida) |
| Channelrhodopsinas (canales catiónicos) | ChrimsonR | Canal activable por luz roja (mutación K176R) | 590 | Excitación (luz roja) |
| Channelrhodopsinas (canales catiónicos) | Chronos | Canal de alta velocidad y sensibilidad a la luz (Stigeoclonium helveticum) | 500 | Excitación (muy rápida) |
| Channelrhodopsinas (canales cloruro) | GtACR1 | Canal de cloruro (Guillardia theta) | 515 | Inhibición rápida |
| Channelrhodopsinas (canales cloruro) | GtACR2 | Canal de cloruro (Guillardia theta) | 470 | Inhibición rápida |
| Halorhodopsinas | NpHR (Halo) | Bomba de cloruro hacia adentro activada por luz amarilla (Natronomonas pharaonis) | 589 | Inhibición (luz amarilla) |
| Halorhodopsinas | eNpHR3.0 | NpHR mejorado con señales de tráfico a membrana | 589 | Inhibición (mayor eficiencia) |
| Halorhodopsinas | Jaws | Bomba de cloruro hacia adentro desplazada al rojo (Haloarcula salinarum) | 632 | Inhibición (luz roja) |
| Archaerhodopsinas | Arch | Bomba de protones hacia afuera (Halorubrum sodomense) | 566 | Inhibición (luz verde-amarilla) |
| Archaerhodopsinas | ArchT | Arch con mayor sensibilidad a la luz | 566 | Inhibición (mayor sensibilidad) |
| Archaerhodopsinas | eArch3.0 | Arch mejorado con señales de tráfico | 566 | Inhibición (mayor eficiencia) |
| Leptosphaeria rhodopsinas | Mac | Bomba de protones hacia afuera (Leptosphaeria maculans) | 540 | Inhibición (luz azul-verde) |
Esta tabla resume algunas de las opsinas más comunes y sus características principales, pero la diversidad de herramientas disponibles es mucho mayor, con variantes diseñadas para necesidades experimentales muy específicas.
Preguntas Frecuentes sobre Herramientas Optogenéticas
Dado el carácter innovador de la optogenética, es común que surjan preguntas sobre su funcionamiento y aplicación. Aquí abordamos algunas de las más frecuentes:
¿Qué es la optogenética en términos sencillos?
La optogenética es una técnica que combina la genética y la luz para controlar la actividad de células vivas, generalmente neuronas. Se introducen genes en las células que las hacen sensibles a la luz, de modo que se pueden activar o desactivar simplemente iluminándolas con una luz del color adecuado.
¿Cómo funcionan las opsinas microbianas?
Las opsinas microbianas son proteínas que se insertan en la membrana de las células. Actúan como canales o bombas que se abren o cierran en respuesta a la luz. Cuando se exponen a una longitud de onda de luz específica, permiten el flujo de iones a través de la membrana, lo que cambia el voltaje eléctrico de la célula y, en el caso de las neuronas, puede provocar que disparen potenciales de acción (excitación) o dejen de hacerlo (inhibición).
¿Cuál es la diferencia entre una herramienta optogenética excitatoria e inhibitoria?
Una herramienta optogenética excitatoria (como la mayoría de las Channelrhodopsinas) provoca que la célula se despolarice, lo que la hace más propensa a activarse o disparar. Una herramienta optogenética inhibitoria (como las Halorhodopsinas, Archaerhodopsinas o GtACRs) provoca que la célula se hiperpolarice, lo que la hace menos propensa a activarse o la silencia.
¿Qué colores de luz se utilizan en optogenética?
Se utilizan diferentes colores de luz dependiendo de la opsina específica. Las Channelrhodopsinas clásicas se activan con luz azul (aprox. 470 nm). Las Halorhodopsinas y Archaerhodopsinas suelen activarse con luz amarilla o verde (aprox. 560-590 nm). Existen variantes diseñadas para ser activadas por luz roja (aprox. 630 nm), que penetra más profundamente en los tejidos.
¿Se pueden usar varias herramientas optogenéticas al mismo tiempo?
Sí, es posible utilizar múltiples opsinas con diferentes espectros de activación en el mismo experimento. Esto permite controlar simultáneamente diferentes poblaciones neuronales o incluso inducir tanto excitación como inhibición en la misma población pero en momentos distintos, utilizando diferentes colores de luz.
¿Cómo se introducen estas herramientas en las neuronas?
Comúnmente, se utilizan vectores virales (como virus adenoasociados, AAVs) modificados para transportar el gen de la opsina. Estos virus se inyectan en el área cerebral de interés. El virus infecta las células y entrega el gen, que luego es expresado por la maquinaria celular. También se pueden usar animales transgénicos que expresan la opsina en tipos celulares específicos de forma constitutiva.
¿Para qué se utiliza la optogenética en la investigación?
La optogenética se utiliza para investigar la función de circuitos neuronales específicos, desentrañar las bases neuronales del comportamiento (aprendizaje, memoria, miedo, recompensa), estudiar la patología de enfermedades neurológicas y psiquiátricas, y desarrollar posibles terapias basadas en la modulación de la actividad neuronal.
Conclusión
Las herramientas optogenéticas han revolucionado la neurociencia al proporcionar un control sin precedentes sobre la actividad celular utilizando la luz. Desde las opsinas microbianas que actúan como fotorreceptores activando o silenciando neuronas, hasta los interruptores ópticos que controlan la función de proteínas intracelulares, este conjunto de herramientas sigue expandiéndose. La capacidad de manipular circuitos neuronales específicos con alta precisión temporal y espacial está desvelando secretos fundamentales sobre el funcionamiento del cerebro y abriendo nuevas vías para entender y tratar trastornos neurológicos. A medida que la tecnología avanza, podemos esperar herramientas aún más sofisticadas que permitan un control cada vez más matizado de la actividad neuronal, acercándonos a una comprensión completa de la compleja red que define nuestra mente y comportamiento. La optogenética es, sin duda, una de las tecnologías más poderosas y transformadoras en la neurociencia moderna.
Si quieres conocer otros artículos parecidos a Optogenética: Controlando Neuronas con Luz puedes visitar la categoría Neurociencia.
