La regulación del apetito y el peso corporal es un proceso asombrosamente complejo controlado por el sistema nervioso central (SNC). Lejos de ser una simple respuesta a las necesidades energéticas, el cerebro humano integra una vasta cantidad de señales internas y externas para modular la homeostasis energética. Comprender estos mecanismos es fundamental, especialmente en el contexto de la creciente epidemia mundial de obesidad, una condición que afecta a una porción significativa de la población en países industrializados y en vías de occidentalización.
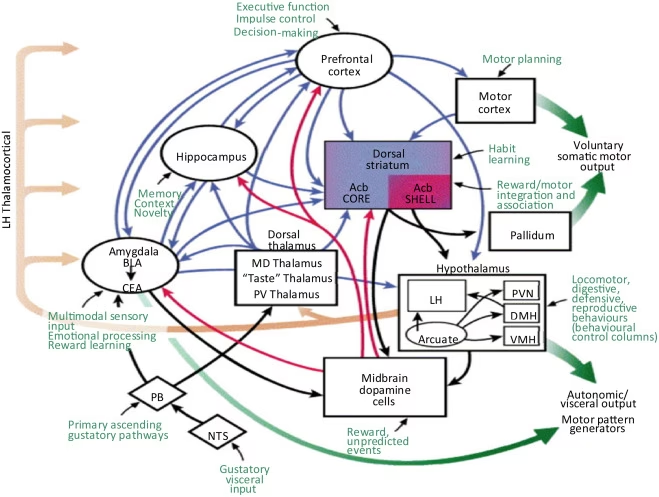
La investigación actual revela que el control de la alimentación en humanos va más allá de la simple regulación homeostática. Si bien el Hipotálamo ha sido históricamente considerado el principal centro de control del apetito, la evidencia más detallada, aunque gran parte proviene de estudios en roedores, sugiere una imagen mucho más intrincada. En humanos, sistemas cerebrales adicionales como los de recompensa, emoción, memoria, atención y control cognitivo juegan roles cruciales. Estos circuitos no actúan de forma aislada, sino que interactúan dinámicamente para determinar cuándo, qué y cuánto comemos, así como para regular el gasto energético.
Técnicas para Estudiar el Cerebro y la Alimentación
Para desentrañar esta complejidad, los neurocientíficos utilizan diversas técnicas de investigación. Las más comunes en estudios clínicos sobre procesos apetitivos en humanos incluyen pruebas neurocognitivas e imágenes por resonancia magnética funcional (fMRI).
Las pruebas neurocognitivas son esencialmente tareas computarizadas diseñadas para evaluar habilidades mentales específicas, como el control inhibitorio. Tareas como la de 'stop signal' o 'go/no-go' miden la capacidad de frenar respuestas automáticas, una habilidad relevante para resistir la tentación de comer. Estudios han demostrado que un control inhibitorio más pobre, medido por tiempos de reacción más largos, se correlaciona con el aumento de peso futuro. Aunque útiles, estas pruebas por sí solas solo proporcionan medidas de rendimiento cognitivo, no revelan la actividad cerebral subyacente.
Aquí es donde la fMRI se vuelve invaluable. Al combinar tareas neurocognitivas (como ver imágenes de comida) con fMRI, los investigadores pueden observar qué áreas o redes cerebrales se activan. La fMRI detecta cambios en el flujo sanguíneo oxigenado, que es un indicador indirecto de la actividad neuronal. Tiene buena resolución espacial para la corteza, aunque presenta limitaciones en áreas profundas como el hipotálamo. A pesar de esto, la fMRI es una de las mejores herramientas para detectar activaciones regionales en respuesta a estímulos o tareas específicas. Diferencias en los patrones de activación cerebral entre individuos obesos y delgados, incluso sin diferencias en el rendimiento de la tarea, sugieren alteraciones o compensaciones neurales.
La fMRI también permite estudiar la conectividad funcional, analizando cómo diferentes áreas cerebrales se comunican entre sí. Esto revela redes cerebrales que trabajan concertadamente. Por ejemplo, la conectividad entre la amígdala (emoción) y áreas prefrontales (control cognitivo) puede estar alterada en personas con alto estrés crónico al ver comida calórica, lo que podría explicar el comer por estrés.
Otra técnica de RM, la Imagen por Tensor de Difusión (DTI), evalúa la conectividad estructural (materia blanca) y su integridad. Estudios han usado DTI para observar cambios en las conexiones entre áreas prefrontales y límbicas en la obesidad, sugiriendo un posible mecanismo para el deterioro cognitivo asociado.
Otras técnicas incluyen Magnetoencefalografía (MEG) y Electroencefalografía (EEG). Estas son no invasivas y tienen mejor resolución temporal que la fMRI, aunque peor resolución espacial. Detectan la actividad eléctrica o magnética directa de las neuronas. Se han usado para estudiar la respuesta temporal a las señales de comida o las diferencias en la actividad frontal relacionadas con la atención y la pérdida de control sobre la alimentación.
Las técnicas de Medicina Nuclear, como la Tomografía por Emisión de Positrones (PET) y la Tomografía Computarizada por Emisión de Fotón Único (SPECT), utilizan trazadores radiactivos. Son invasivas pero permiten mapear la localización y disponibilidad de moléculas específicas, como receptores de neurotransmisores. Los estudios con PET han mostrado consistentemente menor disponibilidad de receptores de Dopamina D2 en el estriado de individuos obesos en comparación con delgados, lo que sugiere una alteración en el sistema de recompensa.
El Control Homeostático: El Hipotálamo
El sistema homeostático, centrado en el Hipotálamo, es crucial para mantener el equilibrio energético. El núcleo arcuato del hipotálamo contiene dos poblaciones principales de neuronas: las que expresan pro-opiomelanocortina (POMC) y transcrito regulado por cocaína y anfetaminas (CART), que disminuyen el apetito (anorexigénicas), y las que expresan proteína relacionada con agouti (AgRP) y neuropéptido Y (NPY), que aumentan el apetito (orexigénicas).

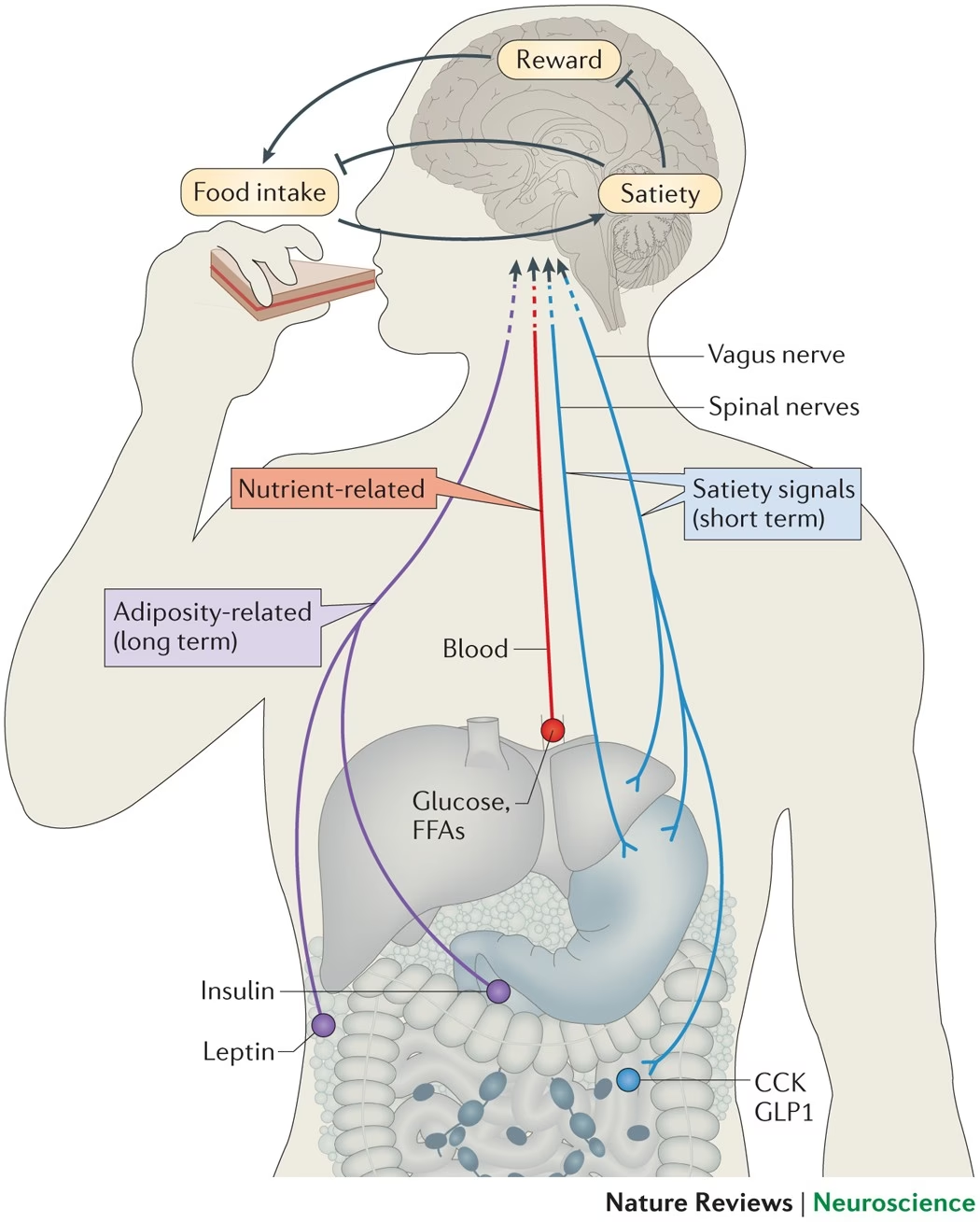
Estas neuronas son moduladas por señales hormonales provenientes de la periferia, como la leptina (tejido adiposo), la ghrelina (tracto gastrointestinal), la insulina y la amilina (páncreas), la adiponectina (tejido adiposo) y la irisin (músculo), así como el GLP-1 (péptido similar al glucagón-1) del intestino. La leptina, por ejemplo, señaliza la cantidad de grasa almacenada y, en condiciones fisiológicas, inhibe el apetito estimulando las neuronas POMC/CART e inhibiendo las AgRP/NPY. En la obesidad, los altos niveles crónicos de leptina pueden llevar a resistencia a la leptina, alterando este mecanismo.
Los estudios de estimulación hipotalámica en roedores han demostrado que la estimulación del hipotálamo lateral aumenta la ingesta, mientras que la estimulación del hipotálamo ventromedial la disminuye. Sin embargo, los hallazgos en humanos son más limitados y sugieren que la activación hipotalámica puede estar influenciada por sistemas cerebrales superiores, lo que subraya la mayor complejidad del control de la alimentación en nuestra especie.
Más Allá del Hambre: Recompensa, Emoción, Memoria, Atención y Cognición
Como se mencionó, el control de la alimentación en humanos involucra una red compleja que va más allá del hipotálamo. Otros sistemas juegan un papel preponderante, especialmente en el contexto de la sobrealimentación y la obesidad.
El Sistema de Recompensa
La comida es intrínsecamente gratificante y activa las vías de recompensa del cerebro. Estas vías incluyen neuronas dopaminérgicas que se originan en el área tegmental ventral (VTA) y la sustancia negra (SN), proyectándose al núcleo accumbens, el estriado y la corteza orbitofrontal (OFC). Estas áreas responden a la vista y al consumo de comida.
Existen dos teorías principales sobre cómo el sistema de recompensa puede estar alterado en la obesidad. Una sugiere hiporrespuesta a la recompensa, donde los individuos requieren más comida, especialmente hipercalórica, para alcanzar el mismo nivel de placer, lo que lleva a comer en exceso. La menor disponibilidad de receptores D2 de Dopamina en el estriado en individuos obesos apoya esta idea. La otra teoría postula hiperrespuesta a las *señales* de comida, donde la exposición a alimentos altamente gratificantes intensifica el deseo, pero el consumo real no cumple la expectativa, creando una desconexión que impulsa a comer más para alcanzar la recompensa esperada. La mayor activación del núcleo accumbens, el mesencéfalo y la OFC en respuesta a señales visuales de comida en la obesidad apoya esta teoría. Ambas hipótesis no son mutuamente excluyentes y sugieren un papel central del sistema de recompensa en la alimentación disfuncional.
Sistemas de Emoción y Memoria
Las emociones son potentes moduladores del apetito. Condiciones como la depresión y la ansiedad son comorbilidades comunes de la obesidad. A corto plazo, emociones como la alegría o el enojo pueden aumentar el apetito y llevar a peores elecciones dietéticas. El estrés también altera el apetito y predispone a la obesidad. La Amígdala es un área clave en la regulación del apetito mediada por emociones. Se activa ante señales de comida, y esta respuesta es mayor en la obesidad. La activación de la amígdala predice el consumo de alimentos hipercalóricos. Una mayor conectividad funcional entre la amígdala y el hipotálamo en estado de saciedad ante señales de comida podría explicar el “hambre emocional” incluso sin necesidad fisiológica. El concepto de comer emocional, a menudo en respuesta a estados afectivos negativos como el estrés o la ansiedad, se relaciona con la teoría psicosomática de la obesidad, que sugiere que la comida se usa como defensa emocional.
La memoria, regulada principalmente por el hipocampo y la formación parahipocampal, también influye. Aunque los ritmos circadianos controlan el horario de las comidas, la memoria y las experiencias a menudo lo anulan. Tanto en roedores como en humanos, las señales o el contexto (como la hora habitual de la comida) pueden inducir a comer incluso estando saciado. El hipocampo recibe información de áreas como la ínsula, la corteza orbitofrontal y el núcleo arcuato. Las lesiones hipocampales en roedores aumentan la ingesta y la obesidad. En humanos, el daño hipocampal puede impedir recordar si se ha comido, llevando a comer repetidamente. Además, la obesidad inducida por la dieta puede afectar la función hipocampal, posiblemente a través de procesos inflamatorios, creando un ciclo vicioso donde la disfunción de la memoria contribuye a la obesidad, que a su vez perjudica más la memoria.
Sistemas de Atención
La atención hacia los alimentos y sus señales también es crucial. Los individuos obesos tienden a prestar más atención a las señales de comida, y las personas con peso normal que lo hacen muestran patrones de sobrealimentación y aumento de peso. Esta “sesgo atencional” hacia alimentos hipercalóricos es más pronunciado en individuos obesos incluso en estado de saciedad. La red cerebral de la atención incluye las cortezas parietal y visual. Los estudios de fMRI muestran mayor activación en las cortezas occipital y parietal en respuesta a imágenes de alimentos hipercalóricos en individuos con obesidad o propensos a ella. Una mayor activación atencional a las señales de comida predice un menor éxito en la pérdida de peso durante las dietas, lo que sugiere que este sesgo puede dificultar los esfuerzos para adelgazar.
Sistemas de Control Cognitivo
El control cognitivo engloba funciones ejecutivas como la inhibición de respuestas automáticas. En el contexto de la alimentación, permite resistir la tentación de un alimento poco saludable a pesar del deseo. La Corteza Prefrontal, incluyendo la corteza cingulada, la corteza frontal inferior, el área motora suplementaria (pre-SMA) y la corteza prefrontal dorsolateral (DLPFC), es clave en esta red. Numerosos estudios han demostrado un control inhibitorio deteriorado en individuos obesos, incluso en tareas no relacionadas con la comida, y esta disfunción se correlaciona con la ingesta de alimentos calóricos y la resistencia a la pérdida de peso. La DLPFC parece estar involucrada en la evaluación de las elecciones alimentarias y se activa durante la autorrestricción. Se ha teorizado que un control cognitivo deficiente podría “liberar” las respuestas del sistema de recompensa, llevando a comer en exceso. Los individuos obesos a menudo muestran menor metabolismo o actividad en la corteza prefrontal, lo que se correlaciona con el IMC. La pérdida de peso puede mejorar la función ejecutiva. Aunque no está claro si el pobre control cognitivo causa obesidad o viceversa, existe una clara relación bidireccional.
Interacciones y la Complejidad del Control
Es fundamental entender que estos sistemas no operan de forma independiente. El hipotálamo recibe señales externas e internas y se comunica directamente con componentes de los sistemas de recompensa y emoción/memoria, y a través del tálamo con las áreas corticales de control cognitivo y atención. La activación del hipotálamo en humanos probablemente está modulada por estos sistemas superiores. Cuando los individuos consumen alimentos por encima de las necesidades homeostáticas (como en la obesidad), estos sistemas 'supra-homeostáticos' pueden ejercer un control mayor sobre el impulso de comer que el dictado únicamente por el hipotálamo.
Resumen de Sistemas Cerebrales Clave en la Alimentación
| Sistema | Áreas Clave | Función Principal en la Alimentación |
|---|---|---|
| Homeostático | Hipotálamo (Núcleo Arcuato, LH, VMH, PVN), Tronco Encefálico | Regulación del balance energético, respuesta a señales de hambre/saciedad (leptina, ghrelina, etc.) |
| Recompensa | VTA, SN, Estriado (Núcleo Accumbens), Corteza Orbitofrontal | Placer y motivación asociados a la comida, deseo y búsqueda de alimentos. |
| Emoción/Memoria | Amígdala, Hipocampo, Corteza Cingulada | Modulación del apetito por estados emocionales y estrés; memoria de comidas y contexto. |
| Atención | Cortezas Parietal y Visual, Áreas Frontales | Sesgo atencional hacia señales de comida, detección y procesamiento de estímulos alimentarios. |
| Control Cognitivo | Corteza Prefrontal (DLPFC, VLPFC, Cingulada, pre-SMA) | Inhibición de impulsos, toma de decisiones sobre alimentos, planificación. |
Preguntas Frecuentes
¿Solo el hipotálamo controla el apetito?
No, aunque el hipotálamo es el centro principal para la regulación homeostática (hambre fisiológica), el control de la alimentación en humanos es mucho más complejo e involucra la interacción con sistemas de recompensa, emoción, memoria, atención y control cognitivo.
¿Cómo afectan las emociones a lo que comemos?
Las emociones y el estrés pueden influir fuertemente en la alimentación. La amígdala y otras áreas cerebrales relacionadas con las emociones y el estrés pueden aumentar el deseo de comer, a menudo alimentos calóricos, incluso sin necesidad fisiológica. Esto se relaciona con el concepto de comer emocional.
¿La obesidad cambia el cerebro o el cerebro cambiado causa obesidad?
La investigación sugiere que es una relación bidireccional compleja. Las alteraciones en la función cerebral, como en el sistema de recompensa o el control cognitivo, pueden predisponer a la sobrealimentación y el aumento de peso. A su vez, la obesidad puede inducir cambios en la estructura y función cerebral, afectando la cognición, la memoria y perpetuando patrones de alimentación disfuncional.
¿Qué es la Homeostasis energética?
Es el estado de equilibrio donde la ingesta de energía a través de la comida se iguala al gasto de energía del cuerpo. El cerebro, especialmente el hipotálamo, trabaja constantemente para mantener este equilibrio mediante señales de hambre y saciedad.
¿Qué técnicas se usan para estudiar estos mecanismos?
Se emplean diversas técnicas de neuroimagen y pruebas conductuales, como la resonancia magnética funcional (fMRI), la tomografía por emisión de positrones (PET), el electroencefalograma (EEG), la magnetoencefalografía (MEG) y la imagen por tensor de difusión (DTI), a menudo combinadas con tareas que implican estímulos alimentarios o cognitivos.
Conclusiones
El control de la alimentación en el cerebro humano es un proceso multifacético que involucra la interacción compleja de varios sistemas corticales y subcorticales, influenciados por procesos cognitivos y afectivos. Aunque los estudios en roedores han proporcionado información fundamental sobre los circuitos neuronales básicos, la complejidad de la alimentación disfuncional en humanos requiere un enfoque más amplio que considere la influencia de los sistemas de recompensa, emoción, memoria, atención y control cognitivo.
Las técnicas de neuroimagen, especialmente la fMRI combinada con tareas conductuales y la PET para estudiar determinantes moleculares como los receptores de Dopamina, son herramientas esenciales para desentrañar cómo estos sistemas interactúan para controlar el apetito y la ingesta. Comprender estas alteraciones cerebrales en la obesidad es crucial para desarrollar estrategias de tratamiento más efectivas, tanto farmacológicas como conductuales, que puedan dirigirse a los mecanismos neurales subyacentes.
Si quieres conocer otros artículos parecidos a Mecanismos Cerebrales de la Alimentación puedes visitar la categoría Neurociencia.

