Durante mucho tiempo, la neurociencia y la endocrinología parecieron disciplinas separadas por un abismo. Una se centraba en el cerebro, las neuronas y la transmisión rápida de señales eléctricas y químicas a través de sinapsis bien definidas. La otra estudiaba las hormonas, secretadas por glándulas distantes, viajando por la sangre para ejercer efectos prolongados en órganos específicos. Sin embargo, la realidad es mucho más intrincada y fascinante. El cerebro no es una isla aislada; está profundamente interconectado con el resto del cuerpo a través de un diálogo constante mediado por moléculas químicas, muchas de las cuales encajan en la definición de hormonas o son parientes cercanos: los neuropéptidos y neurohormonas.

- La Brecha Histórica: Neurotransmisores vs. Hormonas
- Los Neuropéptidos: Un Lenguaje Químico Diverso en el Cerebro
- Funciones Diversas de los Neuropéptidos: Más Allá de la Excitabilidad
- ¿Qué es una Neurohormona?
- Desequilibrios Hormonales y Síntomas Neurológicos
- Tabla Comparativa: Neurotransmisores vs. Neuropéptidos/Neurohormonas
- Preguntas Frecuentes
- Conclusión
La Brecha Histórica: Neurotransmisores vs. Hormonas
La visión clásica definía a los neurotransmisores por su liberación en sinapsis, su dependencia del calcio y la despolarización neuronal, y su acción sobre receptores postsinápticos específicos, con efectos localizados y de corta duración, limitados por mecanismos rápidos de recaptación y degradación. Las hormonas, por otro lado, eran definidas por Starling como sustancias fabricadas por células especializadas, liberadas a la sangre para viajar por todo el cuerpo y actuar en órganos diana distantes con efectos prolongados.
Esta distinción, aunque útil en su momento, creó una separación artificial. Los neurocientíficos se volcaron en la electrofisiología y el mapeo de la conectividad neuronal para entender el procesamiento de la información, mientras que los endocrinólogos se centraban en la medición de hormonas y sus mecanismos de síntesis y acción. A pesar de esta división, la realidad biológica siempre fue más fluida. Los endocrinólogos expandieron su definición de hormonas para incluir esteroides que actúan por difusión y agentes locales como las prostaglandinas. Los neurocientíficos, a regañadientes, admitieron que los neurotransmisores podían desbordarse de la sinapsis para actuar en receptores extrasinápticos.
El Nacimiento de la Neuroendocrinología: La Hipótesis de Harris
Uno de los desafíos más significativos a esta división provino de Geoffrey Harris en la década de 1950. En ese momento, se creía que la ovulación espontánea era controlada por la hipófisis mediante la acción directa del estrógeno. Harris desafió esta idea, proponiendo que el estrógeno actuaba en el cerebro (específicamente en el hipotálamo), lo que resultaba en la liberación de sustancias que viajaban por vasos sanguíneos a la hipófisis para regular la secreción de gonadotropinas. Estas sustancias fueron postuladas como factores liberadores.
La teoría de Harris implicaba una comunicación vascular directa entre el cerebro y la hipófisis anterior, rompiendo el paradigma de control exclusivamente nervioso. Él y sus colaboradores demostraron la existencia de vasos portales que conectaban la eminencia media del hipotálamo con la hipófisis anterior, con flujo sanguíneo del cerebro a la hipófisis. Experimentos de trasplante de hipófisis confirmaron que solo los trasplantes revascularizados por estos vasos portales recuperaban la función normal, apoyando la idea de una señal química transportada por la sangre desde el cerebro.
La teoría de Harris enfrentó la oposición de figuras influyentes como Sir Solly Zuckerman, quien se basó en experimentos con hurones para argumentar que la hipófisis podía funcionar independientemente de las conexiones cerebrales. Sin embargo, Harris y Donovan demostraron que la técnica de Zuckerman no prevenía la regeneración de los vasos portales, y sus propios experimentos con una placa de papel para impedir la revascularización probaron que la ovulación dependía de la conexión vascular hipotálamo-hipófisis. Harris ganó el debate, y su hipótesis sentó las bases para el campo de la neuroendocrinología, que estudia la interacción entre el sistema nervioso y el sistema endocrino.
Los Neuropéptidos: Un Lenguaje Químico Diverso en el Cerebro
Tras la identificación de los factores liberadores como péptidos, se hizo evidente que la clase de neuropéptidos en el cerebro era mucho más extensa. Actualmente se estima que hay más de 300 péptidos diferentes expresados en diversas combinaciones por poblaciones neuronales distintas. Esto desafía la visión clásica de neuronas homogéneas que solo varían en sus conexiones cableadas y que se comunican únicamente mediante la actividad eléctrica y los neurotransmisores convencionales. El cerebro, en realidad, parece estar compuesto por una vasta multitud de tipos neuronales que "hablan" en múltiples lenguajes químicos.
La idea de que los neuropéptidos en el cerebro son simplemente neurotransmisores adicionales es, en gran medida, una simplificación excesiva. Las diferencias en su manejo y acción son significativas:
Liberación de Neuropéptidos: Más Allá de la Sinapsis
Aunque muchas neuronas producen tanto péptidos como neurotransmisores convencionales, estos se empaquetan en vesículas diferentes. Los neurotransmisores se encuentran en pequeñas vesículas sinápticas localizadas en los terminales sinápticos. Los péptidos se empaquetan en grandes vesículas de núcleo denso que se distribuyen por todo el citoplasma neuronal, incluyendo dendritas y soma. Mientras que las vesículas sinápticas se liberan en sitios especializados de la membrana presináptica, las vesículas de núcleo denso pueden liberarse desde diversas partes de la neurona, siempre que estén cerca de la membrana plasmática.
La liberación de vesículas de núcleo denso en la hendidura sináptica, si ocurre, es menos probable y menos eficiente que la de las vesículas sinápticas. Además, las vesículas peptídicas contienen una carga mucho mayor (miles de moléculas del precursor peptídico), lo que, si se liberaran y confinaran en la hendidura sináptica, generarían concentraciones extremadamente altas, muy superiores a la afinidad nanomolar de sus receptores. Esto sugiere que su acción principal no está limitada a la sinapsis.
Regulación de la Liberación Peptídica: No Solo Eléctrica
Si bien la liberación de neuropéptidos puede ser dependiente de la actividad eléctrica, la relación no es tan directa ni determinista como con los neurotransmisores. Por ejemplo, las neuronas de vasopresina que proyectan a la hipófisis posterior liberan vesículas con una probabilidad muy baja por cada potencial de acción (aproximadamente 1 vesícula por cada 5000 picos en condiciones de alta demanda). Esto indica que la liberación es un proceso altamente estocástico a nivel de un solo sitio de liberación.
Además, una gran proporción de vesículas peptídicas se encuentra en las dendritas, que no siempre son liberables por la actividad eléctrica convencional. Ciertos péptidos pueden desencadenar la liberación dendrítica movilizando reservas intracelulares de calcio, incluso inhibiendo la actividad de picos. Otros mecanismos, como el "priming", implican la reorganización del citoesqueleto para acercar las vesículas a la membrana plasmática, permitiendo su liberación en respuesta a la actividad eléctrica. Estos mecanismos modulan la conectividad funcional entre neuronas peptidergicas a través de acciones autocrinas (sobre la misma neurona) y paracrinas (sobre neuronas vecinas).

Acción a Distancia: El Concepto de Transmisión de Volumen
La comunicación neuronal tradicional se basa en la proximidad física de la sinapsis. Sin embargo, con los neuropéptidos, a menudo existe una notable discrepancia entre la densidad de receptores en una región cerebral y la densidad de fibras peptídicas. Esto sugiere que los péptidos actúan a través de la difusión en el espacio extracelular o a través del líquido cefalorraquídeo (LCR), un mecanismo conocido como transmisión de volumen.
Las vesículas de núcleo denso pueden liberarse desde varicosidades axonales distribuidas a lo largo de los axones, no solo en terminales sinápticos definidos. Aunque la probabilidad de liberación en cada sitio puede ser baja, la gran cantidad de sitios potenciales implica que los péptidos pueden alcanzar neuronas diana ampliamente dispersas de manera estocástica. Cuando una región cerebral está densamente inervada por axones de una población de células peptídicas, la señal puede ser más similar a una señal hormonal que a una sináptica localizada.
Un ejemplo notable de acción a distancia proviene de estudios sobre el núcleo supraquiasmático (NSQ), el reloj biológico del cerebro. En hámsteres con lesiones del NSQ, los ritmos circadianos pueden restaurarse trasplantando fragmentos encapsulados del NSQ neonatal en el tercer ventrículo. La cápsula permite la difusión de sustancias pero impide la penetración de fibras nerviosas, demostrando que las señales químicas liberadas por el trasplante (probablemente péptidos) pueden actuar a distancia para restaurar la función.
Funciones Diversas de los Neuropéptidos: Más Allá de la Excitabilidad
Inicialmente considerados principalmente como neuromoduladores que afectan la excitabilidad neuronal, los neuropéptidos tienen un repertorio de funciones mucho más amplio. Muchos neuropéptidos influyen directamente en la expresión génica en sus células diana. Ejemplos canónicos incluyen los efectos del factor liberador de gonadotropina (GnRH) en la expresión de gonadotropinas en la hipófisis, el factor liberador de tirotropina (TRH) en la expresión de TSH, y el factor liberador de hormona del crecimiento (GHRH) en la expresión de hormona del crecimiento. Esta capacidad para regular la expresión génica permite cambios a largo plazo en la función celular.
Otras funciones de los neuropéptidos incluyen:
- Regulación del flujo sanguíneo local.
- Modulación de la morfología de las células gliales.
- Influencia en la sinaptogénesis (formación de nuevas sinapsis).
- Regulación de la síntesis y disponibilidad de otras moléculas de señalización.
La plasticidad del fenotipo peptídico es otro aspecto crucial. En respuesta a estados fisiológicos cambiantes, las neuronas pueden alterar los péptidos que expresan. Por ejemplo, tras estrés crónico, las neuronas del núcleo paraventricular del hipotálamo disminuyen la expresión de CRH y aumentan la de vasopresina, alterando la regulación del eje del estrés. De manera similar, las neuronas dopaminérgicas tuberinfundibulares que regulan la prolactina dejan de liberar dopamina durante la lactancia y, en su lugar, liberan leu encefalina, apoyando la secreción de prolactina.
Además, la acción de un neuropéptido no solo depende de su liberación, sino también de la regulación de la sensibilidad de sus células diana. La expresión de receptores peptídicos puede variar drásticamente en diferentes condiciones fisiológicas. Un ejemplo clásico es el aumento masivo de receptores de oxitocina en el útero durante el parto, lo que lo hace extremadamente sensible a los niveles circulantes de oxitocina. Las diferencias inter-específicas en comportamientos sociales mediados por vasopresina y oxitocina (como el apego en los topillos de la pradera versus la promiscuidad en los topillos de la pradera) a menudo reflejan diferencias en la distribución y densidad de receptores en el cerebro, más que en la liberación de los péptidos.
¿Qué es una Neurohormona?
El término neurohormona se refiere a una sustancia producida y liberada por neuronas, pero que, en lugar de actuar en una sinapsis cercana, viaja a través del torrente sanguíneo (o el LCR) para actuar en células diana distantes. El ejemplo arquetípico es la regulación de la hipófisis por el hipotálamo, como se vio con los factores liberadores de Harris.
Un caso bien estudiado es el control de la secreción de prolactina (PRL) por el hipotálamo. La dopamina (DA), liberada por las neuronas tuberinfundibulares (TIDA) del hipotálamo hacia los vasos portales hipofisarios, actúa como la principal neurohormona inhibitoria de la PRL en la hipófisis anterior. Sin embargo, durante el ciclo estral o la lactancia, se produce un pico de PRL que requiere una disminución en la inhibición dopaminérgica junto con señales estimuladoras. Varias sustancias han sido implicadas como neurohormonas liberadoras de PRL:
- TRH (Factor liberador de tirotropina): Un potente estimulador de PRL, cuyos niveles en sangre portal aumentan durante el pico de PRL.
- Oxitocina (OT): Los niveles de oxitocina en sangre portal también aumentan, y tanto la inmunoneutralización de OT como el bloqueo de sus receptores inhiben el pico de PRL. El estrógeno aumenta la sensibilidad de las lactotropas a la oxitocina.
- VIP (Péptido intestinal vasoactivo): Existe evidencia considerable de que el VIP puede actuar como un factor liberador de PRL.
- PrRP (Péptido liberador de prolactina): Aislado del hipotálamo, este péptido estimula la liberación de PRL, aunque su rol fisiológico aún se está dilucidando, ya que también está implicado en otras funciones como la homeostasis autonómica.
Estas neurohormonas ilustran perfectamente cómo las neuronas pueden utilizar el sistema circulatorio para enviar señales a distancia, uniendo funcionalmente el sistema nervioso y el endocrino de manera íntima.
Desequilibrios Hormonales y Síntomas Neurológicos
Dado el profundo impacto de las hormonas y neurohormonas en la función cerebral, no es sorprendente que los desequilibrios hormonales puedan tener consecuencias neurológicas y psicológicas significativas. La salud mental es particularmente susceptible a las fluctuaciones hormonales.
Efectos de los Desequilibrios Hormonales en el Cerebro
Las hormonas influyen en características innatas y rasgos de personalidad, modulando la actividad de los neurotransmisores y la función neuronal. Los desequilibrios pueden manifestarse como:
- Disfunción Cognitiva: Dificultad para concentrarse, falta de claridad mental, problemas de atención.
- Problemas de Memoria: Niveles bajos de estrógeno u hormonas tiroideas pueden causar olvidos y dificultad para recordar información.
- Alteraciones del Estado de Ánimo: Desequilibrios en serotonina, dopamina, cortisol o esteroides sexuales pueden llevar a depresión, ansiedad, irritabilidad y cambios de humor drásticos.
- Fatiga: La interrupción hormonal puede causar cansancio persistente que afecta la alerta mental y la función cerebral.
- Trastornos del Sueño: Las hormonas desequilibradas pueden provocar insomnio o mala calidad del sueño, impactando negativamente la salud cerebral y el rendimiento cognitivo.
El Impacto de Hormonas Específicas en el Sistema Nervioso
Hormonas del estrés como el cortisol y la adrenalina tienen un impacto directo. El cortisol elevado crónicamente puede sobreestimular el sistema nervioso, causando ansiedad e irritabilidad. La adrenalina alta de forma persistente puede inducir estrés crónico y disfunción nerviosa. Estos desequilibrios pueden contribuir a trastornos como ataques de pánico, depresión, deterioro cognitivo y alteraciones del sueño.
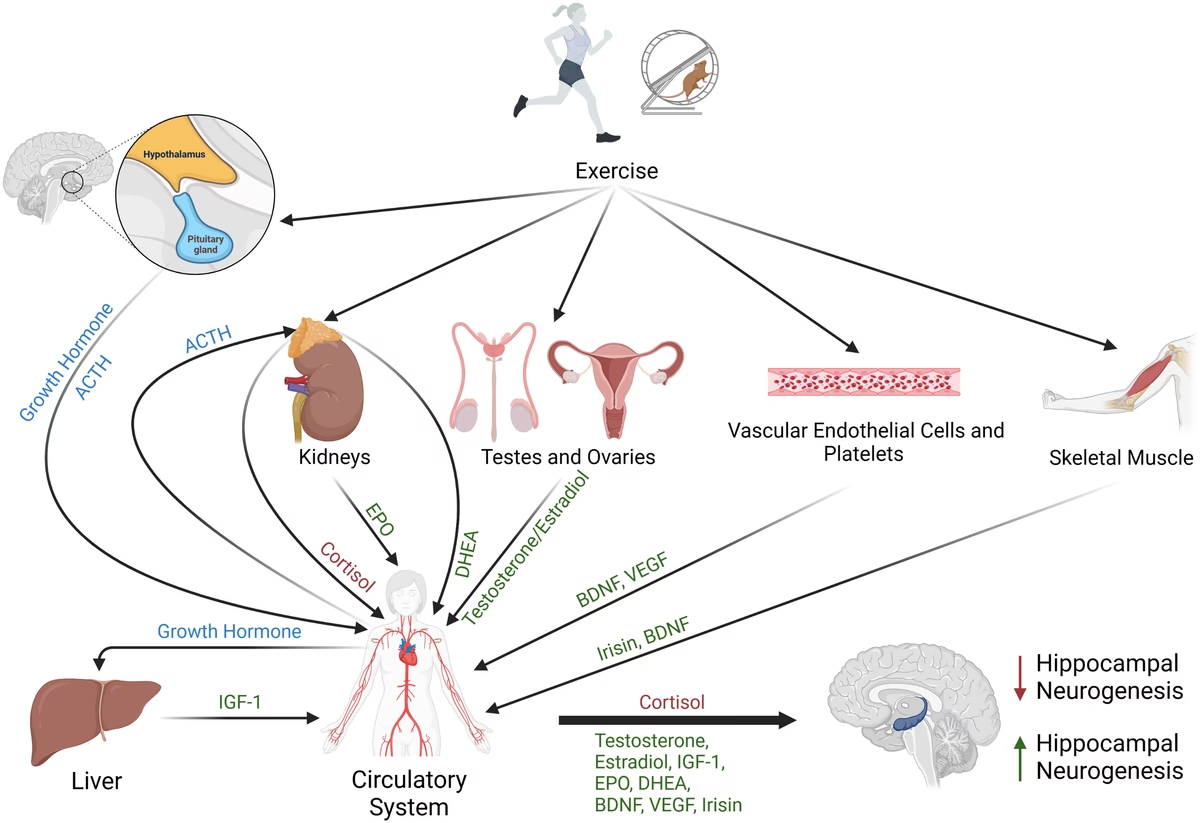
El sistema endocrino, con glándulas como la tiroides, suprarrenales e hipófisis, juega un papel crítico. Las disfunciones en este sistema pueden llevar a trastornos neurológicos. Por ejemplo, los desequilibrios de cortisol, hormonas tiroideas y estrógeno están fuertemente relacionados con la ansiedad, la depresión y el deterioro cognitivo.
El Impacto del Desequilibrio Tiroideo en la Función Cerebral
Las hormonas tiroideas (producidas por la tiroides) son esenciales para el metabolismo y la función cerebral. Tanto el hipotiroidismo (producción baja) como el hipertiroidismo (producción alta) afectan el cerebro:
| Condición | Síntomas Neurológicos/Cognitivos Comunes | Posibles Mecanismos |
|---|---|---|
| Hipotiroidismo | Fatiga severa, pensamiento lento, problemas de memoria, dificultad de concentración, depresión, apatía. | Metabolismo cerebral reducido, alteraciones en la neurotransmisión, cambios estructurales. |
| Hipertiroidismo | Fatiga (por exceso de gasto), pensamiento acelerado, inquietud, ansiedad, nerviosismo, irritabilidad, temblores. | Aumento del metabolismo cerebral, sobreestimulación del sistema nervioso. |
El tratamiento del desequilibrio tiroideo, generalmente con medicación para normalizar los niveles hormonales, es crucial para restaurar la función cognitiva y la estabilidad emocional.
El Estrógeno y sus Efectos en el Cerebro
El estrógeno, especialmente relevante en mujeres, influye en la función cognitiva, el estado de ánimo y la salud neurológica. Afecta la producción de serotonina y dopamina, modulando el humor. Niveles bajos pueden contribuir a la ansiedad y depresión. Es crucial para la formación de memoria y el aprendizaje, promoviendo la neuroplasticidad. La disminución del estrógeno durante la menopausia puede causar niebla mental y problemas de memoria. Existe una correlación entre los niveles de estrógeno y el riesgo de enfermedades neurodegenerativas como Parkinson y Alzheimer.
Las opciones para equilibrar los niveles de estrógeno incluyen terapia de reemplazo hormonal (TRH), ajustes en el estilo de vida (dieta, ejercicio, manejo del estrés) y el uso de fitoestrógenos o suplementos.
Tabla Comparativa: Neurotransmisores vs. Neuropéptidos/Neurohormonas
| Característica | Neurotransmisores Clásicos | Neuropéptidos/Neurohormonas |
|---|---|---|
| Naturaleza Química | Moléculas pequeñas (aminoácidos, aminas, etc.) | Péptidos (cadenas de aminoácidos) |
| Empaquetamiento | Pequeñas vesículas sinápticas | Grandes vesículas de núcleo denso |
| Sitio Principal de Liberación | Terminal sináptico | Terminales sinápticos, varicosidades axonales, dendritas, soma |
| Acoplamiento a la Actividad Eléctrica | Estrecho, alta probabilidad por potencial de acción | Variable, baja probabilidad por potencial de acción, influenciado por otros factores |
| Mecanismo de Acción Principal | Receptores postsinápticos (acción local y rápida) | Receptores (sinápticos, extrasinápticos, en otras células). Acción paracrina, autocrina, neurohormonal (distancia, volumen, lenta/prolongada) |
| Eliminación | Recaptación, degradación enzimática rápida | Degradación enzimática más lenta, difusión |
| Funciones Típicas | Transmisión rápida de señales (excitación/inhibición), procesamiento de información | Modulación de la excitabilidad, regulación de la expresión génica, plasticidad, comportamiento complejo, funciones endocrinas |
Preguntas Frecuentes
¿La neurociencia incluye el estudio de las hormonas?
¡Absolutamente! La neurociencia moderna, especialmente a través del campo de la neuroendocrinología, estudia intensamente la interacción entre el sistema nervioso y el sistema endocrino, incluyendo cómo las hormonas afectan el cerebro y cómo el cerebro regula la función endocrina.
¿Cuál es la diferencia entre un neurotransmisor y una neurohormona?
La principal diferencia radica en su modo de acción y distancia de viaje. Los neurotransmisores actúan localmente y rápidamente en sinapsis cercanas. Las neurohormonas son liberadas por neuronas pero viajan a través del torrente sanguíneo (o LCR) para actuar en células diana distantes, de forma similar a las hormonas endocrinas clásicas, con efectos más prolongados.
¿Cómo afectan los desequilibrios hormonales a mi cerebro y mi estado de ánimo?
Los desequilibrios hormonales pueden tener efectos profundos. Pueden alterar la función de los neurotransmisores, afectar la conectividad neuronal y modificar la expresión génica, lo que se manifiesta en síntomas como dificultad de concentración, problemas de memoria, fatiga, ansiedad, depresión, irritabilidad y trastornos del sueño.
¿Los neuropéptidos son solo otro tipo de neurotransmisor?
No, aunque a veces se liberan en sinapsis, los neuropéptidos tienen características distintas. Se empaquetan y liberan de manera diferente (a menudo fuera de las sinapsis), actúan a través de mecanismos de difusión (transmisión de volumen) y tienen un rango de funciones más amplio que los neurotransmisores clásicos, incluyendo la modulación a largo plazo de la función celular y la expresión génica.
Conclusión
Lejos de ser disciplinas separadas, la neurociencia y la endocrinología están intrínsecamente entrelazadas. El cerebro es un órgano endocrino en sí mismo, produciendo y respondiendo a una vasta gama de péptidos y hormonas que regulan no solo funciones corporales distantes, sino también aspectos fundamentales de la función neuronal, el comportamiento y la cognición. Comprender el papel multifacético de los neuropéptidos y neurohormonas, sus diversos modos de liberación y acción (autocrina, paracrina, neurohormonal) y cómo sus desequilibrios afectan nuestra salud neurológica y mental es fundamental para una visión completa de la biología del cerebro. La conexión entre el cerebro y las hormonas es una avenida vital para futuras investigaciones y estrategias terapéuticas.
Si quieres conocer otros artículos parecidos a Neurociencia y Hormonas: Una Conexión Vital puedes visitar la categoría Neurociencia.
