Cada vez que tomamos un medicamento, pocas veces nos detenemos a pensar en el increíble y extenso viaje que ha recorrido para llegar hasta nosotros. El proceso de Descubrimiento de Fármacos y desarrollo es una odisea científica y logística que puede durar más de una década y costar miles de millones de dólares. Su objetivo es constante: encontrar nuevas medicinas y vacunas capaces de curar o paliar las innumerables enfermedades que aún afectan a la humanidad.

Este proceso no es lineal ni sencillo. Implica múltiples fases y acciones, desde la concepción inicial de una idea terapéutica hasta su desarrollo, pruebas exhaustivas y, finalmente, la aprobación por parte de las autoridades sanitarias. A lo largo de este artículo, desglosaremos las etapas clave, los desafíos inherentes y algunos aspectos cruciales de cómo una sustancia activa se convierte en un medicamento seguro y eficaz disponible en el mercado.
- ¿Qué Implica el Proceso de Descubrimiento de Fármacos?
- Las Cuatro Fases Principales del Desarrollo de Fármacos
- Consideraciones Cruciales en el Proceso
- Carreras en el Campo del Desarrollo de Fármacos
- Los Pilares de la Consultoría en Desarrollo de Fármacos
- Preguntas Frecuentes sobre el Desarrollo de Fármacos
- ¿Cuánto tiempo toma desarrollar un fármaco nuevo?
- ¿Cuánto cuesta investigar y desarrollar un fármaco nuevo?
- ¿Por qué es importante reducir las pruebas en animales?
- ¿Cuáles son las cuatro etapas principales del proceso?
- ¿Qué estudios se realizan en la fase preclínica?
- ¿Qué se busca en cada fase clínica (I, II, III)?
- Conclusión
¿Qué Implica el Proceso de Descubrimiento de Fármacos?
El proceso de descubrimiento de un nuevo fármaco es notablemente largo y desafiante, pudiendo extenderse hasta por 13 años o más. Comienza, típicamente, con la identificación de compuestos que podrían tener un efecto terapéutico sobre una enfermedad específica. Una vez identificados estos candidatos iniciales, se someten a pruebas rigurosas para determinar su seguridad y eficacia.
La tasa de éxito en este campo es desalentadoramente baja. Se estima que, de cada 5,000 a 10,000 candidatos a fármacos que entran en las fases tempranas, solo unos 250 llegan a las pruebas preclínicas. Y la cifra se reduce drásticamente: solo 1 de cada 5,000 compuestos iniciales logra obtener la aprobación para salir al mercado. Este bajo porcentaje subraya la dificultad y la magnitud del desafío.
Las Cuatro Fases Principales del Desarrollo de Fármacos
El proceso puede dividirse en cuatro etapas principales, cada una con sus propios objetivos y metodologías:
- Descubrimiento Temprano (Early Drug Discovery)
- Fase Preclínica
- Fases Clínicas
- Aprobación Regulatoria
Exploremos cada una de ellas en detalle.
Fase 1: Descubrimiento Temprano
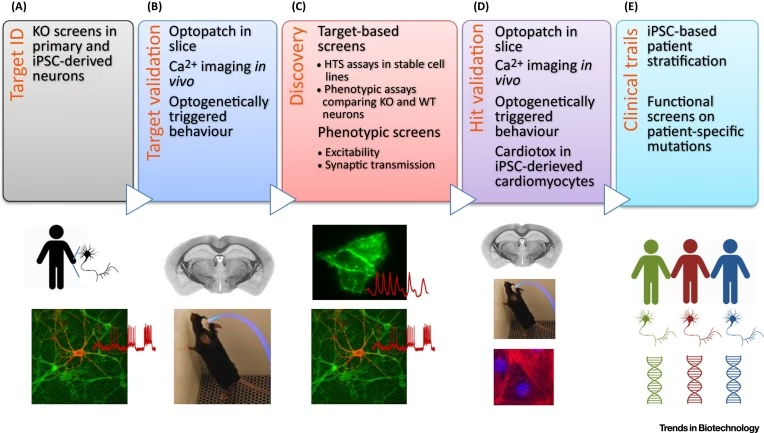
Esta fase inicial es donde se siembran las semillas de las futuras medicinas. Investigadores de diversas disciplinas colaboran para identificar y optimizar posibles candidatos que actúen sobre un objetivo biológico específico implicado en una enfermedad. Este objetivo debe ser 'drogable', es decir, susceptible de ser modificado por una molécula terapéutica ('hit'). La investigación se realiza principalmente en laboratorio, utilizando plataformas computacionales (in silico), ensayos bioquímicos, cultivos celulares y modelos animales.
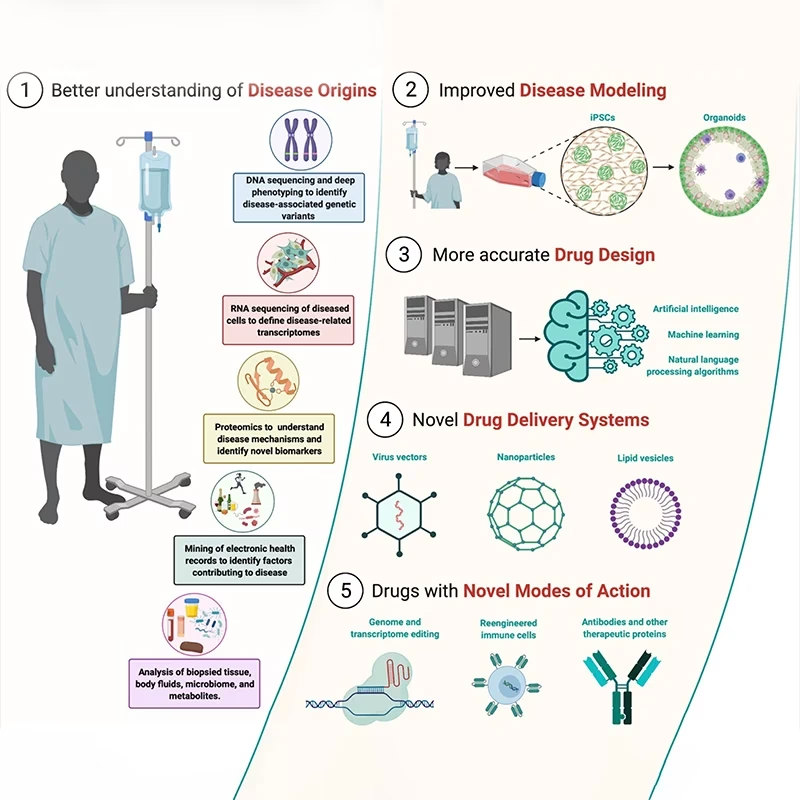
Dentro de esta fase, se suceden varios pasos:
- Identificación y Validación del Objetivo: Comprender la patogénesis de la enfermedad es crucial. Se identifican posibles objetivos (proteínas, genes, etc.) a través de bases de datos y literatura científica, y se valida su relevancia para la enfermedad.
- Cribado de Alto Rendimiento (HTS) o de Alto Contenido (HCS): Se examina un gran número de moléculas para encontrar aquellas que interactúan con el objetivo validado. Se desarrollan ensayos específicos (assays) que permiten probar rápida y fiablemente la efectividad y selectividad de las moléculas. HCS ofrece datos más ricos que HTS.
- Identificación del 'Hit': Se identifica la molécula que interactúa con el objetivo y muestra un efecto terapéutico deseado.
- Desarrollo y Cribado de Ensayos: Se perfeccionan los métodos de prueba. HCS, por ejemplo, utiliza microscopía de alto rendimiento con modelos celulares in vitro o embriones de pez cebra para obtener imágenes detalladas y evaluar múltiples parámetros.
- De 'Hit' a 'Lead' (H2L): Los 'hits' iniciales se refinan y se seleccionan los más prometedores, llamados 'leads'. Se busca mejorar sus propiedades utilizando diversas técnicas de cribado.
- Generación y Optimización de 'Leads': Los 'leads' seleccionados son modificados químicamente para mejorar su efectividad, reducir la toxicidad y optimizar la absorción.
- Ensayos In vivo e In vitro: Los compuestos potenciales se prueban en condiciones que simulan sistemas vivos, utilizando modelos animales, modelos alternativos (como el Pez Cebra) o cultivos celulares para evaluar seguridad y toxicidad.
Fase 2: Fase Preclínica
En esta etapa, las sustancias identificadas en el descubrimiento temprano se refinan, optimizan y prueban extensivamente en laboratorio y en modelos animales o alternativos. El objetivo primordial es obtener evidencia sólida de su seguridad y eficacia antes de que puedan ser administradas a seres humanos en ensayos clínicos. También se utiliza para calcular las dosis adecuadas para los estudios en humanos.
Las autoridades regulatorias exigen estudios preclínicos exhaustivos antes de permitir la presentación de una solicitud de fármaco en investigación (IND, por sus siglas en inglés) para avanzar a las Fases Clínicas. Además de las pruebas, en esta fase se debe asegurar que la producción del compuesto pueda escalar significativamente para satisfacer la demanda de las fases clínicas.
Fase 3: Fases Clínicas
Esta es la etapa donde el fármaco candidato se prueba en seres humanos. Las fases clínicas se dividen en cuatro etapas secuenciales:
- Fase I: Se prueba la seguridad y tolerancia del fármaco en un pequeño grupo de voluntarios sanos (generalmente 20 a 80 personas). Se busca determinar cómo se absorbe, distribuye, metaboliza y excreta el fármaco en el cuerpo (farmacocinética) y qué efectos tiene en el cuerpo (farmacodinámica). El ingrediente activo debe fabricarse bajo condiciones de Buenas Prácticas de Manufactura (GMP).
- Fase II: Si el fármaco es seguro, se prueba en un grupo más grande de pacientes (generalmente 100 a 500) que padecen la enfermedad objetivo. Se evalúa la efectividad, la tolerabilidad y se busca determinar la dosis óptima. Las fases IIa (prueba de concepto) y IIb (determinación de dosis) pueden distinguirse.
- Fase III: Si el fármaco muestra ser efectivo y seguro en la Fase II, se prueba en un grupo aún mayor de pacientes (cientos o miles) para confirmar la efectividad y seguridad en una población más diversa. Se buscan efectos secundarios raros y se estudian las interacciones con otros medicamentos. Estas suelen ser estudios controlados, donde se compara el nuevo fármaco con un placebo o el tratamiento estándar actual.
- Fase IV (Monitoreo Post-Comercialización): Una vez que el fármaco es aprobado, se sigue monitoreando su seguridad y efectividad en una población más amplia de pacientes. Se recopilan datos a largo plazo, se comparan con otros tratamientos disponibles y se registran eventos adversos para asegurar que el perfil riesgo-beneficio se mantenga favorable.
Análisis de Farmacocinética y Farmacodinámica (PK/PD) y la Validación de Métodos Bioanalíticos son procesos continuos durante las fases clínicas y preclínicas, cruciales para entender cómo el cuerpo maneja el fármaco y cómo el fármaco afecta al cuerpo, y para medir con precisión la concentración del fármaco en matrices biológicas.
Fase 4: Aprobación Regulatoria
Una vez completadas las Fases Clínicas con resultados positivos, todos los datos recopilados se presentan a las autoridades regulatorias competentes (como la FDA en Estados Unidos o la EMA en Europa). Estas agencias revisan minuciosamente toda la información para decidir si el fármaco es seguro y efectivo para su uso previsto. La aprobación se basa en un análisis exhaustivo del perfil riesgo-beneficio: los beneficios deben superar los riesgos conocidos o potenciales.
Este procedimiento es muy exigente y requiere una documentación extensa. Si se otorga la aprobación, se genera un documento clave: el 'Resumen de las Características del Producto' (Summary of Product Characteristics), que contiene toda la información esencial para médicos y pacientes sobre el uso, dosificación, contraindicaciones, interacciones y efectos secundarios del fármaco. El monitoreo post-comercialización (Fase IV) es continuo, y si el perfil riesgo-beneficio cambia significativamente, la Aprobación Regulatoria puede verse afectada, llegando incluso a la retirada del mercado.
Consideraciones Cruciales en el Proceso
El Costo y Tiempo del Desarrollo
Llevar un fármaco desde el descubrimiento hasta el mercado es una empresa extremadamente Costosa. Se estima que el costo promedio de investigación y desarrollo (I+D) de un nuevo fármaco ronda los 2.6 mil millones de dólares, según estudios. A esto se suman los costos de monitoreo y desarrollo post-comercialización, que pueden ascender a otros 312 millones de dólares, elevando el costo total del ciclo de vida del I+D a unos 3 mil millones por fármaco. Este elevado costo, sumado al largo tiempo requerido, explica en parte el precio de los medicamentos.

Reducción de Pruebas en Animales y Modelos Alternativos
Antes de probar cualquier candidato a fármaco en humanos, su efectividad y tolerancia deben demostrarse en cultivos celulares (in vitro) y en modelos animales (in vivo). Sin embargo, hay un esfuerzo creciente por reducir y refinar el uso de animales en la investigación, motivado tanto por razones éticas como por la eficiencia en tiempo y Costo. Modelos alternativos, como el Pez Cebra, han ganado relevancia.
Los embriones y larvas de Pez Cebra son transparentes, lo que permite a los investigadores observar sus órganos internos sin necesidad de procedimientos invasivos. Son fáciles de cultivar, se alojan en grandes grupos, producen gran cantidad de huevos y se desarrollan rápidamente. Tienen una alta homología genética con los humanos (70% de los genes, 84% de los genes relacionados con enfermedades), lo que los convierte en un excelente modelo para estudios preclínicos, incluyendo toxicidad y silenciamiento génico.
El uso del Pez Cebra se alinea con las directrices de las 3Rs (Reemplazo, Reducción y Refinamiento) en la ética del uso de animales en experimentos:
- Reemplazo: Se utilizan embriones y larvas en lugar de roedores; legalmente, no se consideran experimentos in vivo hasta los 5 días post-fertilización.
- Reducción: Permiten trabajar con grandes tamaños de muestra a bajo Costo y realizar cribados de alto contenido.
- Refinamiento: Su transparencia permite monitorear y examinar sin causar daño.
Carreras en el Campo del Desarrollo de Fármacos
Para aquellos apasionados por la ciencia, el trabajo de laboratorio y la posibilidad de impactar la salud humana, una carrera como científico farmacéutico puede ser ideal. Estos profesionales investigan, descubren, desarrollan y prueban fármacos. Sus tareas varían pero suelen incluir la recopilación y análisis de datos preclínicos, el diseño y ejecución de experimentos, la optimización de compuestos y la colaboración con equipos multidisciplinarios.
El camino típico para convertirse en científico farmacéutico incluye:
- Explorar Intereses: Tener una curiosidad innata por los sistemas vivos, la salud y la enfermedad.
- Educación: Completar una licenciatura en un área relacionada (como Ciencias Farmacéuticas). Cada vez más, los empleadores prefieren candidatos con maestría o doctorado (PhD) en áreas como Ciencias Farmacéuticas, Biofarmacéutica, Farmacología o Química Medicinal, ya que demuestran la capacidad de manejar conceptos más complejos.
- Desarrollar Habilidades: Adquirir tanto habilidades de laboratorio ('wet lab experimentation') como 'habilidades blandas' (pensamiento crítico, análisis de datos, organización, comunicación, trabajo en equipo), que son cruciales en un entorno colaborativo.
- Ganar Experiencia: Participar en pasantías, cooperativas y otras formas de aprendizaje experiencial durante los estudios para construir el currículum y establecer contactos en la industria.
Los Pilares de la Consultoría en Desarrollo de Fármacos
Dada la complejidad del proceso, muchas empresas farmacéuticas y biotecnológicas recurren a servicios de consultoría especializada para optimizar el desarrollo, minimizar riesgos y acelerar los plazos. Estos servicios suelen agruparse en cinco 'pilares':
- Cumplimiento y Estrategia Regulatoria: Navegar por los complejos requisitos de agencias como FDA o EMA, desarrollar hojas de ruta para la aprobación.
- Diseño y Gestión de Ensayos Clínicos: Diseñar ensayos que cumplan con estándares científicos y regulatorios, gestionar la ejecución, reclutamiento de pacientes y recolección de datos.
- Investigación y Desarrollo Preclínico: Guiar estudios in vitro e in vivo, asegurar el cumplimiento de Buenas Prácticas de Laboratorio (GLP).
- Química, Fabricación y Controles (CMC): Desarrollar procesos de fabricación escalables y conformes, asegurar la calidad del ingrediente activo y el producto final.
- Acceso al Mercado y Comercialización: Estrategias de precios, reembolso, y posicionamiento para que el fármaco llegue a los pacientes.
Estos pilares representan áreas críticas de experiencia necesarias para transformar ideas innovadoras en terapias aprobadas y comercializables.
Preguntas Frecuentes sobre el Desarrollo de Fármacos
¿Cuánto tiempo toma desarrollar un fármaco nuevo?
Puede tomar más de 10 años, a menudo hasta 13 años, desde el descubrimiento inicial hasta la aprobación regulatoria.
¿Cuánto cuesta investigar y desarrollar un fármaco nuevo?
Se estima que el Costo promedio de I+D es de alrededor de 2.6 mil millones de dólares, con costos adicionales post-comercialización que elevan el total a cerca de 3 mil millones por fármaco.
¿Por qué es importante reducir las pruebas en animales?
Reducir las pruebas en animales responde a directrices éticas (las 3Rs) y también puede ahorrar tiempo y Costos en el proceso de investigación, utilizando modelos alternativos más eficientes.
¿Cuáles son las cuatro etapas principales del proceso?
Las cuatro etapas son: Descubrimiento Temprano, Fase Preclínica, Fases Clínicas y Aprobación Regulatoria.
¿Qué estudios se realizan en la fase preclínica?
Se realizan pruebas extensivas de seguridad y eficacia en laboratorio (in vitro) y en modelos animales o alternativos (in vivo) para obtener evidencia suficiente antes de pasar a pruebas en humanos.
¿Qué se busca en cada fase clínica (I, II, III)?
Fase I: Seguridad y tolerancia en voluntarios sanos. Fase II: Efectividad, tolerabilidad y determinación de dosis en pacientes. Fase III: Confirmación de efectividad y seguridad en una población grande de pacientes, identificación de efectos secundarios raros e interacciones.
Conclusión
El camino que recorre un fármaco desde una idea en un laboratorio hasta una píldora en nuestra mano es extraordinariamente largo, caro y lleno de obstáculos científicos y regulatorios. Es un testimonio del esfuerzo colaborativo de miles de científicos, médicos y profesionales de diversas áreas. Comprender este proceso nos permite apreciar la complejidad y el valor de las medicinas que hacen posible una mejor calidad de vida para millones de personas en todo el mundo.
Si quieres conocer otros artículos parecidos a El Viaje de un Fármaco: Del Laboratorio al Paciente puedes visitar la categoría Neurociencia.
