En la era postgenómica, un campo emergente y de rápido crecimiento está redefiniendo nuestra comprensión de la herencia y la biología: la epigenética. Este término, acuñado por Conrad Waddington en el siglo XX, se refiere a los cambios heredables en la expresión génica que no implican alteraciones en la secuencia de bases del ADN. Es, en esencia, la rama de la biología que estudia las interacciones causales entre los genes y sus productos, y cómo estas dan lugar al fenotipo de un organismo. La epigenética nos muestra que la herencia es mucho más compleja que la simple transmisión de la secuencia de ADN.
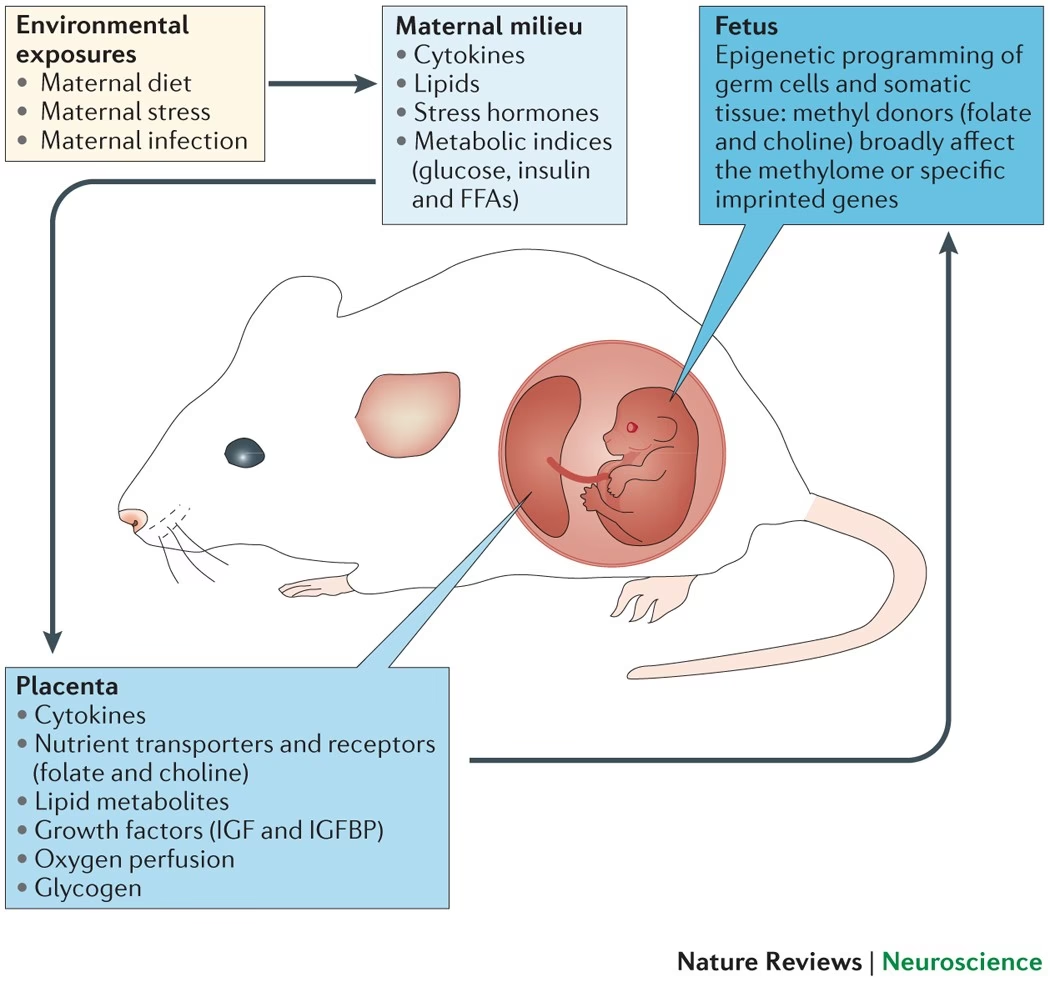
La idea de que la evolución puede favorecer mecanismos de autoguía que maximicen la variabilidad cuando es útil y la minimicen cuando no lo es, una predicción implícita tanto en las teorías de Darwin como de Lamarck, encuentra eco en la epigenética. Esta regulación media la adaptación al entorno, otorgando al genoma una plasticidad que se traduce en el fenotipo observable, especialmente bajo condiciones ambientales 'desajustadas'.
- Los Mecanismos Moleculares de la Epigenética
- Cromatina: El Estado que Define la Expresión
- Reprogramación Epigenética: Un Proceso Dinámico
- El Papel Emergente de los ARN no Codificantes
- Epigenética en Acción: Impacto Biológico y Clínico
- Tecnologías y Desafíos en la Investigación Epigenética
- Terapias Epigenéticas: Una Nueva Frontera Médica
- Adaptación Heredable: La Epigenética como Ciencia
- Preguntas Frecuentes sobre Epigenética
Los Mecanismos Moleculares de la Epigenética
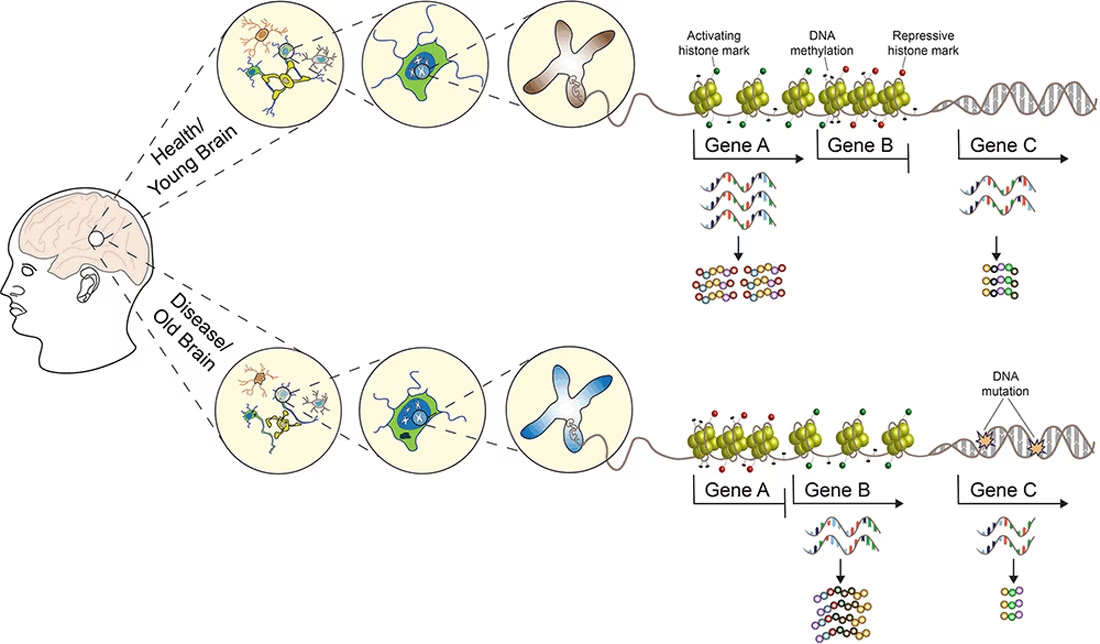
La investigación epigenética se centra principalmente en demostrar modificaciones químicas tanto en la secuencia del ADN como en las proteínas histonas nucleares. Estas modificaciones, a su vez, alteran la configuración de la cromatina, afectando su empaquetamiento y accesibilidad dentro del núcleo celular. El estado de la cromatina es fundamental para la transcripción de los genes.
Metilación del ADN: Silenciando Genes con Marcas Químicas
Una de las modificaciones epigenéticas más estudiadas es la metilación de citosina en los dinucleótidos CpG. Estos cúmulos de CpG, a menudo encontrados cerca de elementos cis-reguladores importantes dentro de los promotores génicos, pueden silenciar un gen cuando se metilan en la posición 5 del carbono. Enzimas como las ADN metiltransferasas (Dnmt1, 3a, 3b) son responsables de esta metilación, y proteínas de dominio de unión a metilo (MBD 1, 2, 3) o proteínas de unión a metil CpG (MeCP 1, 2) son necesarias para mediar o modificar esta reacción. El ADN metilado atrae proteínas de unión a cromodominio (como la proteína de heterocromatina, HP1) que ayudan a mantener un estado de heterocromatina.
La complejidad aumenta con las interacciones de cromatina de largo alcance que pueden no ser evidentes al examinar solo la región promotora. Generalmente, los CpG en regiones ricas en GC y libres de repeticiones Alu dentro de un promotor no están metilados y se conservan entre especies, mientras que los CpG dentro o cerca de transposones o repeticiones suelen estar metilados. El metabolismo de un carbono de los mamíferos proporciona los grupos metilo para todas las reacciones biológicas de metilación, dependiendo de donantes de metilo (metionina, colina) y cofactores (ácido fólico, vitamina B12, piridoxal fosfato).
Ejemplos de regiones del genoma que llevan CpG metilados, vistas en el centrómero o en las regiones de control de impronta (ICRs), caracterizadas por regiones diferencialmente metiladas (DMRs), se denominan "marcas de metilación". Estas improntas, que resultan en el silenciamiento génico, se observan en transposones, la inactivación del cromosoma X y genes con impronta parental que causan expresión monoalélica (como los genes IGF 2, receptor de IGF2, Peg).
Modificaciones de Histonas: El Código de la Cromatina
La estructura de la cromatina se basa en el empaquetamiento del ADN mediante su asociación con proteínas histonas. La unidad básica, el nucleosoma, consiste en 147 pares de bases de ADN envueltos alrededor de un núcleo octamérico de histonas (dos copias de H2A, H2B, H3, H4), compactado aún más por la histona enlazadora H1 y otras proteínas no histonas, formando la fibra de cromatina (10-30 nm) con estructuras de orden superior dentro del núcleo.
La organización de la cromatina no solo limita el acceso físico de las proteínas nucleares al ADN subyacente, sino que las modificaciones postraduccionales de las proteínas histonas pueden alterar su conformación mediante procesos de remodelación dependientes de ATP y jugar roles reguladores directos en la expresión génica. Existe una gran diversidad de modificaciones, como acetilación, fosforilación, metilación, deiminación, ubiquitinación, sumoilación, ADP-ribosilación e isomerización de prolina. Algunas, como la acetilación, fosforilación y ubiquitinación, están implicadas en la activación, mientras que otras como la metilación, ubiquitinación, sumoilación, deiminación e isomerización de prolina, lo están en la represión. Sin embargo, cualquier modificación puede activar o reprimir la transcripción dependiendo de su ubicación específica. Por ejemplo, la metilación en la lisina 36 de la histona H3 (H3.K36) o H3.K9 en la región codificante activa, mientras que en la región promotora reprime la expresión génica.
Modificaciones que alteran la carga, como la acetilación (mediada por histona acetiltransferasas - HATs) y la desacetilación (mediada por histona desacetilasas - HDACs), o la fosforilación (por quinasas) y desfosforilación (por fosfatasas), son reversibles, dinámicas y se asocian a la expresión inducible de genes individuales. Otras modificaciones, como la metilación, se consideraban más estables hasta el descubrimiento de las enzimas desmetilasas (LSD1, enzimas con dominio JmjC como JHDM). Estas modificaciones ocurren en residuos de aminoácidos específicos de las colas N-terminales de las histonas, sugiriendo que actúan como plataformas de señalización que integran vías de señalización para elicitar respuestas nucleares apropiadas.
Las HATs (ej., CBP/p300) reclutan proteínas activadoras, mientras que las HDACs reclutan metilasas (ej., Suv39H1) o histona metiltransferasas (HMTs; ej., Sin3A, EZH2, SETDB1) y la proteína con cromodominio HP1, que juegan un papel importante en el silenciamiento génico y el mantenimiento de la heterocromatina.
La metilación de lisinas (K) puede activar o reprimir genes según el residuo: H3.K4 activa, H3.K9 desactiva. H3.K4 y H3.K36 están implicadas en la elongación de la transcripción, mientras que H3.K9, H3.K27 y H4.K20 están conectadas con la represión. La metilación puede ser mono-, di- o tri- para lisinas, y mono- o di- para argininas, añadiendo diversidad funcional.
Existe evidencia de un "código combinatorio" en el que la fosforilación de serina 10 de H3 inhibe, mientras que la desacetilación de lisina 14 facilita la metilación de lisina 9, lo que a su vez silencia la transcripción. La metilación de arginina (por CARM1, PRMTs) también puede activar o reprimir. La deiminación convierte argininas en citrulina, previniendo su metilación. La ubiquitinación en H2A y H2B recluta el complejo Polycomb asociado a represión. La sumoilación en H4, H2A, H2B antagoniza otras modificaciones en el mismo residuo, causando represión. La ADP-ribosilación (por MART, PARP) está relacionada con la reparación del ADN. La isomerización de prolina (por FPR4) es necesaria para la metilación de H3.K36. Sin embargo, el descubrimiento de dominios bivalentes con modificaciones tanto activadoras como represoras desafía la visión simplista.
Cromatina: El Estado que Define la Expresión
El estado de la cromatina es un factor determinante en la accesibilidad del ADN a la maquinaria transcripcional. Se distinguen principalmente dos estados:
| Característica | Heterocromatina | Eucromatina |
|---|---|---|
| Compactación | Muy empaquetada | Relativamente laxa |
| Accesibilidad del ADN | Impedida | Permitida |
| Estado de Transcripción | Generalmente inactiva (silenciada) | Activa |
| Asociación con HP1 | Sí (mantiene el estado) | No |
| Metilación del ADN (CpG) | Alta en regiones repetidas/promotores silenciados | Baja en promotores activos |
| Modificaciones de Histonas | Marcas represivas (ej. H3K9me, H3K27me) | Marcas activadoras (ej. H3K4me, H3K9ac) |
Mientras que la heterocromatina significa una cromatina fuertemente enrollada que impide el acceso de proteínas nucleares a secuencias específicas, inhibiendo la transcripción génica, la eucromatina es un estado activo donde la cromatina laxamente enrollada permite la unión de proteínas activadoras a la región promotora de los genes, resultando en transcripción activa. Sin embargo, este concepto simple se complica por el transporte nuclear, la compleja disposición nuclear de la cromatina, y el reclutamiento de enzimas y proteínas a los complejos de iniciación de la transcripción.
Reprogramación Epigenética: Un Proceso Dinámico
El genoma de las células germinales primordiales inmaduras del embrión en desarrollo (cigoto y blastómeros) experimenta una extensa desmetilación. Este proceso es crucial para permitir la totipotencia y borrar las marcas de metilación que reprimen el programa somático. Posteriormente, se restablecen patrones apropiados de metilación de citosina, dependientes del sexo, durante la gametogénesis, preparando el escenario para la pluripotencia. Esta pluripotencia se mantiene durante el desarrollo embrionario a través de múltiples rondas de rápida proliferación celular (mitosis) hasta la diferenciación celular final.
El restablecimiento de las improntas de metilación ocurre durante el desarrollo fetal tardío en células germinales masculinas y posnatalmente en las femeninas. El genoma masculino está altamente condensado, en parte por la unión de protaminas que son rápidamente reemplazadas por histonas, un proceso que requiere chaperonas de histonas (Hira) y ocurre antes de la fase S. Aunque el genoma femenino debe desmetilarse, ciertos factores (Stella) lo protegen de la desmetilación masiva.
Cualquier alteración en estos procesos finamente equilibrados puede perturbar el fenotipo final. Se han aprendido lecciones del aumento en la incidencia de trastornos de impronta génica dependientes del progenitor, como los síndromes de Beckwith-Wiedemann y Angelman, reportados en productos de tecnologías de reproducción asistida (TRA). Esto ha llevado a teorías contradictorias sobre si la etiología se debe a la tecnología en sí o a la presencia innata de defectos de impronta en los gametos de individuos subfértiles. Otras afecciones como los síndromes de Prader-Willi, Russel-Silver y la diabetes mellitus neonatal también implican metilación génica diferencial dependiente del progenitor. De manera similar, las molas hidatiformes que afectan la placenta también se deben a la expresión alterada de ciertos genes con impronta.
El Papel Emergente de los ARN no Codificantes
Además de las modificaciones en el ADN y las histonas, los ARN no codificantes pequeños también pueden causar silenciamento de la heterocromatina. El procesamiento cotranscripcional produce productos de ARN pequeños responsables de la interferencia de ARN, un mecanismo regulador importante para el silenciamento génico dependiente de homología. El silenciamento génico postranscripcional (PTGS; siRNA, microRNA) y transcripcional (TGS; ARN antisentido) constituyen mecanismos epigenéticos importantes.
El primer precursor de microRNA implicado en la impronta fue H19 en el caso de la expresión del gen IGF 2. El transcripto antisentido no codificante Air se expresa desde un promotor en el intrón 2 del gen receptor de IGF2 en el alelo reprimido paterno, mientras que la copia materna del promotor no es funcional debido a la metilación del ADN. La terminación prematura de la transcripción de Air con impronta conduce a la pérdida del silenciamento del gen receptor de IGF2.
Epigenética en Acción: Impacto Biológico y Clínico
Si bien los estudios epigenéticos se centraron predominantemente en la cromatina y el uso de inhibidores enzimáticos in vitro, investigaciones más recientes han descubierto su significado in vivo, proporcionando un papel funcional para algunos de estos procesos en el contexto de la fisiología y el fenotipo del organismo completo.
Ejemplos notables incluyen:
- El papel del silenciamento génico de genes supresores de tumores (p53) o genes que median la proliferación/apoptosis (vía de señalización Wnt, familia Bcl 2) resultando en la proliferación cancerosa de células y la formación de tumores.
- La influencia de toxinas ambientales que contienen fitoestrógenos o dietilestilbestrol, un agonista del receptor de estrógeno, o el disruptor endocrino vinclozolina, que afectan la estructura de la cromatina y conducen a la desregulación de la función reproductiva, persistiendo hasta la cuarta generación.
- Un papel crucial en el silenciamento y la reprogramación génica durante el desarrollo embrionario.
- Perturbaciones en la metilación del ADN con el envejecimiento.
- La metilación diferencial dependiente del progenitor, junto con la unión de factores nucleares como CTCF al alelo hipometilado, causando un crecimiento desordenado.
- La influencia del estrés temprano que afecta la metilación de genes neuronales específicos que dictan y modifican permanentemente el comportamiento adulto.
- El papel de la nutrición temprana en la transcripción génica que impacta el fenotipo final, detectado por el color del pelaje (gen Agouti) o el desarrollo de enfermedades crónicas (diabetes/obesidad).
- El papel confirmatorio de la regulación epigenética en la herencia estable transgeneracional.
La persistencia transgeneracional de los cambios fenotípicos tendrá profundos efectos epidemiológicos en la salud y la enfermedad.
Además, mutaciones génicas en la proteína de unión a CREB (CBP), una histona acetiltransferasa, subyacen al síndrome de Rubenstein Taybi, y mutaciones en la proteína MeCP2 son responsables del trastorno del neurodesarrollo síndrome de Rett. Otras aberraciones relacionadas podrían subyacer a trastornos mentales como la esquizofrenia. El uso reciente de un modelo de ratón genéticamente manipulado del síndrome de Rett demostró que imponer niveles normales de MeCP2 en las neuronas revirtió el cuadro similar al autismo del síndrome de Rett, proporcionando esperanza para el futuro desarrollo de estrategias de tratamiento dirigidas a esta condición clínica.
Un número creciente de trastornos de crecimiento no genéticos, como la restricción del crecimiento intrauterino, bebés pequeños para la edad gestacional, el bebé extremadamente prematuro, el producto de fertilización in vitro, y el bebé de una madre obesa o diabética, tienen su etiología asociada a la epigenética, ya que las señales ambientales perturban el medio hormonal/metabólico embrionario.
Tecnologías y Desafíos en la Investigación Epigenética
A medida que la tecnología avanza para permitir el cribado a gran escala de regiones de ADN metilado mediante arrays de baldosas (tiling array) o la secuenciación de bisulfito a nivel de todo el genoma, y las perturbaciones covalentes de la cromatina mediante inmunoprecipitación de cromatina (ChIP)-on-chip, es importante ser consciente de las limitaciones de estas técnicas. El sesgo de amplificación juega un papel importante al intentar determinar las citosinas metiladas en el genoma, con una tendencia a pasar por alto las regiones ricas en repeticiones, mientras que el ChIP-on-chip depende de la calidad del anticuerpo detector. Tecnologías más recientes abordan estas limitaciones, como el enfoque de proteómica 'top-down' con espectrometría de masas.
A medida que se obtiene más información en este campo, es fundamental seguir priorizando la comprensión del significado biológico de estos cambios estructurales en la cromatina con una estrategia de "causa y efecto". Muchas preguntas permanecen sin respuesta en relación con el desarrollo normal; por ejemplo, ante la desmetilación, ¿cómo se conservan las marcas de metilación y se transmiten a la siguiente generación? De manera similar, ¿cómo se conservan y transmiten las modificaciones de histonas a la siguiente generación, especialmente ahora que se han identificado desmetilasas? ¿Cómo se transmiten los cambios en la estructura de la cromatina que ocurren en las células progenitoras a las células hijas sin un elemento de dilución?
Terapias Epigenéticas: Una Nueva Frontera Médica
Aunque estas preguntas requieren respuestas, en el campo del cáncer ya se han desarrollado fármacos dirigidos al tratamiento clínico. Estos incluyen agentes que revierten el silenciamento génico, como los fármacos azanucleósidos que inhiben las enzimas ADN metiltransferasas y que están aprobados por la FDA para el síndrome mielodisplásico. Los inhibidores de histona desacetilasa (ej., SAHA) también han sido aprobados por la FDA para el tratamiento del linfoma cutáneo de células T.
El futuro se centra en la capacidad de capitalizar la acción sinérgica de estas dos clases de agentes contra cánceres no susceptibles a la quimioterapia estándar, ya que solo afectan a las células que proliferan de manera anormal y expresan los genes silenciados relevantes.
Adaptación Heredable: La Epigenética como Ciencia
Los cambios estructurales de la cromatina pueden existir pero no traducirse en un fenotipo en ausencia de las señales ambientales necesarias que sirven como presión de selección (ej., dieta, fármaco, toxina, desarrollo o envejecimiento) y que son requeridas para la ventaja de supervivencia y/o la expresión adaptativa. El mejor ejemplo es la presentación fenotípica diferencial de gemelos monocigóticos mayores.
La epigenética es una ciencia de adaptación biológica heredable, un concepto que se vuelve cada vez más evidente y crucial para entender la salud y la enfermedad en su totalidad.
Preguntas Frecuentes sobre Epigenética
¿Qué diferencia la epigenética de la genética clásica?
La genética clásica estudia los cambios en la secuencia del ADN (mutaciones) que afectan la herencia y la expresión génica. La epigenética estudia los cambios heredables en la expresión génica que *no* implican alteraciones en la secuencia del ADN, sino modificaciones químicas en el ADN o las proteínas asociadas (histonas) que alteran la estructura de la cromatina.
¿Cómo influye el ambiente en los cambios epigenéticos?
El entorno, incluyendo factores como la dieta, la exposición a toxinas, el estrés, la nutrición temprana y el envejecimiento, puede inducir modificaciones epigenéticas en el ADN y las histonas. Estas modificaciones pueden alterar la forma en que los genes se activan o desactivan, influyendo en el fenotipo y la susceptibilidad a enfermedades.
¿Los cambios epigenéticos pueden ser heredados?
Sí, por definición, la epigenética se refiere a cambios heredables. La información proporcionada menciona la herencia transgeneracional de ciertos cambios epigenéticos inducidos por factores ambientales, persistiendo en algunas especies hasta varias generaciones.
¿Es posible revertir los cambios epigenéticos?
Algunas modificaciones epigenéticas, como la acetilación y la fosforilación, son dinámicas y reversibles. Incluso la metilación del ADN, que se consideraba más estable, se sabe ahora que puede ser revertida por enzimas desmetilasas. Esto abre la puerta a terapias que busquen modular el estado epigenético.
¿Tiene la epigenética aplicaciones médicas prácticas?
Absolutamente. La investigación epigenética ayuda a entender la base de enfermedades como el cáncer, trastornos del desarrollo y enfermedades metabólicas. Además, se han desarrollado y aprobado fármacos epigenéticos, principalmente para el tratamiento de ciertos tipos de cáncer, que buscan revertir el silenciamento anómalo de genes.
¿Cómo afecta la epigenética al desarrollo embrionario?
El desarrollo embrionario implica una reprogramación epigenética masiva, incluyendo procesos de desmetilación y remetilación, cruciales para establecer la totipotencia y la pluripotencia de las células. Alteraciones en estos procesos pueden resultar en síndromes y trastornos del desarrollo.
Si quieres conocer otros artículos parecidos a Epigenética: Más Allá del ADN puedes visitar la categoría Neurociencia.