La depresión mayor (TDM) es una de las enfermedades psiquiátricas más comunes y desafiantes en la actualidad. Aunque durante mucho tiempo se simplificó como un mero 'desequilibrio químico', la neurociencia moderna ha revelado una complejidad mucho mayor, implicando redes neuronales, plasticidad cerebral y una intrincada interacción de factores biológicos.

Este artículo busca resumir los hallazgos clave de la investigación clínica sobre la neurobiología del TDM y sus implicaciones. Exploraremos la naturaleza progresiva de la enfermedad, los cambios en las estructuras cerebrales, los procesos moleculares subyacentes y cómo los tratamientos antidepresivos buscan restaurar la fisiología normal.

- La Depresión como una Enfermedad Progresiva
- Cambios Estructurales y Funcionales en el Cerebro Deprimido
- Procesos Moleculares Mediadores de los Cambios Neurobiológicos
- El Papel de los Neurotransmisores en la Recuperación del TDM
- Implicaciones del Modelo Neurobiológico para el Tratamiento
- La Depresión desde una Perspectiva Neurocientífica Integrada
- Preguntas Frecuentes sobre Neurociencia y Depresión
La Depresión como una Enfermedad Progresiva
Estudios epidemiológicos han demostrado consistentemente que el TDM tiene una alta tasa de prevalencia a lo largo de la vida. Lo que es particularmente relevante desde una perspectiva neurobiológica es la naturaleza recurrente de la enfermedad. Para muchos pacientes, la recurrencia es la norma, no la excepción. Con cada episodio depresivo, la probabilidad de episodios futuros aumenta.
Esta recurrencia parece estar impulsada, en parte, por vulnerabilidades neurobiológicas. Los pacientes con episodios múltiples a menudo tienen antecedentes familiares de depresión y un inicio más temprano de su primer episodio. La evidencia apoya la 'hipótesis de la sensibilización' ('kindling hypothesis'), sugiriendo que los episodios depresivos pueden volverse más fácilmente desencadenados con el tiempo. A medida que aumenta el número de episodios, la predicción de futuros episodios se basa más en el número de episodios previos que en el estrés vital reciente. Esto indica un posible efecto progresivo de la enfermedad.
Las experiencias adversas tempranas, como el maltrato infantil, también pueden contribuir a alteraciones neurobiológicas a largo plazo asociadas con la depresión, creando una subtipo especialmente vulnerable. La cronicidad de la depresión, definida como episodios de larga duración (más de 2 años), también sugiere consecuencias neurobiológicas a largo plazo. A medida que la duración de los episodios aumenta, la probabilidad de recuperación disminuye sustancialmente. Incluso después de la remisión, un subconjunto significativo de pacientes continúa experimentando síntomas residuales, lo que aumenta el riesgo de recurrencia y sugiere una vulnerabilidad continua debido a un estado de enfermedad activo. Esta perspectiva ha elevado el objetivo del tratamiento de la mera respuesta (reducción de síntomas) a la remisión (ausencia de síntomas) o recuperación (período prolongado de remisión), lo que implica una restauración de la fisiología subyacente.
Cambios Estructurales y Funcionales en el Cerebro Deprimido
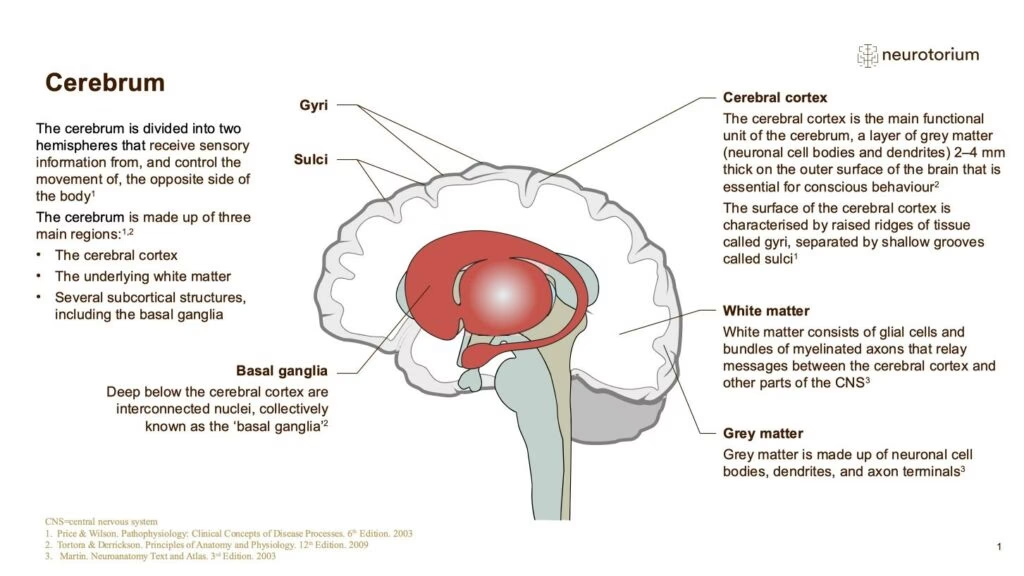
La investigación, particularmente mediante técnicas de neuroimagen, ha comenzado a dilucidar las anomalías neurobiológicas asociadas con el TDM. Se han implicado varias estructuras prefrontales y límbicas, así como sus circuitos interconectados, en la regulación afectiva. Estas áreas incluyen la corteza prefrontal ventromedial (CPFvm), la corteza prefrontal orbital lateral (CPFOL), la corteza prefrontal dorsolateral (CPFdl), la corteza cingulada anterior (CCA), el estriado ventral (incluido el núcleo accumbens), la amígdala y el hipocampo.
Se han observado anomalías en la actividad dinámica entre estas estructuras en pacientes con TDM en comparación con controles sanos. Por ejemplo, estudios de flujo sanguíneo regional sugieren hiperactividad en el CPFvm y CPFOL, y hipoactividad en el CPFdl en pacientes con TDM. Dado que el CPFvm media el dolor, la agresión y la regulación de conductas básicas, y el CPFOL evalúa el riesgo y modula estados afectivos perseverantes, su hiperactividad podría explicar síntomas como rumiaciones depresivas y ansiedad. La hipoactividad del CPFdl, involucrado en la función ejecutiva y la memoria de trabajo, podría manifestarse como retardo psicomotor, apatía y déficits cognitivos.
Los estudios de conectividad funcional también sugieren una disminución en la 'comunicación' entre la amígdala (involucrada en el procesamiento emocional, especialmente el miedo) y la CCA (que monitorea resultados y ajusta el comportamiento/cognición). Una consecuencia de esta pérdida de conectividad podría ser la incapacidad de la CCA para ejercer su papel inhibitorio en la regulación emocional, llevando a una mayor disrupción afectiva y motivacional.
El hipocampo, situado en la intersección de circuitos límbicos, cognitivos/ejecutivos y neuroendocrinos (incluido el eje hipotalámico-hipofisario-adrenal o HHA), parece ser particularmente vulnerable en la depresión. Un hallazgo consistente es la reducción significativa del volumen del hipocampo en pacientes con TDM, que se correlaciona directamente con el número y la duración de los episodios depresivos no tratados. Incluso después de la remisión, los pacientes con TDM recurrente muestran un volumen hipocampal más pequeño. Si bien la herencia y la genética pueden predisponer a diferencias en el volumen hipocampal, los cambios también pueden acumularse durante el curso de la enfermedad, dificultando la recuperación completa.
Tabla Comparativa: Áreas Cerebrales y Cambios en TDM
| Área Cerebral | Función Principal | Cambios Observados en TDM |
|---|---|---|
| Corteza Prefrontal Ventromedial (CPFvm) | Regulación afectiva, dolor, agresión | Hiperactividad |
| Corteza Prefrontal Orbital Lateral (CPFOL) | Evaluación de riesgo, modulación afectiva | Hiperactividad |
| Corteza Prefrontal Dorsolateral (CPFdl) | Función ejecutiva, memoria de trabajo, atención | Hipoactividad |
| Corteza Cingulada Anterior (CCA) | Monitoreo, regulación emocional, motivación | Disminución de conectividad con amígdala, falla en inhibición emocional |
| Amígdala | Procesamiento emocional (miedo) | Hiperreactividad (especialmente izquierda), disminución de conectividad con CCA |
| Hipocampo | Memoria, aprendizaje contextual, regulación HHA | Reducción de volumen, disminución de neuroplasticidad |
| Estriado Ventral (Núcleo Accumbens) | Recompensa, motivación | Alteraciones (implicado en anhedonia) |
Procesos Moleculares Mediadores de los Cambios Neurobiológicos
Las alteraciones en el hipocampo y otras áreas pueden ser el resultado de una retroalimentación perjudicial mediada por la desregulación neuroendocrina. Un hallazgo común en pacientes con TDM son los altos niveles de cortisol, la hormona del estrés. El cortisol elevado puede afectar negativamente la neuroplasticidad y la resistencia celular. Un desequilibrio entre los receptores de glucocorticoides (GR) y mineralocorticoides (MR) en el hipocampo, junto con una alta densidad de GR, puede aumentar la susceptibilidad de esta área al daño neuronal. La atrofia hipocampal resultante podría exacerbar la disfunción neuroendocrina, creando un ciclo vicioso.
Las comparaciones postmortem de tejido cerebral han mostrado encogimiento hipocampal en sujetos deprimidos debido a una mayor densidad celular y una reducción significativa del neurópilo (reducción de ramificaciones dendríticas). Niveles elevados de glucocorticoides y una función hipocampal comprometida también pueden llevar a una desensibilización de los receptores GR, lo que impide que el sistema de retroalimentación negativa 'apague' adecuadamente la respuesta al estrés crónico.
La sobreactividad hipotalámica-hipofisaria-adrenal (HHA), junto con la activación de la amígdala, conduce a un aumento del tono simpático, lo que promueve la liberación de citoquinas de los macrófagos. Un aumento en las citoquinas proinflamatorias se ha asociado con pérdida de sensibilidad a la insulina y los GR, perpetuando la disrupción metabólica y neuroendocrina. Sintomáticamente, estas citoquinas pueden manifestarse como fatiga, pérdida de apetito y libido, e hipersensibilidad al dolor.
Las citoquinas proinflamatorias también pueden disminuir el soporte neurotrófico y la neurotransmisión de monoaminas, lo que puede conducir a apoptosis neuronal y daño glial. Las células gliales, como astrocitos y microglia, interactúan intrincadamente con las neuronas, manteniendo la homeostasis del entorno neuronal. El estrés y la depresión pueden activar la microglia, que libera más citoquinas inflamatorias, exacerbando la disrupción inmune.
Un factor clave en el mantenimiento de estas interacciones glía-neurona es el factor neurotrófico derivado del cerebro (BDNF). Involucrado en la neurogénesis y la plasticidad, el BDNF es el principal neurotrofina del hipocampo. Promueve la resistencia celular y la potenciación a largo plazo al interactuar con los receptores TrkB. Sin embargo, su forma precursora (pro-BDNF) puede inducir reducción de espinas dendríticas y muerte celular al unirse al receptor p75. Así, el BDNF puede podar redes neuronales de manera dependiente de la actividad, regulado por varios neurotransmisores y hormonas.
Estudios preclínicos y clínicos sugieren una desregulación del BDNF en condiciones de estrés crónico y depresión. Los niveles séricos de BDNF son significativamente más bajos en pacientes con TDM no tratados. Los análisis postmortem de cerebros de personas que se suicidaron mostraron BDNF reducido. Esto ha dado lugar a la hipótesis neurotrófica, que postula que el estrés y la vulnerabilidad genética elevan los glucocorticoides y alteran la plasticidad mediante la regulación a la baja de factores de crecimiento como el BDNF. La reducción de BDNF afecta negativamente los procesos estructurales y funcionales dentro del sistema límbico, especialmente el hipocampo. La recuperación del TDM podría depender de la reversión de estos procesos, como un aumento en los niveles de BDNF.
Complementando la hipótesis neurotrófica está la teoría de las monoaminas, que postula que la depresión se asocia con niveles bajos de monoaminas, particularmente serotonina (5-HT) y norepinefrina (NE). Una teoría actualizada sugiere que la pérdida de monoaminas a largo plazo debido a la actividad global de la monoamino oxidasa A (MAO-A), que metaboliza estos neurotransmisores, interactúa con las densidades de transportadores específicas de cada región (5-HT, NE, DA), lo que resulta en la expresión de la enfermedad depresiva. Las fibras ascendentes de 5-HT y NE inervan el sistema límbico y la corteza prefrontal, implicados en la regulación del estado de ánimo. Las vías descendentes regulan el dolor. Dependiendo de las densidades de transportadores en estas regiones, se manifiestan diversos síntomas de depresión (estado de ánimo, cognición, dolor) en el contexto de la reducción global de monoaminas.
El Papel de los Neurotransmisores en la Recuperación del TDM
Terapéuticamente, los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de norepinefrina (IRSN) aumentan los niveles de sus respectivas monoaminas en el cerebro. El tratamiento crónico con estos inhibidores aumenta la activación del AMP cíclico (cAMP), lo que a su vez estimula la proteína quinasa A. Esta enzima regula genes diana, lo que lleva a un aumento en la síntesis de BDNF. La actividad del cAMP inducida por antidepresivos también puede mejorar la sensibilidad de los GR e inhibir la señalización de citoquinas, ayudando a restaurar los circuitos de retroalimentación neurobiológica.
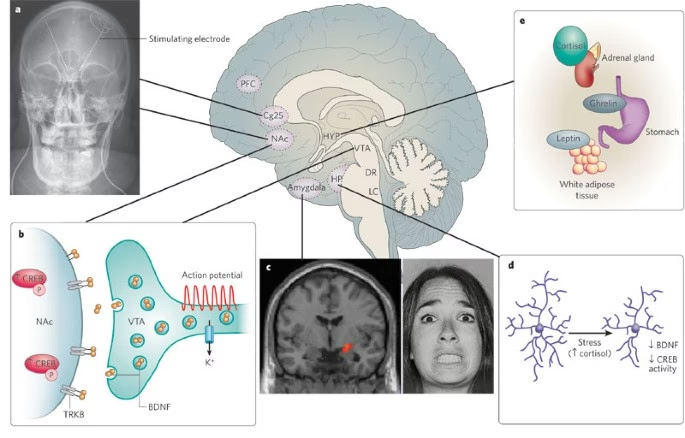
El aumento de los niveles de monoaminas (dopamina, 5-HT y NE) y su efecto sobre el BDNF y los factores de crecimiento pueden ser un mecanismo clave de la respuesta antidepresiva. Estudios preclínicos demuestran que la actividad monoaminérgica (NE, 5-HT) regula positivamente la síntesis de BDNF en astrocitos. Clínicamente, el tratamiento exitoso con antidepresivos normaliza los niveles séricos de BDNF. La respuesta a varios ISRS e IRSN se ha asociado de manera similar con la restauración de los valores normativos de BDNF.
La respuesta terapéutica a los antidepresivos también se asocia con el restablecimiento de la actividad cortical normativa. Estudios de neuroimagen funcional han mostrado que los pacientes que responden al tratamiento con ISRS exhiben una inversión de patrones iniciales de actividad, con disminución de la actividad límbica y aumento de la actividad cortical prefrontal. La normalización en la amígdala y la CCA también se asocia con una respuesta positiva al tratamiento. La restauración de la regulación neurobiológica en el TDM a través de factores neurotróficos y neurogénesis parece ser un factor común en varios tratamientos efectivos, incluidos los farmacológicos, psicológicos y somáticos (como la dieta y el ejercicio).
Implicaciones del Modelo Neurobiológico para el Tratamiento
Las secuelas neurobiológicas de la depresión crónica o recurrente sugieren que las intervenciones deben centrarse en lograr un tratamiento óptimo de manera temprana. Los estudios longitudinales muestran que uno de los mejores predictores del estado de remisión a 2 años fue la respuesta al tratamiento agudo (las primeras 6 semanas). La adecuación del tratamiento inicial también tiene implicaciones pronósticas; los ensayos previos inadecuados pueden reducir las tasas de respuesta a tratamientos posteriores.
Una forma de maximizar la respuesta temprana es aplicar un tratamiento integral que aumente la actividad de múltiples sistemas monoaminérgicos. Estudios comparativos sugieren una modesta pero significativa ventaja en la eficacia con los IRSN (que afectan tanto a la serotonina como a la norepinefrina) en comparación con los ISRS, especialmente en poblaciones de pacientes hospitalizados o crónicos. Apuntar a los sistemas 5-HT y NE también puede mejorar los síntomas físicos asociados, como el dolor, que son prevalentes en el TDM y dificultan la remisión. Existe una superposición fisiopatológica entre la regulación del estado de ánimo y el dolor, y la interacción sinérgica entre 5-HT y NE parece potenciar la analgesia.
Con la remisión y la recuperación como objetivo, las pautas de tratamiento derivadas del modelo neurobiológico enfatizan la necesidad no solo de una intervención temprana e integral, sino también de una atención rigurosa a los síntomas residuales. Los pacientes que logran solo una remisión parcial tienen un riesgo significativamente mayor de recaída que aquellos que alcanzan la remisión completa. Aunque las recomendaciones específicas para el tratamiento de los síntomas residuales no están empíricamente determinadas, probablemente requieran aumentos con otros tratamientos farmacológicos y psicológicos.
La Depresión desde una Perspectiva Neurocientífica Integrada
La depresión mayor es un trastorno complejo con múltiples etiologías (genéticas, epigenéticas, ambientales) que conducen a diversos mecanismos fisiopatológicos. Estos mecanismos operan en diferentes niveles de análisis: neuroquímico (alteraciones de monoaminas, glutamato), tisular y orgánico (inflamación, respuesta al estrés alterada, cambios vasculares), y de neurocircuitos (conectividad alterada, reducción de neuroplasticidad y neurogénesis).
En lugar de ver estos mecanismos de forma aislada, un modelo unificado conceptualiza la depresión como el resultado de una matriz interactiva de factores fisiopatológicos. Una alteración en un nodo de esta matriz puede desencadenar una cascada de efectos biológicos. Por ejemplo, el estrés crónico activa el eje HHA, lo que eleva el cortisol. El cortisol elevado afecta negativamente al hipocampo y a la neuroplasticidad, y también interactúa con el sistema inmune, promoviendo la liberación de citoquinas proinflamatorias. Estas citoquinas, a su vez, pueden alterar el metabolismo del triptófano (precursor de la serotonina) a través de la enzima IDO, reduciendo los niveles de serotonina. La reducción de serotonina puede afectar la neuroplasticidad, creando un ciclo de retroalimentación negativa.
La interacción entre la respuesta al estrés, la inflamación y la neurogénesis es fundamental. La inflamación, que requiere mucha energía, induce 'comportamientos de enfermedad' (fatiga, anhedonia) para conservar energía. La activación del eje HHA y el sistema nervioso simpático por la inflamación moviliza fuentes de energía. Aunque los glucocorticoides se conocen por sus efectos antiinflamatorios, también pueden ser proinflamatorios al potenciar la respuesta inmune. Esta compleja interacción subraya que la depresión no puede reducirse a un solo factor biológico, sino que implica una red de procesos interconectados.
La neuroplasticidad, mediada en parte por el BDNF, es crucial para la adaptación. La reducción de BDNF y neuroplasticidad en la depresión puede hacer que los circuitos cerebrales sean menos capaces de adaptarse a señales externas. Los tratamientos efectivos no solo aumentan los neurotransmisores, sino que también pueden reinstaurar un estado más plástico, permitiendo que el individuo se adapte y cambie. Esto sugiere que los tratamientos biológicos podrían no ser suficientes por sí solos, y que la psicoterapia u otros esfuerzos que fomenten el cambio y la adaptación son necesarios para la mejora clínica.
Preguntas Frecuentes sobre Neurociencia y Depresión
¿Es la depresión solo un 'desequilibrio químico'?
No. Si bien las alteraciones en los neurotransmisores como la serotonina y la norepinefrina están implicadas, la investigación neurocientífica muestra que la depresión es mucho más compleja. Involucra cambios estructurales (como la reducción del hipocampo), funcionales (alteraciones en la actividad de redes cerebrales clave), y procesos moleculares (como la inflamación, el estrés crónico y la reducción de factores neurotróficos como el BDNF). Es una enfermedad que afecta la neuroplasticidad y la conectividad cerebral.
¿Cómo afecta el estrés al cerebro en la depresión?
El estrés crónico activa el eje hipotalámico-hipofisario-adrenal (HHA), lo que lleva a una liberación prolongada de cortisol. Altos niveles de cortisol pueden dañar el hipocampo, reducir la neuroplasticidad y afectar la sensibilidad de los receptores de glucocorticoides. El estrés también interactúa con el sistema inmune, aumentando la liberación de citoquinas proinflamatorias, que a su vez pueden afectar los neurotransmisores y la neurogénesis, perpetuando un ciclo negativo.
¿Por qué la depresión a veces empeora con el tiempo o se vuelve más difícil de tratar?
La depresión puede ser una enfermedad progresiva. Los episodios recurrentes pueden estar asociados con una mayor vulnerabilidad neurobiológica, posiblemente debido a un proceso de 'sensibilización' ('kindling') donde los episodios futuros se desencadenan más fácilmente. La duración prolongada de los episodios no tratados y la presencia de síntomas residuales después de la remisión parcial también se asocian con cambios neurobiológicos que pueden dificultar la recuperación completa y aumentar el riesgo de recaída.
¿Cómo funcionan los antidepresivos desde una perspectiva neurobiológica?
Los antidepresivos no solo aumentan los niveles de neurotransmisores como la serotonina y la norepinefrina. Se cree que, con el tiempo, promueven cambios en la neuroplasticidad, especialmente aumentando la síntesis de BDNF. Esto puede ayudar a restaurar el volumen del hipocampo, mejorar la sensibilidad de los receptores hormonales y normalizar la actividad en los circuitos cerebrales implicados en la regulación del estado de ánimo y el estrés. Buscan revert algunos de los cambios neurobiológicos inducidos por la enfermedad.
¿Puede la psicoterapia o el ejercicio ayudar en la depresión?
Sí. Aunque este artículo se centra en los aspectos biológicos, la investigación sugiere que tratamientos como la psicoterapia y el ejercicio también pueden promover cambios neurobiológicos positivos, incluida la mejora de la neuroplasticidad y el aumento de los niveles de BDNF. Esto refuerza la idea de que la recuperación implica una restauración de la fisiología cerebral y que diferentes abordajes pueden influir en estos procesos.
La comprensión de la depresión desde una perspectiva neurocientífica compleja e integrada es crucial. Reconocer que implica no solo desequilibrios químicos, sino también cambios estructurales, funcionales y moleculares, así como la interacción de factores genéticos, ambientales y psicológicos, nos permite abordarla de manera más efectiva. El objetivo debe ser una intervención temprana y completa, apuntando a la remisión total y la restauración de la salud cerebral subyacente.
Si quieres conocer otros artículos parecidos a Neurociencia: Entendiendo la Depresión puedes visitar la categoría Neurociencia.