El factor neurotrófico derivado del cerebro, conocido universalmente por su acrónimo, BDNF, es una molécula fundamental en el vasto y complejo universo de la neurociencia. Se trata de uno de los miembros más estudiados de la familia de las neurotrofinas, proteínas que desempeñan roles críticos en el desarrollo, la supervivencia y la función de las neuronas a lo largo de la vida. Su influencia se extiende más allá del sistema nervioso, impactando procesos metabólicos, cardiovasculares e inmunes, lo que lo convierte en un protagonista clave en la salud general y en la patología de diversas enfermedades.

Inicialmente identificado por su capacidad para mantener vivas las neuronas, el BDNF ha revelado ser un actor multifacético. Participa activamente en la modulación de neurotransmisores, es indispensable para la plasticidad neuronal – el proceso mediante el cual el cerebro se adapta y cambia en respuesta a la experiencia – y es un componente esencial para funciones cognitivas como el aprendizaje y la memoria. Su amplia distribución en el sistema nervioso central, así como en tejidos periféricos como el intestino, los pulmones y el corazón, subraya su importancia sistémica.

- ¿Qué es el BDNF? Origen y Estructura
- Mecanismos de Acción: Receptores y Señalización
- Funciones Clave del BDNF
- BDNF en Trastornos Neurológicos y Psiquiátricos
- BDNF y Diabetes Mellitus Tipo 2
- Relevancia Clínica y Potencial Terapéutico
- Resumen de BDNF en Diversas Condiciones
- Preguntas Frecuentes sobre el BDNF
- Conclusiones y Perspectivas Futuras
¿Qué es el BDNF? Origen y Estructura
El BDNF pertenece a una familia de factores de crecimiento que incluye también el factor de crecimiento nervioso (NGF), las neurotrofinas-3 (NT-3) y NT4/5. Su síntesis comienza en el retículo endoplasmático como una proteína precursora más grande, llamada pro-BDNF, de 32-35 kDa. Esta precursora viaja a través del aparato de Golgi y la red trans-Golgi, donde es empaquetada en vesículas. La maduración a la forma biológicamente activa, el BDNF maduro (mBDNF) de 13 kDa, implica la escisión del dominio N-terminal por enzimas convertasas específicas. Este proceso de maduración y secreción puede ser dependiente de la actividad neuronal, especialmente en las dendritas postsinápticas.
La estructura del BDNF maduro es notablemente similar a la del NGF, compartiendo aproximadamente un 50% de identidad de aminoácidos con NGF, NT-3 y NT-4/5. Cada neurotrofina existe como un homodímero no unido covalentemente. El gen del BDNF es complejo, con múltiples promotores (al menos cuatro en ratas y nueve en ratones) que permiten una regulación de la expresión génica dependiente de la actividad y específica de cada tejido. En humanos, se han identificado ocho ARNm distintos, con variantes de splicing que determinan su expresión predominante en diferentes áreas cerebrales (como el córtex, hipocampo, hipotálamo) o tejidos periféricos (pulmón, corazón). Los niveles de expresión de BDNF son típicamente bajos durante el desarrollo fetal, aumentan significativamente después del nacimiento y disminuyen en la edad adulta.
Mecanismos de Acción: Receptores y Señalización
La acción del BDNF está mediada principalmente a través de su unión a receptores específicos en la superficie celular. Su receptor de alta afinidad es la tirosina quinasa B (TrkB), una proteína transmembrana que existe en dos isoformas: una forma de longitud completa (gp145TrkB) con dominio tirosina quinasa activo y una forma truncada (gp95TrkB) que carece de este dominio. El BDNF también puede interactuar con el receptor de neurotrofina de baja afinidad (p75NTR), que, aunque tiene menor afinidad, puede modular la unión a los receptores Trk y desempeñar roles duales, tanto pro-supervivencia como pro-apoptosis, dependiendo del contexto celular y de la presencia de co-receptores.
La unión del BDNF al receptor TrkB de longitud completa provoca la dimerización y autofosforilación de los residuos de tirosina intracelulares del receptor. Estos residuos fosforilados actúan como sitios de anclaje para diversas proteínas adaptadoras y enzimas, activando así cascadas de señalización intracelular cruciales para la función neuronal y la supervivencia celular. Las tres vías principales activadas por la señalización de BDNF/TrkB son:
- Vía Ras/MAPK/ERK: Esta vía se activa tras el reclutamiento de proteínas adaptadoras como Shc y Grb2, que a su vez activan la pequeña proteína G Ras. La activación de Ras desencadena una cascada de quinasas (Raf, MEK, ERK) que, al final, fosforilan factores de transcripción y otras proteínas. Esta vía es esencial para la neurogénesis, la promoción de la supervivencia neuronal (inhibiendo proteínas pro-apoptóticas como BAD) y la plasticidad sináptica.
- Vía IRS-1/PI3K/Akt: La unión del BDNF al TrkB también recluta el sustrato del receptor de insulina-1 (IRS-1/2) y activa la fosfoinositida 3-quinasa (PI3K), que a su vez fosforila y activa la proteína quinasa B (Akt). La vía PI3K/Akt es un potente promotor de la supervivencia celular, ya que bloquea las señales apoptóticas y activa genes pro-supervivencia.
- Vía PLCγ/DAG/IP3: La fosfolipasa C-γ (PLCγ) se une al receptor TrkB fosforilado y cataliza la hidrólisis de lípidos de membrana para producir diacilglicerol (DAG) e inositol 1,4,5-trifosfato (IP3). El IP3 aumenta la concentración de calcio intracelular, mientras que el DAG activa la proteína quinasa C (PKC). Esta vía está implicada en la plasticidad sináptica y el crecimiento de neuritas.
La activación de estas vías de señalización por BDNF/TrkB conduce a la regulación de factores de transcripción como CREB (proteína de unión al elemento de respuesta a cAMP) y CBP (proteína de unión a CREB). CREB y CBP controlan la expresión de genes que codifican proteínas involucradas en la neuroplasticidad, la resistencia al estrés y la supervivencia celular, lo que explica la amplia gama de funciones del BDNF.
Funciones Clave del BDNF
Las funciones del BDNF son diversas y críticas para el funcionamiento óptimo del sistema nervioso y otros sistemas corporales:
Neurogénesis y Supervivencia Neuronal
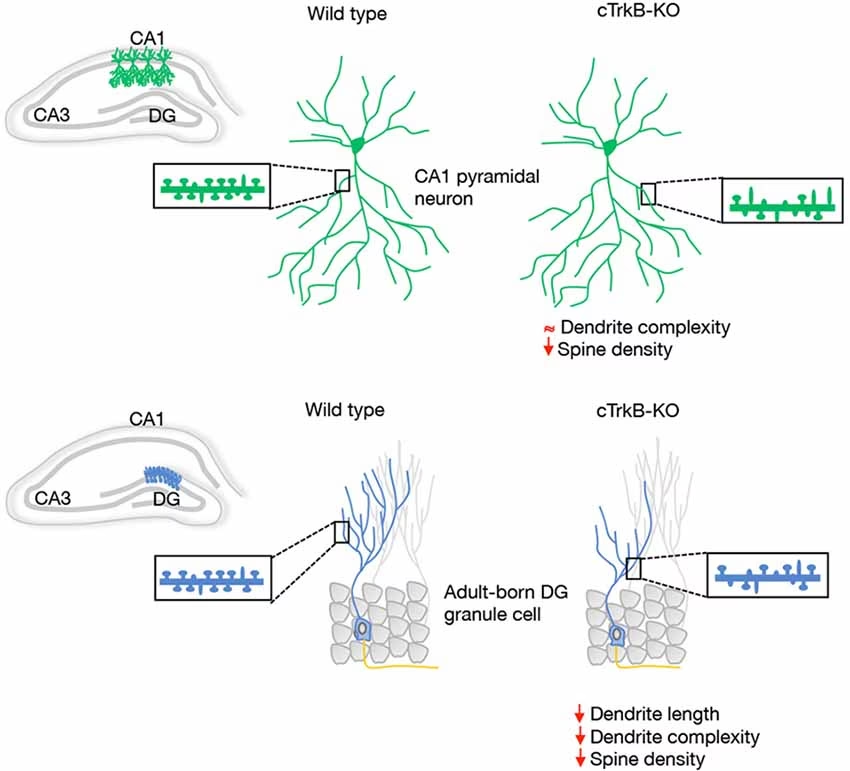
Una de las primeras funciones identificadas del BDNF fue su capacidad para promover la supervivencia de neuronas, tanto durante el desarrollo como en la edad adulta. Estimula la proliferación de células madre neurales y el crecimiento de nuevas neuronas (neurogénesis), particularmente en regiones como el hipocampo. Además, promueve el crecimiento y la complejidad de las dendritas, estructuras cruciales para la recepción de señales sinápticas. Bajo condiciones adversas como isquemia cerebral, hipoglucemia o neurotoxicidad, el BDNF ejerce un efecto neuroprotector, ayudando a las neuronas a resistir el daño.
Plasticidad Sináptica y Aprendizaje
El BDNF es un regulador fundamental de la neuroplasticidad sináptica, los cambios en la fuerza y estructura de las conexiones entre neuronas que subyacen al aprendizaje y la memoria. Participa tanto en mecanismos presinápticos (ciclo de vesículas) como postsinápticos (modulación de receptores de neurotransmisores, como los receptores AMPA y NMDA). Se ha demostrado que el BDNF es necesario para la inducción y el mantenimiento de la potenciación a largo plazo (LTP), un modelo celular de aprendizaje y memoria. Aumenta el tráfico de receptores NMDA y AMPA hacia la sinapsis y promueve cambios estructurales como el aumento de la densidad y el volumen de las espinas dendríticas. La forma precursora, pro-BDNF, puede, por el contrario, estar involucrada en la depresión a largo plazo (LTD), otro tipo de plasticidad sináptica.
Metabolismo Energético y Lipídico
El BDNF juega un papel importante en la regulación del metabolismo energético y el balance de glucosa. La administración de BDNF puede suprimir la ingesta de energía y reducir el peso corporal. Se ha correlacionado positivamente con marcadores de salud metabólica como el colesterol LDL y los triglicéridos en ciertos contextos. En modelos de diabetes, el BDNF mejora el control de la glucosa, reduce la hepatomegalia y previene el agotamiento de las células β pancreáticas, sugiriendo un potencial terapéutico en la diabetes mellitus tipo 2. La interacción con ácidos grasos omega-3 parece modular los niveles de BDNF, influyendo en la homeostasis energética.
Acciones Cardiovasculares
Las neurotrofinas, incluido el BDNF, promueven la angiogénesis y la supervivencia de células endoteliales y musculares lisas vasculares. El BDNF, a través de su receptor TrkB, favorece la neovascularización terapéutica. Las células endoteliales que expresan receptores TrkB activan las vías ERK/MAPK y PI3K/AKT, promoviendo la supervivencia celular. Además, la activación de Akt puede estimular la producción de óxido nítrico, contribuyendo a la relajación vascular y a la protección cardiovascular.
Inflamación e Inmunidad
El BDNF está implicado en la modulación de la respuesta inflamatoria. Puede ser liberado por células inmunes como linfocitos, eosinófilos y macrófagos. En el contexto de la neuroinflamación, la activación de células gliales como la microglía y los astrocitos puede influir en los niveles de BDNF. La neuroinflamación crónica, a menudo asociada a trastornos neurológicos y psiquiátricos, puede alterar las vías de señalización relacionadas con el BDNF. Existe una compleja interacción entre el BDNF y factores inflamatorios como el NF-κB y las citoquinas. El BDNF puede inducir NF-κB, que a su vez influye en la expresión de genes pro y anti-inflamatorios, incluyendo el propio BDNF. Esta relación dual destaca el papel del BDNF en intentar contrarrestar los efectos neurotóxicos de la neuroinflamación.
BDNF en Trastornos Neurológicos y Psiquiátricos
Las alteraciones en los niveles o la función del BDNF se han asociado con una amplia gama de trastornos del sistema nervioso:
Trastornos Neurodegenerativos
En enfermedades caracterizadas por la pérdida neuronal, como el Alzheimer, la enfermedad de Parkinson, la esclerosis múltiple y la enfermedad de Huntington, se observan a menudo niveles reducidos de BDNF en el cerebro y/o en circulación. Esta disminución podría contribuir a la vulnerabilidad neuronal y a la progresión de la enfermedad, dada la función neuroprotectora y promotora de la supervivencia del BDNF. Por ejemplo, en la enfermedad de Huntington, la mutación de la proteína huntingtina afecta la transcripción del BDNF, reduciendo el soporte neurotrófico para las neuronas estriatales. La restauración de los niveles de BDNF podría ofrecer un potencial terapéutico.
Trastornos Psiquiátricos
El BDNF también está implicado en la fisiopatología de trastornos psiquiátricos mayores como la depresión, el trastorno bipolar y la esquizofrenia. Se ha observado una disminución de los niveles de BDNF en suero, plasma y ciertas áreas cerebrales en pacientes con depresión mayor y trastorno bipolar (episodios depresivos y maníacos), así como en esquizofrenia. Esta reducción podría estar relacionada con la disfunción de la neuroplasticidad y la vulnerabilidad al estrés observadas en estos trastornos. Curiosamente, el tratamiento efectivo con antidepresivos o estabilizadores del estado de ánimo a menudo se asocia con la normalización o el aumento de los niveles de BDNF, lo que sugiere que el BDNF es un factor importante en la respuesta terapéutica. Variantes genéticas del BDNF, como el polimorfismo Val66Met, se han asociado con una mayor susceptibilidad a la depresión y una respuesta alterada a ciertos tratamientos.
Otros Trastornos
Niveles alterados de BDNF también se han reportado en otras condiciones, incluyendo el trastorno del espectro autista (donde se observan niveles disminuidos) y la epilepsia del lóbulo temporal (donde la sobreexpresión de BDNF podría contribuir a la hiperexcitabilidad neuronal y la reducción del umbral convulsivo).
BDNF y Diabetes Mellitus Tipo 2
La conexión entre el BDNF y la diabetes tipo 2 es cada vez más clara. Como se mencionó, el BDNF regula el metabolismo de la glucosa y la energía. En modelos animales de diabetes, el BDNF no solo mejora el control glucémico, sino que también protege las células β pancreáticas del agotamiento y el daño, manteniendo su estructura y mejorando la secreción de insulina. En humanos, los niveles plasmáticos de BDNF son a menudo más bajos en individuos con diabetes tipo 2, independientemente de la obesidad, y se correlacionan inversamente con la glucosa en ayunas. La hiperglucemia parece inhibir la liberación de BDNF desde el cerebro. Estos hallazgos sugieren que la deficiencia de BDNF podría ser un factor contribuyente en el desarrollo y la progresión de la diabetes tipo 2. El ejercicio, conocido por sus beneficios en la diabetes, aumenta los niveles de BDNF circulante, lo que podría mediar parte de sus efectos protectores tanto a nivel metabólico como neuronal.
Relevancia Clínica y Potencial Terapéutico
Dada su amplia gama de funciones y su implicación en numerosas patologías, el BDNF tiene una considerable relevancia clínica. Los niveles circulantes de BDNF podrían servir como biomarcadores para el diagnóstico, la monitorización de la progresión de la enfermedad o la respuesta al tratamiento en trastornos como la depresión, el trastorno bipolar, la esquizofrenia, el Alzheimer, el Parkinson o el autismo.
Más allá de ser un biomarcador, el BDNF se perfila como un objetivo terapéutico prometedor. Estrategias que busquen aumentar los niveles de BDNF o potenciar su señalización a través del receptor TrkB podrían ser beneficiosas. La administración directa de BDNF o el uso de miméticos de BDNF se están investigando en modelos preclínicos de enfermedades neurodegenerativas y psiquiátricas con resultados iniciales alentadores. Dado que el BDNF puede cruzar la barrera hematoencefálica, la administración periférica podría ser una vía viable.
Además de los enfoques farmacológicos, las intervenciones conductuales y de estilo de vida que aumentan los niveles endógenos de BDNF son de gran interés. El ejercicio físico regular y la estimulación cognitiva son bien conocidos por su capacidad para aumentar la expresión de BDNF en el cerebro, lo que podría explicar sus efectos beneficiosos en la salud cerebral, el aprendizaje, la memoria y la prevención o el manejo de trastornos neurológicos y psiquiátricos. La dieta, particularmente el consumo de ácidos grasos omega-3, también puede influir en los niveles de BDNF. Integrar estas intervenciones en el tratamiento de enfermedades cerebrales y metabólicas podría potenciar los efectos de las terapias convencionales.

Resumen de BDNF en Diversas Condiciones
Para visualizar rápidamente la asociación entre el BDNF y distintas patologías, podemos resumir los hallazgos reportados en la literatura:
| Condición | Niveles de BDNF Periférico | Niveles de BDNF Cerebral | Observaciones Clave |
|---|---|---|---|
| Depresión Mayor | Disminuidos (suero/plasma) | Disminuidos (hipocampo, córtex prefrontal) | Asociado a severidad y respuesta a antidepresivos. |
| Trastorno Bipolar | Disminuidos (episodios maníacos/depresivos) | Disminuidos (hipocampo en suicidas) | Normalización en fase eutímica, aumento con tratamiento. |
| Esquizofrenia | Disminuidos (suero) | Contradictorio (reportes de aumento o disminución en distintas áreas) | Asociado a síntomas, interacción con neuroinflamación. |
| Enfermedad de Alzheimer | Bajos (suero, correlacionado con demencia) | Disminuidos (hipocampo, córtex frontal) | Asociado a progresión, afectado por placas Aβ. |
| Enfermedad de Parkinson | Variable (bajos en inicio, altos en etapas avanzadas) | Disminuidos (sustancia negra, estriado) | Correlacionado con degeneración estriatal y síntomas motores/cognitivos. |
| Epilepsia | Aumentados (suero post-convulsiones) | Aumentados (hipocampo, córtex en epilepsia del lóbulo temporal) | Asociado a riesgo y excitotoxicidad. |
| Diabetes Mellitus Tipo 2 | Disminuidos (plasma) | Disminuidos (liberación cerebral inhibida por glucosa alta) | Asociado a control glucémico, protección de células β. |
| Trastorno Espectro Autista | Disminuidos (plasma) | No especificado en el texto | Potencial biomarcador temprano. |
Preguntas Frecuentes sobre el BDNF
¿El BDNF solo se encuentra en el cerebro?
No, aunque es abundante en el sistema nervioso central, el BDNF también se encuentra en varios tejidos periféricos, incluyendo el corazón, los pulmones, el intestino y las células sanguíneas como las plaquetas.
¿La disminución de BDNF causa estas enfermedades?
La relación es compleja. Los niveles bajos de BDNF pueden contribuir a la vulnerabilidad y progresión de ciertas enfermedades (como en la neurodegeneración o la diabetes), pero también pueden ser una consecuencia de la propia patología (por ejemplo, la neuroinflamación o el daño neuronal pueden reducir el BDNF). Es probable que sea una interacción bidireccional.
¿Podemos aumentar nuestros niveles de BDNF de forma natural?
Sí. El ejercicio físico regular, una dieta equilibrada rica en omega-3, la estimulación cognitiva y la reducción del estrés crónico son estrategias conocidas que pueden aumentar la expresión y los niveles de BDNF.
¿Se utiliza el BDNF como tratamiento actualmente?
Actualmente, el BDNF no se utiliza como tratamiento clínico estándar, pero es un objetivo de investigación muy activo. Se están explorando terapias basadas en la administración de BDNF, miméticos o enfoques de terapia génica, principalmente en estudios preclínicos y ensayos clínicos tempranos.
¿El polimorfismo Val66Met de BDNF siempre causa problemas?
No necesariamente. Es una variante genética común. Si bien se ha asociado con un mayor riesgo o vulnerabilidad a ciertos trastornos (como depresión, ansiedad o deterioro cognitivo), especialmente en interacción con factores ambientales como el estrés, muchas personas con este polimorfismo no desarrollan estas condiciones. Su impacto depende de la interacción con otros genes y factores ambientales.
Conclusiones y Perspectivas Futuras
El BDNF es una molécula de inmensa importancia en la neurociencia y más allá. Sus roles en la supervivencia neuronal, la neuroplasticidad, el aprendizaje, el metabolismo y la modulación de la neuroinflamación lo posicionan como un jugador clave en la salud y la enfermedad. La evidencia de que la disfunción del BDNF está implicada en trastornos neurológicos, psiquiátricos y metabólicos abre vías prometedoras para la investigación y el desarrollo de nuevas estrategias terapéuticas.
Si bien se ha avanzado mucho en la comprensión de sus mecanismos de acción a través de receptores como TrkB y p75NTR y sus cascadas de señalización, aún quedan muchas preguntas por responder. La complejidad de su regulación génica (con múltiples promotores y variantes de splicing), el papel dual de las formas madura y precursora (pro-BDNF), y la interacción con otros factores (como hormonas, neurotransmisores, factores metabólicos y citoquinas inflamatorias) requieren una investigación continua.
El potencial del BDNF como biomarcador y objetivo terapéutico es considerable. Las estrategias para aumentar los niveles o la actividad de BDNF, ya sean farmacológicas o basadas en intervenciones de estilo de vida como el ejercicio y la dieta, podrían ofrecer nuevas herramientas para la prevención y el tratamiento de enfermedades devastadoras que actualmente carecen de curas efectivas. Un conocimiento más profundo de este péptido endógeno sin duda allanará el camino hacia terapias innovadoras en el futuro cercano.
Si quieres conocer otros artículos parecidos a BDNF: Factor Clave en Cerebro y Salud puedes visitar la categoría Neurociencia.
