La capacidad de registrar y comprender la actividad eléctrica de los sistemas biológicos es fundamental tanto en la investigación básica como en la aplicación clínica. Desde las intrincadas señales de una red neuronal hasta los complejos patrones de activación del corazón, descifrar estos impulsos nos abre la puerta a nuevos diagnósticos y terapias. En este contexto, las matrices de multielectrodos, o Multi-Electrode Arrays (MEA), emergen como una tecnología poderosa y versátil, ofreciendo una ventana sin precedentes a estos fenómenos eléctricos.
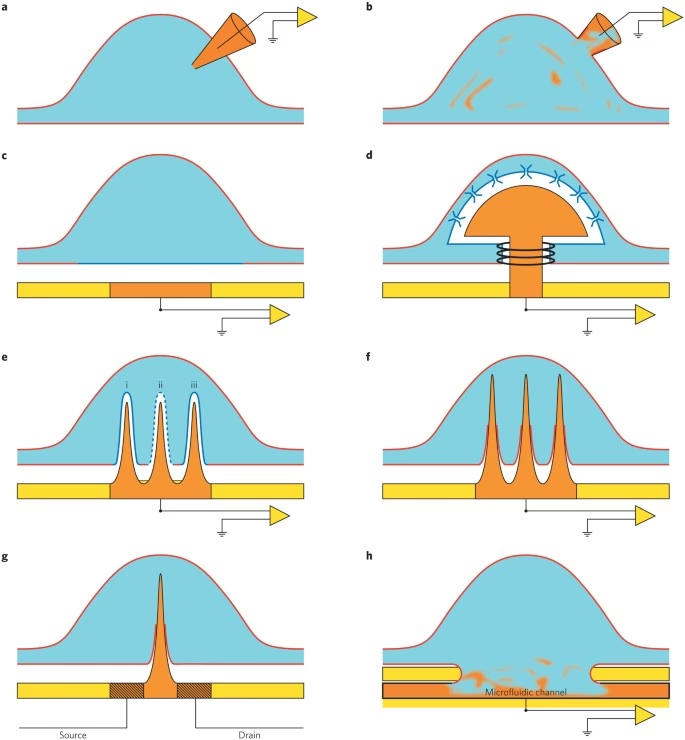
Los MEA representan un avance significativo frente a los métodos de registro de un solo punto, permitiendo capturar datos de múltiples ubicaciones de forma simultánea. Esta capacidad de obtener una visión más global y detallada de la actividad eléctrica es lo que los hace tan valiosos en campos tan diversos como la neurociencia, la farmacología y la electrofisiología cardíaca.
¿Qué es una Matriz de Multielectrodos (MEA)?
En esencia, una matriz de multielectrodos es un conjunto de electrodos dispuestos en un patrón espacial sobre una superficie. Estos electrodos están diseñados para detectar cambios de voltaje extracelulares generados por células o tejidos electroactivos, como neuronas o cardiomiocitos. La configuración y el tamaño de los electrodos y de la matriz varían enormemente dependiendo de la aplicación, desde arreglos microscópicos para cultivos celulares hasta estructuras más grandes montadas en catéteres para mapeo de órganos.
La información recopilada por los electrodos son potenciales de campo extracelulares, que reflejan la actividad eléctrica de las células o redes en su proximidad. Al tener múltiples puntos de registro, los MEA permiten no solo detectar la presencia de actividad eléctrica, sino también estudiar su propagación, frecuencia, conectividad y otras características dinámicas a través de la red o el tejido.
¿Cómo Funciona la Tecnología MEA?
El principio básico detrás del funcionamiento de un MEA implica la detección de pequeñas variaciones de voltaje en el entorno extracelular, causadas por los flujos de iones asociados a los potenciales de acción o potenciales sinápticos de las células electroactivas. Estos cambios de voltaje son captados por los electrodos, que actúan como sensores. La señal eléctrica detectada es generalmente de baja amplitud y requiere ser amplificada y procesada para su análisis.
En aplicaciones con cultivos celulares o cortes de tejido, las células (como neuronas, cardiomiocitos) se cultivan directamente sobre la superficie del MEA, donde los electrodos están integrados en la base de un pocillo o chip. Con el tiempo, estas células pueden formar redes cohesivas. El MEA registra la actividad eléctrica espontánea de estas células o redes. Si la actividad espontánea es baja o nula, se puede aplicar estimulación eléctrica a través de ciertos electrodos para inducir y estudiar respuestas.
Los datos brutos (cambios de voltaje en el tiempo para cada electrodo) son procesados para identificar eventos eléctricos específicos, como picos (disparos neuronales) o potenciales de campo. A partir de estos eventos, se pueden derivar numerosas métricas, incluyendo frecuencia de disparo, patrones de ráfagas, conectividad funcional entre electrodos (y, por extensión, entre áreas del cultivo/tejido), duración del potencial de acción extracelular, y parámetros relacionados con la contractilidad en el caso de cardiomiocitos (periodo de latido, duración del latido).
El análisis de datos de MEA a menudo implica software especializado que puede decodificar la conectividad neuronal o las características del latido cardíaco a partir de las formas de onda registradas. Para estudios a gran escala, como el cribado de fármacos, se utilizan flujos de trabajo de análisis automatizado que pueden aplicar métodos estadísticos como análisis de componentes principales (PCA) para identificar métricas relevantes biológicamente.
Funcionamiento Específico del MEA en Mapeo Cardíaco No Contacto (Sistema EnSite)
En el contexto del mapeo electrofisiológico cardíaco, el funcionamiento de un MEA difiere ligeramente porque no siempre requiere contacto directo con el endocardio. Un ejemplo prominente es el sistema EnSite. Este sistema utiliza un catéter con un balón elipsoidal (de unos 7.5 mL) alrededor del cual se teje una malla de 64 cables finos. Cada cable tiene una pequeña interrupción en su aislamiento que actúa como un electrodo unipolar no contacto.
El balón se posiciona dentro de la cámara cardíaca de interés (aurícula derecha, aurícula izquierda, ventrículo derecho). Los 64 electrodos en el balón registran simultáneamente más de 3000 electrogramas unipolares "de campo lejano" desde todos los puntos de la cámara. Un electrodo de anillo en el eje del catéter sirve como referencia.
La clave de este sistema es que, aunque los electrogramas registrados por los electrodos no contacto son de baja amplitud y frecuencia (campo lejano), el sistema utiliza algoritmos sofisticados y el principio de que el campo de voltaje cardíaco obedece la ecuación de Laplace. Sabiendo la geometría del balón y reconstruyendo la geometría de la cámara cardíaca, el sistema puede calcular una "solución inversa" a la ecuación de Laplace. Esto permite predecir cómo habría sido la señal eléctrica en su origen real: la superficie endocardial. Así, se reconstruyen electrogramas en sitios endocardiales sin contacto físico, conocidos como electrogramas virtuales.
La geometría tridimensional de la cámara cardíaca se reconstruye utilizando un catéter de mapeo convencional. Este catéter, equipado con un emisor de señal localizadora (una corriente de baja frecuencia, 5.68 kHz), se mueve por la superficie endocardial. La señal del catéter es detectada por los electrodos del MEA no contacto, creando un gradiente de potencial. El sistema utiliza este gradiente para determinar la posición espacial exacta del catéter de contacto con respecto al balón del MEA. Al mover el catéter de contacto y trazar el contorno de la cámara, el sistema recopila coordenadas y construye un modelo geométrico anatómico y específico del paciente del endocardio (el endocardio virtual).
Una vez que se tiene la geometría de la cámara y se registran los potenciales en el balón, el sistema reconstruye los más de 3000 electrogramas virtuales y los superpone sobre el endocardio virtual. Estos datos se pueden visualizar como mapas de isopotenciales (donde colores representan voltajes) o mapas isócronos (donde colores representan tiempos de activación). La propagación de la onda de despolarización se puede ver como una "película" tridimensional animada.
El sistema también puede rastrear la posición de cualquier catéter de mapeo o ablación sobre el modelo virtual del endocardio utilizando la misma tecnología localizadora. Esto facilita la navegación, la marcación de puntos de interés y el registro de los sitios donde se aplica energía de ablación.
Además del mapeo de activación, el sistema permite el mapeo de sustrato de forma dinámica. Utilizando el pico de voltaje negativo de los electrogramas virtuales unipolares reconstruidos, se pueden identificar áreas de bajo voltaje en el endocardio virtual. Estas áreas a menudo se correlacionan con tejido cicatrizado o enfermo, que puede ser el sustrato para arritmias reentrantes. Aunque la precisión del mapeo de sustrato puede verse afectada por la distancia al balón (idealmente menos de 40 mm), la capacidad de obtener un mapa de voltaje de alta densidad a partir de un solo ciclo cardíaco es una ventaja significativa.
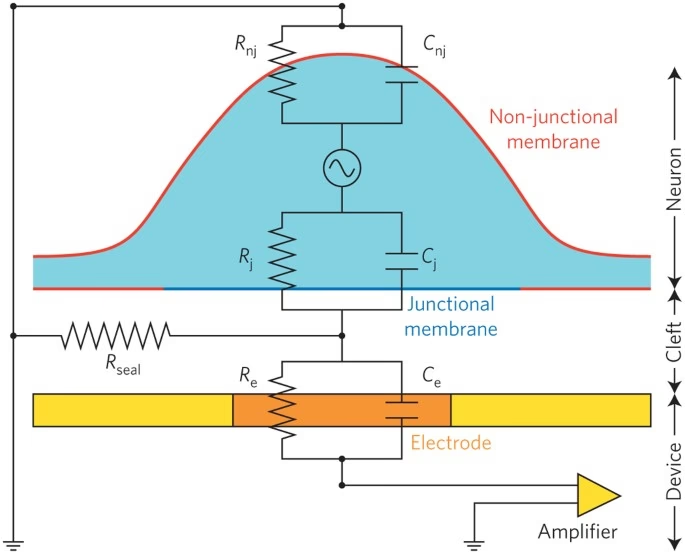
Ventajas Clave de los Multi-Electrode Arrays
La tecnología MEA ofrece múltiples beneficios que superan las limitaciones de los métodos de registro punto a punto o de menor densidad. Las ventajas más destacadas incluyen:
Adquisición Simultánea y de Alta Densidad: A diferencia de los métodos tradicionales que requieren mover un electrodo a diferentes posiciones para registrar la actividad secuencialmente, los MEA capturan datos de múltiples puntos (cientos o miles, dependiendo del sistema) al mismo tiempo. Esto proporciona una visión instantánea y completa de la actividad eléctrica en un área, reduciendo drásticamente el tiempo de mapeo.
Mapeo de Arritmias Inestables o No Sostenidas (Cardiaco): En electrofisiología cardíaca, la capacidad de adquirir datos de toda la cámara en uno (teóricamente) o muy pocos latidos es crucial. Permite mapear taquicardias muy rápidas (como TV rápida) o ritmos irregulares que el paciente podría tolerar mal o que no son sostenidos. Los sistemas convencionales requerirían episodios prolongados de la arritmia.
Visión Global de la Propagación: Al registrar simultáneamente desde múltiples puntos, los MEA permiten visualizar la propagación de las ondas de activación a través de un tejido o cámara cardíaca. Esto es invaluable para identificar el origen de arritmias focales (puntos de "breakthrough") y para delinear circuitos de reentrada complejos.
Reducción de la Inducción Mecánica de Ectopia (Cardiaco No Contacto): En los sistemas de mapeo no contacto, al no requerir que los electrodos estén físicamente tocando el endocardio para el mapeo inicial, se reduce el riesgo de inducir latidos ectópicos o arritmias simplemente por la manipulación del catéter.
Análisis Detallado de Redes y Tejidos (General): En investigación con cultivos celulares o cortes de tejido, los MEA permiten estudiar la conectividad funcional, la sincronización de la red, los patrones de disparo complejos y los efectos de fármacos o manipulaciones genéticas sobre la actividad eléctrica a nivel de red, no solo de células individuales.
Versatilidad en Aplicaciones: Desde el cribado de fármacos y el estudio de modelos de enfermedades in vitro hasta el mapeo y la ablación de arritmias cardíacas complejas en pacientes, la tecnología MEA se adapta a una amplia gama de usos.
Navegación Asistida por Imagen y Catalogación (Cardiaco EnSite): El sistema localizador no solo ayuda a construir la geometría sino que también permite rastrear catéteres de mapeo o ablación sobre el modelo 3D, facilitando la navegación sin necesidad constante de fluoroscopia (reduciendo la exposición a la radiación) y permitiendo registrar con precisión los sitios de ablación.
Mapeo Dinámico de Sustrato (Cardiaco EnSite): La capacidad de generar mapas de voltaje de alta densidad a partir de un solo ciclo cardíaco permite evaluar el sustrato eléctrico (áreas de bajo voltaje, bloqueo) incluso en arritmias rápidas o inestables, combinando información de activación y sustrato para guiar la ablación.
Estas ventajas posicionan a los MEA como una herramienta indispensable para obtener una comprensión profunda de la electrofisiología a diferentes escalas, desde la celular hasta la de un órgano completo.
Comparación: MEA vs. Mapeo Convencional Punto a Punto (Cardiaco)
| Característica | MEA (No Contacto) | Mapeo Contacto Punto a Punto |
|---|---|---|
| Adquisición de Datos | Simultánea desde ~3000+ puntos virtuales | Secuencial, punto por punto |
| Número de Latidos Requeridos | Teóricamente uno, pocos para mapas completos | Múltiples latidos para cubrir el área |
| Mapeo de Arritmias Inestables/No Sostenidas | Altamente eficaz | Difícil o imposible si no se sostiene la arritmia |
| Riesgo de Inducción Mecánica | Menor en el mapeo inicial | Puede ocurrir al manipular el catéter |
| Visión de la Propagación | Global, en tiempo real (película 3D) | Reconstruida a partir de puntos secuenciales |
| Mapeo de Sustrato | Dinámico, desde un ciclo (con restricciones de distancia) | Requiere mapeo punto a punto prolongado |
| Tiempo del Procedimiento (Mapeo) | Potencialmente más rápido para mapeos complejos/inestables | Puede ser largo para mapeos extensos |
Aplicaciones de la Tecnología MEA
La versatilidad de los MEA les permite ser utilizados en diversos campos:
- Neurociencia: Estudio de la actividad neuronal en cultivos primarios, líneas celulares iPSC-derivadas, o cortes de cerebro. Investigación de la formación de redes neuronales, plasticidad sináptica, efectos de neurotoxinas, y modelos de enfermedades neurológicas. Cribado de compuestos para efectos sobre la excitabilidad neuronal o el riesgo de convulsiones.
- Farmacología: Cribado de alto rendimiento de compuestos para evaluar su impacto en la actividad eléctrica de células o tejidos. Especialmente útil para evaluar la cardiotoxicidad (efectos sobre la frecuencia, duración y regularidad del latido cardíaco) y neurotoxicidad.
- Electrofisiología Cardíaca Clínica: Mapeo de arritmias complejas (taquicardias auriculares, fibrilación auricular, taquicardias ventriculares) para identificar el origen y los circuitos de reentrada. Guía en procedimientos de ablación.
Preguntas Frecuentes sobre MEA
Aquí respondemos algunas preguntas comunes sobre los Multi-Electrode Arrays:
¿Qué es un electrograma virtual?
En el contexto del mapeo cardíaco no contacto, un electrograma virtual es una representación matemática de cómo se vería la actividad eléctrica en un punto de la superficie endocardial, calculada por el sistema (usando la solución inversa) a partir de los potenciales registrados por los electrodos del balón MEA que están a distancia.
¿Cómo se crea el modelo 3D de la cámara cardíaca en el mapeo no contacto?
El modelo 3D se crea utilizando un catéter de mapeo convencional que se mueve por la superficie interna de la cámara. Este catéter emite una señal localizadora que es detectada por la matriz de electrodos en el balón. El sistema utiliza la información de la señal detectada para determinar la posición espacial del catéter de contacto y así reconstruye la geometría de la cámara al trazar su contorno.
¿Puede un sistema MEA mapear cualquier tipo de arritmia cardíaca?
Los sistemas MEA no contacto son particularmente útiles para mapear arritmias focales, macroreentradas y ritmos inestables o no sostenidos, ya que capturan datos de toda la cámara rápidamente. También pueden proporcionar información valiosa en arritmias más complejas, aunque su utilidad puede depender del tipo específico de arritmia y la calidad de la señal reconstruida.
En mapeo de activación, ¿cuál es la diferencia entre el sitio de activación más temprana y el sitio de 'breakout'?
El sitio de activación más temprana (Earliest Activation Site) se define como el punto en el endocardio virtual donde el electrograma unipolar reconstruido muestra la primera desviación significativa de la línea de base (generalmente el pico negativo más temprano). El sitio de 'breakout' se refiere al punto desde el cual la activación se propaga rápidamente de forma centrífuga, identificado en los mapas de propagación como el centro de donde irradian las líneas de isocronas o los cambios de color en los mapas de isopotenciales. Aunque a menudo están relacionados, no siempre son idénticos y pueden estar separados por cierta distancia.
Conclusión
La tecnología de Multi-Electrode Arrays representa un salto cualitativo en nuestra capacidad para registrar y analizar la actividad eléctrica en sistemas biológicos. Ya sea desentrañando los secretos de las redes neuronales en una placa de laboratorio o mapeando con precisión las arritmias en el corazón de un paciente, los MEA ofrecen una visión de alta densidad, simultánea y detallada que es difícil de conseguir con métodos convencionales. Sus ventajas en términos de velocidad, capacidad para estudiar eventos transitorios y visión global los convierten en una herramienta indispensable para la investigación y la clínica modernas, prometiendo seguir impulsando descubrimientos y mejorando los tratamientos.
Si quieres conocer otros artículos parecidos a MEA: Ventajas y Funcionamiento Explicado puedes visitar la categoría Neurociencia.
