El control motor se define como la capacidad de regular o dirigir los movimientos. En el campo de la neurología, se centra en el estudio del movimiento y cómo el sistema nervioso lo controla. Este control complejo involucra la cooperación de numerosas estructuras dentro del sistema nervioso central y periférico, trabajando de manera coordinada para permitirnos interactuar con nuestro entorno y realizar acciones voluntarias con precisión y fluidez. Comprender el control motor es fundamental para abordar las diversas deficiencias que pueden surgir tras una lesión o enfermedad neurológica.
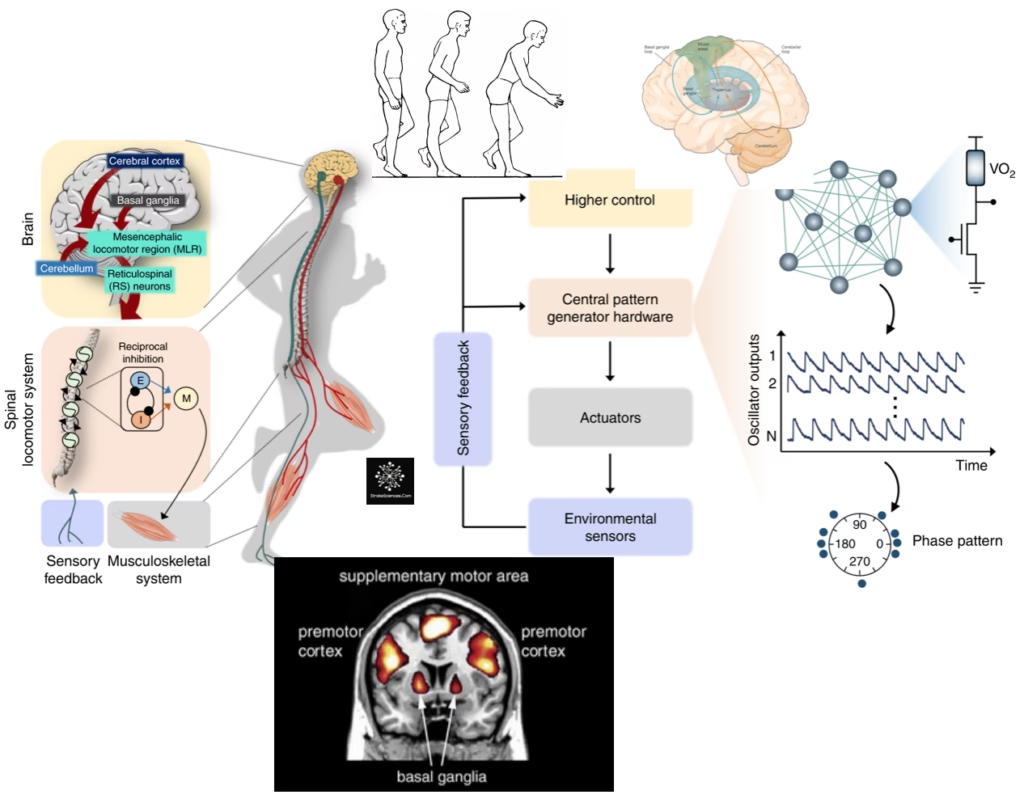
El control neural del movimiento es un proceso intrincado que depende de la comunicación y la integración de información a través de múltiples niveles del sistema nervioso. Desde las áreas corticales superiores que planifican una acción, pasando por las vías descendentes que transmiten las órdenes, hasta los circuitos de la médula espinal que activan directamente los músculos, cada componente juega un papel vital. Además, estructuras subcorticales como el cerebelo y los ganglios basales modulan y refinan continuamente el movimiento. La información sensorial, tanto del propio cuerpo como del entorno, es utilizada constantemente, tanto para la planificación anticipada (feedforward) como para la corrección de movimientos en curso (feedback).
- Estructuras Clave del Control Motor
- Deficiencias Comunes del Control Motor
- Evaluación de las Deficiencias del Control Motor
- Diagnóstico y Pronóstico
- Enfoque de Rehabilitación: Remediación vs. Compensación
- Intervenciones Basadas en la Tarea Específica
- Evidencia Actual y Consideraciones Prácticas
- Preguntas Frecuentes
- ¿Qué estructuras cerebrales controlan el movimiento voluntario?
- ¿Qué parte del cerebro es clave en la coordinación del movimiento?
- ¿Qué lóbulo cerebral está principalmente involucrado en el control motor?
- ¿Cuál es la diferencia entre paresia y plegia?
- ¿Qué diferencia hay entre espasticidad y rigidez?
- ¿Por qué el entrenamiento debe ser específico de la tarea?
Estructuras Clave del Control Motor
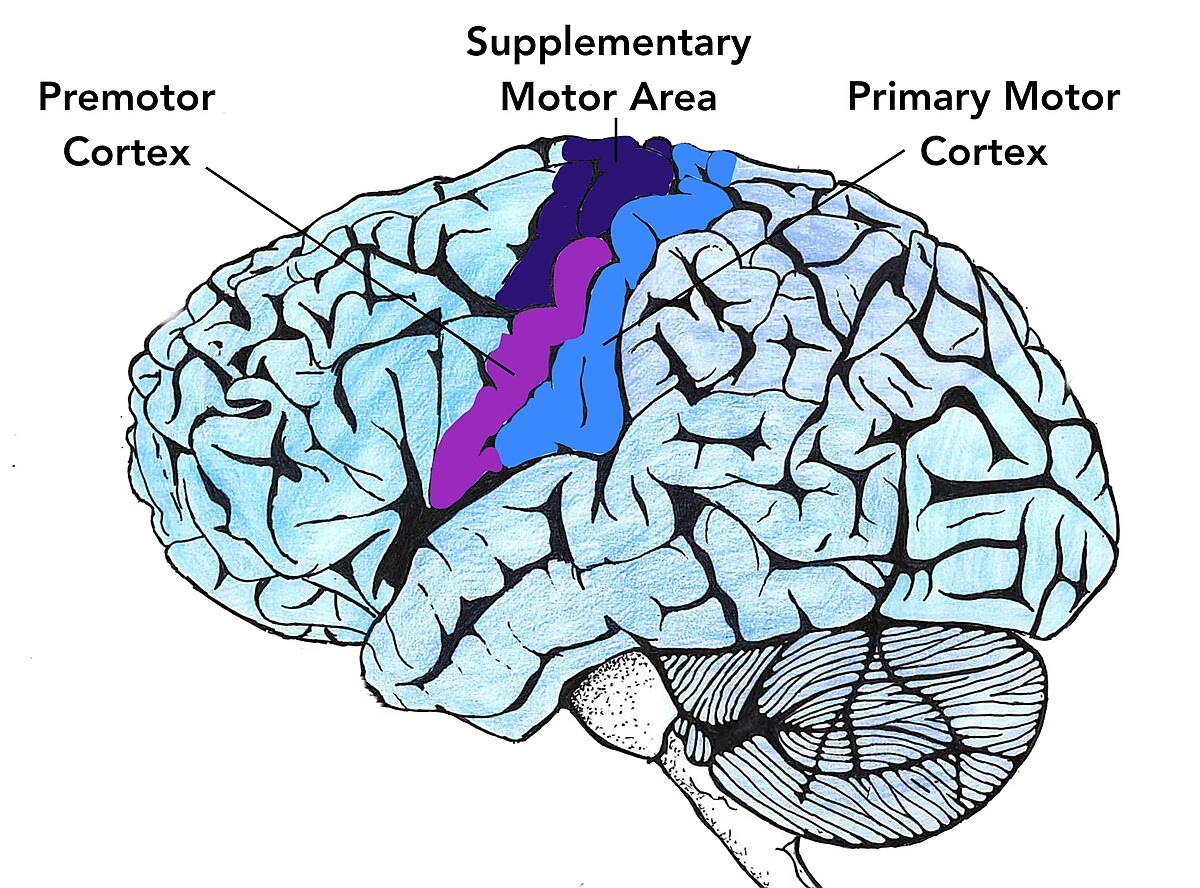
Las áreas corticales motoras son el punto de partida para los movimientos voluntarios. Estas incluyen la corteza motora primaria, responsable de la ejecución directa de los movimientos, y las áreas motoras no primarias, como la corteza premotora y el área motora suplementaria. Estas últimas se encargan de la planificación, secuencia y coordinación de movimientos complejos. Trabajan en conjunto, comunicándose con la médula espinal y los músculos principalmente a través del tracto corticoespinal. Este tracto establece conexiones directas (monosinápticas) e indirectas (di o polisinápticas) con las motoneuronas espinales que controlan los músculos del tronco y las extremidades. El tracto reticuloespinal complementa al corticoespinal, transmitiendo información de movimiento desde estructuras subcorticales a la médula espinal.
La circuitería de la médula espinal, compuesta por aferentes periféricos (neuronas sensoriales), interneuronas y motoneuronas, trabaja en concierto con los comandos motores descendentes para generar el movimiento final. El cerebelo, a menudo descrito como el centro de coordinación, juega un papel crucial en la corrección de errores y la adaptación del movimiento, asegurando que sea fluido y preciso. Por su parte, los ganglios basales se enfocan en la selección de los movimientos deseados e inhiben los movimientos competitivos o no deseados, actuando como un filtro para refinar la acción.
La información sensorial es indispensable para el control motor. La propiocepción (sentido de la posición corporal), el tacto, la visión y otros sentidos proporcionan la retroalimentación necesaria para ajustar los movimientos en tiempo real y para planificar acciones futuras basadas en experiencias previas y el estado actual del cuerpo y el entorno.
Deficiencias Comunes del Control Motor
Las deficiencias en el control motor son frecuentes en diversas condiciones neurológicas, especialmente en adultos mayores afectados por accidentes cerebrovasculares, enfermedad de Parkinson, esclerosis múltiple, lesiones cerebrales traumáticas, entre otras. Es común que los pacientes presenten múltiples deficiencias simultáneamente.
Paresia y Plegia
La deficiencia motora más común es la paresia, que es la reducción en la capacidad de activar voluntariamente las motoneuronas espinales. La plegia es el caso extremo de la paresia, donde hay una pérdida completa de esta capacidad. Clínicamente, la paresia se manifiesta como debilidad muscular, observable al mover las extremidades sin gravedad, contra gravedad o contra resistencia. Puede ser causada por una amplia gama de condiciones neurológicas que afectan el sistema corticoespinal (corteza motora, tracto corticoespinal, médula espinal). La distribución y gravedad de la paresia varían según la condición subyacente. La paresia es fundamentalmente un problema de ejecución del movimiento. La interrupción del sistema corticoespinal altera la activación de unidades motoras, músculos individuales y grupos musculares, lo que explica las alteraciones en el movimiento y las estrategias compensatorias que se observan. Por ejemplo, la dificultad para activar suficientemente los extensores de cadera y rodilla puede llevar a un tiempo prolongado y múltiples intentos al levantarse de una silla, o la falta de activación de flexores de cadera y dorsiflexores de tobillo puede resultar en la circunducción de la cadera al caminar en pacientes post-ictus. La gravedad de la paresia impacta directamente la capacidad para realizar actividades diarias como vestirse, bañarse, caminar o subir escaleras.
Tono Muscular Anormal
El tono muscular es la resistencia del músculo a la elongación o estiramiento pasivo. El tono anormal se divide en hipotonía e hipertonía.
- Hipotonía: Es la disminución del tono muscular. La flacidez es la forma más severa, con pérdida total del tono. Se manifiesta como una resistencia disminuida al movimiento pasivo y reflejos de estiramiento disminuidos o ausentes. Las extremidades se mueven con facilidad y las articulaciones pueden ser hiperextensibles. Puede ser causada por daño en los nervios periféricos o daño en el sistema nervioso central que resulta en una disminución de la señal neural al músculo.
- Hipertonía: Es el aumento del tono muscular. Se manifiesta como una resistencia aumentada al movimiento pasivo. Las extremidades son difíciles de mover y el rango de movimiento puede estar limitado. Es común en condiciones que dañan el sistema nervioso central, como el ictus (donde a menudo aparece después de una fase inicial de hipotonía), lesión medular, lesión cerebral traumática, esclerosis múltiple y parálisis cerebral. La hipertonía se debe en gran parte a la pérdida de la inhibición supraspinal sobre la médula espinal.
La espasticidad es un tipo específico de hipertonía que depende de la velocidad del movimiento pasivo: cuanto más rápido se estira el músculo, mayor es la resistencia. A menudo es más fuerte en una dirección que en otra. Se diferencia de la rigidez, que no depende de la velocidad y es similar en todas las direcciones. La rigidez se asocia a menudo con patología de los ganglios basales y se observa comúnmente en la enfermedad de Parkinson avanzada y las distonías. La hipertonía rara vez se presenta de forma aislada y a menudo coexiste con paresia. Aunque la hipertonía (o espasticidad) se correlaciona con la limitación de la actividad, la evidencia actual sugiere que no es la causa principal de estas limitaciones funcionales; por ejemplo, la toxina botulínica reduce la espasticidad pero no mejora significativamente la función.
Déficits en el Movimiento Fraccionado
El movimiento fraccionado es la capacidad de aislar el movimiento de un segmento corporal mientras otros segmentos adyacentes permanecen quietos, algo esencial para la manipulación fina de las extremidades superiores. Una capacidad reducida para fraccionar el movimiento limita severamente la realización de tareas funcionales. Estos déficits resultan del daño al sistema corticoespinal, afectando la capacidad de activar músculos selectivamente. Clínicamente, se observan como movimientos sinérgicos anormales, donde al intentar mover una articulación, otras articulaciones proximales o distales se mueven simultáneamente de forma no deseada. Por ejemplo, intentar levantar el hombro puede activar también los flexores de codo o los pronadores del antebrazo. Estos déficits están relacionados con la gravedad de la paresia y la hipertonía. Las personas con distonía, que presentan contracciones musculares sostenidas e involuntarias que causan posturas anormales, también exhiben una forma de déficit de movimiento fraccionado. Las distonías a menudo se asocian con patología de los ganglios basales, donde se cree que una vía indirecta hipoactiva resulta en una inhibición reducida del tálamo y una incapacidad para suprimir la actividad muscular no deseada.
Ataxia
La ataxia es una falta de coordinación entre los movimientos y/o partes del cuerpo. Se caracteriza por la dismetría, que es la incapacidad de medir con precisión la distancia del movimiento, resultando en hipermetría (sobrepasar el objetivo) o hipometría (quedarse corto). Las personas con ataxia tienden a ser hipermétricas al moverse rápido e hipométricas al moverse lento. La ataxia es causada por daño en el cerebelo, sus entradas o salidas. Se diferencia de los problemas de coordinación debidos a paresia o déficits de movimiento fraccionado en que la persona con ataxia aún puede moverse rápidamente, y la ataxia generalmente empeora a velocidades de movimiento más altas. El cerebelo es crucial para integrar movimientos multisegmentarios y controlar las fuerzas de interacción (fuerzas rotacionales generadas por el movimiento de un segmento sobre otro). El daño cerebeloso dificulta el control de estas fuerzas, haciendo que los movimientos sean influenciados por ellas en lugar de por las acciones musculares intencionadas. La ataxia limita principalmente la marcha y el equilibrio, aunque las dificultades en la marcha a menudo se deben a problemas de control del equilibrio durante el movimiento.
Hipokinesia
La hipokinesia es una deficiencia motora primaria asociada principalmente con la enfermedad de Parkinson y condiciones parkinsonianas. Se caracteriza por movimientos lentos (bradicinesia) o ausencia de movimiento (acinesia). En la enfermedad de Parkinson, coexiste con temblor en reposo y rigidez. Es causada por daño en los ganglios basales, particularmente la pérdida de células dopaminérgicas en la sustancia negra pars compacta. La hipótesis subyacente es una vía indirecta de los ganglios basales hiperactiva, que resulta en una inhibición casi constante del tálamo y una incapacidad para seleccionar el plan motor deseado. Clínicamente, se manifiesta como frecuente co-contracción muscular, dificultad para iniciar el movimiento (congelación), una postura flexionada hacia adelante con inestabilidad y una marcha lenta y arrastrada. Los problemas en las extremidades superiores incluyen temblor y escritura pequeña (micrografía). Estos síntomas empeoran con la progresión de la enfermedad.
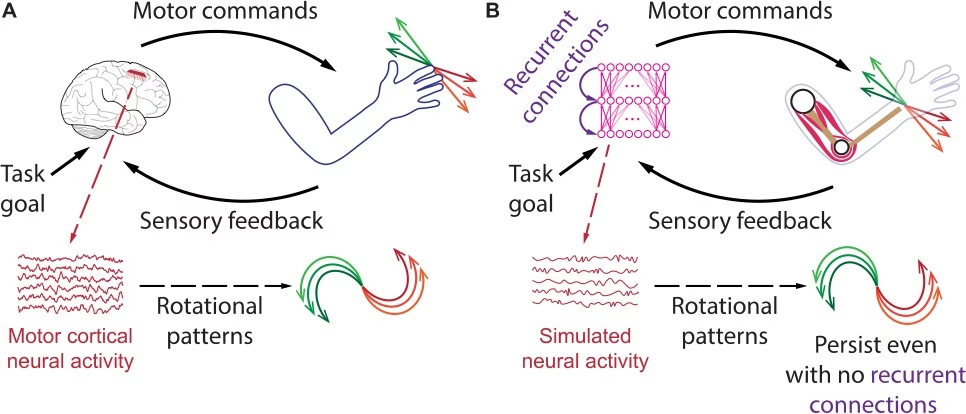
Pérdida Somatosensorial
La pérdida somatosensorial (del tacto, propiocepción, etc.) es común en adultos mayores y puede afectar significativamente el control motor. Puede ser de origen periférico (daño nervioso) o central (daño en vías o corteza somatosensorial). La principal consecuencia es una monitorización menos efectiva del movimiento en curso. El sistema somatosensorial proporciona retroalimentación rápida sobre las consecuencias del movimiento (ej. sentir que un vaso se resbala para aumentar la fuerza de agarre). La visión puede compensar parcialmente, pero no completamente, la falta de somatosensación. Las personas con pérdida somatosensorial a menudo se mueven lentamente para depender de la retroalimentación visual, y sus movimientos empeoran en condiciones de baja visibilidad. Esta deficiencia a menudo coexiste con otras, especialmente paresia.
Déficits Perceptuales
Los déficits perceptuales pueden causar problemas significativos de control motor. El síndrome del empujador es un ejemplo. Pacientes con este síndrome (a menudo tras ictus, lesión cerebral traumática o tumores) empujan con las extremidades no afectadas hacia el lado afectado. A pesar de tener entradas visuales y vestibulares intactas, parecen tener una percepción distorsionada de la orientación corporal respecto a la gravedad. El empuje y la resistencia a la corrección postural pueden ser una estrategia compensatoria para una discrepancia sensorial/perceptual. Aunque a menudo mejora en los primeros meses post-ictus, su persistencia a los 3 meses se asocia con un mal pronóstico funcional. Las características incluyen postura inclinada hacia el lado parético, extremidades no afectadas abducidas/extendidas empujando hacia el lado parético, y resistencia a la corrección pasiva. A menudo coexiste con negligencia del lado afectado y/o afasia, y la paresia suele ser severa.
Evaluación de las Deficiencias del Control Motor
La evaluación neurológica del control motor difiere de una evaluación musculoesquelética. El enfoque está en identificar qué deficiencias, que a menudo se presentan agrupadas, contribuyen a la pérdida de actividad y participación. Gran parte de la evaluación se basa en la observación y el análisis de los movimientos funcionales. El objetivo es determinar cómo las deficiencias presentes se asocian o contribuyen a los déficits funcionales.
Tradicionalmente, se ha puesto mucho énfasis en la evaluación detallada de las deficiencias individuales. Sin embargo, la evidencia sugiere que algunas de estas medidas de deficiencia pueden tener una relación limitada con el rendimiento funcional, especialmente en las extremidades superiores post-ictus (ej. tacto ligero, sentido de posición articular). Es más útil realizar un cribado rápido de una modalidad sensorial en una ubicación clave (ej. tacto ligero en la punta de un dedo) para educación del paciente, en lugar de un examen exhaustivo para el diagnóstico del problema de movimiento. En la extremidad inferior, el sentido de posición articular puede ser más relevante debido a su importancia para la colocación del pie al caminar.
Una evaluación eficaz tiene dos objetivos principales: (1) determinar el problema subyacente del sistema de movimiento (diagnóstico) y (2) establecer un nivel inicial de deficiencia, actividad y participación para medir el progreso futuro (evaluación de resultados). Algunas herramientas sirven para ambos propósitos.
La paresia es una de las deficiencias más importantes y más fáciles de evaluar. El rango de movimiento activo (RMA) y el test muscular manual son medidas indirectas de la capacidad de activar voluntariamente las motoneuronas. El RMA puede ser útil para capturar déficits leves, mientras que el test muscular manual (como en el Índice de Motricidad) es mejor para déficits más severos. El Índice de Motricidad, que evalúa solo tres grupos musculares por extremidad, es una herramienta útil y ampliamente utilizada para evaluar la fuerza global de la extremidad post-ictus. La capacidad de fraccionar el movimiento está altamente correlacionada con la paresia; evaluar el RMA puede proporcionar información suficiente sobre ambas deficiencias.
La lentitud del movimiento es una observación común en pacientes con deficiencias motoras, pero puede deberse a diferentes razones según la deficiencia subyacente (déficits de activación en paresia, estrategia compensatoria en ataxia o pérdida somatosensorial, o característica central en hipokinesia). Es importante relacionar la lentitud observada con las deficiencias específicas presentes.
Las medidas de resultados deben evaluar la actividad y la participación. Herramientas comunes incluyen la velocidad de la marcha, el Timed Up and Go, el test de marcha de 6 minutos para las extremidades inferiores/marcha, y el Action Research Arm Test o la Canadian Occupational Performance Measure (COPM) para las extremidades superiores. La evaluación también debe incluir el estado mental, el entorno vital y las deficiencias secundarias que pueden surgir de la falta de movimiento (contracturas, atrofia muscular, desacondicionamiento cardiovascular), ya que estas influyen en el plan de tratamiento.
| Deficiencia Común | Descripción Breve | Mecanismo Principal | Manifestación Clínica |
|---|---|---|---|
| Paresia/Plegia | Reducción/Pérdida de activación voluntaria muscular. | Daño al sistema corticoespinal. | Debilidad muscular, dificultad para generar fuerza, estrategias compensatorias. |
| Hipotonía | Disminución del tono muscular. | Disminución/Ausencia de señal neural al músculo. | Resistencia disminuida al movimiento pasivo, reflejos disminuidos, flacidez. |
| Hipertonía | Aumento del tono muscular. | Pérdida de inhibición supraspinal (corticoespinal). | Resistencia aumentada al movimiento pasivo, reflejos aumentados. |
| Espasticidad | Tipo de hipertonía dependiente de la velocidad. | Daño al sistema corticoespinal. | Resistencia aumentada que varía con la velocidad del estiramiento. |
| Rigidez | Tipo de hipertonía no dependiente de la velocidad. | Patología de ganglios basales. | Resistencia aumentada constante al movimiento pasivo. |
| Déficit Movimiento Fraccionado | Reducción capacidad aislar movimiento articular. | Daño al sistema corticoespinal; patología de ganglios basales (distonía). | Movimientos sinérgicos anormales, dificultad manipulación fina, posturas anormales (distonía). |
| Ataxia | Falta de coordinación de movimientos. | Daño cerebeloso. | Dismetria (hiper/hipometría), dificultad control interacción torques, marcha/equilibrio inestables. |
| Hipokinesia | Movimiento lento/ausente. | Daño de ganglios basales (enfermedad de Parkinson). | Bradicinesia/Acinesia, dificultad inicio/fin movimiento, congelación, rigidez, temblor, postura flexionada. |
| Pérdida Somatosensorial | Pérdida de sensación (tacto, propiocepción). | Daño vías/corteza sensorial (periférico o central). | Monitorización del movimiento afectada, dependencia visual, movimientos lentos. |
| Déficit Perceptual | Percepción distorsionada (ej. orientación espacial). | Daño en áreas cerebrales (ej. tálamo posterolateral). | Conductas motoras anormales (ej. empujar hacia un lado), resistencia a la corrección postural. |
Diagnóstico y Pronóstico
El fisioterapeuta diagnostica el problema del sistema de movimiento (deficiencias que limitan la actividad), no la condición médica subyacente. Las deficiencias del control motor coexisten y no son exclusivas de una sola condición médica. El pronóstico está fuertemente influenciado por la condición médica: en condiciones no progresivas (ictus, lesión medular), la recuperación ocurre principalmente al inicio; en condiciones progresivas (Parkinson, esclerosis múltiple), se espera que las deficiencias empeoren con el tiempo.
En condiciones no progresivas, la severidad inicial de las deficiencias es el mejor predictor de los déficits motores y funcionales finales. Los pacientes con déficits más leves se recuperan más rápido y completamente. La mayor parte de la recuperación motora post-ictus ocurre en los primeros 3 meses. Factores que predicen un peor pronóstico post-ictus incluyen la presencia de múltiples deficiencias no motoras (pérdida sensorial, déficits visuales), falta de mejoras tempranas en las deficiencias motoras, y la presencia de déficits severos (ej. mínima fuerza de agarre, flexión de hombro/cadera contra gravedad) un mes o más después del ictus.
Al determinar el pronóstico de rehabilitación, se deben considerar tres preguntas clave: (1) ¿El control motor empeorará, se mantendrá o mejorará? (2) ¿Se pueden mejorar las limitaciones de actividad y participación incluso si el control motor no cambia? (3) ¿La intervención de rehabilitación marcará una diferencia? La respuesta a estas preguntas guía los objetivos del tratamiento y si el enfoque debe ser de remediación o compensación.
Enfoque de Rehabilitación: Remediación vs. Compensación
| Enfoque | Objetivo Principal | Cuándo Usar (Ejemplos) | Ejemplo de Intervención |
|---|---|---|---|
| Remediación | Restaurar la capacidad motora y función perdidas. | Condiciones no progresivas (ictus agudo/subagudo) con capacidad de movimiento fraccionado voluntario significativo. | Práctica intensiva de tareas para recuperar destreza manual o patrón de marcha normal. |
| Compensación | Maximizar la función dentro de las limitaciones motoras existentes. | Condiciones progresivas (Parkinson) o condiciones no progresivas crónicas con mínima capacidad de movimiento fraccionado voluntario. | Enseñar estrategias adaptativas, uso de dispositivos de asistencia (ortesis, andadores), entrenamiento para usar extremidad afectada como soporte. |
La decisión entre un enfoque de remediación o compensación es crucial y se basa en el pronóstico del paciente. Un enfoque de remediación busca restaurar la función perdida, mientras que un enfoque compensatorio se centra en maximizar la función actual a pesar de las limitaciones. Por ejemplo, en un paciente con Parkinson, un enfoque compensatorio suele ser más apropiado ya que la enfermedad es progresiva. En un paciente post-ictus temprano con cierto movimiento voluntario, la remediación puede ser el objetivo para recuperar la destreza o un patrón de marcha más normal. Para un paciente post-ictus crónico con déficits severos, un enfoque compensatorio se centraría en mantener la salud de la extremidad (prevenir contracturas) y usarla como apoyo o asistencia.
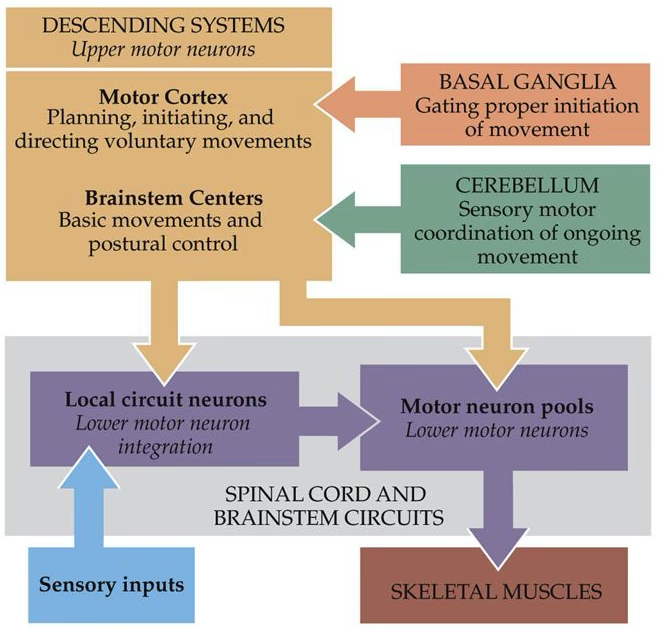
Intervenciones Basadas en la Tarea Específica
Las intervenciones para las deficiencias del control motor deben dirigirse a mejorar la función, no a tratar las deficiencias de forma aislada. El soporte para esto proviene de los mecanismos de aprendizaje motor y neuroplasticidad. El aprendizaje motor es la adquisición o readquisición de movimientos, mientras que la neuroplasticidad es la capacidad del sistema nervioso para modificarse (neuronas, conexiones, representaciones). La evidencia sugiere que los cambios inducidos por la experiencia son específicos de las estructuras neurales utilizadas durante la práctica. La práctica repetida de un movimiento refuerza y remodela las conexiones neuronales específicas de la red neural utilizada para esa tarea. Practicar parte de un movimiento de forma aislada probablemente no activará la misma red neuronal que se necesita para la actividad funcional completa. Por lo tanto, el entrenamiento específico de la tarea es fundamental para optimizar la función.
La evidencia de la investigación clínica también respalda el entrenamiento específico de la tarea. Por ejemplo, la práctica del equilibrio mejora el equilibrio, pero no la marcha, mientras que la práctica de la marcha mejora la marcha. El entrenamiento de fuerza mejora la fuerza, pero solo mejora la función si se realiza en el contexto de la tarea funcional (ej. levantarse de una silla para mejorar la fuerza del cuádriceps en la transferencia). Por lo tanto, la intervención debe centrarse en el nivel de actividad, e incluso de participación.
Evidencia Actual y Consideraciones Prácticas
La evidencia sobre el tratamiento de las deficiencias del control motor, especialmente post-ictus, está en constante evolución. Recursos como el Evidence-Based Review of Stroke Rehabilitation (EBRSR) resumen la evidencia actual para guiar la práctica clínica.
Para las extremidades superiores, es imposible practicar todas las tareas funcionales. Las tareas se componen de elementos básicos: alcanzar, agarrar, mover/manipular y soltar. Se deben seleccionar tareas funcionalmente importantes para el paciente que desafíen sus habilidades motoras. La dificultad de una tarea puede graduarse (ej. cambiando tamaño/peso de objetos, posición del paciente) para mantenerla desafiante pero alcanzable (idealmente, que una repetición tome entre 6 y 15 segundos). Los programas domiciliarios también deben enfocarse en la práctica de tareas funcionales. Algunas intervenciones comúnmente usadas tienen evidencia limitada o nula de beneficio funcional (ej. férulas para reducir contracturas/mejorar función, estiramientos generales para espasticidad, biofeedback EMG, técnicas de neurodesarrollo no son superiores a la terapia convencional). Otras tienen fuerte evidencia de beneficio en circunstancias específicas (ej. Terapia de Movimiento Inducido por Restricción en ictus subagudo/crónico con cierto movimiento activo, Estimulación Eléctrica Funcional para pacientes de menor nivel). La toxina botulínica reduce temporalmente la espasticidad, pero no mejora la función.
Para las extremidades inferiores y la marcha, el entrenamiento específico de la marcha y el equilibrio tiene fuerte evidencia de beneficio. El entrenamiento cardiovascular también es importante para mejorar la resistencia necesaria para la participación. Las ortesis de tobillo-pie y la Estimulación Eléctrica Funcional son beneficiosas para la paresia moderada a severa. El entrenamiento de marcha robótica no ha demostrado ser superior al entrenamiento de marcha tradicional sobre el suelo, posiblemente porque el robot hace parte del trabajo en lugar del paciente.
| Enfoque de Intervención | Evidencia Clave (Basado en EBRSR para ictus) | Consideraciones |
|---|---|---|
| Entrenamiento Específico de la Tarea (General) | Fuerte evidencia de beneficio para función (marcha, equilibrio, UE). | Debe ser relevante para el paciente, desafiante pero alcanzable. |
| Entrenamiento de Fuerza | Mejora fuerza; mejora función si se realiza en contexto funcional. | Integrar en tareas funcionales (ej. sentarse-levantarse). |
| Entrenamiento Cardiovascular | Mejora fitness y función (resistencia). | Monitorear signos vitales, intensidad apropiada. |
| Terapia de Movimiento Inducido por Restricción (CIMT) | Fuerte evidencia para UE en ictus subagudo/crónico con cierto movimiento activo. | No clara evidencia en fase aguda. Requiere capacidad motora mínima. |
| Estimulación Eléctrica Funcional (FES) | Fuerte evidencia de beneficio para UE/LE con paresia moderada/severa. | Útil en diferentes fases post-ictus. |
| Toxina Botulínica | Fuerte evidencia en reducción temporal de espasticidad. | No mejora la función motora de la UE. |
| Férulas (UE) | Moderada/Fuerte evidencia de mínimo/nulo beneficio para reducción contracturas/mejora función. | Principalmente para mantener longitud muscular, no para mejorar función activa. |
| Estiramiento General/Férulas (Espasticidad) | Moderada/Fuerte evidencia de nulo beneficio para reducción espasticidad. | La espasticidad es variable y compleja. |
| Técnicas de Neurodesarrollo (Bobath, PNF) | Fuerte evidencia de no ser superiores a terapia convencional. | Aunque usadas, la evidencia no respalda su superioridad. |
| Entrenamiento de Marcha Robótica | Evidencia sugiere menos efectivo que entrenamiento sobre suelo. | Puede ser útil para otros propósitos (ej. resistencia, carga ósea) pero no primariamente para mejorar patrón de marcha. |
Preguntas Frecuentes
¿Qué estructuras cerebrales controlan el movimiento voluntario?
El movimiento voluntario es controlado por una red compleja que incluye áreas corticales motoras (corteza motora primaria, premotora, suplementaria), ganglios basales, cerebelo y vías descendentes como el tracto corticoespinal.
¿Qué parte del cerebro es clave en la coordinación del movimiento?
El cerebelo es la estructura cerebral principal responsable de la coordinación, corrección y adaptación del movimiento, asegurando fluidez y precisión.
¿Qué lóbulo cerebral está principalmente involucrado en el control motor?
El lóbulo frontal contiene la corteza motora, que incluye las áreas motoras primaria, premotora y suplementaria, cruciales para la planificación, control y ejecución de movimientos voluntarios.
¿Cuál es la diferencia entre paresia y plegia?
La paresia es la reducción de la capacidad de activar voluntariamente los músculos (debilidad), mientras que la plegia es la pérdida completa de esta capacidad (parálisis total).
¿Qué diferencia hay entre espasticidad y rigidez?
Ambas son formas de hipertonía (aumento del tono muscular). La espasticidad es dependiente de la velocidad (resistencia aumenta con mayor velocidad de estiramiento), mientras que la rigidez no depende de la velocidad (resistencia constante).
¿Por qué el entrenamiento debe ser específico de la tarea?
La neuroplasticidad y el aprendizaje motor sugieren que el sistema nervioso se reorganiza de manera específica en las redes neurales utilizadas durante la práctica. Entrenar una tarea funcional completa es más efectivo para mejorar esa tarea que entrenar componentes aislados, ya que activa las redes neuronales relevantes para la actividad deseada.
Si quieres conocer otros artículos parecidos a Control Motor en Neurociencia: Guía Completa puedes visitar la categoría Neurociencia.